Léčba teriflunomidem − data z reálné praxe
Informace z reálné klinické praxe jsou u každého léku pečlivě sledovány a zaznamenávány. Dokáží o léčbě konkrétních nemocných s jejich různorodostí poskytnout cenné informace, které nemusejí klinické studie s přesně specifikovanými skupinami pacientů postihnout. Mohou potvrdit předpokládaná očekávání, doložit dlouhodobé účinky terapie, nebo naopak odhalit nežádoucí účinky léčby nezaznamenané během klinického hodnocení.
V roce 2019 byly publikovány zajímavé práce sledující v reálném prostředí léčbu teriflunomidem (studie fáze IV) [1,2]. Teriflunomid je imunomodulační lék s protizánětlivými účinky indikovaný k terapii relabující remitující roztroušené sklerózy (RS), je schválen ve více než 80 zemích. Teriflunomid redukuje proliferaci aktivovaných T a B lymfocytů. Je podáván perorálně jednou denně v dávce 14 mg.
Průběh RS je variabilní a těžko predikovatelný, hlavním cílem léčby je snížení rizika relapsu a progrese disability. Demografické parametry a management pacientů s tímto onemocněním se liší podle oblasti. Některá sledování ukazují rozdíly v geografické distribuci s vyšší prevalencí RS v oblastech dále od rovníku [3,4], jiné práce poukazují na rozdíly v incidenci RS podle etnik – vyšší incidence a rychlejší progrese onemocnění byla doložena u černošské populace [5,6]. Rozdíly je možné zaznamenat také ve vedení léčby – v dostupné léčbě modifikující onemocnění i ve schválených doporučených postupech a praxi. Není zatím zcela jasné, jestli/jak tyto rozdíly ovlivňují výsledky léčby.
Studie TAURUS MS
Cílem klinického hodnocení TAURUS MS fáze IV bylo získat data o účinnosti, snášenlivosti a subjektivní spokojenosti s léčbou teriflunomidem v reálném prostředí u pacientů s RS [2]. Tato prospektivní observační studie probíhala v Německu, celkem bylo k analýze účinnosti zavzato 1 128 pacientů. Zahrnuti byli pacienti starší 18 let s diagnózou relabující remitující RS, u nichž nebyla žádná kontraindikace k podávání léčby. Průměrný věk nemocných byl 44,9 (± 10,2) roku, 67,5 % tvořily ženy. Většina nemocných (70,4 %) měla skóre disability (Expanded Disability Status Scale, EDSS) ≤ 3,5. Míra disability zahrnovala široké rozpětí, průměrná hodnota EDSS představovala 2,3 ± 1,5. Průměrná doba od stanovení diagnózy RS byla 8,9 ± 7,6 roku. V průběhu 24měsíční periody byl průměrný počet relapsů onemocnění 0,95 ± 1,10.
Bez předchozí léčby před vstupem do klinického hodnocení bylo 280 nemocných (24,8 %). Z 848 již dříve léčených pacientů (75,2 %) se jich 37,2 % rozhodlo ukončit léčbu samo, u 24,5 % rozhodl o ukončení lékař a u 33,1 % šlo o společné rozhodnutí (žádná data nemáme u 5,2 %). Důvodem ukončení předchozí terapie byly u 59,0 % nežádoucí účinky, u 24,2 % nedostatečná účinnost léčby, u 16,2 % přání přejít na perorální léčbu modifikující onemocnění (disease modifying therapy, DMT) a v 10,4 % případů šlo o požadavek přerušení léčby. Dříve léčení pacienti dostávali nejčastěji glatiramer acetát (10,6 %), subkutánní interferon β 1a (9,3 %), intramuskulární interferon β 1a (6,6 %) nebo β 1b (6,6 %).
Teriflunomid byl podáván denně
v dávce 14 mg, nemocní byli sledováni po dobu 24
měsíců (průměrně 16,3 ± 9,1 měsíce). Po 12 měsících
léčby teriflunomidem byl průměrný roční počet relapsů
(annualized relapse rate, ARR) 0,24 ± 0,53 (95% interval
spolehlivosti [CI] 0,20−0,28) a po 24 měsících léčby
0,35 ± 0,68 (95% CI 0,29−0,41). Rozdíl ve výskytu
relapsů ukazuje graf 1.
Zaznamenávány byly tzv. výsledky hlášené pacienty
(patient reported outcomes, PRO). K subjektivnímu
hodnocení spokojenosti byl užit dotazník TSQM 9 (Treatment
Satisfaction Questionnaire for Medication). V průběhu
sledování došlo ke zlepšení ve všech třech doménách.
Skóre zaznamenávající účinnost léčby se od začátku
sledování zvýšilo průměrně o 5,8 ± 29,9 bodu.
Na stupnici hodnotící míru únavy (Fatigue Severity Scale,
FSS) byly v průběhu léčby zaznamenány pouze nepatrné
změny.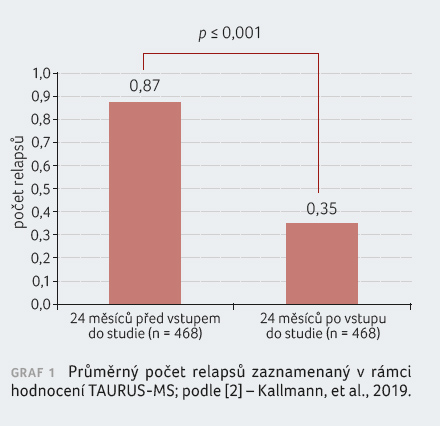
Studie fáze IV Teri PRO
Klinická studie fáze IV Teri PRO se zaměřila na hodnocení léčby vnímané pacienty (PRO, viz výše) [1]. Tato zjištění mohou přinést další informace o vlivu léčby na běžný život nemocného a vzhledem k reálnému prostředí a širšímu spektru pacientů mohou pomoci najít vodítka pro výběr konkrétního léku pro konkrétního pacienta.
Teriflunomidem bylo léčeno po dobu 48 týdnů celkem 1 000 nemocných. Primárním cílovým ukazatelem studie byla spokojenost pacientů s léčbou zaznamenávaná pomocí dotazníku TSQM, verze 1.4. Sekundárními cílovými ukazateli byla skóre hodnocení disability EDSS, MSPS (Multiple Sclerosis Performance Scale), PDDS (Patient Determined Disease Steps) a výskyt nežádoucích účinků.
U pacientů byla zaznamenána vysoká spokojenost s léčbou (skóre TSQM v týdnu 48 bylo 68,2), u nemocných, kde došlo ke změně léčby (tzv. switch) na teriflunomid, byl zaznamenán nárůst spokojenosti. Výskyt nežádoucích účinků byl srovnatelný s registračními klinickými studiemi [1]. Spokojenost pacientů s podávanou léčbou zvyšuje adherenci nemocných a přispívá tak k lepším léčebným výsledkům.
Post hoc analýza
Jak již bylo zmíněno, demografické
charakteristiky i management pacientů s RS (schválené
guidelines, dostupná léčiva, předepisovací zvyklosti) se liší
podle geografické oblasti a není zcela jasné, do jaké
míry tyto rozdíly ovlivňují výsledky terapie. Cílem post
hoc analýzy, jejíž výsledky byly publikovány
v letošním roce [7], bylo zhodnotit podávání teriflunomidu
ve Spojených státech (US – ve Spojených státech
amerických; n = 545) a ve „zbytku světa“ (ROW –
rest of world; n = 455). Nemocní s relabující
formou RS dostávali léčbu teriflunomidem podle lokálních
doporučení. Charakteristiky pacientů obou skupin uvádí tabulka 1. Zvlášť byla zkoumána skupina černošské populace,
u níž je doložena vyšší závažnost onemocnění.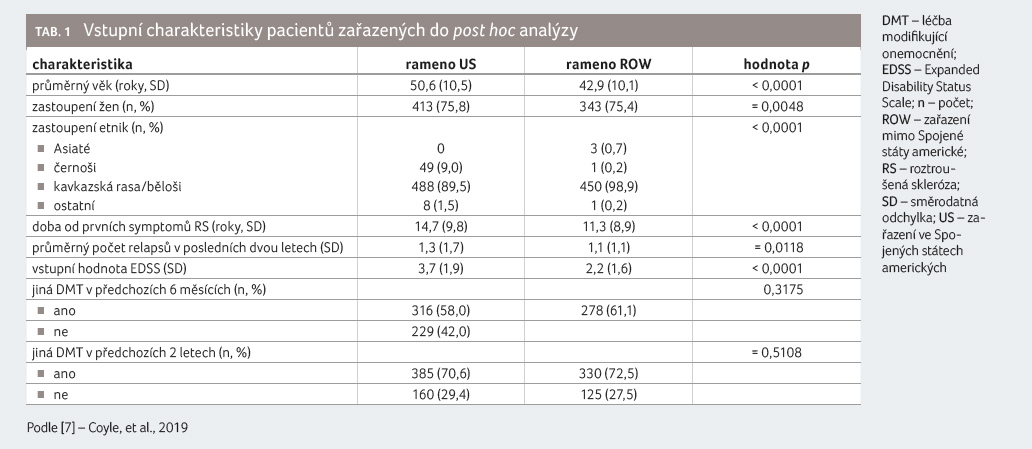
V rameni ROW byl zaznamenán nižší průměrný věk pacientů, kratší doba od prvních symptomů a nižší průměrné skóre EDSS na počátku hodnocení v porovnání s ramenem US (p < 0,0001). Hodnocená skóre vykazovala ve 48. týdnu zlepšení v obou skupinách, míra disability byla stabilní v obou skupinách (navzdory rozdílné počáteční úrovni). Podíl pacientů, kteří zaznamenali během sledování nežádoucí účinky, byl v obou skupinách rovněž podobný. Méně pacientů v rameni US uvádělo ztenčení vlasů (16,1 % vs. 31,2 %). Při srovnání v rámci US ramene vykazovala černošská populace srovnatelné počáteční charakteristiky a obdobnou změnu PRO.
Autoři publikace shrnují, že navzdory rozdílným charakteristikám pacientů v obou ramenech a odlišnostem ve vedení léčby (daných regionálně i charakterem pacientů) byly spokojenost s léčbou i účinnost teriflunomidu (stabilita disability) v obou skupinách srovnatelné. V této analýze nebyly u černošské populace doloženy odlišnosti ve vstupních charakteristikách ani změny během léčby oproti zbytku pacientů v rameni US (kde bylo jejich zastoupení analyzovatelné, nicméně vzorek populace není pro závěry ještě dostatečně reprezentativní).
Redakčně zpracovala PharmDr. Kateřina Viktorová
Seznam použité literatury
- [1] Coyle PK, Khatri B, Edwards KR, et al. Patient‑reported outcomes in relapsing forms of MS: Real‑world, global treatment experience with teriflunomide from the Teri‑PRO study. Mult Scler Relat Disord 2017; 17: 107−115.
- [2] Kallmann BA, Tiel‑Wilck K, Kullmann JS, et al. Real‑life outcomes of teriflunomide treatment in patients with relapsing multiple sclerosis: TAURUS‑MS observational study. Ther Adv Neurol Disord 2019; 12: 1−14.
- [3] Leray E, Moreau T, Fromont A, Edan G. Epidemiology of multiple sclerosis. Rev Neurol 2016; 172: 3−13.
- [4] Simpson S Jr, Blizzard L, Otahal P, et al. Latitude is significantly associated with the prevalence of multiple sclerosis: a meta‑analysis. J Neurol Neurosurg Psychiatry 2011; 82: 1132−1141.
- [5] Langer‑Gould A, Brara SM, Beaber BE, Zhang JL. Incidence of multiple sclerosis in multiple racial and ethnic groups. Neurology 2013; 80: 1734−1739.
- [6] Ventura RE, Antezana AO, Tamar B, Ilya K. Hispanic Americans and African Americans with multiple sclerosis have more severe disease course than Caucasian Americans. Mult Scler J 2017; 23: 1554–1557.
- [7] Coyle PK, Khatri B, Edwards KR, et al. Teriflunomide reald‑world evidence: Global differences in the phase 4 Teri‑PRO study. Mult Scler Relat Dis 2019; 31: 157−164.