Nintedanib – zkušenosti z klinické praxe
Souhrn:
Venclíček O. Nintedanib – zkušenosti z klinické praxe. Remedia 2018; 28: 350–352.
Článek podává základní informace o nintedanibu, mechanismu jeho účinku, léčebných indikacích a nežádoucích účincích a předkládá zkušenosti z klinické praxe formou dvou kazuistik pacientů léčených nintedanibem.
Summary:
Venclicek O. Nintedanib – experience from clinical practice. Remedia 2018; 28: 350–352.
The article provides basic information on nintedanib, its mechanism of action, therapeutic indications, adverse effects, and presents clinical experience in the form of two clinical cases of patients treated with nintedanib.
Key words: non‑small cell lung cancer, nintedanib, angiogenesis inhibition.
Úvod
V České republice je bronchogenní karcinom ve srovnání incidencí všech nádorových onemocnění u mužů i žen na druhém místě, v mortalitě pak u mužů na první a u žen na třetí pozici. Celosvětově se ČR na žebříčku výskytu bronchogenního karcinomu nachází na 13. příčce [1,2].
Většinu případů plicních nádorů tvoří nemalobuněčný plicní karcinom (non small cell lung cancer, NSCLC). V rámci této kategorie se u mužů častěji vyskytuje skvamózní karcinom, u žen adenokarcinom. Pouze malá část pacientů je diagnostikována v době, kdy je možná radikální léčba, více než 70 % případů je zachyceno v klinickém stadiu III nebo IV. Prognóza pacientů ve IV. klinickém stadiu je velmi nepříznivá, v letech 2010–2015 bylo pětileté přežití v této kategorii 2,9 % [1,2].
Nintedanib je perorálně dostupný inhibitor angiogeneze působící na několik cílů, které se procesu angiogeneze účastní. Jedná se o receptory pro vaskulární endoteliální růstový faktor (vascular endothelial growth factor receptor, VEGFR), receptory pro destičkový růstový faktor (platelet derived growth factor receptor, PDGFR) a receptory pro fibroblastový růstový faktor (fibroblast growth factor receptor, FGFR). Díky svému vícečetnému mechanismu účinku působí nintedanib nejen proti nádorové angiogenezi, ale i antifibroticky, a je proto využíván v léčbě idiopatické plicní fibrózy (IPF) [3,4].
Nintedanib je v kombinaci s docetaxelem registrován k léčbě dospělých pacientů s metastazujícím nebo lokálně pokročilým adenokarcinomem po selhání chemoterapie první linie. Je podáván dvakrát denně v celkové dávce 400 mg 2.–22. den léčebného cyklu. V léčbě nintedanibem lze po ukončení podávání docetaxelu pokračovat do známek progrese nádorového onemocnění, či do nepřijatelné toxicity léčby [4].
Mezi nežádoucí účinky léčby nintedanibem patří neutropenie, elevace hodnot jaterních enzymů a krvácení. Dále při léčbě hrozí vyšší riziko tromboembolických příhod, horšího hojení ran a riziko gastrointestinálních perforací. Pacienti s aktivními mozkovými metastázami byli z klinických studií vyřazeni a léčba nintedanibem se u takovýchto nemocných nedoporučuje [4].
Mezinárodní randomizovaná, zaslepená studie fáze III LUME Lung 1 zkoumala u skupiny pacientů s pokročilým inoperabilním NSCLC efekt nintedanibu v kombinaci s docetaxelem po selhání první linie léčby. Komparátorem byl docetaxel plus placebo. Celkem 1 314 pacientů bylo do obou ramen rozděleno v poměru 1 : 1. Primárním cílovým ukazatelem studie bylo přežití do progrese (progression free survival, PFS), sekundárním pak celkové přežití (overall survival, OS). Pacienti v rameni s docetaxelem a nintedanibem dosáhli mediánu PFS 3,4 měsíce, v rameni docetaxelu s placebem pak 2,7 měsíce. Nejlepších výsledků parametru OS dosáhli pacienti s adenokarcinomy – medián OS 12,6 měsíce v případě léčby kombinací docetaxel plus nintedanib versus 10,3 měsíce při léčbě docetaxelem a placebem. Celkové přežití v celé populaci bez ohledu na histologii bylo 10,1 měsíce ve skupině s nintedanibem a 9,1 měsíce ve skupině s placebem. Ze závažných nežádoucích účinků se v nintedanibové skupině častěji vyskytoval průjem a elevace hodnot jaterních enzymů. V obou byly pozorovány neutropenie, leukopenie, nevolnost, zvracení, únava, epistaxe a další [5].
Kazuistika 1
Žena, v době diagnózy 24 let, bez komorbidit, bez trvalé medikace. Kuřačka zhruba od 15 let, postupně až 20 cigaret denně. Zaměstnána jako servírka v kuřácké restauraci, oba rodiče kuřáci.
V květnu 2014 navštívila lékaře
pro bolesti žeber vpravo, provedený skiagram hrudníku zachytil
infiltraci v pravém horním plicním poli. Následně bylo
ve spádové nemocnici provedeno vyšetření výpočetní
tomografií (CT) hrudníku s nálezem tumorózní formace
maligních rysů v pravém plicním hrotu s postižením
mediastinálních a hilových lymfatických uzlin a ložisko
12. hrudního obratle nejistého původu (obr. 1).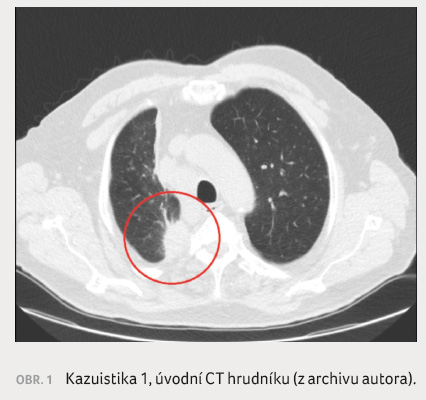
Na témže pracovišti následovalo bronchoskopické vyšetření, při kterém byly nalezeny nepřímé známky nádoru v bronchu pro pravý horní lalok. Na konci května byla pacientka k další diagnostice a léčbě odeslána na naše pracoviště. Protože první bronchoskopické vyšetření morfologickou diagnózu nepřineslo, byla bronchoskopie zopakována – s nálezem přímých i nepřímých známek nádoru v oblasti pravého horního bronchu. Z provedených odběrů byla histologicky stanovena diagnóza nízce diferencovaného primárně plicního adenokarcinomu, bez přítomnosti řídících mutací v genu receptoru pro epidermální růstový faktor (epidermal growth factor receptor, EGFR) či v genu pro anaplastickou lymfomovou kinázu (ALK).
V rámci dokončení stagingu proběhla scintigrafie skeletu – s nálezem mnohočetného metastatického postižení, včetně prominující metastázy čelní kosti. Magnetická rezonance hlavy přímé metastatické postižení mozku neprokázala. Výsledný staging byl T3N3M1b, klinické stadium IV, performance status (PS) před zahájením léčby 1.
Bylo zahájeno sycení kyselinou listovou a 20. června 2014 byl započat I. cyklus 1. linie paliativní chemoterapie ve složení cisplatina a pemetrexed. O tři dny později dostala pacientka první dávku denosumabu v rámci paliativní léčby kostních metastáz. Za hospitalizace byla také titrována terapie bolesti pomocí opioidů.
Kontrolní CT hrudníku po II. cyklu chemoterapie konstatovalo progresi onemocnění, byla popsána progrese tumoru pravé plíce s infiltrací mediastina, progrese infiltrace pediklu Th9 s jeho destrukcí a s infiltrací páteřního kanálu. Progrese měkkotkáňové složky při postižení 4. a 10. žebra vpravo, nově okrajově zachycena infiltrace lopaty kosti kyčelní vlevo.
Vzhledem k morfologii nádoru a k přetrvávajícímu PS 1 byl do 2. linie léčby zvolen nintedanib v kombinaci s docetaxelem, v rámci specifického léčebného programu. Léčba byla zahájena 21. srpna 2014 v dávce 400 mg nintedanibu denně podávané 2.–22. den cyklu v kombinaci s docetaxelem každé tři týdny. Po zahájení terapie došlo k ústupu prominující metastázy čelní kosti, po dvou cyklech léčby byl nález na skiagramu hrudníku stacionární. Z nežádoucích účinků byla zaznamenána anémie stupně 2, hepatotoxicita stupně 1, gastrointestinální toxicita (nauzea a zvracení) stupně 1. Ihned po zahájení léčby udávala pacientka průjem, který ustoupil při krátkodobém podávání loperamidu. Průběh léčby komplikoval soor, který bylo nutno léčit flukonazolem, a rozvoj hypokalcemie, přetrvávající i přes substituční léčbu. Kvůli hypokalcemii byla přerušena léčba denosumabem.
Podezření na další progresi onemocnění potvrdilo CT hrudníku provedené 7. listopadu 2014. Léčba nintedanibem byla po třech cyklech ukončena. V dalším průběhu došlo k hospitalizaci na chirurgické klinice pro enteroragii a 13. listopadu 2014 podstoupila pacientka z vitální indikace operaci krvácejícího duodenálního vředu. Po překladu z chirurgie na pneumoonkologické oddělení neumožňoval stav pacientky jinou než symptomatickou léčbu (PS 3−4). Exitus letalis za známek terminální progrese nádorového plicního onemocnění nastal v listopadu 2014.
Kazuistika 2
Muž, v době diagnózy 74 let, kuřák − od mládí kolem deseti cigaret za den. Dlouhodobě se léčil s ischemickou chorobou srdeční, s arteriální hypertenzí, hyperlipidemií a s glaukomem. Lékaře navštívil začátkem května 2014 kvůli bolestem zad, na provedeném skiagramu páteře byla náhodně zjištěna infiltrace horního laloku pravé plíce, poté byl odeslán k další diagnostice a léčbě na naše pracoviště. Kromě bolesti zad trpěl pacient chrapotem.
Na CT hrudníku byl popsán periferní tumor pravé plíce s metastatickým postižením plic a mediastinálních uzlin, s destrukcí těla druhého hrudního obratle a s intraspinální propagací. Bronchoskopie přinesla nález mírné cirkulární stenózy hlavního bronchu vpravo, vyklenutí na laterální stěně hlavního bronchu vpravo a stenózu horního bronchu vpravo jak tlakem, tak infiltrací. Zároveň byla konstatována paréza pravé hlasivky, vysvětlující dysfonii (obr. 2).
Dne 26. května 2014 byla
histologicky potvrzena diagnóza nízce diferencovaného, primárně
plicního adenokarcinomu, následná molekulárně genetická
analýza nepotvrdila přítomnost aktivační mutace v genu pro
EGFR či přestavbu v genu pro ALK. Staging byl T4N2M1b,
klinické stadium IV, PS 1.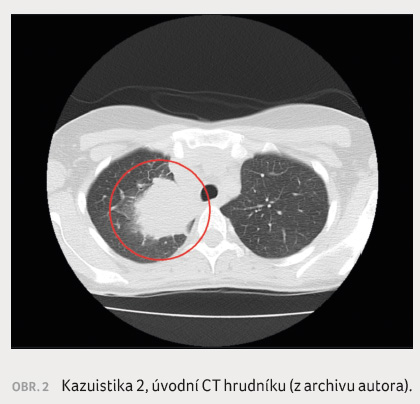
Bylo zahájeno sycení kyselinou listovou a 12. června 2014 byl započat I. cyklus 1. linie paliativní chemoterapie ve složení pemetrexed a cisplatina. Na restage CT hrudníku po II. cyklu chemoterapie byla popsána stabilizace onemocnění. Nejvýraznějšími nežádoucími účinky léčby byly anémie stupně 3, s nutností substituční léčby, a febrilní neutropenie stupně 4, s rozvojem pneumonie v terénu nádorem postižené plíce. Restaging po IV. cyklu 1. linie chemoterapie prokázal progresi onemocnění − progrese velikosti centrální části tumoru pravé plíce, progrese karcinomatózní lymfangiopatie, stacionární mediastinální lymfadenopatie, stacionární metastatický rozsev do obou plic, lytický proces Th2 beze změny.
Vzhledem k dobrému celkovému stavu (PS 1) byla 7. října 2014 zahájena 2. linie léčby ve složení nintedanib a docetaxel, v rámci specifického léčebného programu. Dle kontrolního CT hrudníku po III. cyklu léčby došlo k regresi velikosti centrální části tumoru, karcinomatózní lymfangiopatie a oboustranného metastatického plicního postižení, beze změny zůstaly mediastinální lymfadenopatie a lytický proces Th2. Pacient absolvoval celkem šest cyklů této terapie, nejhorším nežádoucím účinkem léčby byla neutropenie stupně 4, v menší míře se vyskytovaly i nevolnosti a zvracení. Progrese onemocnění byla konstatována v březnu 2015.
Přetrvávající PS 1 umožnilo nasazení erlotinibu do 3. linie léčby. Terapie erlotinibem probíhala pouze měsíc, než došlo k dalšímu zhoršení stavu (PS 3) vlivem progrese nádorového onemocnění. Exitus letalis nastal v červnu 2015.
Závěr
Prognóza obou pacientů byla od počátku velmi nepříznivá, odpověď nádorového onemocnění na jakoukoliv podávanou léčbu nebyla valná a nežádoucí účinky byly nezanedbatelné. Není vyloučen podíl samotné léčby nintedanibem na rozvoji gastrointestinální perforace v prvním případě. V obou kazuistikách došlo při léčbě nintedanibem k částečné odpovědi, která ale netrvala dlouho – v prvním případě byly podány tři a ve druhém šest cyklů léčby s nintedanibem, než byla konstatována opětovná progrese onemocnění. Nintedanib byl v roce 2014 podáván oběma pacientům v rámci specifického léčebného programu, k 30. 6. 2018 neměl v ČR stanovenu úhradu ze zdravotního pojištění. Dle aktuálního Souhrnu údajů o přípravku je nintedanib v kombinaci s docetaxelem indikován k léčbě dospělých pacientů s lokálně pokročilým metastazujícím nebo lokálně rekurentním NSCLC, histologicky prokázaným adenokarcinomem, po chemoterapii první linie [4].
Seznam použité literatury
- [1] Dušek L, Mužík J, Kubásek M, et al. Epidemiologie zhoubných nádorů v České republice [online]. Masarykova univerzita, [2005]. Dostupné na: http://www.svod.cz. Verze 7.0 [2007], ISSN 1802–8861, navštíveno 8. 6. 2018.
- [2] Dušek L, Májek O, Krejčí D, et al. Epidemiologie zhoubných nádorů plic, průdušnice a průdušek v ČR. In: Skřičková J, a kol. Základy moderní pneumoonkologie, 2. vydání. Praha: Maxdorf, 2017; 20−47.
- [3] Hilberg F, Roth GJ, Krssak M, et al. BIBF 1120: Triple angiokinase inhibitor with sustained receptor blockade and good antitumor efficacy. Cancer Research [online] 2008, 68: 4774−4782. Dostupné na: http://cancerres.aacrjournals.org/content/68/12/4774
- [4] Souhrn údajů o přípravku Vargatef. Dostupné na: http://www.sukl.cz/, navštíveno 8. 6. 2018.
- [5] Reck M, Kaiser R, Mellemgaard A, et al. Docetaxel plus nintedanib versus docetaxel plus placebo in patients with previously treated non‑small‑cell lung cancer (LUME‑Lung 1). Lancet Oncology [online]. 2014, 15: 143−155. Dostupné na: https://www.thelancet.com/journals/lanonc/article/PIIS1470‑2045(13)70586‑2/fulltext