Omalizumab – nová možnost léčby chronické spontánní kopřivky, naše zkušenosti
Souhrn:
Nečas M. Omalizumab – nová možnost léčby chronické spontánní kopřivky, naše zkušenosti. Remedia 2019; 29: 496–500.
Chronická spontánní kopřivka je poměrně časté dermatologické onemocnění, které významným způsobem snižuje kvalitu života pacientů. V poslední době je pro tyto pacienty k dispozici nová léčebná metoda v podobě monoklonální protilátky proti molekule imunoglobulinu E – omalizumab. Autor popisuje vlastní zkušenosti s léčbou omalizumabem u souboru 17 pacientů s chronickou spontánní kopřivkou. V tomto souboru je nápadná současná přítomnost onemocnění štítné žlázy a atopie. Efekt léčby omalizumabem je hodnocen jako velmi dobrý, po ukončení léčby však dochází většinou k relapsu onemocnění. Odpověď na léčbu omalizumabem, její stupeň, rychlost i délka remise je přitom dle poznatků autora zcela individuální a nezávislá na závažnosti, délce trvání či předchozí léčbě kopřivky, stejně tak na komorbiditách, věku či na jakýchkoliv jiných faktorech. Na základě zjištěných poznatků by autor uvítal větší flexibilitu stávajících úhradových kritérií ve smyslu možnosti individualizace dávky, intervalu podávání i délky léčby omalizumabem.
Summary:
Necas M. Omalizumab – new option in the treatment of chronic spontaneous urticaria from our perspective. Remedia 2019; 29: 496–500.
Chronic spontaneous urticaria is a relatively common dermatological condition that significantly reduces the quality of life of patients. Recently, a new treatment method has been available for these patients in the form of a monoclonal antibody against the IgE molecule – omalizumab. The author describes his own experience with omalizumab treatment in a group of 17 patients with chronic spontaneous urticaria. The presence of thyroid disease and atopy has been significant in this group. The effect of treatment with omalizumab is assessed as very good, even if after discontinuation, the disease usually relapses. The response to omalizumab treatment, its degree, rate and duration of remission is, according to the author's knowledge, completely individual and independent of the severity, duration or previous treatment of urticaria, as well as of comorbidities, age or any other factors. Based on the findings, the author would welcome greater flexibility in the existing reimbursement criteria in terms of dose individualization, administration interval and duration of omalizumab treatment.
Key words: chronic spontaneous urticaria, treatment, omalizumab.
Úvod
Kopřivka je polyetiologické onemocnění charakterizované tvorbou kopřivkových pupenů neboli pomfů (otok horního koria), angioedému (rozsáhlejší a hlubší otok měkkých tkání) nebo obojího [1]. Typické je často silné svědění a prchavost pomfů, které odeznívají většinou v řádu hodin, či dokonce minut, nikdy nepřetrvávají déle než 24 hodin, zatímco angioedém ustupuje v řádu dnů (zhruba do 3 dnů) [2]. Pomfy se mohou s angioedémem i kombinovat (asi v 30−60 % případů). Kopřivka je onemocnění velmi časté – řadí se mezi 20 nejčastějších dermatóz [2]. Jedná se o onemocnění zprostředkované především žírnými buňkami. Jejich aktivace může nastat imunologickými či neimunologickými mechanismy [2]. Z imunologických mechanismů je to nejčastěji klasická reakce časného neboli I. typu dle Coombse a Gella, dále se může jednat o imunokomplexovou reakci (III. typ dle Coombse a Gella) nebo o aktivaci komplementu, případně o autoimunitní, resp. autoreaktivní mechanismy, které budou diskutovány níže. Z neimunologických mechanismů mohou kopřivku vyvolat tzv. histaminoliberátory (např. opiáty, některá analgetika či kontrastní látky), blokátory cyklooxygenázy (např. kyselina acetylsalicylová, některá nesteroidní antiflogistika či aditiva), mediátory obsažené v potravinách (histamin, tyramin, serotonin) nebo i fyzikální faktory (teplo, chlad, tlak, vibrace apod.) [2].
Při
aktivaci mastocytů dochází k jejich tzv. degranulaci, kdy se
z cytoplazmatických granul mastocytů uvolní preformované –
tzv. primární – mediátory, jako je histamin, heparin či
proteázy (chymáza, tryptáza nebo karboxypeptidáza). Sekundární
mediátory se potom tvoří z fosfolipidů membrán aktivovaných
buněk (prostaglandiny, leukotrieny nebo faktor aktivující krevní
destičky). Terciární mediátory mastocytů vznikají následně de
novo
proteosyntézou a zahrnují chemotaxiny, cytokiny a adhezní
molekuly [2]. To vše vede k vazodilataci a následné
extravazaci plazmy do okolí cév za vzniku otoku horní
škáry, který je podkladem pomfu. Podráždění senzorických
nervů je potom zodpovědné za doprovodné svědění.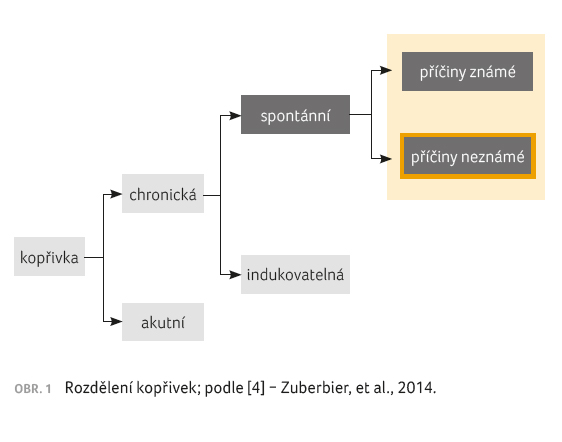
Kopřivka, která přetrvává déle než šest týdnů, je považována za chronickou na základě pozorování, že akutní výsevy kopřivky mají tendenci ustupovat během 1–3 týdnů [3]. Akutní kopřivka je obvykle způsobena exogenní identifikovatelnou noxou, jako jsou potraviny nebo léky, případně může být spojena s virovým infektem, což je častým případem u dětí [3]. U chronických kopřivek bývá naopak exogenní příčina vzácná [3]. Chronické kopřivky můžeme podle nových doporučení Evropské akademie pro alergologii a klinickou imunologii, Globální evropské sítě pro alergie a astma a Světové organizace pro alergii (EAACI/GA2LEN/EDF/WAO) rozdělit do dvou velkých skupin, a to na kopřivky indukovatelné a spontánní – viz obrázek 1 [4]. Indukovatelné kopřivky bývají vyvolány nějakým přesně definovaným zevním faktorem, který často pacient sám zná a již ví, že expozice tomuto faktoru u něj vyvolá výsev kopřivky. Do této kategorie patří tzv. fyzikální kopřivky, např. solární, chladová, tepelná či tlaková či tzv. urticaria factitia nebo také kontaktní kopřivky, a dále cholinergní a aquagenní kopřivka [5−7]. Druhou hlavní kategorií je chronická spontánní kopřivka (chronic spontaneous urticaria, CSU).
Chronická spontánní kopřivka a její
léčba
Chronická spontánní kopřivka postihuje celosvětově asi 0,5−1 % dospělé populace, u dětí je vzácná [8]. Vyskytuje se častěji u žen než u mužů, a to nejčastěji mezi čtvrtou a pátou dekádou života [8]. Uvádí se, že většina případů CSU ustoupí během 1−5 let, nicméně v 10−20 % případů může přetrvávat i více než 10 let. To značně omezuje každodenní aktivity, a to jak pracovní, tak volnočasové, ovlivňuje výběr oblečení, sociální kontakty a celkově snižuje pacientovo sebevědomí, což může vést až k depresivním projevům [9]. Kvalita života pacientů s CSU tedy bývá značně snížená [9,10]. Až 45 % CSU má autoimunitní, resp. autoreaktivní podklad. Bylo zjištěno, že u části pacientů (asi 35−40 %) dochází k tvorbě protilátek typu IgG proti receptoru pro imunoglobulin E (Fc epsilon RI) nebo přímo proti molekule IgE (asi 5−10 % pacientů s CSU), což vede k aktivaci a degranulaci mastocytů. Nově se pro tento typ kopřivky používá termín autoreaktivní [8]. Menší část pacientů s CSU tvoří protilátky typu IgE proti různým vlastním strukturám jako např. proti tyreoidální peroxidáze, dvojšroubovici DNA a zřejmě i proti dalším autoantigenům – tomuto podtypu CSU říkáme autoimunitní [8].
Co
se týče vyšetřovacích postupů u CSU, v nejnovějších
doporučeních je vidět značná tendence omezit rozsáhlá
laboratorní vyšetření – u CSU je doporučeno
vyšetřovat  pouze krevní obraz s diferenciálem, zánětlivé
markery (sedimentace nebo C-reaktivní protein) a případně
vynechat suspektní léky či potraviny [1]. Další vyšetření
jsou dle těchto doporučení indikována pouze v případě
anamnestického či klinického suspicia [1]. Na naší klinice
však používáme spíše rozšířený diagnostický postup, který
zahrnuje i vyloučení skryté (tzv. fokální) infekce, infekce
Helicobacter
pylori,
parazitóz, virových hepatitid, dále vyloučení tyreopatie,
autoimunitního onemocnění, případně také základní
onkologický screening apod., viz tabulku 1.
Existuje také nespecifický screeningový test s autologním
sérem (autologous serum skin test, ASST), jenž bývá pozitivní
u pacientů s autoreaktivním typem CSU, kteří mají
v séru protilátky proti vysoce afinitnímu receptoru FceRI
nebo proti molekule IgE [11]. Test s autologním sérem se
provádí tak, že se do volární
plochy předloktí aplikuje 50 µl autologního séra. Odečítá
se za 15 a 30 minut a test je pozitivní, pokud se
vytvoří v místě aplikace pomfus, který je o více než
2 mm větší než negativní kontrola (pomfus vyvolaný
aplikací fyziologického roztoku). Na našem
pracovišti prozatím tento test neprovádíme.
pouze krevní obraz s diferenciálem, zánětlivé
markery (sedimentace nebo C-reaktivní protein) a případně
vynechat suspektní léky či potraviny [1]. Další vyšetření
jsou dle těchto doporučení indikována pouze v případě
anamnestického či klinického suspicia [1]. Na naší klinice
však používáme spíše rozšířený diagnostický postup, který
zahrnuje i vyloučení skryté (tzv. fokální) infekce, infekce
Helicobacter
pylori,
parazitóz, virových hepatitid, dále vyloučení tyreopatie,
autoimunitního onemocnění, případně také základní
onkologický screening apod., viz tabulku 1.
Existuje také nespecifický screeningový test s autologním
sérem (autologous serum skin test, ASST), jenž bývá pozitivní
u pacientů s autoreaktivním typem CSU, kteří mají
v séru protilátky proti vysoce afinitnímu receptoru FceRI
nebo proti molekule IgE [11]. Test s autologním sérem se
provádí tak, že se do volární
plochy předloktí aplikuje 50 µl autologního séra. Odečítá
se za 15 a 30 minut a test je pozitivní, pokud se
vytvoří v místě aplikace pomfus, který je o více než
2 mm větší než negativní kontrola (pomfus vyvolaný
aplikací fyziologického roztoku). Na našem
pracovišti prozatím tento test neprovádíme.
Ke sledování
aktivity, resp. závažnosti kopřivky doporučují
EAACI/GA2LEN/EDF/WAO používat průměrné
sedmidenní skóre aktivity kopřivky (tzv. UAS 7 skóre, tab. 2)
[1]. To spočívá v každodenním hodnocení dvou hlavních
symptomů kopřivky, což je výsev kopřivkových pomfů a svědění,
a to na škále od 0 do 3 pro každý
ze symptomů. Součet za jeden den proto může být
maximálně 2 × 3 = 6 a za celý týden
6 × 7 = 42 bodů, což je maximální týdenní
aktivita kopřivky. Pokud je UAS 7 skóre 0, je pacient zhojen, bez
kopřivky; jako stabilizovaná kopřivka se hodnotí pacienti se
skóre v rozmezí 1−6; skóre 7−15 představuje kopřivku
mírnou; skóre 16−28 kopřivku středně závažnou a konečně
UAS 7 > 28 značí kopřivku závažnou [12].
Co se týče léčby CSU, antihistaminika stále zůstávají jejím základním kamenem a přibližně polovina pacientů s CSU zareaguje na tuto léčbu dostatečně [13]. Navíc antihistaminika druhé generace mají výrazně méně nežádoucích účinků, jako je sedace či suchost sliznic, ve srovnání s první generací antihistaminik. Pokud však efekt antihistaminik není dostatečný, je vhodné dle nejnovějších doporučení odborných společností (EAACI/GA2LEN/EDF/WAO) po dvou týdnech léčby navýšit dávku antihistaminik druhé generace na dvojnásobek až čtyřnásobek standardní dávky [1]. Pokud ani to nevede do čtyř týdnů ke kýženému snížení aktivity onemocnění, doporučuje se jako třetí linie léčby zahájení biologické terapie omalizumabem [1]. Případná terapie cyklosporinem byla odsunuta v nejnovějších doporučeních až do čtvrté linie léčby [1]. Je sice relativně účinná, ale z dlouhodobého hlediska s sebou nese celou řadu potenciálních nežádoucích účinků [14]. Z nových doporučení byla zcela vyřazena terapie antagonisty leukotrienů pro jejich malou účinnost v léčbě CSU [1].
Je také dobré mít na paměti, že systémové kortikoidy dle nejnovějších doporučení EAACI/GA2LEN/EDF/WAO mají být použity v případě nutnosti pouze krátkodobě (po dobu do jednoho týdne), a to ke zvládnutí akutní exacerbace CSU, což se však v praxi neděje, a stále ještě vidíme pacienty s CSU léčené systémovými kortikoidy po řadu měsíců, někdy i let!
Je samozřejmě i řada dalších možností, jak léčit pacienta s refrakterní CSU – hydroxychlorochin, dapson, metotrexát, sulfasalazin, tricyklická antidepresiva, kromoglykát sodný, plazmaferéza, léčba intravenózními imunoglobuliny či fototerapie a další. Všechny tyto léčebné modality však nemají dostatečné opodstatnění z hlediska medicíny založené na důkazech, tedy dostatek kvalitních studií, které by prokázaly jejich účinnost [8]. Naopak na základě řady studií, z nichž stěžejními byly zejména ASTERIA I a II a GLACIAL, i poznatků z klinické praxe je zřejmé, že prozatím nejúčinnějším lékem s nejlepším bezpečnostním profilem pro terapii CSU je omalizumab (Xolair®) [15,16].
Omalizumab v léčbě chronické
spontánní kopřivky
Omalizumab
je humanizovaná monoklonální protilátka proti molekule IgE [17].
Z 95 % je tvořena lidským imunoglobulinem IgG1
a z 5 % myší anti IgE komponentou – viz
obrázek 2.
Omalizumab se selektivně váže na cirkulující protilátky
typu IgE v krvi pomocí interakce s Cε3
regionem molekuly IgE, přičemž se vytvářejí malé biologicky
inertní komplexy, které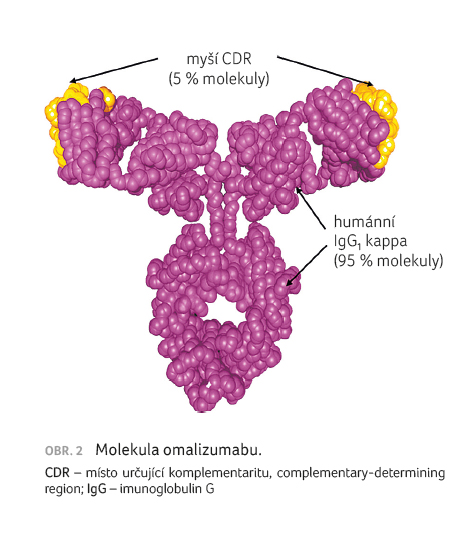 neaktivují komplement. Omalizumab se
neváže na IgE, který je již navázán na vysokoafinitní
receptor pro IgE (FceRI) mastocytů, bazofilů a dendritických
buněk [17].
Hlavní mechanismus účinku omalizumabu spočívá v tom, že
blokuje vazbu IgE na uvedené efektorové buňky. Vazbou na IgE
také nepřímo snižuje množství volných alergenů a zřejmě
také autoalergenů, jako je tyreoidální peroxidáza
či dvojšroubovice DNA [18].
To může být příčinou rychlé odpovědi na omalizumab
u části pacientů, a to v řádu hodin až dnů.
Po aplikaci omalizumabu totiž dochází velmi rychle ke snížení
koncentrace volného IgE až o 99 % s maximem
neutralizace přibližně za tři dny po podání léku.
Přesný mechanismus účinku u autoreaktivního subtypu CSU
není jasný, ale předpokládá se, že snížení koncentrace volně
cirkulujícího IgE vede ke snížení hustoty receptorů pro
IgE (FceRI) na povrchu mastocytů a bazofilů (tzv.
downregulace), na které se potom nemohou navázat autoreaktivní
IgG protilátky [18].
Tato downregulace nastává v řádu dnů až týdnů. Proto
část pacientů odpovídá na léčbu omalizumabem pomaleji
[18].
neaktivují komplement. Omalizumab se
neváže na IgE, který je již navázán na vysokoafinitní
receptor pro IgE (FceRI) mastocytů, bazofilů a dendritických
buněk [17].
Hlavní mechanismus účinku omalizumabu spočívá v tom, že
blokuje vazbu IgE na uvedené efektorové buňky. Vazbou na IgE
také nepřímo snižuje množství volných alergenů a zřejmě
také autoalergenů, jako je tyreoidální peroxidáza
či dvojšroubovice DNA [18].
To může být příčinou rychlé odpovědi na omalizumab
u části pacientů, a to v řádu hodin až dnů.
Po aplikaci omalizumabu totiž dochází velmi rychle ke snížení
koncentrace volného IgE až o 99 % s maximem
neutralizace přibližně za tři dny po podání léku.
Přesný mechanismus účinku u autoreaktivního subtypu CSU
není jasný, ale předpokládá se, že snížení koncentrace volně
cirkulujícího IgE vede ke snížení hustoty receptorů pro
IgE (FceRI) na povrchu mastocytů a bazofilů (tzv.
downregulace), na které se potom nemohou navázat autoreaktivní
IgG protilátky [18].
Tato downregulace nastává v řádu dnů až týdnů. Proto
část pacientů odpovídá na léčbu omalizumabem pomaleji
[18].
Mezi nejčastější nežádoucí účinky omalizumabu patří reakce v místě aplikace injekce (bolestivost, zduření, zarudnutí a svědění), bolesti hlavy, méně často bývá popisována faryngitida, synkopy, parestezie, závratě, somnolence, posturální hypotenze, zarudnutí kůže, alergický bronchospasmus, kašel, dyspepsie, průjem, nauzea, zvýšená citlivost na světlo, kopřivka, vyrážka, svědění, onemocnění podobné chřipce, otoky paží, zvýšení hmotnosti či zvýšená únava. Vzácně může dojít v průběhu léčby k parazitární infekci, poruchám imunitního systému, rozvoji anafylaktické reakce (v literatuře se nejčastěji uvádí výskyt do 0,2 %), jiných vážných alergických stavů včetně otoku laryngu či angioedému [17].
Omalizumab byl původně určen k léčbě pacientů s těžkým perzistujícím astmatem, nicméně v roce 2014 byla schválena jeho nová indikace, a to právě léčba chronické spontánní kopřivky. Podmínky úhrady omalizumabu ze zdravotního pojištění byly stanoveny v roce 2015. Podle poslední úpravy těchto podmínek z 1. 6. 2018 je omalizumab indikován jako přídatná terapie k léčbě CSU u dospělých a dospívajících pacientů (ve věku 12 let a více), kteří splňují jedno ze dvou uvedených kritérií:
- a) nedostatečná odpověď (UAS 7 ≥ 28 nebo UAS 7 ≥ 16, pokud je zároveň přítomen angioedém) po předchozí šestitýdenní léčbě H1 antihistaminiky, při které byl minimálně po dobu dvou týdnů podáván minimálně dvojnásobek obvyklé dávky H1 antihistaminik v monoterapii nebo byla podávána kombinace H1 antihistaminik v dávkách, jejichž součet odpovídá minimálně dvojnásobku obvykle podávané dávky H1 antihistaminik, nebo
- b) nedostatečná odpověď (UAS 7 ≥ 28 nebo UAS 7 ≥ 16, pokud je zároveň přítomen angioedém) po předchozí čtyřtýdenní léčbě H1 antihistaminiky ve standardních dávkách v případě, že z důvodů toxicity, intolerance nebo kontraindikací nelze použít zvýšenou dávku H1 antihistaminik [19].
Omalizumab je podáván v dávce 300 mg subkutánně, a to ve čtyřtýdenních intervalech. Jeden léčebný cyklus zahrnuje šest aplikací omalizumabu, poté se léčba ukončuje. Ukončit léčbu je také zapotřebí, pokud klesne UAS 7 skóre před podáním 4., 5., 6. dávky na hodnotu 0 (pacient je tedy zcela zhojen), nebo pokud naopak nedojde ve 12. týdnu ke snížení UAS 7 skóre o více než 11 bodů (u pacientů se středně těžkou CSU a angioedémem je kromě toho zapotřebí léčbu také ukončit, pokud u nich UAS neklesne na hodnotu 10 a méně). Nový cyklus léčby omalizumabem lze potom znovu zahájit, pokud dojde k relapsu onemocnění, pacient splňuje kritéria uvedená výše a v minulém cyklu odpověděl dobře na léčbu, a navíc absolvoval všech šest aplikací omalizumabu [19].
Náš soubor pacientů léčených
omalizumabem
Léčbu pacientů s CSU omalizumabem jsme na našem pracovišti zahájili přibližně v polovině roku 2015 a do současné doby jsme Xolairem léčili či léčíme celkem 17 pacientů. Zajímavé je to, že ve všech případech se jedná o ženy, prozatím na našem pracovišti nebyl omalizumabem léčen ani jeden muž. Průměrný věk pacientek byl 43 let. Na naše pracoviště byly odeslány převážně terénními dermatology (8 pacientek), případně alergologem (5 pacientek), ve dvou případech odeslal pacientku praktický lékař a ve dvou případech se pacientka na naše pracoviště dostavila sama. Délka trvání kopřivky ke dni prvního vyšetření na naší klinice byla u jednotlivých pacientek značně rozdílná a pohybovala se v širokém rozmezí od tří měsíců do 15 let (průměrně to bylo 40 měsíců, tedy asi 3 a čtvrt roku). Současný výskyt angioedému udávalo 12 pacientek (z toho velmi často – alespoň jednou týdně – 2 pacientky, občasný výskyt – alespoň jednou do měsíce – 6 pacientek a ojedinělý výskyt angioedému udávaly 4 pacientky).
Spouštěči výsevů kopřivky byly u našich pacientek nejčastěji infekty (např. streptokokové – angíny, v jednom případě kolpitida, dále faryngitidy, běžné infekty horních cest dýchacích, ve třech případech to byla infekce Helicobacter pylori a v jednom případě zánět středního ucha). Čtyři pacientky udávaly jako spouštěče výsevů kopřivky stresové situace, u dvou pacientek bylo spouštěčem nepravidelné užívání nesteroidních antiflogistik. Z asociovaných onemocnění bylo u sedmi pacientek přítomno onemocnění štítné žlázy (41,2 % souboru), u pěti pacientek to byla polinóza (29,4 %), čtyři pacientky měly alergické astma (23,5 %), tři pacientky atopický či dyshidrotický ekzém (17,6 %), u dvou pacientek bylo současně vitiligo, u dvou chronická gastritida a jedna pacientka se současně léčila s revmatoidní artritidou.
Z patologických laboratorních výsledků jsme se nejčastěji u našich pacientek setkali s elevací hodnot celkového IgE (8 pacientek, tedy 47 % souboru), dále s pozitivitou protilátek proti štítné žláze, resp. proti tyreoidální peroxidáze (7 pacientek, tedy 41,2 % souboru), pozitivitu antinukleárních protilátek (ANA) jsme zjistili u čtyř našich pacientek (23,5 % souboru). Všech 17 pacientek bylo před zahájením léčby omalizumabem léčeno nejrůznějšími antihistaminiky, a to finálně i ve 2−4násobně vyšších dávkách oproti standardním, což je i podmínkou k zahájení biologické léčby. Systémovými kortikoidy bylo v různé fázi kopřivky léčeno 15 pacientek, tedy převážná část našeho souboru. Většinou se jednalo o léčbu nárazovou, ale několik pacientek bylo kortikoidy léčeno i dlouhodobě, a jedna pacientka dokonce několik let. Jedna pacientka byla v předchorobí léčena antagonisty leukotrienů, jedna podstoupila léčbu cyklosporinem A a jedna terapii metotrexátem.
Naše zkušenosti s léčbou
omalizumabem
Co
se týče léčebné odpovědi, na terapii omalizumabem
jednoznačně příznivě zareagovalo 12 ze 16 pacientek (75 %
souboru), viz graf 1.
U poslední, sedmnácté pacientky teprve probíhá první
cyklus léčby, proto je zatím předčasné hodnotit její efekt.
U zbylých čtyř pacientek nebyl efekt léčby přesvědčivý.
U jedné pacientky bylo příznivého efektu dosaženo až při
léčbě vyšší dávkou omalizumabu a při zkráceném
intervalu aplikací (450 mg každé 3 týdny). U druhé
pacientky došlo v průběhu léčby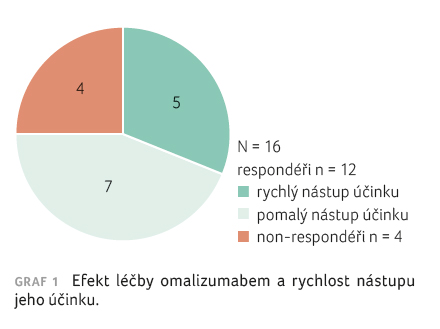 omalizumabem dokonce
ke zhoršení kopřivky, což však bylo možné přičíst
akutnímu zubnímu zánětu. Po jeho přeléčení se však již
pacientka k další léčbě omalizumabem nedostavila. U třetí
pacientky sice nedošlo po ukončení terapeutického cyklu
k poklesu skóre UAS o více než 11 bodů, ale s odstupem
zhruba jednoho měsíce po ukončení léčby kopřivka téměř
zcela ustoupila. U čtvrté pacientky nedošlo po třetí
aplikaci omalizumabu k dostatečnému zmírnění kopřivky,
navýšení dávky pacientka odmítla, proto byla léčba
omalizumabem ukončena.
omalizumabem dokonce
ke zhoršení kopřivky, což však bylo možné přičíst
akutnímu zubnímu zánětu. Po jeho přeléčení se však již
pacientka k další léčbě omalizumabem nedostavila. U třetí
pacientky sice nedošlo po ukončení terapeutického cyklu
k poklesu skóre UAS o více než 11 bodů, ale s odstupem
zhruba jednoho měsíce po ukončení léčby kopřivka téměř
zcela ustoupila. U čtvrté pacientky nedošlo po třetí
aplikaci omalizumabu k dostatečnému zmírnění kopřivky,
navýšení dávky pacientka odmítla, proto byla léčba
omalizumabem ukončena.
U šesti
pacientek, které příznivě zareagovaly na léčbu, byl stupeň
léčebné odpovědi při ukončení prvního léčebného cyklu
vynikající − skóre UAS 0, tedy plná remise kopřivky,
u dvou pacientek byl efekt léčby dobrý – skóre UAS
kleslo pod hodnotu 6 (stabilizovaná CSU) – a u čtyř
pacientek byl efekt léčby ještě uspokojivý − skóre
UAS pokleslo na hodnotu < 15, což je mírná
aktivita kopřivky, viz graf 2.
Pokud bylo nutné léčebné cykly opakovat, stupeň léčebné
odpovědi v následujících cyklech byl vždy u dané
pacientky podobný, pouze u jedné pacientky jsme pozorovali
mírný pokles léčebné odpovědi při opakovaných cyklech léčby
omalizumabem.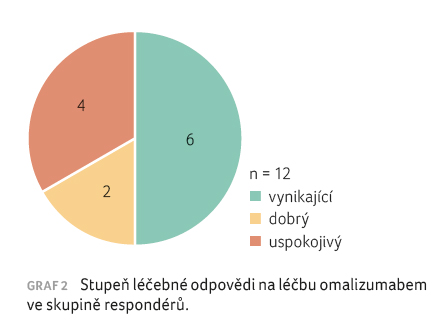
Ve skupině 12 pacientek, které příznivě zareagovaly na léčbu omalizumabem, byla zajímavá rychlost odpovědi na léčbu: u pěti pacientek byla reakce rychlá – došlo k poklesu skóre UAS na 0 (tedy k úplnému vymizení kopřivky), a to nejpozději po třetí dávce omalizumabu, což vedlo k ukončení terapeutického cyklu. U sedmi pacientek byla reakce pomalejší a musely absolvovat všech šest dávek v rámci léčebného cyklu – viz graf 1. Ze skupiny 12 pacientek, respondérů, došlo pouze u dvou k remisi (1× úplná, 1× částečná remise po prvním cyklu omalizumabu), ve zbylých 10 případech bylo nutné léčit naše pacientky opakovanými cykly biologické léčby. Jedna z pacientek recentně zahájila již devátý cyklus biologické léčby omalizumabem. Jedná se o pacientku, která vždy velmi rychle zareaguje na léčbu. Terapie se proto vždy po třetí aplikaci ukončuje, ale do dvou měsíců dojde k relapsu kopřivky, což si vyžádá zahájení nového léčebného cyklu. U této pacientky by jistě byla přínosná dlouhodobá léčba, případně i v delším intervalu aplikací – např. po osmi týdnech, což však stávající úhradová kritéria neumožňují. Délka remise byla u našich pacientek velmi individuální, ale vždy přibližně stejná, pouze u jedné pacientky se doba remise postupně prodlužovala (po prvním cyklu byla 1 měsíc, po druhém cyklu 5 měsíců a po třetím cyklu trvá dosud – nyní je to asi 2 roky). U zbylých pacientek se délka remise pohybovala od dvou týdnů do tří měsíců, s průměrem kolem šesti týdnů.
Co se týče nežádoucích účinků u našich pacientek, vyskytovaly se zcela sporadicky a byly vesměs zcela nezávažné. Tři pacientky udávaly občasné bolesti hlavy, jedna pacientka měla přechodně reakci v místě vpichu omalizumabu, jedna pacientka opakovaný výsev herpes labialis, kterým trpěla již před zahájením léčby omalizumabem, a jedna pacientka si stěžovala na nárůst hmotnosti v průběhu léčby omalizumabem.
Závěr
Omalizumab představuje u pacientů trpících chronickou spontánní kopřivkou novou účinnou možnost léčby, která může řadě nemocných výrazně zlepšit kvalitu života včetně možnosti ukončit často dlouhodobou léčbu systémovými kortikoidy. Z naší zkušenosti mohu potvrdit, že u řady pacientek, které byly kopřivkou sužovány až stigmatizovány, a to často po řadu let, znamenala léčba omalizumabem doslova zlom v jejich životě, samozřejmě v pozitivním slova smyslu. Reakce na léčbu omalizumabem je značně individuální a nezaznamenali jsme jakoukoliv souvislost se závažností a délkou trvání kopřivky, s přidruženými onemocněními, věkem pacientek či s dalšími faktory. Nedá se tedy zřejmě vůbec predikovat, jaká bude léčebná odpověď u konkrétního pacienta.
Velká většina našich pacientek zareagovala na léčbu omalizumabem velmi dobře (v našem souboru 75 % pacientek), ale zaznamenali jsme i několik případů, kdy reakce na léčbu nebyla dostatečná. V takových případech je dobré zaměřit se na to, zda není přítomen ještě nějaký jiný faktor, který udržuje aktivitu kopřivky (např. skrytý zánět v těle, reakce na různé potravinové doplňky, které pacient ani nepovažuje za důležité, apod.). Pokud je toto vyloučeno, za pokus stojí navýšení dávky omalizumabu či zkrácení intervalu jeho podávání, což se vyplatilo u jedné z našich pacientek. Problémem ovšem potom může být úhrada příslušnou pojišťovnou, je zde nutný souhlas revizního lékaře. U převážné většiny našich pacientů (83,3 % pacientů souboru) však došlo po ukončení léčby omalizumabem k relapsu kopřivky, což vede k nutnosti opakování léčebných cyklů. Problémem je opět to, že dle stávajících úhradových kritérií je nutno vyčkat relapsu až do závažnosti splňující tato kritéria, což samozřejmě zhoršuje kvalitu života pacienta. Řešením by byla opět úprava úhradové vyhlášky ve smyslu možnosti kontinuální, nebo alespoň dlouhodobější léčby u pacientů s opakovanými relapsy kopřivky po ukončení terapie omalizumabem.
Seznam použité literatury
- [1] Zuberbier T, Aberer W, Asero R, et al. The EAACI/GA2LEN/EDF/WAO guideline for the definition, classification, diagnosis and management of urticaria. Allergy 2018; 73: 1393–1414.
- [2] Viktorinová M. Kopřivka a angioedém. Praha: Galén 2001.
- [3] Bernstein JA, Lang DM, Khan DA, et al. The diagnosis and management of acute and chronic urticaria: 2014 update. J Allergy Clin Immunol 2014; 133: 1270–1277.
- [4] Zuberbier T, Aberer W, Asero R, et al. The EAACI/GA(2) LEN/EDF/WAO Guideline for the definition, classification, diagnosis, and management of urticaria: the 2013 revision and update. Allergy 2014; 69: 868−887.
- [5] Sussman G, Hebert J, Gulliver W, et al. Insights and advances in chronic urticaria: a Canadian perspective. Allergy Asthma Clin Immunol 2015; 11: 7.
- [6] Abajian M, Mlynek A, Maurer M. Physical urticaria. Curr Allergy Asthma Rep 2012; 12: 281–287.
- [7] Trevisonno J, Balram B, Netchiporouk E, et al. Physical urticaria review on classification, triggers and management with special focus on prevalence including a meta‑analysis. Postgrad Med 2015; 127: 565–570.
- [8] Kaplan AP. Diagnosis, pathogenesis, and treatment of chronic spontaneous urticaria. Allergy Asthma Proc 2018; 39: 184−190.
- [9] Kang MJ, Kim HS, Kim HO, et al. The impact of chronic idiopathic urticaria on quality of life in korean patients. Ann Dermatol 2009; 21: 226−229.
- [10] Baiardini I, Giardini A, Pasquali M, et al. Quality of life and patients’ satisfaction in chronic urticaria and respiratory allergy. Allergy 2003; 58: 621–623.
- [11] Konstantinou GN, Asero R, Maurer M, et al. EAACI/GA(2)LEN task force consensus report: the autologous serum skin test in urticaria. Allergy 2009; 64: 1256−1268.
- [12] Hawe E, Stull DE, McBride D, et al. Estimating Utility Data for Patient Symptom Severity in Chronic Spontaneous Urticaria. Value Health 2014; 17: A610−A611.
- [13] Bousquet J, Anto JM, Demoly P, et al. WHO Collaborating Center for Asthmaand Rhinitis. Severe chronic allergic (and related) diseases: a uniform approach‑a MeDALL‑GA2LEN‑ARIA position paper. Int Arch Allergy Immunol 2012; 158: 216–231.
- [14] Guaragna MA, Albanesi M, Stefani S, et al. Chronic urticaria with high IgE levels: first results on oral cyclosporine A treatment. Clin Ter 2013; 164: 115–118.
- [15] Maurer M, Rosén K, Hsieh HJ, et al., Omalizumab for the treatment of chronic idiopathic or spontaneous urticaria. N Engl J Med 2013; 368: 924−935.
- [16] Kaplan A, Ledford D, Ashby M, et al., Omalizumab in patients with symptomatic chronic idiopathic/spontaneous urticaria despite standard combination therapy. J Allergy Clin Immunol 2013; 132: 101−109.
- [17] Souhrn údajů o přípravku Xolair 150 mg injekční roztok, datum poslední revize 31. 5. 2018. Dostupné na www.sukl.cz
- [18] Chang TW, Chen C, Lin CJ, et al. The potential pharmacologic mechanisms of omalizumab in patients with chronic spontaneous urticaria. J Allergy Clin Immunol 2015; 135: 337−342.
- [19] Indikační omezení úhrady Xolairu. Dostupné na: http://www.sukl.cz/modules/medication/detail.php?code=0149028&tab=prices