Onemocnění štítné žlázy – zkušenosti z praxe
Souhrn:
Onemocnění štítné žlázy je časté a postihuje především ženy. Mimo plně rozvinuté formy porušené funkce je nutné věnovat pozornost i formám subklinickým. Od roku 1984, kdy byla zavedena dostatečně citlivá metoda stanovení hodnoty thyreostimulačního hormonu (TSH) schopná rozeznat rozdíl mezi normální a nízkou koncentrací, stala se diagnostika thyreoidálních onemocnění snadným lékařským postupem. U osob s hyperfunkcí je koncentrace TSH téměř nedekovatelná a u osob s hypothyreózou je zvýšená. Variace v prevalenci funkčních thyreoidálních chorob lze vysvětlit především rozdílností toho, co se považuje za normální rozmezí pro TSH i pro periferní hormony (thyroxin a trijodthyronin). Ve skupině osob se zvýšeným rizikem (tj. u žen, u osob s pozitivní rodinnou anamnézou autoimunitních a/nebo thyreoidálních onemocnění) dosahuje prevalence chorob štítné žlázy nejméně 10 %. Na několika případech demonstrujeme nezbytnost spolupráce mezi endokrinology a ostatními specialisty – kardiology, osteology, onkology. Zvláštní pozornost je nutné věnovat pacientům čekajícím na transplantaci orgánu a osobám léčeným monoklonálními protilátkami.
Key words: thyroid diseases – TSH – FT4 – monoclonal antibodies – oncological therapy – organ transplantation.
Summary:
Thyroid diseases are frequent, more frequent in women than in men. Besides overt forms of thyroid dysfunction, it is important to pay attention to subclinical forms as well. Since the introduction of assays for serum thyrotropin (TSH) that are sensitive enough to distinguish between normal and low thyrotropin concentrations in 1984, the diagnosis of thyroid dysfunction has become an easy medical process. TSH levels are usually almost undetectable in patients with hyperthyroidism and elevated in those with hypothyroidism. The variation in prevalence of thyroid dysfunction can be explained largely by differences in what is considered a normal range for TSH and for peripheral hormones, i.e. thyroxine and triiodothyronine. In groups of patients at higher risk (i.e. women, people with family history of autoimmune and/or thyroid disease), the prevalence of thyroid disease is at least 10%. We use several case studies to demonstrate necessity of cooperation between the endocrinologist and other specialists – cardiologist, osteologists, oncologists. Special attention is required in patients waiting for transplantation or those treated by monoclonal antibodies.
Onemocnění štítné žlázy (ŠŽ) se v současné době vyskytuje v populaci často, častěji u žen než u mužů. Onemocnění můžeme posuzovat s hlediska velikosti – struma je charakterizována jako zvětšení přesahující 18 ml u žen a 22 ml u mužů, přestavba může být benigní či maligní. Struma je v mladší populaci vzácná, ale nacházíme ji ještě u osob narozených před zahájením jodace jedlé soli v roce 1950. Přestože je karcinom štítné žlázy vzácný, je uzlům ve ŠŽ nadále nutné věnovat pozornost. Dalším hlediskem je posouzení onemocnění dle funkce – podstatně častější je výskyt hypothyreózy (hypofunkce) než hyperthyreózy (hyperfunkce). Vedle plně rozvinutých forem onemocnění, které se manifestují klinickými příznaky, nesmíme opomíjet ani formy subklinické, jejichž diagnóza je založena především na laboratorním nálezu. V rizikových skupinách, tj. především v ženské populaci, u osob s autoimunitními chorobami a u těch, kteří mají v blízkém příbuzenstvu určité typy thyreoidálních chorob [1], se prevalence thyreopatií odhaduje až na 10 % i více [2,3].
Dnes je nejčastějším onemocněním ŠŽ autoimunitní postižení – chronická lymfocytární thyreoiditida (CLT), jejím důsledkem je obvykle hypothyreóza. Léčba hypothyreózy podáváním levothyroxinu je zavedena téměř sto let, je snadná a při dodržení základních pravidel zajištujících správnou absorpci léku i radostná [4]. Někteří jedinci jsou dlouhodobě eufunkční, nicméně porucha funkce může být vyvolána iatrogenně léky (zvýšenou náloží jodu, podáním cytokinů a/nebo některých monoklonálních protilátek, určitými léky – například amiodaronem) nebo nezvyklou zátěží organismu včetně gravidity [5,6].
Základní diagnostika poruchy funkce ŠŽ zahrnuje vyšetření hodnot thyreostimulačního hormonu (TSH) a thyroxinu (T4), výhodnější je stanovit jeho volnou frakci (FT4). Diagnózu CLT opíráme o vyšetření protilátek proti thyreoidální peroxidáze (TPOab) a proti thyreoglobulinu (Tgab) a/nebo o vyšetření ŠŽ ultrazvukem. Zda je v terénu CLT častější výskyt karcinomu ŠŽ, je dlouhodobě diskutováno [7] a jednoznačné důkazy chybějí, další zvažovanou příčinou vzniku karcinomu je dědičnost.
Thyreoidální hormony zasahují do činnosti řady orgánů, proto diagnostika i léčba thyreopatií vyžaduje mnohdy mezioborovou spolupráci, především kardiologů, gastroenterologů, gynekologů (časná diagnostika a léčba těhotných s thyreopatiemi), s rychlým rozvojem oborů se do popředí dostává transplantologie a onkologie.
Choroby ŠŽ jsou dobře léčitelné: podávání levothyroxinu u osob se sníženou funkcí ŠŽ je výborně tolerováno, je však nutné zajistit správné vstřebání léku. Substituční léčba bývá většinou celoživotní s nutností dodržet aplikaci lege artis, u složitějších případů je nezbytné, aby kontroly prováděl endokrinolog, v jednodušších případech a u stabilizovaných osob může v tomto bodě endokrinologa nahradit praktický lékař [8].
Hyperfunkce ŠŽ je podstatně méně častá, léčba bývá časově omezená, protože při její neúspěšnosti či při relapsu onemocnění je indikováno definitivní řešení, tj. odstranění štítné žlázy chirurgicky nebo radiojodem. Tento postup má pochopitelně za následek hypothyreózu.
V následujících kasuistikách předkládáme tři skupinky případů, vždy dvojici z nich spojuje společná problematika.
V kasuistikách první skupiny (1a a 1b) upozorňujeme na nutnost důsledného dodržování běžného požadavku, kterým je dlouhodobé sledování osob nejen s hypothyreózou, ale i s prodělanou atakou thyreotoxikózy. V kasuistikách druhé skupiny (2a a 2b) se věnujeme diagnostice a léčbě solitárních uzlů ve štítné žláze, rychlé diagnostice pomocí aspirační biopsie tenkou jehlou (fine needle aspiration biopsy, FNAB), cytologickou diagnózu lze stanovit během 12 hodin. Třetí dvojice kasuistik (3a a 3b) se hraničně týká onkologie, a to podávání monoklonálních protilátek (v našem případě pembrolizumabu), které může u disponovaných jedinců vyvolat destrukční thyreoiditidu s následnou těžkou hypothyreózou. Léčbu nemusíme přerušit, ale je nutné zahájit adekvátní substituční léčbu, jak uvádí Souhrn údajů o přípravku [9]. Poslední kasuistika (4) dokumentuje provázanost medicínských oborů i neetičnost dlouhodobého neřešení thyreotoxikózy u polymorbidní pacientky s polyautoimunitním syndromem [6]. Vybrané normy laboratorních ukazatelů jsou přehledně uvedeny na konci článku. Pro hodnoty FT4 jsou uvedeny dvě normy, které se liší podle výrobce diagnostické soupravy, a jsou tudíž v těsné spojitosti s časem vyšetření.
Kasuistika 1
1a) Muž, V. R., 60 let. Ve 35 letech podstoupil odstranění ŠŽ pro objemnou strumu a po léta byla následná hypothyreóza výborně substituována stabilní dávkou levothyroxinu, pacient byl bez obtíží. Při jedné z pravidelných kontrol byl laboratorní nález TSH překvapivý – elevace hodnot TSH na 20,4 mIU/l a FT4 na 10,5 pmol/l. Pacient přiznal mírnou únavu, přičítal ji stárnutí. Léčbu dodržoval přesně, dávku neměnil, užíval nalačno, respektoval naše doporučení 30 minut po podání přípravku nejíst. Další medikaci (antihypertenzivum) užíval až po snídani. Na poslední můj již zoufalý dotaz, čím užívaný přípravek zapíjí, se rozjasnil: na doporučení kamaráda sportovce začal levothyroxin zapíjet effervescentním magnesiem. Po návratu k tradiční čisté vodě se laboratorní nález normalizoval a jeho „únava“ se vrátila do normy.
Poselství: Levothyroxin je nutné užívat lege artis – nalačno, odděleně od ostatních léků, nejméně 30 minut po požití přípravku nejíst ani nebrat další medikaci, zapít čistou vodou.
1b) Muž, K. F., 66 let. Zdráv, pouze Gilbertova choroba, od svých 51 let do 53 let byl léčen thyreostatiky pro Gravesovu–Basedowovu chorobu s lehčí endokrinní oftalmopatií. Po dvou letech bylo možno léčbu ukončit, pacient byl bez obtíží a kontroly potvrzovaly eufunkci štítné žlázy. Ve věku 61 let se o dovolené koupal v Mrtvém moři, asi za pět týdnů se objevily palpitace, tachykardie, svalová slabost, pocit písku v očích, zvýšené pocení, úbytek hmotnosti. Dostavil se ke kontrole, relaps thyreotoxikózy byl zřejmý, patrně se jednalo o tzv. jodbasedow na podkladě zvýšeného přísunu jodu v Mrtvém moři. Po zklidnění thyreostatiky jsme indikovali definitivní řešení – léčbu radiojodem. Následná hypothyreóza je kompenzována substitucí levothyroxinem a pacient se opět cítí zdráv.
Poselství: I po ukončené léčbě pro Gravesovu–Basedowovu chorobu jsou kontroly v rámci dispenzarizace nutné, relaps vzniká i po letech remise. Příčinou relapsu může být interkurentní choroba, stres, ale i nadměrný příjem jodu (léky, lázně, pobyt u moře s vysokou koncentrací jodu). Definitivní řešení je při relapsu thyreotoxikózy indikováno.
Kasuistika 2
2a) Žena, Z. K., 34 let. Ve 28 letech byla pacientka doporučena k endokrinologickému vyšetření pro hmatnou rezistenci o velikosti 14 mm × 20 mm v levém laloku ŠŽ. Pacientka o rezistenci nevěděla, je zcela bez obtíží. Matka je po operaci ŠŽ pro papilární karcinom. Pacientka trpí od mládí obezitou, má deficit laktázy, mimo častější katary horních cest dýchacích je bez obtíží. Dva roky před naším vyšetřením porodila zdravé dítě. Na krku je přítomna spíše nenápadná tužší rezistence velikosti 15 mm × 20 mm s hladkým povrchem, která je vůči spodině pohyblivá, uzliny nejsou zvětšené, klinicky i laboratorně je eufunkční. Laboratorní nález podporuje diagnózu CLT a tomu také odpovídají laboratorní hodnoty – FT4 13,6 pmol/l, TSH 3,408 mIU/l, Tgab 134 IU/l, TPOab 3 214,0 IU/l – a ultrazvukové vyšetření ŠŽ – štítná žláza je nehomogenní, echogenita je středně snížená, perfuze je snížená, pohyblivost je zachována. Pravý lalok má velikost 19 mm × 18 mm × 54 mm,tj. 9 ml, levý lalok 21 mm × 22 mm × 51 mm, tj. 11,5 ml. V levém laloku je ventrokraniálně uložený solidní uzel o velikosti 13 mm × 13 mm × 18 mm, hypoechogenní, s normální vaskularizací, neostře ohraničený. Uzliny nejsou zvětšené. Výsledek FNAB s ohledem na přítomnost intranukleárních pseudoinkluzí koincidujících v zánětlivém terénu zněl: suspekce z malignity v terénu chronické thyreoiditidy s klasifikací Bethesda V. Pacientka byla indikována k totální thyreoidektomii a histologické vyšetření potvrdilo diagnózu papilokarcinomu v levém laloku ŠŽ, v terénu Hashimotovy thyreoiditidy, s rozsáhlými úseky onkocytární transformace. Následovala léčba radiojodem, supresní léčba levothyroxinem. Za tři roky po léčbě pacientka otěhotněla a porodila zdravého chlapce.
Poselství: Každé rezistenci ve ŠŽ má být věnována pozornost, především při nálezu protilátek TPOab nebo Tgab a zvláště u osob s pozitivní rodinnou anamnézou. Dědičnost je uváděna mezi rizikovými faktory vzniku karcinomu ŠŽ.
2b) Žena, M. S., 60 let. Případ této pacientky je zajímavý z několika aspektů: 52letá žena byla připravována k autologní transplantaci kostní dřeně v době medikamentózní remise akutní myeloidní leukemie. Při vyšetření pozitronovou emisní tomografií (PET) se zobrazila aktivní oblast ve ŠŽ, proto byla pacientka urgentně odeslána k endokrinologickému řešení. Zatímco rodinná anamnéza pacientky je bezvýznamná, v osobní anamnéze se vyskytly dvě malignity: v 50 letech prodělala operaci prsu pro duktální karcinom a poté šest cyklů chemoterapie a ozařování, po ukončení léčby se cítila výborně. V 52 letech byla pro celkové zhoršení stavu vyšetřena a byla stanovena diagnóza akutní leukemie. Podstoupila chemoterapii a byla připravována k transplantaci kostní dřeně. O uzlu ve ŠŽ pacientka několik let věděla, ten dosud nebyl podrobněji vyšetřen. Pacientka je v dobrém stavu, na krku je patrná nodozita o velikosti 30 mm × 25 mm, která je proti spodině pohyblivá, uzliny nejsou zvětšené. Vyšetření ukázalo, že funkční ukazatele ŠŽ jsou v normě, protilátky jsou negativní. Na ultrazvuku ŠŽ je v levém laloku popsán oválný solidní hypoechogenní uzel nehomogenní struktury o velikosti 30 mm × 27 mm s lehce nepravidelnou vaskularizací, ohraničený, ostatní tkáň je bez nápadností. Uzel byl sonograficky suspektní. Výsledky vyšetření FNAB nesvědčí jednoznačně pro malignitu, nález je hraniční (Bethesda III). Následně jsme indikovali totální thyreoidektomii a histologie svědčila pro adenom z onkocytárních buněk bez prorůstání do pouzdra. Pooperační hypothyreóza byla okamžitě substituována. Za měsíc po operaci ŠŽ proběhla po přípravě imunosupresivy úspěšná transplantace kostní dřeně. Pacientka je nyní osm let po operaci ve výborném stavu a obě malignity (karcinom prsu i hematologická) jsou v remisi. Trvá dispenzarizace na endokrinologii nejen pro kontrolu thyreoidální substituce, ale i vzhledem k nejistému biologickému charakteru onkocytárních adenomů.
Poselství: Při vyšetření PET se nevzácně zobrazuje ŠŽ, mimo metastázy do ŠŽ se zobrazují primární karcinomy ŠŽ, některé adenomy a velmi často i CLT (Hashimotova thyreoiditida). Včasné vyšetření endokrinologem je vždy
namístě.
Kasuistika 3
3a) Žena, K. O., 37 let. Až na zjištěný deficit laktázy byla pacientka do 33 let zdráva. Tehdy prodělala operaci a následnou onkologickou léčbu pro maligní melanom a po dva roky byla léčena interferonem α‑2a (Roferon). V té době byl pacientce přechodně podáván levothyroxin, údajně pro lehčí hypothyreózu. Ve 36 letech absolvovala pro nález metastáz do uzlin a páteře další léčbu (radioterapii a chemoterapii). Ukazatele funkce ŠŽ (TSH a FT4) jsou již dokumentovány a byly v normě. Pět měsíců před naším vyšetřením byla zahájena infuzní terapie pembrolizumabem podávaným jednou za 3 týdny a hodnoty TSH a FT4 byly pravidelně sledovány. Pro 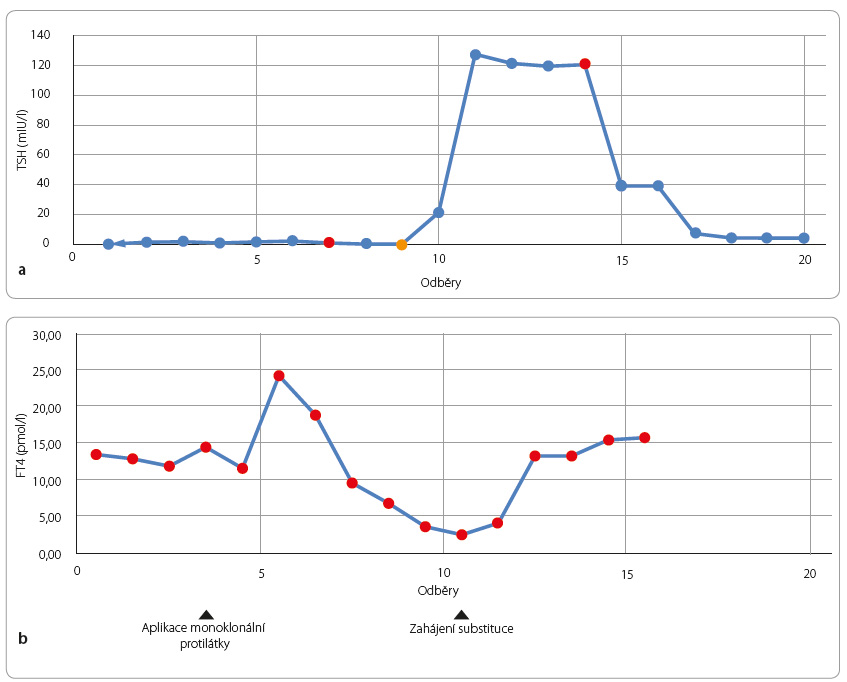 dlouhodobější nález elevace hodnot TSH se jmenovaná posléze dostavila k endokrinologickému vyšetření. Uvádí pouze únavu, ale její stav jí umožňuje nadále zastávat funkci manažerky. Je patrné prosáknutí obličeje, aker, hlas je hrubší, ochlupení řídké, struma není. Prostudováním dokumentace zjišťuji, že za pět týdnů po první aplikaci pembrolizumabu dochází k elevaci hodnot FT4 a k poklesu koncentrace TSH, v dalších týdnech se rozvíjí hypothyreóza s elevací TSH a s poklesem hodnot FT4, viz graf 1a, b. Protilátky TPOab i Tgab jsou trvale negativní. Ultrazvukové vyšetření ŠŽ svědčí pro chronický zánět (ŠŽ je zmenšená, se sníženou echogenitou a nehomogenní strukturou, pravý lalok příčně 8 mm × 7 mm, levý lalok 10 mm × 12 mm s nálezem ohraničeného hypoechogenního uzlu o velikosti 12 mm v pravém laloku). Po zahájení substituce se normalizují laboratorní ukazatele, ustupuje únava, mizejí otoky. V programu je ještě dovyšetření uzlu v pravém laloku ŠŽ pomocí FNAB. Pacientka bude sledována nadále i na endokrinologii.
dlouhodobější nález elevace hodnot TSH se jmenovaná posléze dostavila k endokrinologickému vyšetření. Uvádí pouze únavu, ale její stav jí umožňuje nadále zastávat funkci manažerky. Je patrné prosáknutí obličeje, aker, hlas je hrubší, ochlupení řídké, struma není. Prostudováním dokumentace zjišťuji, že za pět týdnů po první aplikaci pembrolizumabu dochází k elevaci hodnot FT4 a k poklesu koncentrace TSH, v dalších týdnech se rozvíjí hypothyreóza s elevací TSH a s poklesem hodnot FT4, viz graf 1a, b. Protilátky TPOab i Tgab jsou trvale negativní. Ultrazvukové vyšetření ŠŽ svědčí pro chronický zánět (ŠŽ je zmenšená, se sníženou echogenitou a nehomogenní strukturou, pravý lalok příčně 8 mm × 7 mm, levý lalok 10 mm × 12 mm s nálezem ohraničeného hypoechogenního uzlu o velikosti 12 mm v pravém laloku). Po zahájení substituce se normalizují laboratorní ukazatele, ustupuje únava, mizejí otoky. V programu je ještě dovyšetření uzlu v pravém laloku ŠŽ pomocí FNAB. Pacientka bude sledována nadále i na endokrinologii.
Poselství: U osob, které mají v anamnéze léčbu ŠŽ, je rozvoj poruchy funkce ŠŽ při podávání cytokinů nebo monoklonálních protilátek častý. Substituce je při vzniku hypothyreózy, zvláště destrukčního typu, nezbytná. Protilátky TPOab nebo Tgab nemusejí být přítomny. Odhalený uzel ve ŠŽ musí být u onkologického pacienta cytologicky vyšetřen.
3b) Muž, M. M., 44 let. V dětství pacient prodělal mononukleózu a pneumonii, později jen recidivující katary horních cest dýchacích, pro které byl vyšetřen imunologem. Ve 40 letech byl pro mírně zvětšenou ŠŽ doporučen k endokrinologickému vyšetření. Nacházíme mírně zvětšenou ŠŽ s jemně nerovným povrchem a na podkladě laboratorního nálezu (FT4 12,2 pmol/l, TSH 9,718 mIU/l, Tgab 49,2 kIU/l, Tp oab 5 677 kIU/l) a ultrazvukového vyšetření ŠŽ (mírně zvětšené oba laloky: pravý lalok 22 mm × 16 mm × 52 mm, levý 21 mm × 14 mm × 50 mm se sníženou echogenitou, s oboustranně nehomogenní a skvrnitou strukturou a s normální perfuzí) diagnostikujeme lehčí hypothyreózu na podkladě chronické CLT (tab. 1, A: vstupní vyšetření). Po zahájení substituční léčby levothyroxinem 50 μg/den se pacient dostavil na kontrolu pouze jedenkrát. Ve 41 letech prodělal operaci pro malignitu tonsily, pro metastatický rozsev následovalo zevní záření a chemoterapie. Později byly zjištěny i kostní metastázy. Ve 44 letech, šest měsíců před naším vyšetřením, byla zahájena další onkoterapie – v rámci studie mu byly každé tři týdny podávány infuze obsahující monoklonální protilátky (název léku nezná). Pacient údajně užíval levothyroxin a dávku určoval onkolog. Na endokrinologii se dostavil po třech letech od posledního vyšetření (na přímluvu své rodiny) s nálezem TSH 155 mIU/l. Z obtíží uvádí jen únavu, a to pouze krátce po aplikaci infuzí, v mezidobí se cítí celkem dobře. V objektivním nálezu je dobrý kontakt, snížení hodnoty BMI, hrubší hlas. Údajně užívá levothyroxin 100 μg denně. Zopakovali jsme vyšetření protilátek a ultrazvukové vyšetření ŠŽ (tab. 1, A: vstupní vyšetření, B: kontrola).
oab 5 677 kIU/l) a ultrazvukového vyšetření ŠŽ (mírně zvětšené oba laloky: pravý lalok 22 mm × 16 mm × 52 mm, levý 21 mm × 14 mm × 50 mm se sníženou echogenitou, s oboustranně nehomogenní a skvrnitou strukturou a s normální perfuzí) diagnostikujeme lehčí hypothyreózu na podkladě chronické CLT (tab. 1, A: vstupní vyšetření). Po zahájení substituční léčby levothyroxinem 50 μg/den se pacient dostavil na kontrolu pouze jedenkrát. Ve 41 letech prodělal operaci pro malignitu tonsily, pro metastatický rozsev následovalo zevní záření a chemoterapie. Později byly zjištěny i kostní metastázy. Ve 44 letech, šest měsíců před naším vyšetřením, byla zahájena další onkoterapie – v rámci studie mu byly každé tři týdny podávány infuze obsahující monoklonální protilátky (název léku nezná). Pacient údajně užíval levothyroxin a dávku určoval onkolog. Na endokrinologii se dostavil po třech letech od posledního vyšetření (na přímluvu své rodiny) s nálezem TSH 155 mIU/l. Z obtíží uvádí jen únavu, a to pouze krátce po aplikaci infuzí, v mezidobí se cítí celkem dobře. V objektivním nálezu je dobrý kontakt, snížení hodnoty BMI, hrubší hlas. Údajně užívá levothyroxin 100 μg denně. Zopakovali jsme vyšetření protilátek a ultrazvukové vyšetření ŠŽ (tab. 1, A: vstupní vyšetření, B: kontrola).
Po zvýšení substituční dávky na 150 μg denně a po upozornění na nutnost užívání lege artis se laboratorní hodnoty zvolna zlepšují, viz graf 2a, b.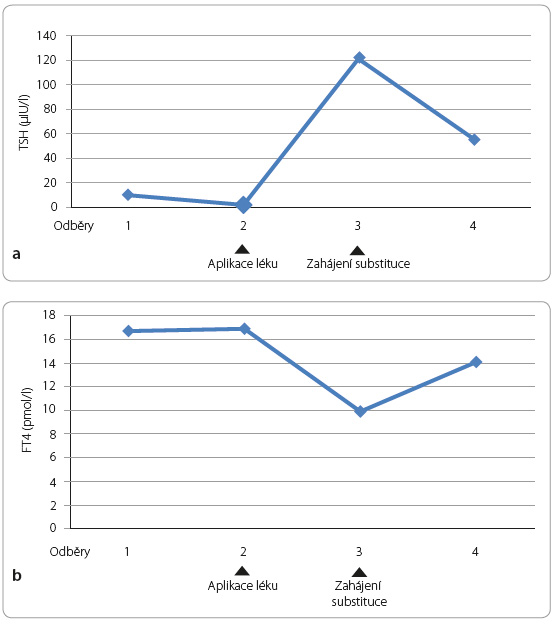
Poselství: U nemocného s již diagnostikovanou hypothyreózou na podkladě CLT s vysokým titrem protilátek je při zahájení onkologické léčby vhodná spolupráce s endokrinologem, prohloubení hypothyreózy lze při podávání monoklonálních protilátek očekávat. Klinické známky i těžké hypothyreózy se nemusejí ihned projevit.
4) Žena, E. K., 56 let. Ke konsiliárnímu vyšetření na endokrinologii byla doporučena pro nález osteoporózy, s žádostí o posouzení vlivu letité a na jiném pracovišti nesystematicky léčené thyreotoxikózy (13 let) na kostní problematiku. Od 25 let je pacientka sledována pro dysrytmie – SV (supraventrikulární) extrasystoly (podáván Rytmonorm), od dětství trpí skoliózou páteře (odmítla operaci), obtíže vertebrogenní etiologie se zhoršují tak, že nyní chodí o francouzských holích a převážně polehává. Od 48 let je pro tuto diagnózu v invalidním důchodu. Trpí astmatem (obvyklá terapie), od 52 let má psoriázu, zhoršují se myalgie, dysrytmie, pro podezření na Sjögrenův syndrom byla vyšetřena na revmatologii, kde bylo vysloveno podezření navíc na myositidu. Pro svalovou hypotrofii a nález osteoporózy na denzitometriii byla konsiliárně odeslána na endokrinologické pracoviště. V rodinné anamnéze nejsou mimo hematologickou malignitu (matka zemřela v 57 letech) závažná onemocnění, pacientka prodělala tři úspěšné gravidity, klimakterium v 54 letech, bez další léčby. Ve 43 letech jí byla diagnostikována thyreotoxikóza a od té doby je trvale léčena thyreostatiky v různých dávkách, je v péči několika specialistů. Stěžuje si především na progredující bolesti páteře a na myalgie. Současná léčba viz výše, navíc Lexaurin 1,5 mg denně a Thyrozol – nyní 10 mg denně, analgetika. V objektivním nálezu: zřetelně depresivní, chůze o francouzských holích, oční příznaky jsou negativní, struma I. st., svaly jsou hypotrofické na horních i dolních končetinách, taburetový příznak pro instabilitu nelze vyšetřit. Laboratorní nálezy potvrzují hyperfunkci ŠŽ na podkladě Gravesovy–Basedowovy choroby: FT4 24,6 pmol/l, TSH 0,008 mIU/l, Tgab 25,0 kIU/l, TPOab 47 kIU/l, TRAK (protilátky proti receptorům TSH) 3,04 IU/l. Klinický obraz je jednoznačný a souhlasný je i nález na ultrazvukovém vyšetření ŠŽ: obraz odpovídá imunogenní thyreopatii – dlouholeté Gravesově–Basedowově chorobě, velikost ŠŽ celkem 19,5 ml. Denzitometrie svědčila pro osteoporózu. Indikovali jsme léčbu radiojodem, do tří měsíců se rozvinula očekávaná hypothyreóza a ta je substituována levothyroxinem. Celkově se zlepšuje psychický i fyzický stav pacientky. Jedna z několika chorob je zvládnuta a je možné se soustředit na řešení dalších chorob, především osteoporózy a vertebrogenních a svalových problémů.
Poselství: Polymorbidní pacientka s polyautoimunitním syndromem (Gravesova–Basedowova thyreotoxikóza, psoriáza, Sjögrenův syndrom, asthma bronchiale) s řadou obtíží (SV tachykardie, myalgie a svalová slabost) byla pro thyreotoxikózu po léta nedostatečně léčena a choroba nebyla řešena. Další choroby – psoriáza, asthma bronchiale – celkový stav zhoršovaly. Po zvládnutí thyreotoxikózy radiojodem je možné se intenzivněji věnovat především osteoporóze, kardiálním a vertebrogenním obtížím, které byly dosud připisovány především thyreotoxikóze.
Závěr
Levothyroxin je jedním z nejčastěji předepisovaných léků, jeho perorální aplikace je snadná, ale k zajištění maximální a standardní absorpce je nezbytné dodržet zásadu podávat přípravek nalačno, odděleně od ostatních léků, zapít čistou vodou a 30 minut nic nejíst. S faktem, že o těchto zásadách nevědí zdravotničtí profesionálové a často na ně zapomínají i pacienti, se setkáváme v praxi často. Navíc jsou známy léky, které absorpci snižují.
Přítomnost protilátek proti ŠŽ (TPOab a/nebo Tgab) je ukazatelem thyreoidální autoimunity. Osoby s průkazem protilátek považujeme za rizikové. Je možný nejen pozdější rozvoj poruchy činnosti ŠŽ, ale v terénu CLT mohou uzly proliferovat. Proto každá rezistence ve ŠŽ má být řádně vyšetřena a sledování rizikových osob zvláště při podávání cytokinů a monoklonálních protilátek je žádoucí. U onkologických nemocných, obdobně jako u osob s perspektivou transplantace orgánů, by při pozitivním zobrazení ŠŽ na PET mělo následovat endokrinologické posouzení. Příčinou může být jak zánět, tak benigní adenom nebo i karcinom ŠŽ.
Malignita ŠŽ je sice vzácná, ale její záchyt v celém světě stoupá. Pro odhalení charakteru uzlu ve ŠŽ je významný nález na ultrazvuku a výsledek cytologického vyšetření z materiálu získaného při FNAB. Díky FNAB lze získat výsledek do 12–24 hodin. Nález malignity ŠŽ je kontraindikací transplantace a vyžaduje rychlé řešení. S ohledem na známý vliv dědičnosti nejen u onemocnění ŠŽ, ale i při postižení diferencovaným karcinomem ŠŽ, a snad i v případě vztahu karcinomu a CLT (Hashimotovy thyreoiditiy), věnujeme rizikovým osobám zvýšenou péči [7]. Karcinom ŠŽ má při včasném záchytu velmi dobrou prognózu. Po příslušné léčbě diferencovaného karcinomu ŠŽ je možná gravidita, pacienti vedou normální život.
Monoklonální protilátky mohou akcentovat již existující CLT a mohou vyvolat destrukční thyreoiditidu. Ta se projeví krátkou fází hyperfunkce s následným přechodem do hluboké hypothyreózy. Po atace destrukční thyreoiditidy nemusejí být protilátky prokazatelné, nacházíme však u nich typický nález na ultrazvukovém snímku ŠŽ. Poruchy funkce ŠŽ vyvolané podáváním monoklonálnch protilátek se mají léčit, jak uvádí výrobce v Souhrnu údajů o přípravku [9] (vyjímám a cituji):
Pembrolizumab je protilátka, která se váže na receptor programované buněčné smrti PD‑1 (programmed cell death‑1) a blokuje jeho interakci s ligandy PD‑L1 a PD‑L2. Receptor PD‑1 je negativním regulátorem aktivity T‑buněk, u kterého bylo prokázáno, že se podílí na regulaci T‑buněčné imunitní odpovědi. Pembrolizumab zesiluje odpověď T‑buněk, včetně protinádorové odpovědi, blokádou vazby receptoru PD‑1 na ligandy PD‑L1 a PD‑L2. Pembrolizumab je spojen s imunitně podmíněnými nežádoucími účinky. Léčba pembrolizumabem musí být trvale ukončena: při toxicitě stupně 4 kromě endokrinopatií, které jsou zvládnuty substitučními léky.
Vzhledem k vlivu hormonů ŠŽ na řadu orgánů je v populaci „sváděno na štítnou žlázu“ všechno špatné. Odlišení kauzální příčiny obtíží při onemocnění ŠŽ od koincidence důsledků více chorob a léčba thyreopatií je podmínkou úspěšné terapie. Na dlouhodobé neřešení choroby doplácí především pacient.
Laboratorní ukazatele funkce ŠŽ a jejich norma hodnot
- Tgab – protilátka proti thyreoglobulinu (< 60 kIU/l)
- TPOab – protilátka proti thyreoidální peroxidáze (< 60 kIU/l
- TRAK – protilátka proti receptoru TSH (< 1,5 IU/l)
- TSH – thyreostimulační hormon (0,500–4,900 mIU/l)
- FT4 – volný thyroxin FT4 (do začátku roku 2015 11,5–22,7 pmol/l, počínaje rokem 2015 10,5–18,5 pmol/l)
Seznam použité literatury
- [1] Boelaert K, Newby PR, Simmonds MJ, et al. Prevalence and relative risk of other autoimmune diseases in subjects with autoimmune thyroid disease. Am J Med 2010; 123: 183.
- [2] Hollowell JG, Staehling NW, Flanders WD, et al. Serum TSH, T(4), and thyroid antibodies in the United States population (1988 to 1994): National Health and Nutrition Examination Survey (NHANES III). J Clin Endocrinol Metab 2002; 87: 489–499.
- [3] Jonklaas J, Bianco AC, Bauer AJ, et al. American Thyroid Association Task Force on Thyroid Hormone Replacement. Guidelines for the treatment of hypothyroidism: prepared by the American Thyroid Association Task Force on Thyroid Hormone Replacement. Thyroid 2014; 24: 1670–1751.
- [4] Burman KD. Factors affecting thyroid hormone gastrointestinal absorption. Thyroid International 2000; 5: 3–11.
- [5] Tajtáková M. Lieky a štítna žlaza. Vnitř Lék 2012; 58: 140–144.
- [6] Benvenga S. When thyroid hormone replacement is ineffective? Curr Opin Endocrinol Diabetes Obes 2013; 20: 467–477.
- [7] Azizi G, Keller J, Lewis M. Association of Hashimotoś thyroiditis with thyroid cancer. Endocr Relat Cancer 2014; 21: 845–852.
- [8] Límanová Z, Jiskra J, Moravčíková D, Karen I. Diagnostika a léčba tyreopatií. Centrum doporučených postupů pro praktické lékaře CDPP 2015.
- [9] Souhrn údajů o přípravku Keytruda, dostupné na www.ema.europa.eu (ze dne 15. 7. 2015)