Siponimod v léčbě pacientů se sekundárně progresivní roztroušenou sklerózou: studie EXPAND a její analýzy
Sekundárně progresivní fáze představuje fenotyp roztroušené sklerózy, který se objevuje u velké části pacientů s relabující‑remitující roztroušenou sklerózou. Během 15−20 let k němu dospěje více než 50 % nemocných. Disabilita pacientů při sekundárně progresivní roztroušené skleróze (SP-RS) kontinuálně progreduje, relapsy jsou méně frekventní nebo nejsou přítomny. Pro SP-RS byly léčebné možnosti doposud velmi omezené.
Siponimod je selektivní modulátor sfingosin 1 fosfátových receptorů S1P1 a S1P5. Působí jako jejich funkční antagonista a brání vycestování periferních lymfocytů z mízních uzlin a jejich recirkulaci do centrální nervové soustavy (CNS). Siponimod přestupuje hematoencefalickou bariéru a preklinické studie naznačují, že účinkuje i v prevenci synaptické neurodegenerace a podporuje remyelinizaci v CNS [1,2].
Klinická studie fáze III EXPAND (NCT01665144), která probíhala v 31 zemích světa, si dala za cíl zhodnotit účinnost a bezpečnost podávání siponimodu u pacientů se SP-RS [3].
Metodika
Toto dvojitě zaslepené klinické
hodnocení typu event driven/exposure driven kontrolované
placebem randomizovalo celkem 1 651 pacientů v poměru 2 : 1
(1 105 do větve se siponimodem, 546 do větve
s placebem). Zařazeni byli pacienti ve věku 18−60 let
se SP-RS a se skóre hodnotícím disabilitu (Expanded
Disability Status Scale, EDSS) v rozmezí 3,0−6,5. Vstupní
charakteristiky pacientů byly obdobné (tab. 1).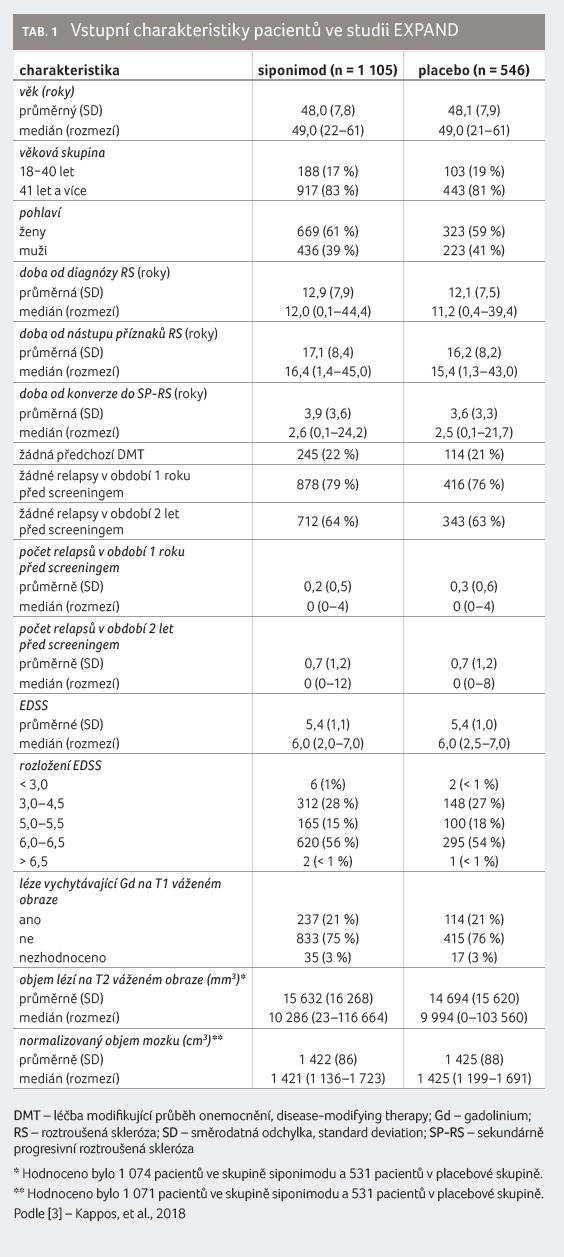
Pacientům byl podáván buď siponimod v dávce 2 mg denně, nebo placebo. Ve dnech 1−6 byla dávka studijní medikace postupně titrována od počátečních 0,25 mg po udržovací dávku 2 mg.
Primárním cílovým ukazatelem studie byla doba do tříměsíční potvrzené progrese disability (confirmed disability progression, CDP). Ta byla definována jako vzestup EDSS alespoň o 1 při počáteční hodnotě v rozmezí 3,0−5,0 nebo o 0,5 při počátečním skóre EDSS 5,5−6,5. Dále byly sledovány doba do tříměsíčního potvrzení alespoň 20% zhoršení T25WT (Timed 25 foot Walk Test), změna v objemu T2 lézí, doba do šestiměsíční CDP, roční počet relapsů (annualized relapse rate, ARR), doba do prvního relapsu, podíl pacientů bez relapsu, počet nových a zvětšujících se T2 lézí, počet T1 lézí vychytávajících gadolinium a změna objemu mozku. Předmětem hodnocení byl rovněž bezpečnostní profil siponimodu.
Výsledky
Medián expozice studijní medikaci byl
18 měsíců (0−37 měsíců). Studii dokončilo 80 % (1 327
z 1 651) pacientů. Tříměsíční CDP dosáhlo 26 % (288
z 1 096) pacientů, kteří dostávali siponimod, a 32 %
(173 z 545) pacientů z placebové skupiny; léčba
siponimodem tak vedla k 21% relativnímu snížení rizika
(poměr rizik [HR] 0,79; 95% interval spolehlivosti [CI]: 0,65−0,95;
p = 0,013),
graf 1A, B.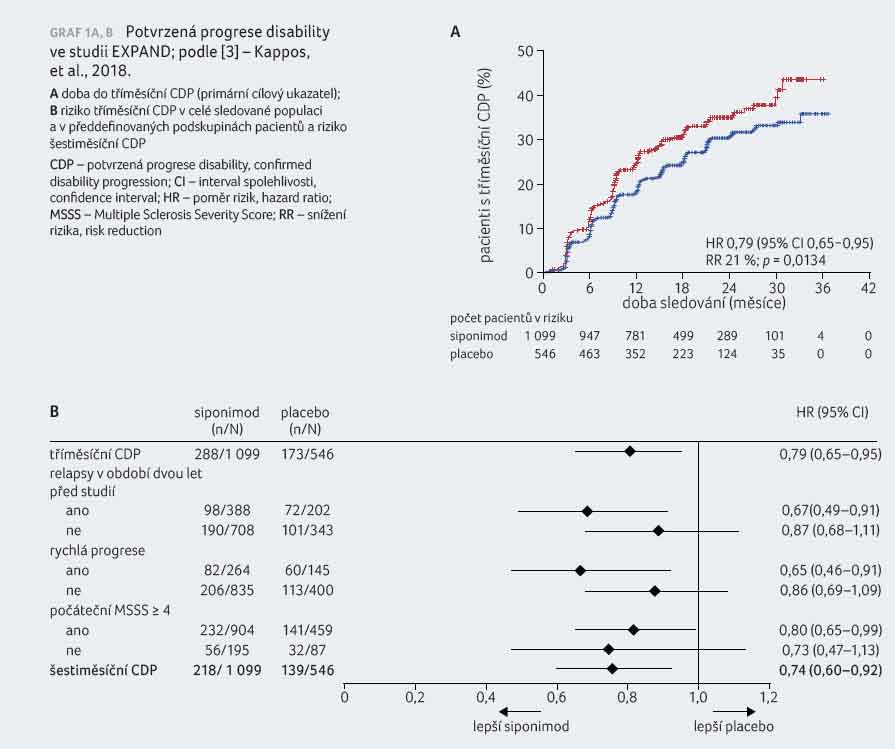
Siponimod redukoval riziko šestiměsíční CDP o 26 % (HR 0,74: CI 0,60–0,92, p = 0,058), ARR o 55 % (rate ratio 0,45; 95% CI 0,34−0,59, p < 0,0001) i riziko výskytu prvního relapsu o 46 % (HR 0,54; 95% CI 0,41−0,70, p < 0,0001). Ve skupině se siponimodem byl zaznamenán nižší nárůst objemu T2 lézí (−695,3 mm3 mezi skupinami, p < 0,0001), nižší procentuální pokles objemu mozku (o 15 %, p = 0,0002), vyšší podíl pacientů bez lézí vychytávajících gadolinium (89 % vs. 67 %) a bez nových nebo se zvětšujících T2 lézí (57 % vs. 37 %). Výrazný efekt na T25WT nebyl doložen, důvodem může být i nižší citlivost měření změny v populaci pacientů, z nichž většina je odkázána na nějakou pomůcku pro chůzi.
Nejčastěji hlášenými nežádoucími účinky (uváděny u více než 10 % pacientů) byly bolest hlavy, nazofaryngitida, infekce močových cest a pády. Hypertenze byla zaznamenána celkem u 115 pacientů (10 %), kteří dostávali siponimod, a u 41 (8 %) pacientů z placebové skupiny. Mezi závažné nežádoucími účinky, které byly dokumentovány u nejméně 0,5 % pacientů v obou skupinách, patřily zvýšení aktivity jaterních aminotransferáz, bazaliom, otřes mozku, deprese, infekce močových cest, pokus o sebevraždu, poruchy chůze, relaps roztroušené sklerózy a paraparéza.
Hlavní dvojitě zaslepená fáze hodnocení byla uzavřena po výskytu 374 událostí a poté, co alespoň 95 % pacientů bylo ve skupinách zařazeno minimálně po dobu 12 měsíců. Studie nicméně pokračuje dál v podobě otevřené extenze, jejímž záměrem je poskytnout data o účinnosti a bezpečnosti dlouhodobé léčby.
Další analýzy
Na posledním kongresu ECTRIMS, který se konal 11.−13. září 2019 ve švédském Stockholmu, byly v posterové sekci prezentovány další výsledky a post hoc analýzy populace pacientů zařazených do studie EXPAND.
Douglas L. Arnold a kol. [4]
prezentovali rozbor kombinovaného souboru dat (pooled MRI dataset)
studie EXPAND, který dokládá zpomalení progrese atrofie mozku,
šedé kůry mozkové i thalamu při léčbě siponimodem oproti
placebu (graf 2−4A, B).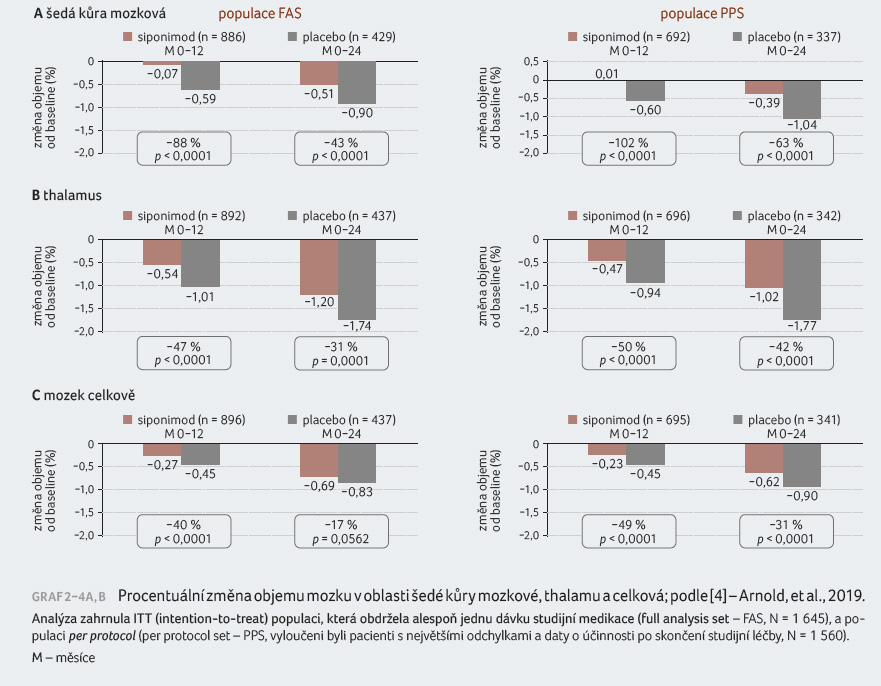
Další analýza Douglase L. Arnolda se spolupracovníky [5] hodnotila možnou asociaci mezi počáteční hodnotou objemu mozkové tkáně a dobou do šestiměsíční CDP nebo mírou zhoršení kognitivních funkcí. Ukázalo se, že atrofie mozkové kůry má prediktivní hodnotu pro dobu do šestiměsíční CDP dle EDSS i pro klinické zhoršení kognice (měřeno pomocí Symbol Digit Modalities Test, SDMT). Celkový objem mozku a objem thalamické oblasti byl asociován pouze se změnou kognitivních procesů, nikoliv se zhoršením EDSS. Ukazuje se tak, že patologické mechanismy progrese disability se u pacientů se SP-RS mohou lišit od nemocných v relabující remitující fázi onemocnění.
Další post hoc analýza studie EXPAND, kterou prezentoval R. Gold se spolupracovníky [6], si dala za cíl sledovat účinnost siponimodu u podskupiny pacientů s aktivní SP-RS. Ukázalo se, že siponimod redukoval progresi disability napříč spektrem pacientů se SP-RS, nicméně ve skupině nemocných s aktivním onemocněním byl efekt ještě výraznější. Snížení rizika tříměsíční CDP činilo 31 %, pro šestiměsíční CDP riziko pokleslo o 37 % oproti placebu.
Gary Cutter prezentoval analýzu dat studie EXPAND [7], která ukazuje na možné klinické využití různých podškál definujících disabilitu. Efekt léčby siponimodem byl hodnocen pomocí dalších dvou podškál EDSS (Motor Integration Subscale − MIS, Collateral Subscale − CS). Účinnost siponimodu na stupnici MIS se výrazněji projevila u pacientů s relapsy a lézemi vychytávajícími gadolinium než bez nich a projevila se dříve než na stupnici CS. Efekt na škále CS byl výraznější u nemocných, kteří měli léze vychytávající gadolinium v počátku sledování.
Závěry další post hoc analýzy [8] ukazují, že siponimod oddaluje dobu, kdy je pacient zcela odkázán na invalidní vozík. Za předpokladu stabilní účinnnosti v čase prodloužil siponimod v porovnání s placebem střední čas do hodnoty EDSS ≥ 7 o 4,3 roku v celkové populaci (12,0 let vs. 16,3 roku).
Shrnutí
Na kongresu ECTRIMS byla prezentována rovněž nová studie, která zatím přijímá pacienty ke sledování [9]. EXCHANGE (NCT03623243) je prospektivní studie, jejímž cílem je hodnotit bezpečnost a snášenlivost siponimodu při okamžité konverzi z léčby modifikující průběh onemocnění u pacientů s pokročilou relabující roztroušenou sklerózou.
Siponimod představuje první chorobu modifikující léčivo, které u pacientů se SP-RS signifikantně redukuje progresi disability, pokles kognitivních funkcí a ztrátu objemu mozku. Další klinická hodnocení poskytnou data pro jeho zařazení do palety používaných léčiv.
Redakčně zpracovala PharmDr. Kateřina Viktorová
Komentář: Siponimod v léčbě pacientů se sekundárně progresivní roztroušenou sklerózou (studie EXPAND a její analýzy)
MUDr. Veronika Tichá, Ph.D.
Neurologická klinika a Centrum klinických neurověd 1. LF UK a VFN, Praha
Studie EXPAND je první randomizovanou dvojitě zaslepenou studií, která prokázala účinnost léku v sekundárně progresivní fázi roztroušené sklerózy (SP RS). V minulosti byly provedeny takové studie např. s natalizumabem (ASCEND) nebo s interferonem beta, obě ale s negativním výsledkem.
Pacienti ve studii EXPAND představovali typickou populaci sekundárně progresivních pacientů, ve velké míře byli zahrnuti nemocní i v pokročilé fázi SP RS. U více než 50 % pacientů ve větvi s aktivní léčbou i v placebové větvi byla míra postižení posuzovaná pomocí stupnice EDSS (Expanded Disability Status Scale) v rozmezí hodnot 6,0−6,5, u malé části pacientů byla nemoc hodnocena jako aktivní; léze vychytávající gadolinium byly na vstupním zobrazení magnetickou rezonancí (MRI) přítomny pouze u 20 % pacientů a u tří čtvrtin zahrnutých pacientů nebyl v předchozím roce zaznamenán žádný relaps. Přestože se jednalo o populaci s pokročilou a málo aktivní RS, prokázala léčba účinnost na klinické i MRI parametry aktivity i progrese nemoci.
Riziko tříměsíční konfirmované progrese bylo nižší o 21 % u léčené populace, riziko šestiměsíční konfirmované progrese se snížilo o 26 % u aktivně léčené populace oproti placebové větvi. Toto snížení rizika progrese bylo ještě výraznější u skupiny pacientů s aktivní nemocí (s přítomnými relapsy před vstupem do studie nebo s gadolinium enhancujícími ložisky na vstupní MRI). V jejich případě bylo riziko tříměsíční progrese sníženo o 33 %.
Výskyt nežádoucích účinků byl velmi podobný u obou skupin, alespoň jeden nežádoucí účinek se vyskytl u 89 % léčených a u 82 % pacientů v placebové větvi, závažný nežádoucí účinek potom u 18 % léčených a u 15 % pacientů ve větvi s placebem. V obou skupinách byla zaznamenána čtyři úmrtí, v léčené skupině byl příčinou generalizovaný melanom gastrointestinálního traktu, sepse při terminálním stavu kolorektálního karcinomu, urosepse a suicidium. Nežádoucí účinky související s léčbou agonisty sfingosin 1-fosfátových receptorů se objevily dle očekávání více v aktivně léčené skupině (bradyarytmie, převodní poruchy apod. u 3 % pacientů oproti 0,4 % v placebové větvi), dvakrát častěji se vyskytly i herpetické infekce u pacientů léčených siponimodem. Naopak závažné nežádoucí účinky související s progresí a aktivitou nemoci byly pozorovány častěji u placebové skupiny.
Velmi důležité je zpomalení progrese nemoci a nárůstu neurologického deficitu zejména pro skupinu pacientů s již vysokým vstupním EDSS (6,0 nebo 6,5), pro které znamená zhoršení byť jen o 0,5 bodu nutnost užívat oboustrannou oporu při chůzi místo jedné hole nebo omezení dosahu chůze na několik kroků a tím i významné omezení soběstačnosti.
Ačkoliv byla účinnost siponimodu ve studii jasně závislá na předchozí aktivitě nemoci, věku a délce trvání nemoci, pozitivní efekt oproti placebu byl prokázán napříč celým spektrem zařazených pacientů. Zpomalení progrese i v pokročilých fázích RS je vzácným jevem při terapii léky s protizánětlivým účinkem. Autoři se zabývají otázkou, zda je siponimod kromě potlačení aktivity zánětu schopen působit i na patogenetické mechanismy progrese. Odpovědí je v tuto chvíli ale jen nutnost dalšího výzkumu.
Výsledky studie EXPAND sice prokazují účinnost i v pokročilých stadiích RS, ale na druhou stranu jednoznačně ukazují, že zahájení léčby co nejdříve po diagnostikování sekundární progrese, tedy ve fázi s nižší mírou neurologického postižení a kratším trváním nemoci, vede k lepšímu efektu léčby a umožňuje zachování lepšího klinického stavu pacienta.
Seznam použité literatury
- [1] Aslanis V, Faller T, Van de Kerkhof E, et al. Siponimod (BAF312) (and/or its metabolites) penetrates into the CNS and distributes to white matter areas. Mult Scler 2012; 18(Suppl. 4): 279–508.
- [2] Gentile A, Musella A, Bullitta S, et al. Siponimod (BAF312) prevents synaptic neurodegeneration in experimental multiple sclerosis. J Neuroinflammation 2016; 13: 207.
- [3] Kappos L, Bar‑Or A, Cree BAC, et al. Siponimod versus placebo in secondary progressive multiple sclerosis (EXPAND): a double‑blind, randomised, phase 3 study. Lancet 2018; 391: 1263–1273.
- [4] Arnold D. Effect of siponimod on cortical grey matter and thalamic volume in patients with secondary progressive multiple sclerosis – results of the EXPAND study. ECTRIMS Online Library. 09/11/19; 278743; P382.
- [5] Arnold D. Relationship between grey matter atrophy, disability and cognition in patients with secondary progressive multiple sclerosis: analysis from the EXPAND study. ECTRIMS Online Library. 09/12/19; 278259; P1057.
- [6] Gold R. Efficacy of Siponimod in secondary progressive multiple sclerosis patients with active disease: the EXPAND study subgroup analysis. ECTRIMS Online Library. 09/12/19; 279110; P750.
- [7] Cutter G. Effect of siponimod on disability in EXPAND re‑examined with two new subscales of the Expanded Disability Status Scale in patients with secondary progressive multiple sclerosis. ECTRIMS Online Library. 09/11/19; 278796; P435.
- [8] Vermersch P. Siponimod delays the time to wheelchair in patients with SPMS: results from the EXPAND study. ECTRIMS Online Library. 09/12/19; 279456; 158.
- [9] Bar‑Or A. Exploring the safety and tolerability of conversion to siponimod in patients with relapsing forms of multiple sclerosis: design of the 6‑month prospective EXCHANGE study. ECTRIMS Online Library. 09/13/19; 278607; P1407.