Studie AFFIRM‑AHF
Souhrn:
Melenovský V. Studie AFFIRM‑AHF. Remedia 2021; 31: 166–167.
Klinická studie AFFIRM‑AHF se zabývala intravenózním podáváním karboxymaltózy železa u pacientů po dekompenzaci srdečního selhání a hodnotila efekt korekce sideropenie na četnost hospitalizací a kardiovaskulárních úmrtí. Článek přibližuje výsledky hodnocení, které potvrdilo klinický přínos aplikace karboxymaltózy železa.
Summary:
Melenovsky V. AFFIRM‑AHF trial. Remedia 2021; 31: 166–167.
The AFFIRM‑AHF clinical trial evaluated intravenous administration of ferric carboxymaltose in patients admitted for acute heart failure and assessed the effect of iron deficiency correction on the number of hospitalizations and cardiovascular death. The review recounts the results of the trial that confirmed clinical benefit of ferric carboxymaltose administration.
Key words: ferric carboxymaltose, heart failure, hospitalization, mortality.
Na virtuální konferenci Scientific Sessions of American Heart Association prezentoval 13. listopadu 2020 profesor Piotr Ponikowski výsledky studie AFFIRM AHF.
Kontext
Deficit železa (sideropenie) u pacientů se srdečním selháním je častým nálezem a je spojen se závažnějšími symptomy, intolerancí námahy, horší kvalitou života, vyšším rizikem úmrtí a hospitalizace. Toto riziko je nezávislé na přítomnosti anémie. Železo totiž není důležité pouze pro krvetvorbu, ale je součástí řady enzymů energetického metabolismu a má důležitou roli v udržení normální bioenergetiky svalu včetně srdečního [1,2]. Deficit železa u pacientů se srdečním selháním vzniká v důsledku omezené interní recyklace, okultních krevních ztrát, zejména však z důvodu zhoršeného vstřebávání železa v přítomnosti srdečního selhání. Více než dvě třetiny pacientů s akutně dekompenzovaným srdečním selháním trpí sideropenií, a tak deficit železa představuje jednu z jejich nejčastějších komorbidit. Předchozí studie ukázaly, že korekce deficitu železa u těchto pacientů zlepšuje kvalitu života [3], toleranci zátěže [4] a může mít i příznivý vliv na průběh nemoci, i když průkazy o efektu na klinické události či mortalitu zatím chybějí.
Je jednoznačně prokázáno, že perorální podávání přípravků k suplementaci železa je u pacientů se srdečním selháním neúčinné [5] a ke korekci sideropenie je nutné zvolit parenterální podání. Karboxymaltóza železa (ferric carboxymaltose, FCM) je přípravek umožňující bezpečné jednorázové podání i vysoké dávky (až 1 000 mg) v pomalé intravenózní injekci. Toto množství železa představuje téměř jednu třetinu normálního celotělového obsahu a často stačí již v jedné dávce ke korekci deficitu. Cílem projektu AFFIRM AHF bylo ověřit efekt korekce sideropenie pomocí FCM u pacientů čerstvě hospitalizovaných pro srdeční selhání a srovnat účinek na riziko rehospitalizace či kardiovaskulárního úmrtí (primární kombinovaný cílový ukazatel) proti placebu.
Uspořádání studie a výsledky
AFFIRM AHF byla randomizovaná, paralelní, dvojitě zaslepená studie porovnávající intravenózní podání FCM nebo placeba [6]. Pacienti dostali celkem 500 až 2 000 mg FCM/placeba podle tělesné hmotnosti a sérové koncentrace hemoglobinu, a to v podobě 1–2 replečních dávek (před dimisí a pak po 6 týdnech) následovaných v případě potřeby udržovací dávkou za 12 a 24 týdnů. Zařazovací kritéria studie AFFIRM AHF představovaly: hospitalizace pro srdeční selhání s dosažením klinické stability s předpokladem brzkého propuštění, ejekční frakce levé komory (left ventricular ejection fraction, LVEF) < 50 %, deficit železa definovaný jako sérová koncentrace feritinu < 100 ng/ml nebo sérová koncentrace feritinu 100–299 ng/ml a saturace transferinu < 20 %. Nebyli zařazováni pacienti s koncentrací hemoglobinu < 80 g/l nebo > 150 g/l, s aktivní infekcí nebo s nedávnou kardiovaskulární událostí.
Do studie bylo zařazeno celkem
1 132 pacientů průměrného věku 71 let, 53 % z nich
ve třídě NYHA III–IV podle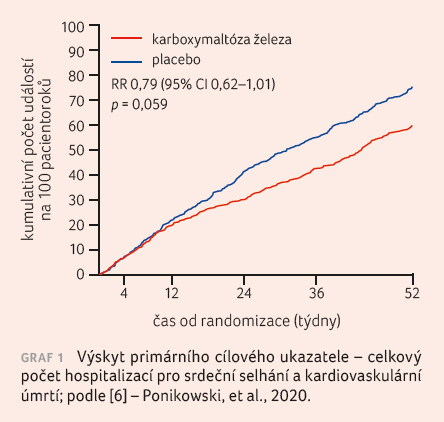 klasifikaci New York Heart
Association, 54 % tvořily ženy, 41 % trpělo diabetes
mellitus. Vstupní hodnota natriuretického peptidu B byla
1 068 pg/ml pro skupinu FCM a 1 204 pg/ml pro placebovou
skupinu, šlo tedy o výrazně symptomatické pacienty se
srdečním selháním. Průměrná délka sledování byla 52 týdnů.
Průměr celkové dávky FCM podané během studie činil
1 352 ± 528 mg/pacient. U 80 % pacientů léčených
FCM stačilo podání jedné nebo dvou dávek k dostatečnému
efektu. Během studie došlo jen k malému nárůstu sérové
koncentrace hemoglobinu (+8 g/l u FCM vs. +3 g/l
u placeba).
klasifikaci New York Heart
Association, 54 % tvořily ženy, 41 % trpělo diabetes
mellitus. Vstupní hodnota natriuretického peptidu B byla
1 068 pg/ml pro skupinu FCM a 1 204 pg/ml pro placebovou
skupinu, šlo tedy o výrazně symptomatické pacienty se
srdečním selháním. Průměrná délka sledování byla 52 týdnů.
Průměr celkové dávky FCM podané během studie činil
1 352 ± 528 mg/pacient. U 80 % pacientů léčených
FCM stačilo podání jedné nebo dvou dávek k dostatečnému
efektu. Během studie došlo jen k malému nárůstu sérové
koncentrace hemoglobinu (+8 g/l u FCM vs. +3 g/l
u placeba).
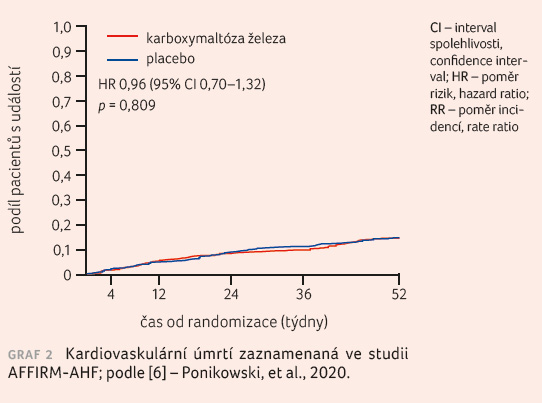
Hlavním cílovým ukazatelem studie byl výskyt hospitalizace pro srdeční selhání nebo kardiovaskulární úmrtí po 52 týdnech sledování, který nastal u 52,5 % pacientů skupiny léčené FCM a u 67,6 % z placebové skupiny (rate ratio [RR] 0,79, p = 0,059), graf 1; studie tedy formálně dopadla na hranici statistické významnosti. Mezi skupinami nebyl rozdíl ve výskytu kardiovaskulárního úmrtí (13,8 % vs. 14,2 %, p = 0,8), graf 2, avšak výskyt všech hospitalizací pro srdeční selhání byl významně nižší ve skupině léčené FCM (217 proti 294; RR 0,74, p = 0,013), viz grafy 3, 4. Podobně byl nižší i počet ztracených dní v důsledku hospitalizace či úmrtí (369 dní vs. 548 dní/100 pacientoroků, p = 0,035). Subanalýza podskupin ukázala, že pacienti s ischemickou etiologií dysfunkce srdce mají z podání FCM významně vyšší prospěch než pacienti s neischemickou dysfunkcí (p interakce: 0,015). Na výsledcích studie se mohla projevit již probíhající epidemie COV
ID 19. Ukazuje se totiž, že během aktivní epidemické fáze dochází k poklesu počtu hospitalizací pro srdeční selhání až o 40 %, resp. se stírá rozdíl mezi virovou pneumonií a obrazem dekompenzovaného srdečního selhání. Pokud byla ze studie analyzována pouze data posbíraná před nástupem epidemie COVID 19 v jednotlivých participujících zemích, studie by ukázala statisticky významný efekt FCM na primární cílový ukazatel (RR 0,75, p = 0,024).
Léčba FCM prokázala svoji
bezpečnost, protože závažné nežádoucí účinky byly
pozorovány častěji ve skupině s placebem (51 %) než
ve skupině s FCM (45 %). Studijní medikace byla předčasně
ukončena u 28 % pacientů léčených FCM a u 29 %
pacientů s placebem.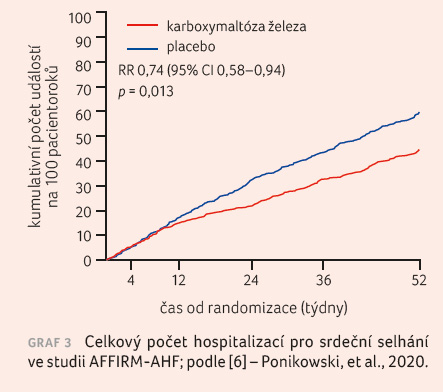
Závěr a interpretace
Studie ukázala, že intravenózní
podání FCM u pacientů po dekompenzaci srdečního
selhání je bezpečné, má příznivý klinický efekt a vede
k poklesu rizika rehospitalizace v následujícím roce.
Studie ukazuje, že korekce sideropenie parenterálním podáním
železa nevede pouze k symptomatickému zlepšení a ke zlepšení
kvality života, nýbrž 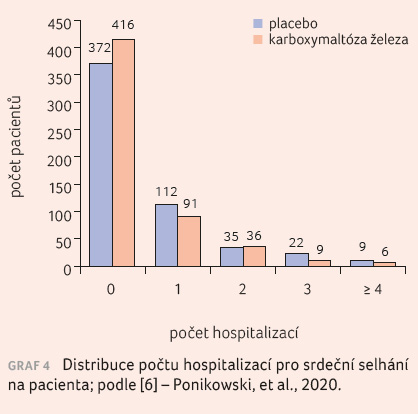 má i efekt na výskyt událostí,
jako je hospitalizace pro srdeční selhání. Nedostatečný efekt
na kardiovaskulární mortalitu je v této studii zřejmě
spíše důsledkem malé statistické síly a relativně krátké
doby sledování než projevem skrytých rizik léčby. Vliv FCM
na celkovou a kardiovaskulární mortalitu pacientů
s chronickým srdečním selháním bude objasněn po ukončení
dalších velkých studií, které nyní probíhají (HEART FID,
FAIR HF2, FAIR HFpEF). Již nyní je jisté, že FCM
podávaná intravenózně představuje jednoduchý a relativně
levný prostředek k symptomatickému zlepšení stavu pacientů
s chronickým srdečním selháním.
má i efekt na výskyt událostí,
jako je hospitalizace pro srdeční selhání. Nedostatečný efekt
na kardiovaskulární mortalitu je v této studii zřejmě
spíše důsledkem malé statistické síly a relativně krátké
doby sledování než projevem skrytých rizik léčby. Vliv FCM
na celkovou a kardiovaskulární mortalitu pacientů
s chronickým srdečním selháním bude objasněn po ukončení
dalších velkých studií, které nyní probíhají (HEART FID,
FAIR HF2, FAIR HFpEF). Již nyní je jisté, že FCM
podávaná intravenózně představuje jednoduchý a relativně
levný prostředek k symptomatickému zlepšení stavu pacientů
s chronickým srdečním selháním.
Seznam použité literatury
- [1] van der Meer P, van der Wal HH, Melenovsky V. Mitochondrial Function, Skeletal Muscle Metabolism, and Iron Deficiency in Heart Failure. Circulation 2019; 139: 2399–2402.
- [2] Melenovsky V, Petrák J, Mraček T, et al. Myocardial iron content and mitochondrial function in human heart failure: a direct tissue analysis. Eur J Heart Fail 2017; 19: 522–530.
- [3] Anker SD, Colet JC, Filippatos G, et al.; on behalf of FAIR‑HF Trial Investigators. Ferric carboxymaltose in patients with heart failure and iron deficiency. N Engl J Med 2009; 361: 2436–2448.
- [4] Ponikowski P, van Veldhuisen DJ, Comin‑Colet J, et al.; on behalf of CONFIRM‑HF Investigators. Beneficial effects of long‑term intravenous iron therapy with ferric carboxymaltose in patients with symptomatic heart failure and iron deficiency. Eur Heart J 2015; 36: 657–668.
- [5] Lewis GD, Malhotra R, Hernandez AF, et al. Effect of Oral Iron Repletion on Exercise Capacity in Patients With Heart Failure With Reduced Ejection Fraction and Iron Deficiency: The IRONOUT HF Randomized Clinical Trial. JAMA 2017; 317: 1958–1966.
- [6] Ponikowski P, Kirwan BA, Anker SD, et al.; on behalf of AFFIRM‑AHF Investigators. Ferric carboxymaltose for iron deficiency at discharge after acute heart failure: a multicentre, double‑blind, randomised, controlled trial. Lancet 2020; 396: 1895–1904.