Studie MERLIN TIMI 36 Vliv ranolazinu na riziko kardiovaskulárních příhod u nemocných s akutním koronárním syndromem bez ST elevací
Přes pokroky v antitrombotické terapii a širší dostupnost časné invazivní terapie pacientů s akutním koronárním syndromem bez elevací úseku ST zůstává riziko rekurentních ischemických atak relativně vysoké (cca 20–30%). Ranolazin je látka s novými antianginózními a antiischemickými vlastnostmi, které jsou podmíněny především jeho schopnostmi ovlivňovat metabolismus kardiomyocytů směrem k méně náročným metabolickým pochodům se sníženou spotřebou kyslíku v myokardu. Tento efekt byl prokázán snížením myokardiální ischémie a zvýšenou tolerancí zátěže u pacientů se stabilní anginou pectoris, přičemž nebyly ovlivněny základní hemodynamické parametry jako krevní tlak, tepová frekvence nebo vedení atrioventrikulárním uzlem, kontraktilní funkce. Data získaná z experimentálních i klinických studií podporují hypotézu, že přidání ranolazinu k stávající medikamentózní kombinaci zlepší krátkodobou i dlouhodobou prognózu u pacientů s akutním koronárním syndromem bez elevací úseku ST.
Myokardiální metabolismus během ischémie
Ischémie a reperfuze kardiomyocytů je spojena s poruchou sodíkové a vápníkové homeostázy, která vede k buněčné dysfunkci (mechanické, energetické a elektrické nestabilitě) a pokud není stav upraven, vede v konečném důsledku k buněčné smrti. Během ischémie dochází k převážení influxu sodíku nad jeho vyplavováním a tím k přetížení buňky sodíkem. Zvýšená hladina sodíku v kardiomyocytu podněcuje aktivaci Na+/Ca2+ pumpy a způsobuje následné přetížení buňky i vápníkem [1]. Přetížení vápníkem vede k posílení aktinomyozinových komplexů, porušena je zejména relaxace – diastolická funkce, narůstá enddiastolický tlak levé komory. Zvyšují se nároky na spotřebu kyslíku, je komprimováno koronární řečiště, což dále zhoršuje zásobení kyslíkem a ischémii. Výsledkem je bludný kruh prohlubující se ischémie myokardu.
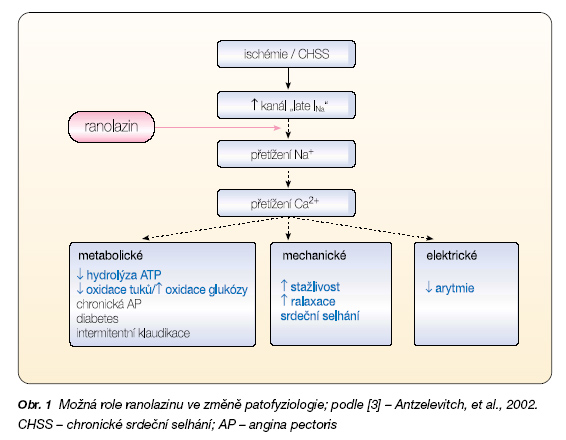
V experimentálních studiích s ranolazinem byl prokázán jeho kardioprotektivní efekt u ischemicko-reperfuzního postižení a chronického srdečního selhání. Předpokládán byl zejména vliv na oxidaci mastných kyselin, jejíž inhibice byla in vitro prokázána, ale v koncentracích vyšších, než je terapeutická hladina. V dalších experimentech bylo objeveno, že ranolazin selektivně inhibuje pozdní sodíkový kanál (late INa) v membráně kardiomyocytů. Tento kanál za normálních okolností zabezpečuje cca 1 % celkového influxu sodíku během trvání akčního potenciálu, a to mimo fázi rychlé depolarizace (fáze 0) [2]. V podmínkách ischemicko-reperfuzního poškození a zpomalené nebo opožděné depolarizace se však zvýšený influx sodíku tímto kanálem spolupodílí na přetížení kardiomyocytu sodíkem. Selektivní blokáda kanálu INa ranolazinem tedy snižuje přetížení kardiomyocytu sodíkem, vápníkem, vede ke snížení intramyokardiální tenze, spotřeby kyslíku a zlepšení myokardiální perfuze – přetíná onen bludný kruh (obr. 1) [3].
Ranolazin – dosavadní klinické zkušenosti
Dosud bylo provedeno 5 randomizovaných dvojitě zaslepených studií s ranolazinem, které prokazují jeho účinnost u pacientů s chronickou stabilní anginou pectoris. První 3 z těchto studií zkoumaly zejména okamžitou účinnost a dávkování při perorálním podávání, testována byla zátěžová tolerance. Všechny tyto studie prokázaly zvýšenou toleranci zátěže při podání ranolazinu.
Další z těchto studií byla studie MARISA (Monotherapy Assessment of Ranolazine In Stable Angina) porovnávající efekt 3 dávek ranolazinu (500, 1000, 1500 mg 2krát denně) oproti placebu u 191 pacientů se stabilní anginou pectoris. Podávání ranolazinu vedlo k signifikantnímu prodloužení tolerance zátěže při zátěžovém testu, a to v závislosti na velikosti dávky [4].
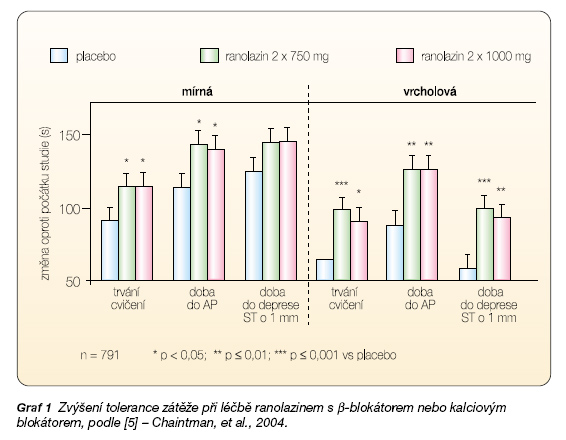
Paralelní studií byla studie CARISA (Combination Assessment of Ranolazine In Stable Angina) porovnávající efekt 2 dávek ranolazinu (750 a 1000 mg 2krát denně) v kombinaci s diltiazemem, amlodipinem nebo atenololem oproti placebu u 823 pacientů se stabilní anginou pectoris. Po 12 týdnech terapie došlo k signifikantnímu zvýšení tolerance zátěže, verifikovanému opět dle zátěžového testu (graf 1) [5].
Informace o bezpečnosti podávání ranolazinu byly shromážděny od více než 3000 pacientů, jimž byla tato látka dosud podávána. Nejčastějšími nežádoucími účinky s četností větší než v placebové skupině byly vertigo, zácpa, nauzea, slabost, bolesti hlavy, dyspepsie, s jednotlivou četností do 10 %. Nejčastějším závažným vedlejším účinkem bylo vertigo, vyskytovalo se v 0,3 %. Většina nežádoucích účinků se objevila na začátku podávání ranolazinu a byla reverzibilní po snížení dávky nebo po jeho vysazení. Podávání ranolazinu bylo spojeno pouze s minimálním prodloužením intervalu QT, nebyly dokumentovány epizody komorových arytmií typu torsade de pointes.
Na základě těchto klinických zkušeností a ověření účinnosti a bezpečnosti ranolazinu je nutno jeho předpokládaný potenciál ke snížení rizika úmrtí a rekurentní ischémie potvrdit i u pacientů s akutní ischémií myokardu.
Uspořádání studie MERLIN
Primárním cílem studie MERLIN TIMI 36 (Metabolic Efficiency with Ranolazine for Less Ischemia in Non-ST elevation Acute Coronary Syndromes) je porovnat účinnost ranolazinu na snížení počtu kardiovaskulárních úmrtí, infarktu myokardu (IM) nebo rekurentní ischémie během dlouhodobé terapie pacientů s akutním koronárním syndromem (AKS) bez elevací úseku ST oproti placebu.
Do studie jsou zařazováni pacienti s akutním koronárním syndromem, s klidovými anginózními symptomy v předchozích 48 hodinách se středním až zvýšeným rizikem (pozitivní kardiomarkery nebo deprese ST ≥ 0,1 mV nebo diabetes mellitus nebo TIMI risk score ≥ 3). Celkem je plánováno k zařazení cca 6500 pacientů v aktivních 469 centrech v 17 zemích po celém světě. Randomizace na léčbu ranolazinem a podávání placeba probíhá co nejdříve po hospitalizaci pro AKS v poměru 1 : 1. Ranolazin/placebo je podáván zpočátku v infuzi v dávce 200 mg/hod po dobu 1 hodiny, dále v dávce 80 mg/hod. Dávka je redukována při případných nežádoucích účincích, při renální insuficienci nebo při prodloužení intervalu QT. Intravenózní fáze terapie trvá 12–96 hodin, potom je pacient převeden na perorální dávky podávané po 12 hodinách, tedy 2krát denně. Velikost perorální dávky (1000, 750, 500, 375 mg 2krát denně) je opět určena dle tolerance. Perorální medikace je podávána do ukončení sledování ve studii. Ostatní terapie je standardní dle stávajících doporučení, včetně invazivní terapie a revaskularizace.
Pacientům je ihned po zahájení léčby studovanou medikací napojen na 7 dnů EKG-Holter k monitoraci deviací segmentů ST a detekci ischemických změn, dále jsou dle protokolu prováděna laboratorní vyšetření a standardní klinická vyšetření. Po propuštění z iniciální hospitalizace následují ambulantní kontroly, první po 14 dnech, a dále po 4 měsících. Po 8 měsících je dle protokolu studie proveden zátěžový test. Ve vybraných centrech dále probíhají některé substudie, jako např. echokardiografická, genetická, analýzy hodnotící biomarkery nekrózy – ischémie myokardu, farmakokinetiku a kvalitu života.
Průběh studie a stav v současnosti
Studie byla zahájena v říjnu 2004, v České republice byl první pacient randomizován 12. 5. 2005 v našem centru. Sledování pacientů je plánováno průměrně na 8–12 měsíců (očekávané maximum cca 22 měsíců). Ukončení je plánováno po dosažení statisticky významného počtu primárních a sekundárních cílů (kardiovaskulárních úmrtí, IM, rekurentní ischémie, celkové úmrtnosti).
Dosud (březen 2006) bylo po celém světě zařazeno 5650 pacientů, při četnosti zařazování cca 100 pacientů za týden je očekáváno ukončení náběru pacientů v květnu 2006. Česká republika patří mezi státy s největším počtem zařazených pacientů – v současné době bylo v 14 centrech zařazeno 330 pacientů.
Seznam použité literatury
- [1] Eigel BN, Halley RW. Antisense inhibition of Na+/Ca2+ exchange during anoxia/reoxygenation in ventricular myocytes. Am J Physiol (Heart Circ Physiol) 2001; 281: H2184–90.
- [2] Saint DA, Yu YK, Gage PW. A persistent sodium current in rat ventricular myocytes. J Physiol 1992; 453: 219–231.
- [3] Antzelevitch C, Belardinelli L. Electrophysiological effects of ranolazine in ventricular myocytes from dogs with chronic heart failure. Circ Res 2002; 91: 278–280.
- [4] Chaintman BR, Skettino SL, Parker JO, et al. Antiischemic effects and long-term survival during ranolazine monotherapy in patients with chronic severe angina. J Am Coll Cardiol 2004; 43: 1375–1382.
- [5] Chaintman BR, Pepine CJ, Parker JO, et al. Effects of ranolazine with atenolol, amlodipine, or diltiazem on exercise tolerance and angina frequency in patients with severe chronic angina. A randomized controlled trial. JAMA 2004: 291: 309–316.