Těžká forma psoriázy s ulcerózní kolitidou léčená adalimumabem
Souhrn:
Psoriáza je chronické zánětlivé onemocnění postihující kolem 2–4 % středoevropské populace. V současné době již víme, že lupénka není omezena pouze na kožní povrch, ale je rovněž spojena s řadou komorbidit, jakými jsou psoriatická artritida (přibližně u 25 % nemocných), Crohnova choroba, ulcerózní kolitida, Bechtěrevova choroba a zejména nemoci tzv. metabolického syndromu, jako je např. diabetes mellitus 2. typu, arteriální hypertenze nebo dyslipi-demie. Zde popisujeme případ pacientky, která trpí souběžně psoriázou a ulcerózní kolitidou a je úspěšně léčena jedním přípravkem indikovaným pro obě choroby.
Key words: psoriasis – comorbidities – ulcerative colitis – adalimumab.
Summary:
Psoriasis is a chronic inflammatory skin disease, affecting around 2–4% of Central European population. Nowadays, we know that psoriasis is not only limited to the skin surface but is connected with various comorbidities like psoriatic arthritis (about 25%), Crohn’s disease, ulcerative colitis, Bechterev disease, and a complex of disorders known as metabolic syndrome, including type 2 diabetes mellitus, arterial hypertension, and dyslipidemia. In our article, we present the case of a female patient who suffers from both psoriasis and ulcerative colitis and is treated with the same medication for both diseases.
Úvod
Psoriáza je chronická dermatitida postihující kolem 2–4 % středoevropské populace. I když přesná etiologie není dosud známa, předpokládá se genetický podklad onemocnění, kdy u predisponovaných jedinců dojde ke spuštění patogenetických pochodů, ve kterých hrají zásadní roli T‑lymfocyty [1]. Choroba neohrožuje život pacienta přímo, avšak má nesporný vliv na fyzické, sociální a psychické aspekty života [2]. Dle současného hodnocení jsou pacienti se středně těžkou až těžkou psoriázou řazeni na druhé místo v žebříčku negativního dopadu chorob na kvalitu života – ihned za depresí – a jejich postižení je srovnatelné s jinými závažnými onemocněními (revmatoidní artritida, malignity, choroby srdce) [3].
V současné době již víme, že lupénka není omezena pouze na kožní povrch, ale je rovněž spojena s řadou komorbidit, jakými jsou psoriatická artritida (přibližně u 25 % nemocných), Crohnova choroba, ulcerózní kolitida, Bechtěrevova choroba a zejména nemoci tzv. metabolického syndromu, jako je např. diabetes mellitus 2. typu, arteriální hypertenze nebo dyslipidemie, což může zkrátit délku života psoriatika o 3,5 roku až 10 let ve srovnání se zdravou populací [4,5].
Vzhledem k chronickému průběhu onemocnění je naším hlavním cílem dlouhodobá kontrola choroby, v ideálním případě dosažení úplného vymizení psoriatických ložisek. Možnosti léčby jsou lokální nebo celkové, často ve vzájemné kombinaci. Mezi klasické systémové léčebné metody se řadí fototerapie (UVB, PUVA – psoralen + ultrafialové záření A), podávání methotrexatu, ciclosporinu a acitretinu. Pokud má pacient i nějakou z výše uvedených komorbidit, snažíme se vybrat léčbu, která by mohla být účinná jak na psoriázu, tak i na konkrétní komorbiditu [6].
Nejnovější skupinu celkových léčiv tvoří tzv. biologika. Tyto látky cíleně interferují na molekulární úrovni s patogenetickými pochody vzniku psoriázy. Biologická léčba je určena pouze pro středně závažné až závažné ložiskové formy psoriázy s postižením více než 10 % povrchu těla, u kterých nebyla jiná celková léčba dostatečně účinná, případně je léčba kontraindikována nebo ji pacient netoleruje [7].
Dostupnou biologickou léčbu psoriázy bylo možno ještě donedávna rozdělit podle mechanismu působení do dvou skupin, nyní už do tří: léčiva blokující nádorový nekrotizující faktor alfa (TNFα, tumor necrosis factor alpha) – adalimumab, etanercept, infliximab; léčiva blokující interleukin 12 a 23 (IL‑12/23) – ustekinumab – a nově i léčiva blokující interleukin 17 – secukinumab [8,9]. Některé přípravky, jež se svým mechanismem účinku řadí do první skupiny, jsou indikovány i k léčbě jiných nedermatologických onemocnění, např. k léčbě Crohnovy choroby nebo ulcerózní kolitidy.
Kasuistika
Jedná se o 38letou pacientku trpící psoriázou osm let. Dále jí byla před pěti lety diagnostikována ulcerózní kolitida, poslední tři roky je však onemocnění v remisi bez medikace. Před dvěma lety se pacientka začala léčit s depresí. V minulosti byla léčena fototerapií a acitretinem, ale jen s parciálním efektem. Tři měsíce před prvním vyšetř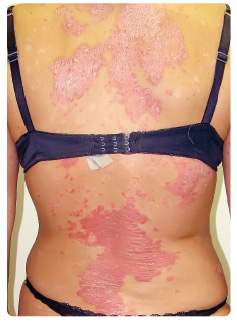 ením na našem pracovišti došlo k exacerbaci nejen psoriázy, ale i ulcerózní kolitidy, pro kterou musela být zahájena léčba prednisonem 60 mg denně (tělesná hmotnost pacientky 68 kg) a mesalazinem v dávce 500 mg 3× denně. Po dvou týdnech léčby došlo k potlačení gastrointestinálních potíží a dle pacientky postupně začalo docházet i ke zklidnění psoriázy, zřejmě v důsledku celkové léčby prednisonem. Léčba kortikosteroidy byla postupně omezována a po dvou měsících byl pacientce podáván prednison v dávce 20 mg denně, při této léčbě ale došlo k opětovné exacerbaci lupénky. Dávka mesalazinu byla snížena na 500 mg 2× denně. Když pacientka navštívila naši ambulanci, užívala již dva týdny 10 mg prednisonu denně a psoriáza byla výrazně zhoršena – skóre PASI (Psoriasis Area Severity Index) činilo 19 (obr. 1).
ením na našem pracovišti došlo k exacerbaci nejen psoriázy, ale i ulcerózní kolitidy, pro kterou musela být zahájena léčba prednisonem 60 mg denně (tělesná hmotnost pacientky 68 kg) a mesalazinem v dávce 500 mg 3× denně. Po dvou týdnech léčby došlo k potlačení gastrointestinálních potíží a dle pacientky postupně začalo docházet i ke zklidnění psoriázy, zřejmě v důsledku celkové léčby prednisonem. Léčba kortikosteroidy byla postupně omezována a po dvou měsících byl pacientce podáván prednison v dávce 20 mg denně, při této léčbě ale došlo k opětovné exacerbaci lupénky. Dávka mesalazinu byla snížena na 500 mg 2× denně. Když pacientka navštívila naši ambulanci, užívala již dva týdny 10 mg prednisonu denně a psoriáza byla výrazně zhoršena – skóre PASI (Psoriasis Area Severity Index) činilo 19 (obr. 1).
Po konzultaci s gastroenterologem byla zahájena léčba methotrexatem v dávce 10 mg týdně. Po týdnu byla dávka zvýšena na 15 mg týdně. Po třech měsících léčby methotrexatem nedošlo k žádnému zlepšení kožního nálezu. Podávaná dávka prednisonu byla stále 10 mg denně a mesalazinu 500 mg 2× denně. Pacientka byla kandidátkou na biologickou léčbu – v minulosti byla léčena acitretinem, fototerapií, nyní methotrexatem; skóre PASI a BSA (Body Surface Area) převyšovalo 10. Plicní vyšetření vyloučilo latentní tuberkulóz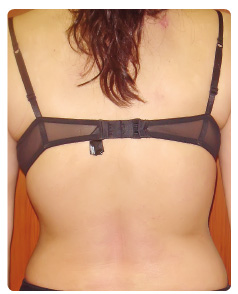 u. Vzhledem ke komorbiditě ulcerózní kolitidy jsme upřednostnili biologikum, které by mohlo mít příznivý účinek i na tuto chorobu. Proto jsme se rozhodli zahájit léčbu adalimumabem v klasickém schématu pro psoriázu (1. den subkutánní aplikace 80 mg, po týdnu 40 mg a poté jedenkrát za 2 týdny 40 mg). Dávku prednisonu jsme snížili po dvou týdnech na 5 mg denně a po dalších dvou týdnech bylo podávání prednisonu ukončeno, stejně tak podávání mesalazinu. Po třech měsících léčby adalimumabem pacientka dosáhla kompletní remise – PASI 100 (obr. 2) – a z hlediska ulcerózní kolitidy je bez symptomatologie. Monoterapie adalimumabem je doposud podávána devět měsíců s výborným působením na obě choroby.
u. Vzhledem ke komorbiditě ulcerózní kolitidy jsme upřednostnili biologikum, které by mohlo mít příznivý účinek i na tuto chorobu. Proto jsme se rozhodli zahájit léčbu adalimumabem v klasickém schématu pro psoriázu (1. den subkutánní aplikace 80 mg, po týdnu 40 mg a poté jedenkrát za 2 týdny 40 mg). Dávku prednisonu jsme snížili po dvou týdnech na 5 mg denně a po dalších dvou týdnech bylo podávání prednisonu ukončeno, stejně tak podávání mesalazinu. Po třech měsících léčby adalimumabem pacientka dosáhla kompletní remise – PASI 100 (obr. 2) – a z hlediska ulcerózní kolitidy je bez symptomatologie. Monoterapie adalimumabem je doposud podávána devět měsíců s výborným působením na obě choroby.
Diskuse
V posledních letech přibývá důkazů o tom, že psoriáza není jen kožním onemocněním, ale že je spojena s řadou dalších komorbidit. Jednou z nich jsou i zánětlivá onemocnění střev (Crohnova choroba a ulcerózní kolitida). Genetické spojení mezi těmito chorobami bylo popsáno v literatuře a nachází se na lokusu 6p21 [5]. I patofyziologie výše uvedených onemocnění se jeví podobná. Klíčovou roli hrají subpopulace T‑lymfocytů Th1 a Th17 a produkce jejich prozánětlivých cytokinů, jako je TNFα, IL‑17 a IL‑23 [5].
Zřejmě i proto existuje léčba, zejména biologická, která je účinná jak na psoriázu, tak i na zánětlivé onemocnění střev. Indikace pro léčbu psoriázy, Crohnovy choroby a ulcerózní kolitidy má adalimumab a infliximab. Adalimumab je plně humánní protilátka IgG1 proti TNFα. Váže s vysokou afinitou a specifitou solubilní i membránový TNFα (p55 a p75). Díky vazbě na membránový TNFα může vést k cytolýze indukované komplementem. Adalimumab je připravován rekombinantní DNA technologií v savčí buňce expresního systému. Aplikuje se subkutánně, dávkování záleží na konkrétní indikaci. Například u psoriázy je iniciálně podána jednorázová dávka 80 mg, po týdnu 40 mg a pak následuje aplikace jedenkrát za 14 dní [10]. Klinický účinek ve studiích u pacientů s psoriázou nastupoval rychle a přetrvával až tři roky při kontinuálním podávání. Z dosud provedených studií vyplývá, že odpovědi na léčbu se skóre PASI 75 (nejméně 75% zlepšení PASI) dosáhlo v 16. týdnu 71–80 % pacientů [11].
V případě ulcerózní kolitidy je dávkování mírně odlišné od dávkování u psoriázy, iniciálně se podává 160 mg, po dvou týdnech 80 mg a poté následuje aplikace jedné injekce 40 mg každé dva týdny. Účinnost adalimumabu u pacientů s ulcerózní kolitidou byla ověřena klinickými studiemi UC‑I (ULTRA I) a UC‑II (ULTRA II) [12]. Pacienti léčení účinnou látkou dosáhli klinické remise v 8. týdnu v signifikantně vyšším procentu v porovnání s placebem. Nežádoucí účinky byly mírné až střední intenzity (zejména infekce horních cest dýchacích, reakce v místě vpichu). Před zahájením léčby adalimumabem je nutno stejně jako před aplikací ostatních biologických přípravků vyloučit maligní onemocnění, latentní onemocnění tuberkulózou, hepatitidou nebo jiné infekce u rizikových pacientů.
Naše pacientka měla koincidenci psoriázy a ulcerózní kolitidy. Při léčbě prednisonem došlo ke zmírnění obou chorob, ale jak víme z klinické praxe, při snižování dávky celkově podaných kortikosteroidů hrozí nejen riziko zhoršení psoriázy, ale navíc i tzv. rebound fenomén (výrazná exacerbace psoriázy s rizikem vzniku erytrodermie). Proto jsme i po zahájení léčby adalimumabem podávání prednisonu hned neukončili, ale pokračovali v něm první měsíc souběžně s biologickou léčbou, než nastoupil její účinek. Při dobré účinnosti a snášenlivosti léčby je plánováno dlouhodobé podávání adalimumabu.
Biologická léčba je velmi přínosná zejména v situacích, kdy má pacient dvě imunitně zprostředkované choroby, jejichž léčba by jinak vyžadovala kombinaci imunosupresivních přípravků.
Seznam použité literatury
- [1] Nestle FO, Kaplan DH, Barker J. Psoriasis. N Engl J Med 2009; 361: 496–509.
- [2] Gkalpakiotis S, Arenberger P, Adenubiová E. Psychosociální aspekty života pacientů s psoriázou v České republice. Čes slov Derm 2013; 4: 189–196.
- [3] Schmitt JM, Ford DE. Role of depression in quality of life for patients with psoriasis. Dermatology 2007; 215: 17–27.
- [4] Christophers E. Comorbidities in psoriasis. J Eur Acad Dermatol Venerol 2006; 20: 52–55.
- [5] Cohen AD, Dreiher J, Birkenfeld S. Psoriasis associated with ulcerative colitis and Crohn’s disease. J Eur Acad Dermatol Venerol 2009; 23: 561–565.
- [6] Cetkovská P, Kojanová M. Česká doporučení k biologické léčbě závažné chronické ložiskové psoriázy. Čes slov Derm 2012; 87: 1–30.
- [7] Menter A, Griffiths CE. Current and future management of psoriasis. Lancet 2007; 370: 272–284.
- [8] Van De Kerkhof PC. Novel biologic therapies in development targeting IL 12/IL 23. J Eur Acad Dermatol 2010; 24: 5–9.
- [9] Mrowietz U, Leonardi CL, Girolomoni G, et al. Secukinumab retreatment as needed versus fixed interval maintenance regimen for moderate to severe plaque psoriasis: A randomized, double blind, noninferiority trial (SCULPTURE). J Am Acad Dermatol 2015; 73: 27–36.
- [10] Souhrn údajů o přípravku Humira, dostupné na www.ema.europa.eu, datum poslední revize textu: 04/2015.
- [11] Saurat J, Stingl G, Dubertret L, et al. Efficacy and safety results from the randomized controlled comparative study of adalimumab vs. methotrexate vs. placebo in patients with psoriasis (CHAMPION). Br J Dermatol 2008; 158: 558–566.
- [12] Colombel JF, Sandborn WJ, Ghosh S, et al. Four year maintenance treatment with adalimumab in patients with moderately to severely active ulcerative colitis: Data from ULTRA 1, 2, and 3. Am J Gastroenterol 2014; 109: 1771–1780.