Účinnost anti‑CGRP terapie u pacientů s obtížně léčitelnou migrénou
Společnost Teva zahájila v lednu 2021 sérii webinářů o přístupu k pacientům s chronickou a těžkou epizodickou migrénou, respektive o pacientech s bolestmi hlavy/migrénou z nadužívání medikace (medication overuse headache, MOH). V prvním webináři hovořil profesor Hans Christoph Diener (Univerzita v Duisburgu‑Essenu, Německo) o tom, jak zlepšit terapeutické výsledky u pacientů s obtížně léčitelnou migrénou z pohledu dat klinických studií. Jeho prezentace nesla název „Optimizing Patient Outcomes in Difficult‑to treat Migraine: What Do the Data Tell Us?“.
Chronická migréna postihuje více než 2 % populace, uvedl profesor Diener v úvodu své prezentace, což znamená, že v Německu žije 1,6 milionu pacientů s chronickou migrénou. Je velmi důležité předejít chronifikaci původně epizodické migrény správnou a včasnou léčbou a vyhnout se tak nadužívání analgetik [1].
Rizikové faktory vzniku obtížně léčitelné migrény
K rizikovým faktorům chronifikace patří nadužívání (medication overuse, MO) nebo neúčinnost akutní analgetické medikace, obezita, psychiatrické komorbidity (jako jsou deprese a úzkost), stresující životní události, nadužívání kofeinu a chrápání [1,2]. Je velmi obtížné pacienty s rizikovými faktory identifikovat a začít u nich co nejdříve s preventivní léčbou.
Richard Lipton se svými kolegy uveřejnil práci, v níž sledoval 8 233 pacientů s epizodickou migrénou, kteří užívali akutní léčbu. Celkem 54 % z nich udávalo nedostatečnou úlevu od bolesti za 24 hodin po podání léku [3]. Klíčovými rizikovými faktory nedostatečného analgetického účinku byly určité typy bolesti (více dnů s migrénou v měsíci, kožní alodynie, více migrenózních symptomů a velmi těžká migréna), MO, deprese a úzkost.
Monoklonální protilátky proti CGRP pro prevenci migrény
Podle doporučení European Headache
Federation (EHF) mají být nabídnuty anti CGRP (calcitonin
gene related peptide) monoklonální protilátky pacientům
s epizodickou nebo chronickou migrénou, u nichž selhaly
alespoň dvě předchozí preventivní léčby, respektive kteří
nemohou užívat jinou preventivní terapii pro komorbidity,
nežádoucí účinky a nedostatečnou compliance.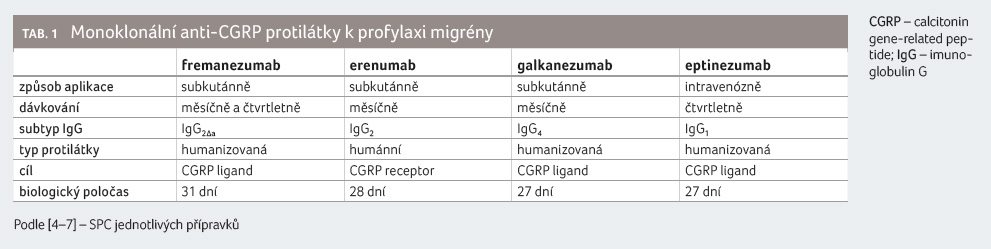
V současnosti jsou v Evropské unii dostupné tři monoklonální protilátky cílené proti CGRP – fremanezumab, erenumab a galkanezumab. Čtvrtou monoklonální protilátkou je eptinezumab, který čeká na schválení pro EU. Charakteristiky jednotlivých monoklonálních protilátek shrnuje tabulka 1 [4‒7].
Co říkají doporučené postupy
- Pacientům s chronickou migrénou, u nichž nedošlo k adekvátní odpovědi na jakoukoliv perorální preventivní léčbu, by měl být nabídnut fremanezumab, erenumab nebo galkanezumab a ukončení podávání perorálních léků by mělo být zváženo později.
- Doporučení EHF z roku 2019 říká, že u pacientů, kteří nedostatečně reagovali na léčbu onabotulotoxinem A, by nejprve mělo dojít k ukončení aplikace onabotulotoxinu A a následně je možné zahájit terapii monoklonálními protilátkami. Od té doby byla zveřejněna data prokazující, že onabotulotoxin A nesnižuje účinnost monoklonálních protilátek v prevenci migrény.
Data u migrény s neadekvátní odpovědí na předchozí preventivní léčbu
Fremanezumab
Studie FOCUS, jejíž výsledky byly
uveřejněny v časopise Lancet [8], sledovala pacienty (ve věku
od 18 do 70 let)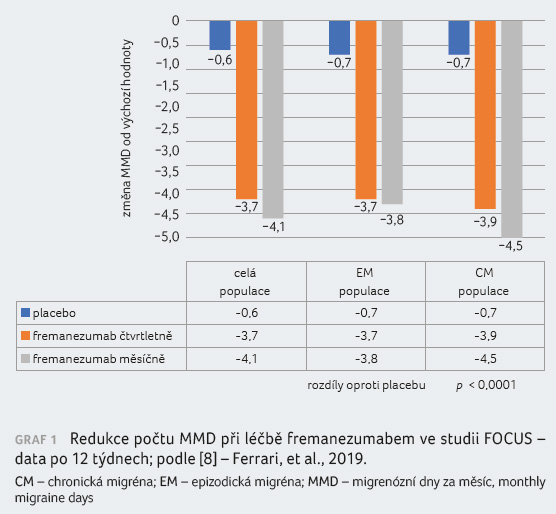 s epizodickou a chronickou
migrénou, u nichž selhaly dva až čtyři předchozí
profylaktické léky (z různých skupin), a to pro
nedostatečnou účinnost (bez odpovědi po třech měsících
léčby) nebo pro nesnášenlivost, respektive pro existující
kontraindikace (například valproát u žen v plodném
věku). Primárním cílovým ukazatelem byla změna od výchozí
hodnoty v 12. týdnu v průměrném počtu dní
s migrénou za měsíc (monthly migraine days, MMD),
graf 1. Sekundární cílové ukazatele pak zahrnovaly
podíl pacientů, u nichž došlo k 50% redukci počtu
MMD za čtyři týdny a 12 týdnů (graf 2).
Výsledky studie svědčí o setrvalém účinku fremanezumabu
v čase [8].
s epizodickou a chronickou
migrénou, u nichž selhaly dva až čtyři předchozí
profylaktické léky (z různých skupin), a to pro
nedostatečnou účinnost (bez odpovědi po třech měsících
léčby) nebo pro nesnášenlivost, respektive pro existující
kontraindikace (například valproát u žen v plodném
věku). Primárním cílovým ukazatelem byla změna od výchozí
hodnoty v 12. týdnu v průměrném počtu dní
s migrénou za měsíc (monthly migraine days, MMD),
graf 1. Sekundární cílové ukazatele pak zahrnovaly
podíl pacientů, u nichž došlo k 50% redukci počtu
MMD za čtyři týdny a 12 týdnů (graf 2).
Výsledky studie svědčí o setrvalém účinku fremanezumabu
v čase [8].
Z grafu 3 je patrný
trend snižování významu placeba se stoupajícím počtem tříd
perorálních přípravků, které v prevenci selhaly,
a do jisté míry pokleslo i očekávání účinnosti
u fremanezumabu v závislosti na počtu předchozích
neúčinných/selhávajících terapií [9].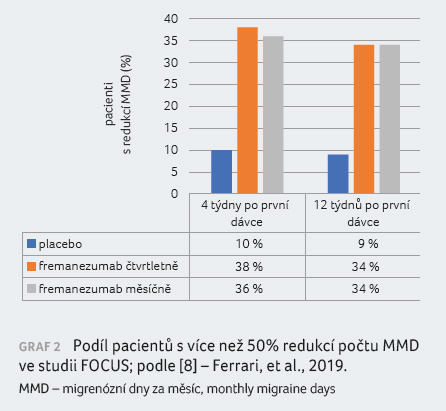
Erenumab
Studie LIBERTY sledovala pacienty
(ve věku 18–65 let) trpící epizodickou migrénou
navzdory terapii dvěma až čtyřmi preventivními přípravky (tj.
bez efektu po dobu 2–3 měsíců léčby) léčené erenumabem
[10]. Primárním cílovým ukazatelem byl podíl pacientů, kteří
dosáhnou alespoň 50% redukce počtu MMD za 9–12 týdnů
(graf 4). Sekundární cílové ukazatele zahrnovaly
změnu od výchozí hodnoty v počtu MMD (graf 5)
a pacienty s redukcí přesahující 75 % nebo se 100%
redukcí počtu MMD. „S tak výraznou redukcí počtu dní
s migrénou jsme se nikdy nesetkali u předchozích typů
preventivní léčby, toto očekávání máme až u monoklonálních
protilátek,“ uvedl profesor Diener. Všechny rozdíly oproti
placebu jsou statisticky signifikantní.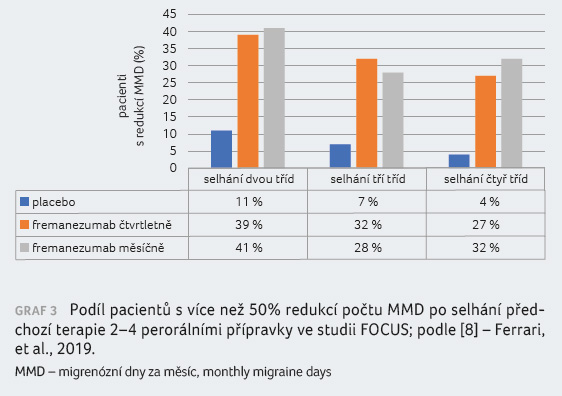
Data reálné praxe (real world data,
RWD) z jednoho italského centra pro léčbu bolestí hlavy
vycházejí ze sledování 89 pacientů s migrénou
léčených erenumabem po neúspěšné terapii dvěma a více
preventivními přípravky. Celkem 13 (14,6 %) nemocných
léčbu erenumabem ukončilo: 12 pro neúčinnost, jeden pacient pro
nežádoucí účinky; 64 (71,9 %) nemocných zaznamenalo více než
50% redukci počtu MMD; redukce mediánu činila 19–4 dny.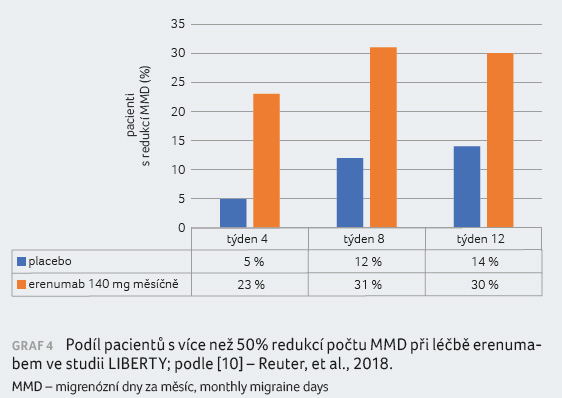
Galkanezumab
Studie CONQUER sledovala účinky
galkanezumabu u pacientů s epizodickou a chronickou
migrénou, kteří měli za měsíc minimálně čtyři dny
s migrénou a alespoň jeden den v měsíci bez
bolesti po dobu posledních tří měsíců [11]. Podmínkou
vstupu do studie byly 2–4 předchozí neúspěšné
preventivní léčby. Primárním cílovým ukazatelem byla průměrná
změna od výchozí hodnoty v počtu MMD po tříměsíční
léčbě galkanezumabem. Sekundární cílové ukazatele
představovaly podíl počtu nemocných s více než 50%, 75%
a 100% redukcí počtu MMD a změna skóre MSQ RFR
(Migraine Specific Quality of Life Questionnaire role
function restrictive) ve třetím měsíci. Galkanezumab
redukoval počet MMD v průměru o 4,1 (placebo o jeden
den; p < 0,0001), graf 6.
Všechny rozdíly oproti placebu jsou statisticky signifikantní.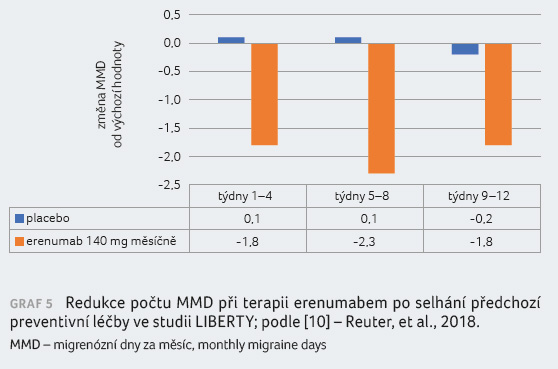
Tabulka 2 shrnuje charakteristiky a výsledky vybraných klinických studií.
Klinická data anti CGRP přípravků u pacientů s migrénou a nadužíváním medikace
Definice podle EHF
Nadužívání medikace
(medication overuse, MO): užívání jednoduchých analgetik po více
než 15 dní v měsíci nebo užívání specifických
antimigrenózních přípravků (například triptanů) častěji než
po 10 dní v měsíci.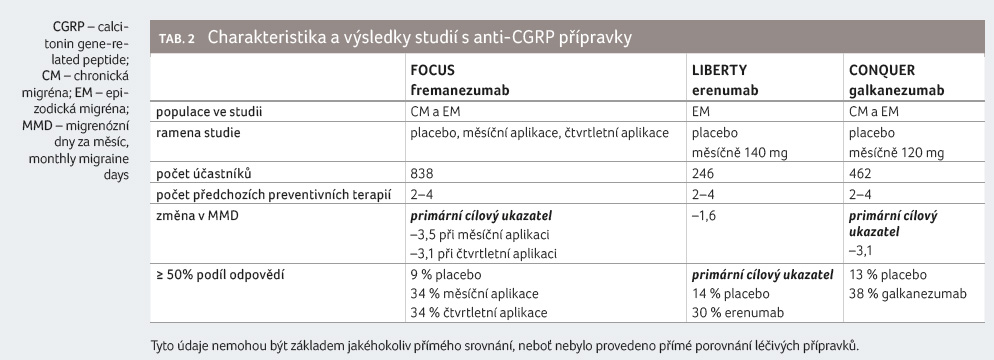
Bolesti hlavy z nadužívání medikace (medication overuse headache, MOH):
- Užívání delší než tři měsíce:
- neopioidní analgetika častěji než 15 dní v měsíci,
- specifická antimigrenika, kombinace analgetik nebo opioidů po více než 10 dní v měsíci.
- Více než 15 dní bolestí hlavy v měsíci u pacientů s již dříve existujícími bolestmi hlavy.
Bolesti hlavy z nadužívání medikace jsou časté, ale u různých populací se jejich četnost výrazně liší. Jako nejméně časté jsou pozorovány v Číně – u 0,6 % populace, v Německu u 1,1 % a nejvyšší v Rusku – u 7,2 %. Zda jsou v pozadí genetické příčiny, či zvyk užívat všechnu předepsanou medikaci, to se lze jen domnívat.
Podle EHF se mají pacientům s MOH nabídnout nejprve anti CGRP monoklonální protilátky a následně je snižována a ukončována akutní medikace. Dříve se doporučoval obrácený postup (guidelines z roku 2019): nejprve ukončit/změnit akutní medikaci a teprve po 2–4týdenní wash out periodě zahájit preventivní léčbu. U obtížně léčitelných pacientů se vážila možnost dosáhnout snížení/ukončení podávání léků (zejména opioidů, benzodiazepinů a barbiturátů) za hospitalizace. Stejně tak se mělo postupovat v přítomnosti komorbidit (deprese) nebo při relapsu po ukončení léčby. Současně je nutné s pacientem spolupracovat na behaviorálních změnách (vyhýbání se spouštěcím faktorům, přiměřená fyzická aktivita, stres management, kognitivně behaviorální terapie apod.).
Nová doporučení pro management MOH
- Edukace a poradenství.
- Preventivní léčba (onabotulotoxin, topiramát nebo anti-CGRP protilátky) při současném zmírňování MO, přičemž je možné aplikaci nadužívaných léků ukončovat postupně (slow tapering).
- Vliv fremanezumabu na MOH – post hoc analýza studií HALO a FOCUS
V těchto studiích nebylo
pacientům poskytováno poradenství ohledně MO a nebyla
prováděna detoxikace, ale byl sledován pouze efekt fremanezumabu
na MO a MOH. U pacientů s chronickou migrénou
a MOH došlo ke statisticky významné redukci počtu dní
se středně těžkou až těžkou bolestí hlavy v prvních 12
týdnech léčby fremanezubamem [12], graf 7. „Před čtyřmi
lety jsme se domnívali, že preventivní léčba u pacientů
s nadužíváním medikace nefunguje,“ vzpomínal profesor
Diener. Podle subanalýzy studie HALO je redukce počtu dní
s bolestí hlavy srovnatelná u pacientů s MO i bez
něj: fremanezumab ve čtvrtletní/měsíční aplikaci dosahuje
50% redukce počtu dní s bolestí hlavy u 41 %/42 %
pacientů bez MO, u nemocných s MO v 35 %/39 %.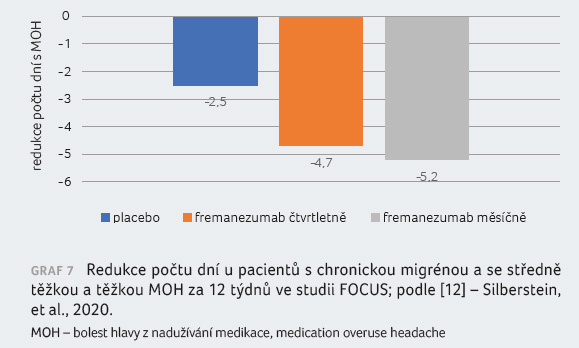
Další otázkou je, jaký podíl pacientů po tříměsíční léčbě fremanezumabem stále spadá do kategorie MO. Ve 12. týdnu léčby došlo k redukci počtu dní s akutní medikací o 9,0, resp. o 8,9. Nadužívání medikace se zbavilo 55 % pacientů léčených fremanezumabem ve čtvrtletní aplikaci a 61 % při měsíční aplikaci (u placeba to bylo 46 %) [12]. V analýze studie FOCUS se prokázalo, že fremanezumab snižuje počet MMD i u pacientů s MO a po selhání 2–4 preventivních léků o 3,7, resp. 4,7 na rozdíl od placeba (rozdíl 0 dní) ve čtvrtém týdnu od první aplikace. Za 12 týdnů činila redukce počtu MMD při léčbě fremanezumabem 3,2, resp. 4,6 (u placeba 0,5) [12].
Erenumab a galkanezumab
Efekt erenumabu u chronické migrény a MO ověřila randomizovaná, dvojitě zaslepená a placebem kontrolovaná studie s 667 pacienty. U nemocných bez MO snížil erenumab počet MMD průměrně o 6,7 (placebo o 4,7) a u nemocných s MO došlo k redukci o 6,6 (u placeba o 4,6). Zajímavé je, že efekt na redukci počtu dní se specifickou léčbou migrény u pacientů s MO nebyl závislý na dávce erenumabu a podobné výsledky vykazovalo dávkování 70 mg erenumabu měsíčně, podobně jako 140 mg erenumabu za měsíc (po třech měsících léčby erenumabem). Stejně tak podíl pacientů s 50% redukcí počtu MMD byl u obou dávkování téměř totožný (36 %, resp. 35 %).
Post hoc analýzy byly provedeny také u galkanezumabu (studie EVOLVE 1 a EVOLVE 2, REGAIN), které prokázaly efekt této léčby i u obtížně léčitelné skupiny pacientů s MO. U nemocných s epizodickou migrénou došlo k redukci počtu MMD průměrně o 6,26 (120 mg měsíčně) a o 5,77 (240 mg měsíčně). U chronické migrény bylo pozorováno snížení počtu MMD o 4,76, resp. o 4,51. Galkanezumab taktéž redukoval podíl nemocných s MO. Výrazným prospěchem z léčby monoklonálními protilátkami zaměřenými proti CGRP je vynikající bezpečnostní profil a nízký výskyt nežádoucích účinků (ve 2–5 %).
Tipy a triky profesora Dienera
Na závěr přidal profesor Diener zkušenosti ze své praxe, poznatky kolegů a nedávno publikovaná RWD.
- Za nejprůkaznější důkaz účinnosti považuje profesor Diener podíl pacientů s 50% redukcí počtu MMD. Alternativou je průměrná redukce počtu MMD. Důležité je sdělení pacienta, zda u něj léčba funguje.
- Efekt léčby je optimální hodnotit nejdříve po třech měsících. U většiny nemocných se efekt projeví již v prvních čtyřech týdnech, ale u některých je nutné čekat déle.
- Podle kolegů profesora Dienera dosahuje podíl pacientů s dosaženou 50% redukcí počtu MMD 60–70 % (RWD), což svědčí o velmi vysoké účinnosti monoklonálních protilátek proti CGRP.
- Za neúčinnou lze monoklonální protilátku u konkrétního pacienta prohlásit ne dříve než po třech měsících léčby. Bohužel neexistuje jednoduchý prediktivní marker, který by naznačoval, zda bude efekt léčby dostatečný. Pravděpodobně půjde o genetický podklad neúčinnosti.
- Kdy léčbu ukončit? Pokud je po 12 měsících dosaženo nízké frekvence migrenózních záchvatů, můžeme se pokusit léčbu ukončit. Pokud dojde k návratu k původnímu stavu před léčbou, pak je namístě s léčbou začít znovu.
- Anti CGRP monoklonální protilátky lze kombinovat s tradiční preventivní léčbou, tyto lékové třídy neinteragují a nesnižují svou účinnost.
- Diskutovanou otázkou je možná interakce nových gepantů s monoklonálními protilátkami, ale předběžná data naznačují, že půjde o bezpečnou kombinaci.
- Eskalace na vyšší dávku anti CGRP monoklonální protilátky (je li dostupná) může být u suboptimální odpovědi přínosem. Je možné rovněž zkusit použít monoklonální protilátku, která cílí na jinou strukturu (receptor vs. ligand), pokud je zvolená alternativa neúčinná (RWD).
- Při volbě měsíčního versus čtvrtletního dávkovacího schématu představuje pro pacienta tříměsíční injekce komfortnější variantu.
- Nejčastějším důvodem k ukončení léčby u erenumabu je obstipace (objeví se u 20 % léčených), proto je dobré tomuto příznaku věnovat pozornost, chceme li erenumab doporučit.
Redakčně zpracovala MUDr. Marta Šimůnková
Seznam použité literatury
- [1] May A, Schulte LH. Chronic migraine: risk factors, mechanisms and treatment. Nat Rev Neurol 2016; 12: 455‒464.
- [2] Bigal M. Migraine chronification‑concept and risk factors. Discov Med 2009; 8: 145‒150.
- [3] Lipton RB, Munjal S, Buse DC, et al. Predicting Inadequate Response to Acute Migraine Medication: Results From the American Migraine Prevalence and Prevention (AMPP) Study. Headache 2016; 56: 1635‒1648.
- [4] SPC Ajovy. Dostupné na: https://www.ema.europa.eu/en/documents/product‑information/ajovy‑epar‑product‑information_cs.pdf
- [5] SPC Aimovig. Dostupné na: https://www.ema.europa.eu/en/documents/product‑information/aimovig‑epar‑product‑information_cs.pdf
- [6] SPC Emgality. Dostupné na: https://www.ema.europa.eu/en/documents/product‑information/emgality‑epar‑product‑information_cs.pdf
- [7] SPC Vyepti, FDA. Dostupné na: https://www.accessdata.fda.gov/drugsatfda_docs/label/2020/761119s000lbl.pdf
- [8] Ferrari MD, Diener HC, Ning X, et al. Fremanezumab versus placebo for migraine prevention in patients with documented failure to up to four migraine preventive medication classes (FOCUS): a randomised, double‑blind, placebo‑controlled, phase 3b trial. Lancet 2019; 394: 1030‒1040.
- [9] Pazdera L, Ning X, Galic M, et al. Efficacy of fremanezumab in patients with migraine and documented inadequate response to 2, 3, or 4 classes of migraine preventive treatments: results of the international, multicentre, randomised, placebo‑controlled FOCUS study. 13th European Headache Congress 2019; Athens, Greece; e‑Poster 020.
- [10] Reuter U, Goadsby PJ, Lanteri‑Minet M, et al. Efficacy and tolerability of erenumab in patients with episodic migraine in whom two‑to‑four previous preventive treatments were unsuccessful: a randomised, double‑blind, placebo‑controlled, phase 3b study. Lancet 2018; 392: 2280‒2287.
- [11] Mulleners WM, Kim B‑K, Láinez MJA, et al. Safety and efficacy of galcanezumab in patients for whom previous migraine preventive medication from two to four categories had failed (CONQUER): a multicentre, randomised, double‑blind, placebo‑controlled, phase 3b trial. Lancet Neurol 2020; 19: 814‒825.
- [12] Silberstein SD, Cohen JM, Seminerio MJ, et al. The impact of fremanezumab on medication overuse in patients with chronic migraine: subgroup analysis of the HALO CM study. J Head Pain 2020; 21: 114.