Výběr vhodného pacienta pro léčbu sarilumabem
V rámci satelitního sympozia společnosti sanofi‑aventis na letošních Zimních revmatologických dnech, které se konaly 8.–10. ledna 2020 v Ostravě, se prof. MUDr. Ladislav Šenolt, Ph.D., z Revmatologického ústavu v Praze věnoval tématu identifikace vhodného pacienta pro terapii sarilumabem (Kevzara). Druhou přednášku, jež byla součástí sympozia, zpracoval její autor prof. MUDr. Karel Pavelka, DrSc., do podoby samostatného článku, který rovněž publikujeme v aktuálním čísle časopisu.
„Možná už za několik let by
mohli mít nejen revmatologové k dispozici možnost analýzy
velkého RNA profilu, jenž by nám na počátku nemoci pomohl
identifikovat pacienty, kteří budou odpovídat, nebo naopak nebudou
dostatečně odpovídat na terapii konkrétním lékem,“ uvedl
hypotézou svoji přednášku profesor Šenolt. „Zatím není ani
v běžné klinické praxi reálné, abychom se řídili nedávno
popsanou znalostí tří základních typů synoviální tkáně,
v nichž lze podle počtu imunitních buněk odhadnout
pacientovu horší či lepší odpověď na terapii konkrétním
přípravkem – pauciimunitní fibroidní profil synoviální
tkáně představuje riziko zvýšené rezistence k léčbě,“
doplnil přednášející [1]. Následně představil účastníkům
sympozia kazuistiku, na níž ukázal postup při výběru
vhodného léku pro daného pacienta.
Kazuistika
Žena (narozená 1953) s poměrně nevýznamnou osobní anamnézou (asymptomatický prolaps mitrální chlopně v roce 2000, redukční plastika prsů v roce 2004) byla v listopadu 2015 v ambulanci časné artritidy Revmatologického ústavu vyšetřena pro kloubní obtíže. U nemocné byla zjištěna artritida tří malých kloubů se zvýšenými hodnotami reaktantů akutní fáze zánětu a s vysoce pozitivními autoprotilátkami. „Prakticky každý pacient s nově zjištěnou revmatoidní artritidou (RA) je podle doporučených postupů vhodným adeptem pro léčbu metotrexátem a většina pacientů na včas podaný lék odpovídá dobře. Nicméně přibližně třetina nemocných vyžaduje změnu iniciálně zavedené léčby během prvního roku,“ vysvětlil k volbě vhodného léku profesor Šenolt.
Tato pacientka byla zařazena do lékového hodnocení a měla to štěstí, že mohla být v časné fázi onemocnění léčena abataceptem v kombinaci s metotrexátem. Po dvouleté terapii se nacházela v kompletní remisi, při kontrolním vyšetření, kdy už biologickým lékem nebyla léčena, však nastala exacerbace onemocnění (polyartritida, bolesti kloubů, únava). Pacientce byla navýšena dávka metotrexátu na 25 mg týdně a došlo ke zlepšení klinického stavu. Pro následné zhoršení klinického stavu bylo provedeno lokální ošetření vybraných kloubů glukokortikoidem a léčba byla optimalizována o aplikaci metotrexátu parenterálně. Finálně byla podána žádost o biologickou terapii. Při kontrole o měsíc později byla u nemocné zaznamenána úleva na ošetřených kloubech, ale nastala exacerbace nemoci na ostatních kloubních lokalitách, byla zjištěna vysoká aktivita nemoci podle indexu DAS28 CRP (Disease Activity Score) 6,48; byla naměřena vysoká hodnota C reaktivního proteinu (CRP 48 mg/l). Stav byl uzavřen jako selhání léčby metotrexátem a pacientce byl podáván leflunomid v kombinaci s glukokortikoidem – při této léčbě došlo k mírnému zlepšení, avšak nemocná měla stále aktivní onemocnění, šest aktivních kloubů a vysokou hodnotu CRP.
V září 2018 byla zahájena léčba biosimilárním etanerceptem v dávce 50 mg s.c. v kombinaci s leflunomidem v dávce 20 mg. Po třech měsících této terapie neměla nemocná žádný aktivní kloub a subjektivně se cítila dobře, podle DAS28 CRP byla navozena remise choroby. Na jaře 2019 musela být kvůli nežádoucím účinkům léčba leflunomidem ukončena. Po půlroce monoterapie biosimilárním etanerceptem došlo k exacerbaci choroby do podobného stavu jako před zahájením biologické léčby: artritidou bylo zasaženo 11 kloubů z 28 hodnocených, nemocná si stěžovala na těžkou únavu a dlouhou ranní ztuhlost a v laboratoři byly zjištěny vysoké hodnoty reaktantů akutní fáze zánětu. Z tohoto důvodu byla indikována změna biologického přípravku a pro pacientku byla vybrána terapie sarilumabem v dávce 200 mg s.c. každé dva týdny. Sarilumab ovlivňuje signalizaci interleukinu 6 (IL 6, pleiotropní prozánětlivý cytokin produkovaný jak makrofágy, tak synoviálními fibroblasty). Působí na imunitní i rezidentní buňky, ovlivňuje nejen zánět, ale pravděpodobně působí rovněž v oblasti centrální senzitizace bolesti [2‒6]. Po měsíci léčby sarilumabem měla pacientka projevy artritidy u jednoho kloubu, aktivita nemoci podle DAS28 CRP klesla na hodnotu 2,48 a po třech měsících léčby (prosinec 2019) se nemocná nacházela v hluboké remisi s minimálními známkami onemocnění ‒ DAS28 CRP 1,27, nebyl žádný aktivní kloub, hodnoty reaktantů akutní fáze zánětu byly normální. Pacientka tedy splňovala kritéria zlepšení pro pokračování v biologické terapii.
Manifestace choroby spojené s interleukinem 6
„Správná individualizace léčby je stále problematická. Je nutné identifikovat takovou skupinu pacientů, u nichž lék nebude toxický a bude účinný, to je však v praxi velmi složité a nemáme k tomu jednoznačné návody,“ okomentoval profesor Šenolt. „U dané pacientky jsme postupovali podle doporučených postupů pro léčbu RA, byl zvolen biosimilární etanercept, který byl farmakoekonomicky výhodný a obdobně účinný jako ostatní přípravky. Nevíme ale, jak dlouho a jak konkrétně bude účinkovat u vybraného pacienta. Víme pouze to, že pokud má pacient systémové příznaky, trpí anémií, únavou nebo většími bolestmi kloubů, může mít prospěch z léků, které ovlivňují právě IL 6,“ doplnil přednášející. Řada pacientů s RA má příznaky, které jsou určitým způsobem spjaty se signalizací IL 6 [7‒12]:
- únava (až 90 % pacientů s RA),
- anémie (přibližně u 30 % pacientů s RA),
- zvýšená hodnota CRP (přibližně u 30 % pacientů s RA),
- ranní ztuhlost (přibližně u 50 % pacientů s RA, kteří jsou v remisi nebo mají nízkou aktivitu choroby),
- středně silná až silná bolest (přibližně u 80 % pacientů s RA).
V některých případech je únava
pacientů s RA přirovnávána k únavě, kterou udávají
onkologičtí pacienti, rovněž sociální konsekvence jsou
u pacientů s RA v některých aspektech horší než
u onkologických pacientů [13]. Například z francouzské
kohorty pacientů s časnou RA téměř polovina udávala
na počátku sledování únavu, která byla při léčbě
redukována zhruba na čtvrtinu, více než každý pátý
pacient udával rezistentní únavu po celou dobu pětiletého
sledování [14]. V klinických studiích se sarilumabem
u pacientů, kteří nedostatečně odpovídali na metotrexát
nebo na konvenční syntetické chorobu modifikující léky
(MOBILITY, TARGET), nebo ve studii porovnávající adalimumab
se sarilumabem (MONARCH) byl prokázán lepší efekt sarilumabu
na zmírnění únavy oproti placebu a statisticky
nevýznamně i oproti adalimumabu [15‒17], graf 1.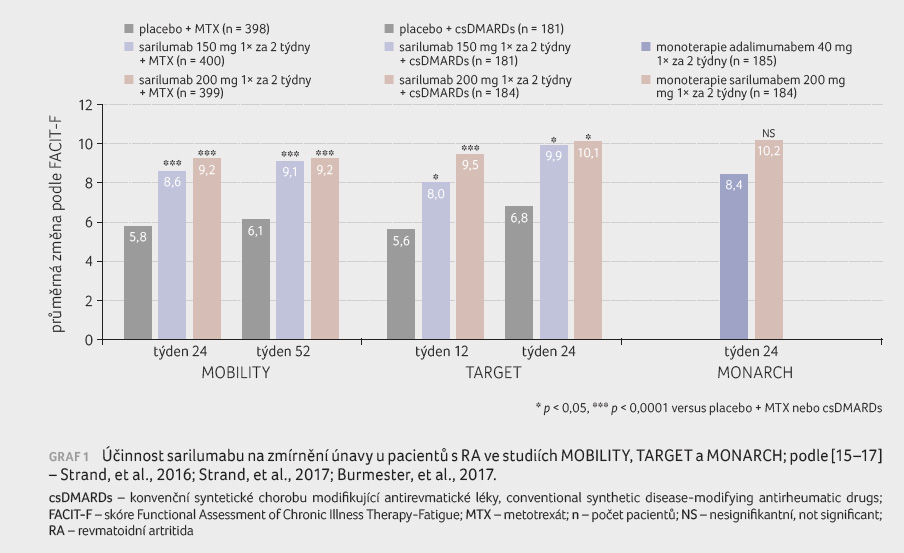
S únavou je spojena anémie, při níž hepcidin (peptidový hormon, který je syntetizován v játrech a indukován prozánětlivými cytokiny, převážně IL 6) znemožňuje uvolňování železa z buněk, zejména z enterocytů a z makrofágů. Hepcidin je tedy zodpovědný za anémii, která reflektuje systémové projevy a aktivitu RA, má také vztah k funkční disabilitě, a dokonce předurčuje RTG progresi, jež jde většinou ruku v ruce se zánětlivou aktivitou onemocnění [18‒22]. Při podávání sarilumabu ve studii MOBILITY bylo zjištěno, že dochází k pozitivním změnám hodnot hemoglobinu v průběhu celých 52 týdnů sledování oproti placebu, ve studii MONARCH byla zaznamenána významná změna v koncentracích hemoglobinu oproti adalimumabu [23‒25].
Revmatoidní artritida je asociována se systémovým zánětem, který může do jisté míry ovlivňovat centrální senzitizaci. Prozánětlivé cytokiny, zejména IL 6, působí na tři úrovně v oblasti adenohypofýzy a tyto procesy pak zapříčiňují větší míru bolesti a únavy. Padesátiprocentní a větší redukce míry bolesti byla pozorována u pacientů ve studiích MOBILITY, TARGET a MONARCH jak oproti placebu, tak oproti adalimumabu. Čas dosažení minimálně 50% redukce bolesti byl rychlejší při léčbě sarilumabem oproti placebu a oproti adalimumabu [26], graf 2.
V případě ranní ztuhlosti byly
ve studiích TARGET a MONARCH doloženy na základě
změn na škále VAS rozdíly ve prospěch sarilumabu
oproti placebu a oproti adalimumabu [15,16]. Necelá třetina
pacientů se střední a nízkou aktivitou nemoci má zvýšenou
hodnotu CRP, na druhou stranu u některých pacientů
s vysokou aktivitou onemocnění je zaznamenána nízká hodnota
[11,12]. Existuje tedy přibližně třetina pacientů s vysokým
CRP se systémovým zánětem, kteří mohou být vhodnými kandidáty
pro léčbu blokátory IL 6. U pacientů, u nichž
v rámci studie MOBILITY selhala léčba metotrexátem, byl
prokázán větší efekt sarilumabu na snížení hodnoty CRP
oproti placebu, ve studii TARGET byla redukce významnější
u sarilumabu oproti adalimumabu (větší pokles CRP v průběhu
půlročního sledování) [17,24,27].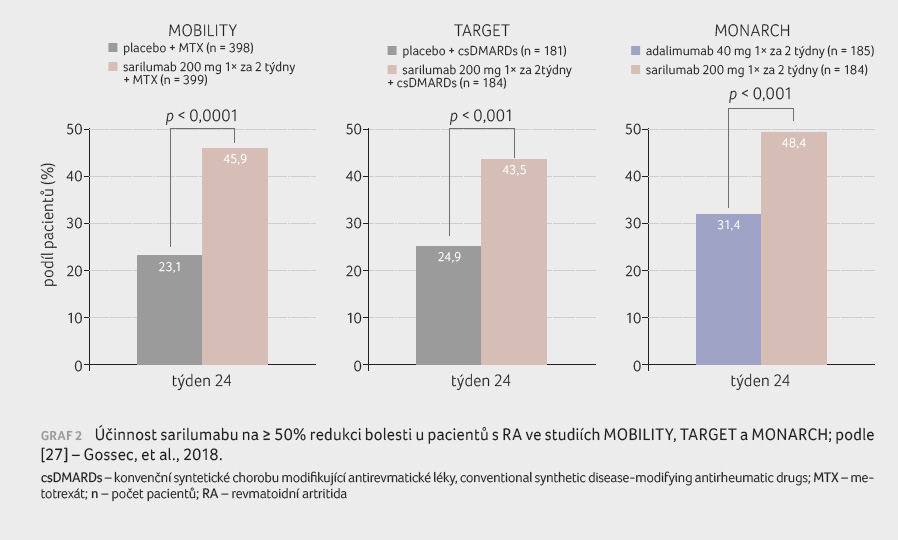
„Zejména anémie a hodnota CRP jsou u pacientů s RA predisponujícími faktory pro výběr léku, který ovlivňuje signalizaci IL 6. Máme tedy k dispozici alespoň určité klinické ukazatele, jež nám mohou pomoci identifikovat skupinu pacientů se známkami systémového zánětu a anémií, kteří mohou lépe odpovídat na přípravky s uvedeným mechanismem účinku,“ uzavřel profesor Šenolt.
Redakčně zpracovala PhDr. Nikola
Homolová Richtrová
Seznam použité literatury
- [1] Lewis MJ, Barnes MR, Blighe K, et al. Molecular Portraits of Early Rheumatoid Arthritis Identify Clinical and Treatment Response Phenotypes. Cell Rep 2019; 28: 2455‒2470.
- [2] Chomarat P, Banchereau J, Davoust J, Palucka AK. IL‑6 switches the differentiation of monocytes from dendritic cells to macrophages. Nat Immunol 2000; 1: 510–514.
- [3] Choy E. Understanding the dynamics: pathways involved in the pathogenesis of rheumatoid arthritis. Rheumatology (Oxford) 2012; 51(Suppl 5): v3–v11.
- [4] Castell JV, Gomez‑Lechon MJ, David M, et al. Recombinant human interleukin 6 (IL‑6/BSF‑2/HSF) regurates the synthesis of acute phase proteins in human hepatocytes. FEBS Lett 1988; 232: 347–350.
- [5] Imai T, Koike K, Kubo T, et al. Interleukin‑6 supports human megakaryocytic proliferation and differentiation in vitro. Blood 1991; 78: 1969–1974.
- [6] SchellerJ, Garbers C, Rose‑John S. Interleukin‑6: from basic biology to selective blockade of pro‑inflammatory activities. Semin Immunol 2014; 26: 2–12.
- [7] Hewlett S, Hehir M, Kirwan JR. Measuring fatigue in rheumatoid arthritis: a systematic review of scales in use. Arthritis Rheum 2007; 57: 429–439.
- [8] Dayer JM, Choy E. Therapeutic targets in rheumatoid arthritis: the interleukin‑6 receptor. Rheumatology 2010; 49: 15–24.
- [9] Taylor P, Manger B, Alvaro‑Gracia J, et al. Patient perceptions concerning pain management in the treatment of rheumatoid arthritis. J Int Med Res 2010; 38: 1213–1224.
- [10] Khan NA, Yazici Y, Calvo‑Alen J, et al. Reevaluation of the role of duration of morning stiffness in the assessment of rheumatoid arthritis activity. Rheumatol 2009; 36: 2435–2442.
- [11] Kay J, Morgacheva O, Messing SP, et al. Clinical disease activity and acute phase reactant levels are discordant among patients with active rheumatoid arthritis: acute phase reactant levels contribute separately to predicting outcome at one year. Arthritis Res Ther 2014; 16: R40.
- [12] Graf J, Scherzer R, Grunfeld C, Imboden J. Levels of C‑reactive protein associated with high and very high cardiovascular risk are prevalent in patients with rheumatoid arthritis. PLoS ONE 2009; 4: e6242.
- [13] Kuipers JG, Koller M, Rueffer U, et al. Fatigue in Patients with Rheumatoid Arthritis As Compared to Different Groups of Cancer Patients. ACR 2018; Abstr 1387. Dostupné na: https://acrabstracts.org/
- [14] Rodriguez‑Muguruza S, Combe B, Gullemin F, et al. Predictors of Fatigue and Persistent Fatigue in Early Rheumatoid Arthritis: A Longitudinal Observational Study. ACR 2018; Abstr 1507. Dostupné na: https://acrabstracts.org/
- [15] Strand V, Kosinski M, Chen CI, et al. Sarilumab plus methotrexate improves patient‑reported outcomes in patients with active rheumatoid arthritis and inadequate responses to methotrexate: results of a phase III trial. Arthritis Res Ther 2016; 18: 198.
- [16] Strand V, Reaney M, Chen CI, et al. Sarilumab improves patient‑reported outcomes in rheumatoid arthritis patients with inadequate response/intolerance to tumour necrosis factor inhibitors. RMD Open 2017; 3: e000416.
- [17] Burmester GR, Yong L, Patel R, et al. Efficacy and safety of sarilumab monotherapy versus adalimumab monotherapy for the treatment of patients with active rheumatoid arthritis (MONARCH): a randomised, double‑blind, parallel‑group phase III trial. Ann Rheum Dis 2017; 76: 840–847.
- [18] Moreland LW, Curtis JR. Systemic nonarticular manifestations of rheumatoid arthritis: focus on inflammatory mechanisms. Semin Arthritis Rheum 2009; 39: 132–143.
- [19] Nemeth E, Rivera S, Gabayan V, et al. IL‑6 mediates hypoferremia of inflammation by inducing the synthesis of the iron regulatory hormone hepcidin. J Clin Invest 2004; 113: 1271–1276.
- [20] Han C, Rahman MU, Doyle MK, et al. Association of anemia and physical disability among patients with rheumatoid arthritis. J Rheumatol 2007; 34: 2177‒2182.
- [21] Möller B, Scherer A, Förger F, et al. Anaemia may add information to standardised disease activity assessment to predict radiographic damage in rheumatoid arthritis: a prospective cohort study. Ann Rheum Dis 2014; 73: 691‒696.
- [22] van Steenbergen HW, van Nies A, van der Helm‑van Mil AH, et al. Anaemia to predict radiographic progression in rheumatoid arthritis. Ann Rheum Dis 2013; 72: e16.
- [23] Dougados M, Choy EH, Kameda H, et al. IL‑6R Blockade with Sarilumab Plus Methotrexate Results in Changes in Clinical and Laboratory Parameters Associated with Chronic Inflammation in Patients with Moderate‑to‑Severe RA in a Phase 3 Study. ACR 2015; Abstr 2761. Dostupné na: https://acrabstracts.org/
- [24] Genovese MC, Smolen JS, Weinblatt ME, et al. Efficacy and Safety of ABT‑494, a Selective JAK‑1 Inhibitor, in a Phase IIb Study in Patients With Rheumatoid Arthritis and an Inadequate Response to Methotrexate. Arthritis Rheumatol 2016; 68: 2857–2866.
- [25] Burmester GR, Hagino O, Dong Q, et al. Unique Changes in Hemoglobin with Sarilumab Versus Adalimumab Are Independent of Better Disease Control in Patients with Rheumatoid Arthritis (RA). ACR/ARHP 2018; Abstr 1528. Dostupné na: https://www.acrabstracts.org/
- [26] Gossec L, Boclage S, St. John G, et al. Pain Is Improved in Around 50% of Patients and Fatigue in 40% of Patients with Rheumatoid Arthritis Treated with Sarilumab in the Target, Mobility and Monarch Trials. ACR/ARHP 2018; Abstr 1523. Dostupné na: https://www.acrabstracts.org/
- [27] Fleischmann R, Genovese MC, Lin Y, et al. Long‑term safety of sarilumab in rheumatoid arthritis: an integrated analysis with up to 7 years’ follow‑up. Arthritis Rheumatol 2017; 69: 277–290.