Aktivita ceftarolinu in vitro vůči izolátům vyvolávajícím komplikované infekce kůže a měkkých tkání v České republice v roce 2012
Ceftarolin fosamil je cefalosporinové antibiotikum s aktivitou vůči grampozitivním i gramnegativním mikrobům. Účinnost tohoto antibiotika byla sledována v 15 laboratořích České republiky u 921 izolátů vyvolávajících infekce kůže a měkkých tkání. Hodnoty minimální inhibiční koncentrace (MIC) byly stanoveny pomocí E-testu. Ceftarolin vykazoval velmi dobrou účinnost (MIC50/90 0,25 mg/l) vůči kmenům Staphylococcus aureus citlivým k oxacilinu/meticilinu (n = 339) i vůči 118 kmenům rezistentním k oxacilinu/meticilinu (MIC50 0,5 mg/l; MIC90 1 mg/l). Excelentní aktivita byla zjištěna také vůči betahemolytickým streptokokům (Streptococcus pyogenes, Streptococcus agalactiae a Streptococcus dysgalactiae subsp. equisimilis). Kmeny enterobakterií (n = 340) byly inhibovány koncentrací ? 0,5 mg/l, výjimku tvořilo několik izolátů druhu Klebsiella pneumoniae (n = 2) a Citrobacter freundii (n = 3), jejichž hodnoty MIC se pohybovaly v rozmezí 1–16 mg/l. Tyto výsledky potvrzují dobrou aktivitu ceftarolinu in vitro vůči mikrobům vyvolávajícím infekce kůže a měkkých tkání v České republice.
Spolupracovníci:
MUDr. Václava Adámková, Antibiotické středisko VFN Praha;
MUDr. Markyta Bártová, Antibiotické středisko Fakultní Thomayerovy nemocnice, Praha;
MUDr. Nataša Bartoníková, Antibiotické středisko Nemocnice Tomáše Bati, Zlín;
MUDr. Eva Bendová, CSc., Antibiotické středisko FNKV, Praha;
MUDr. Tamara Bergerová, Oddělení bakteriologie FN Plzeň;
MUDr. Markéta Hanslianová, Oddělení klinické mikrobiologie FN Brno;
MUDr. Magdalena Horníková, Antibiotické středisko Nemocnice České Budějovice;
MUDr. Blanka Horová, Antibiotické středisko Nemocnice na Bulovce, Praha;
RNDr. Eva Chmelařová, Antibiotické středisko, Zdravotní ústav Ostrava;
prof. MUDr. Milan Kolář, Ph.D., Antibiotické středisko FN Olomouc;
MUDr. Vojtěch Hanulík, Antibiotické středisko FN Olomouc;
MUDr. Otakar Nyč, Ph.D., Antibiotické středisko FN Motol, Praha;
MUDr. Vladimír Petkov, Oddělení klinické mikrobiologie IKEM, Praha;
MUDr. Lenka Ryšková, Antibiotické středisko FN Hradec Králové;
MUDr. Marta Štolbová, Oddělení klinické mikrobiologie Masarykovy nemocnice Ústí nad Labem;MUDr. Renata Tejkalová, Antibiotické středisko FN U sv. Anny Brno
Úvod
Ceftarolin fosamil, respektive jeho aktivní metabolit ceftarolin, je cefalosporinové antibiotikum určené k parenterálnímu podání pro léčbu akutních bakteriálních infekcí kůže a měkkých tkání a komunitní bakteriální pneumonie [1–3]. Ceftarolin je účinný vůči grampozitivním bakteriím včetně kmenů Staphylococcus aureus rezistentních k oxacilinu/meticilinu (MRSA) i vůči gramnegativním bakteriím z čeledi Enterobacteriaceae (vyjma kmenů produkujících širokospektrou betalaktamázu – ESBL, AmpC betalaktamázu a karbapenemázu) [3–5].
Obdobně jako je tomu u dalších betalaktamových antibiotik, je antibakteriální aktivita ceftarolinu zprostředkována vazbou na esenciální PBP (penicillin-binding proteins) a následnou inhibicí syntézy buněčné stěny mikroba. Unikátní vlastností ceftarolinu je jeho afinita k PBP2a proteinům, jejichž syntéza je řízena mecA genem a které jsou typické pro kmeny MRSA [3, 5].
Klinické studie zaměřené na sledování terapeutického efektu ceftarolinu pro léčbu akutních bakteriálních infekcí kůže a měkkých tkání (acute bacterial skin and skin structure infections, ABSSSI) a komunitní bakteriální pneumonie (community-acquired bacterial pneumonia, CABP) potvrdily srovnatelnou klinickou účinnost tohoto antibiotika s použitými komparátory (vankomycin + aztreonam v případě léčby ABSSSI a ceftriaxon v léčbě CABP) vůči těmto infekcím způsobeným grampozitivními i gramnegativními původci [6–8].
Na základě výsledků klinických studií zaregistroval v říjnu 2010 americký úřad Food and Drug Administration (FDA) ceftarolin fosamil pro léčbu ABSSSI způsobených citlivými izoláty mikroorganismů Staphylococcus aureus (včetně MRSA), Streptococcus pyogenes, Streptococcus agalactiae, Escherichia coli, Klebsiella pneumoniae a Klebsiella oxytoca a pro léčbu CABP vyvolanou Streptococcus pneumoniae (včetně bakteriemické formy pneumonie), Staphylococcus aureus (pouze kmeny citlivé k oxacilinu/meticilinu), Haemophilus influenzae, Klebsiella pneumoniae, Klebsiella oxytoca a Escherichia coli [1].
European Medicines Agency (EMA) schválila v září 2012 ceftarolin fosamil pro nitrožilní léčbu komplikovaných infekcí kůže a měkkých tkání a komunitní pneumonie u dospělých pacientů [2].
V této práci jsou předloženy výsledky vyšetření účinnosti ceftarolinu in vitro v souboru klinicky relevantních recentních izolátů bakterií z rodu Streptococcus, Staphylococcus a čeledi Enterobacteriaceae (Escherichia, Klebsiella, Enterobacter, Citrobacter, Morganella a Proteus), které byly získány v 15 laboratořích České republiky.
Materiál a metody
Laboratoře
V průběhu jednoho měsíce (od 1. 5. do 31. 5. 2012) byla v 15 mikrobiologických laboratořích lokalizovaných obvykle v nemocnicích terciárního typu napříč celou Českou republikou vyšetřována citlivost k ceftarolinu u požadovaných druhů bakterií a tyto údaje byly spolu s informací o původu izolátu zaznamenávány do protokolu.
Bakterie
Vyšetřovaný soubor zahrnoval bakteriální izoláty vyvolávající komplikované infekce kůže a měkkých tkání získané z krve, ze stěru z rány nebo hnisu. Každá laboratoř měla shromáždit celkem 63 izolátů zahrnujících 30 kmenů Staphylococcus aureus (z toho 10 MRSA); 5 kmenů Escherichia coli, Klebsiella pneumoniae a Klebsiella oxytoca, 2 kmeny Citrobacter freundii, Citrobacter koseri, Proteus mirabilis, Morganella morganii a Enterobacter cloacae; 3 kmeny Streptococcus pyogenes a Streptococcus agalactiae a po třech kmenech Streptococcus dysgalactiae. Opakované izoláty kmenů stejného druhu od jednoho pacienta byly vyloučeny, dále byly vyloučeny kmeny Enterobacteriaceae produkující širokospektrou betalaktamázu (ESBL). Všechny kmeny C. freundii, C. koseri a S. dysgalactiae izolované v laboratořích byly zaslány do Národní referenční laboratoře pro antibiotika (NRL/ATB) k ověření identifikace a k vyšetření minimální inhibiční koncentrace (MIC) ceftarolinu. K retestaci byly NRL/ATB dále vyžadovány kmeny, které se jevily jako necitlivé k ceftarolinu při primárním testování v lokální laboratoři.
Vyšetřování citlivosti
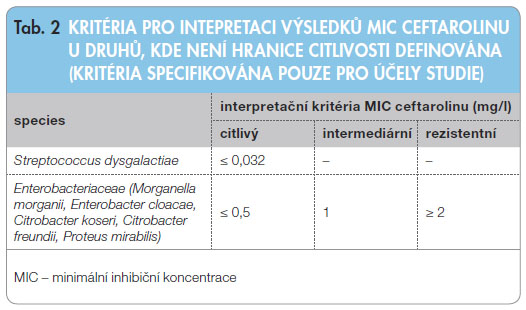
 MIC ceftarolinu u vyšetřovaného souboru kmenů byly stanoveny E-testem podle pokynů výrobce [9]. Hranice citlivosti (breakpointy, BP) pro interpretaci výsledků citlivosti jsou uvedeny v tab. 1 a tab. 2.
MIC ceftarolinu u vyšetřovaného souboru kmenů byly stanoveny E-testem podle pokynů výrobce [9]. Hranice citlivosti (breakpointy, BP) pro interpretaci výsledků citlivosti jsou uvedeny v tab. 1 a tab. 2. Kontrola kvality vyšetření citlivosti
Kvalita vyšetření MIC byla ověřována kontrolními kmeny se známou citlivostí k ceftarolinu. Přípustné rozmezí MIC ceftarolinu u Staphylococcus aureus CNCTC 5480 (ATCC 25213) je 0,125–0,5 mg/l, u Escherichia coli CNCTC 5276 (ATCC 29922) 0,032–0,125 mg/l a u Streptococcus pneumoniae CNCTC 2043 (ATCC 49619) 0,008–0,032 mg/l [1].
Výsledky
Zúčastněné laboratoře shromáždily celkem 926 kmenů, pro další analýzu byl ze souboru vyřazen druh C. koseri, kde se podařilo v průběhu studie shromáždit pouze 5 kmenů tohoto druhu. Druhové zastoupení a původ kmenů uvádí tab. 3.
Účinnost ceftarolinu u vyšetřovaného souboru bakterií je v tab. 4 prezentována jako rozmezí MIC, MIC50 a MIC90 (koncentrace, které inhibují 50 %, respektive 90 % kmenů). Výsledky MIC vyšetřené E-testem, který obsahuje další 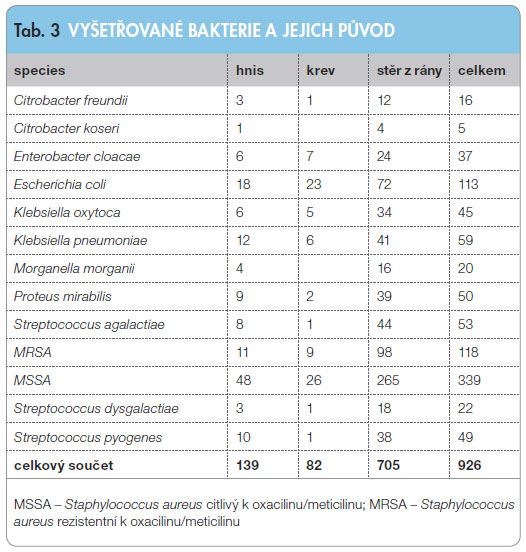
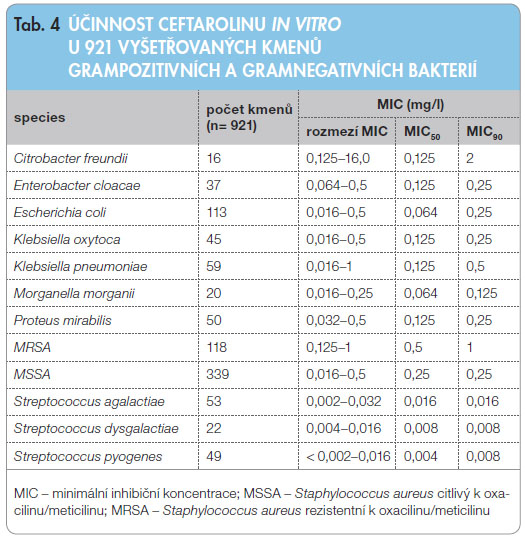 hodnoty MIC oproti klasické geometrické řadě používané ve standardní diluční metodě stanovení MIC, byly pro vyhodnocení zaokrouhleny na vyšší hodnotu v případě, že se naměřená hodnota pohybovala v rozmezí dvojnásobné geometrické řady.
hodnoty MIC oproti klasické geometrické řadě používané ve standardní diluční metodě stanovení MIC, byly pro vyhodnocení zaokrouhleny na vyšší hodnotu v případě, že se naměřená hodnota pohybovala v rozmezí dvojnásobné geometrické řady.
Výsledky u grampozitivních bakterií
(S. aureus, S. pyogenes, S. agalactiae,
S. dysgalactiae subsp. equisimilis)
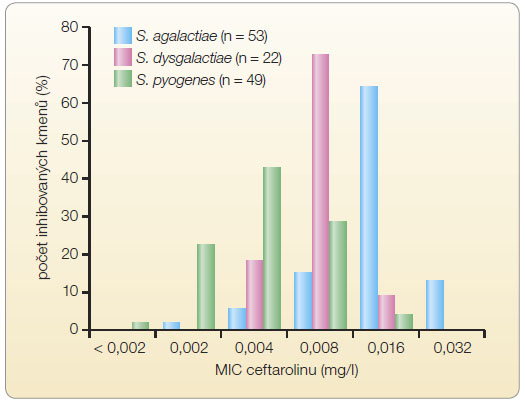
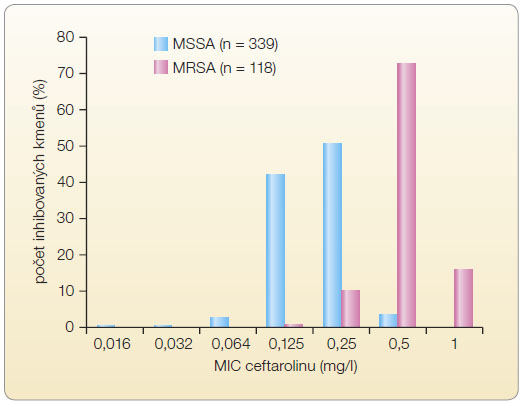 Nejvyšší hodnota MIC ceftarolinu vůči kmenům S. aureus bez ohledu na citlivost k oxacilinu/meticilinu byla 1 mg/l, graf 1. Hodnoty MIC50 a MIC90 byly u kmenů S. aureus citlivých k oxacilinu/meticilinu (MSSA) identické (0,25 mg/l). U kmenů MRSA byly hodnoty MIC50 a MIC90 oproti MSSA vyšší (MIC50 0,5 mg/l, MIC90 1 mg/l). Ceftarolin vykazoval rovněž velmi dobrou aktivitu vůči betahemolytickým streptokokům (S. pyogenes, S. agalactiae a S. dysgalactiae subsp. equisimilis), graf 2. Nejvyšší hodnota MIC90 byla zjištěna u betahemolytických streptokoků skupiny B (S. agalactiae) – 0,016 mg/l, avšak i tato hodnota je o řád nižší než BP doporučený pro tento druh.
Nejvyšší hodnota MIC ceftarolinu vůči kmenům S. aureus bez ohledu na citlivost k oxacilinu/meticilinu byla 1 mg/l, graf 1. Hodnoty MIC50 a MIC90 byly u kmenů S. aureus citlivých k oxacilinu/meticilinu (MSSA) identické (0,25 mg/l). U kmenů MRSA byly hodnoty MIC50 a MIC90 oproti MSSA vyšší (MIC50 0,5 mg/l, MIC90 1 mg/l). Ceftarolin vykazoval rovněž velmi dobrou aktivitu vůči betahemolytickým streptokokům (S. pyogenes, S. agalactiae a S. dysgalactiae subsp. equisimilis), graf 2. Nejvyšší hodnota MIC90 byla zjištěna u betahemolytických streptokoků skupiny B (S. agalactiae) – 0,016 mg/l, avšak i tato hodnota je o řád nižší než BP doporučený pro tento druh.
Výsledky u gramnegativních bakterií
(E. coli, K. pneumoniae, K. oxytoca, P. mirabilis, E. cloacae, M. morganii, C. freundii)
Nejnižší hodnoty MIC byly zjištěny u druhu M. morganii, následoval druh E. coli, který byl také v souboru vyšetřovaných Enterobacteriaceae nejpočetněji zastoupen (n = 113). Vyšší hodnoty MIC90 byly nalezeny u K. pneumoniae (0,5 mg/l) a C. freundii (2 mg/l). Pouze u těchto dvou druhů se také vyskytly kmeny s intermediární citlivostí k ceftarolinu (MIC = 1 mg/l; C. freundii, n = 1; K. pneumoniae, n = 2) a kmeny rezistentní (MIC ? 2 mg/l; C. freundii, n = 2), graf 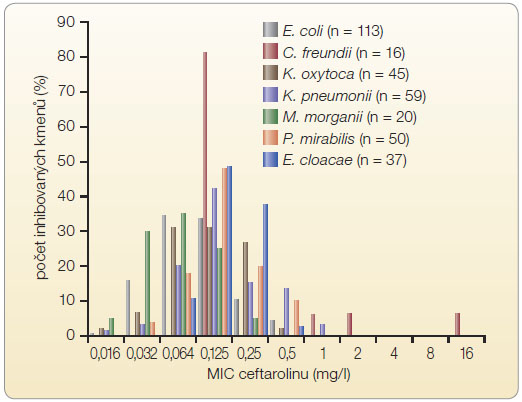 3. U všech necitlivých kmenů (n = 5) byla fenotypovými testy ověřena produkce ESBL a AmpC betalaktamázy. Zatímco příčinou rezistence u kmenů C. freundii byla dereprimovaná produkce AmpC betalaktamázy, u kmenů K. pneumoniae nebyla zjištěna přítomnost uvedených typů betalaktamáz.
3. U všech necitlivých kmenů (n = 5) byla fenotypovými testy ověřena produkce ESBL a AmpC betalaktamázy. Zatímco příčinou rezistence u kmenů C. freundii byla dereprimovaná produkce AmpC betalaktamázy, u kmenů K. pneumoniae nebyla zjištěna přítomnost uvedených typů betalaktamáz.
Celkově bylo do NRL/ATB zasláno 9 kmenů (P. mirabilis, n = 5, K. pneumoniae, n = 2, K. oxytoca, n = 1 a E. cloacae, n = 1), které byly lokálními laboratořemi označeny jako hraničně citlivé nebo rezistentní. Pouze u jediného kmene K. pneumoniae byla v NRL/ATB potvrzena intermediární citlivost k ceftarolinu (MIC 1 mg/l). Vyšší hodnoty MIC naměřené spolupracujícími laboratořemi byly zřejmě zapříčiněny nestandardním inokulem nebo prodloužením inkubační doby.
Diskuse
Ceftarolin je širokospektré cefalosporinové antibiotikum s aktivitou vůči řadě grampozitivních i gramnegativních bakterií. Zatímco indikace použití tohoto antibiotika schválené FDA se omezují jen na několik mikrobiálních druhů, které dominovaly jako původci infekcí ve studiích, kde byla potvrzena klinická účinnost ceftarolinu, u dalších studií aktivity ceftarolinu in vitro byl demonstrován efekt tohoto antibiotika i na další druhy bakterií (S. dysgalactiae, C. koseri, C. freundii, E. cloacae, E. aerogenes, M. morganii, P. mirabilis a koaguláza-negativní stafylokoky). Ty se u nozologických jednotek, pro které byl ceftarolin registrován, také uplatňují a představují tak případný další potenciál tohoto antibiotika [1, 5, 10, 11].
Vzhledem k dlouhodobě příznivému stavu rezistence nejčastějších bakteriálních původců komunitních pneumonií k lékům volby (penicilin, amoxicilin) v ČR byla tato práce zaměřena na sledování účinnosti ceftarolinu vůči mikrobiálním druhům, které se uplatňují u infekcí kůže a měkkých tkání [12]. Výsledky této studie prokázaly aktuálně dobrou účinnost tohoto antibiotika v ČR, necitlivé kmeny se vyskytly jen velmi vzácně (0,5 %).
Dobrá aktivita ceftarolinu vůči MRSA byla potvrzena i v této práci, žádný z testovaných izolátů neměl MIC vyšší než 1 mg/l. Jak vyplývá z výsledků multicentrické studie zaměřené na testování účinnosti ceftarolinu in vitro v zemích Evropy a Středního východu v letech 2008–2009, aktivita ceftarolinu vůči MRSA může být patrně ovlivněna i klonálním typem izolátu [10]. Molekulární analýza 53 izolátů MRSA s MIC ceftarolinu 2 mg/l rozdělila tento soubor do 4 klonálních skupin, z nichž dominoval tzv. Brazilský klon (sekvenační typ – ST 239). Tento typ MRSA, rozšířený zejména v 80. letech a náležející mezi typické nemocniční MRSA, se nyní v ČR prakticky nevyskytuje. Příznivá situace ohledně velmi dobré citlivosti MRSA zjištěné v této studii může tedy souviset i s faktem, že v ČR převládá klon MRSA náležející ke klonálnímu komplexu ST 5, u kterého nebyla rezistence k ceftarolinu zatím detekována [10, 13].
Naprostá většina kmenů vyšetřovaných enterobakterií měla nízké hodnoty MIC ceftarolinu. Obdobně jako cefalosporiny 3. generace není ani ceftarolin účinný u kmenů produkujících ESBL a u izolátů Enterobacteriaceae s dereprimovanou produkcí AmpC betalaktamázy [1, 11]. Kmeny s intermediární citlivostí byly zaznamenány u druhů K. pneumoniae a C. freundii, rezistentní izoláty pouze u druhu C. freundii. Zatímco příčinou necitlivosti ceftarolinu u kmenů C. freundii byla právě přítomnost AmpC betalaktamázy, u druhu K. pneumoniae nebyl mechanismus rezistence prokázán. Příčinou může být tzv. inokulový efekt, který u kmenů E. coli a P. mirabilis produkujících klasické betalaktamázy typu TEM nebo SHV a u kmenů K. pneumoniae rezistentních k piperacilinu vede k elevaci MIC ceftarolinu, a to i při použití standardního inokula. U kmenů E. coli a P. mirabilis citlivých k ampicilinu a kmenů K. pneumoniae citlivých k piperacilinu je tento efekt méně výrazný, ale může se rovněž vyskytnout. To zřejmě souvisí se skutečností, že samotný inokulový efekt je dán nejen přítomností enzymu, ale i množstvím produkované betalaktamázy [11].
Výsledky testování ceftarolinu u reprezentativního souboru kmenů potvrdily velmi dobrou účinnost tohoto nového cefalosporinového antibiotika vůči grampozitivním i gramnegativním izolátům bakterií vyvolávajících infekce kůže a měkkých tkání v podmínkách ČR.
Poděkování
Děkujeme společnosti AstraZeneca s.r.o. za poskytnutí E-testů a substance pro projekt testování nového antibiotika in vitro.
Seznam použité literatury
- [1] FDA.gov. Maryland: Teflaro label and approval history. [Updated daily, cited Nov 2010]. Přístupné na: www.accessdata.fda.gov/drugsatfda-docs/label/2011/200237s0011bl.pdf. Navštíveno 3. září 2012.
- [2] EMA.europa.eu: Assessment report – Zinforo – ceftaroline fosamil. [21 June 2012]. Dostupné na: www.ema.europa.eu/docs/en_GB/document_library/EPAR_-_Public_assessment_report/human/002252/WC500132587.pdf. Navštíveno 26. září 2012.
- [3] Ishikawa T, Matsunaga N, Tawada H, et al. TAK-599, a novel N-phosphono type prodrug of anti-MRSA cephalosporin T-91825: synthesis, physicochemical and pharmacological properties. Bioorg Med Chem 2003; 11: 2427–2437.
- [4] Sader HS, Fritsche TR, Kaniga K, et al. Antimicrobial activity and spectrum of PPI-0903M (T-91825), a novel cephalosporin, tested against a worldwide collection of clinical strains. Antimicrob Agents Chemother 2005; 49: 3501–3512.
- [5] Iizawa Y, Nagai J, Ishikawa T, et al. In vitro antimicrobial activity of T-91825, a novel anti-MRSA cephalosporin, and in vivo anti-MRSA activity of its prodrug, TAK-599. J Infect Chemother 2004; 10: 146–156.
- [6] Talbot GH, Thye D, Das A, Ge Y. Phase 2 study of ceftaroline versus standard therapy in treatment of complicated skin and skin structure infections. Antimicrob Agents Chemother 2007; 51: 3612–3616.
- [7] Corey GR, Wilcox M, Talbot GH, et al. Integrated analysis of CANVAS 1 and 2: phase 3 multicenter, randomized, double-blind studies to evaluate the safety and efficacy of ceftaroline versus vancomycin plus aztreonam in complicated skin and skin-structure infections. Clin Infect Dis 2010; 51: 641–650.
- [8] File TM Jr, Low DE, Eckburg PB, et al. Integrated analysis of FOCUS1 and FOCUS 2: randomized, double-blinded, multicenter phase 3 trials of the efficacy and safety of ceftaroline fosamil versus ceftriaxone in patients with community-acquired pneumonia. Clin Infect Dis 2010; 51: 1395–1405.
- [9] E-test application guide. Dostupné na https://techlib.biomerieux.com/wcm/techlib/techlib/documents/docLink/Supplementary_Inserts/30949001-30950000/Supplementary_Inserts_-_16273_-_B_-_en_-_EAG_-_Etest_Application_Guide.pdf
- [10] Morrissey I, Leakey A, Blackman Northwood J. In vitro activity of ceftaroline and comparator antimicrobials against European and Middle East isolates from complicated skin and skin-structure infections collected in 2008–2009. Int J Antimicrob Agents 2012; 40: 227–234.
- [11] Mushtaq S, Warner M, Ge Y, et al. In vitro activity of ceftaroline (PPI-0903M, T-91825) against bacteria with defined resistance mechanisms and phenotypes. J Antimicrob Chemother 2007; 60: 300–311.
- [12] Žemličková H. Antibiotická rezistence bakteriálních původců nejčastějších komunitních infekcí v České republice. První linie 2012; 2: 13–15.
- [13] Nübel U, Dordel J, Kurt K, et al. A Timescale for Evolution, Population Expansion, and Spatial Spread of an Emerging Clone of Methicillin-Resistant Staphylococcus aureus. PLoS Pathog 2010; 6(4): e1000855. doi:10.1371/journal.ppat.1000855.