Klinické aspekty použití dapagliflozinu
Dapagliflozin je první registrovaný inhibitor transportéru SGLT2 společného pro glukózu a sodík. Jeho antidiabetický účinek není vázán na inzulin či inzulinový receptor, proto lze dapagliflozin použít v jakékoliv fázi vývoje diabetu 2. typu a současně v jakékoliv kombinaci s jiným druhem antidiabetické terapie.
Úvod
Diabetes mellitus 2. typu představuje heterogenní skupinu onemocnění, kterou zařazujeme pouze z nedostatku reálné možnosti diferenciace pod společnou nozologickou jednotku, jejímž základním a hlavním symptomem je hyperglykemie, přičemž u pacientů je na rozdíl od diabetu 1. typu zachována sekrece inzulinu. Etiologicky se v různé míře u různých pacientů podílí na rozvoji hyperglykemie inzulinová rezistence (periferních tkání a hepatocytů), kvalitativní a kvantitativní porucha sekrece inzulinu, porucha funkce inkretinové osy a celá řada dalších vlivů. Při dlouhodobé expozici organismu hyperglykemii je důsledek však vždy stejný – vznik a progrese mikrovaskulárních komplikací a akcentace vzniku a rozvoje komplikací makrovaskulárních. Proto, bez ohledu na etiologii, je hyperglykemie vždy cílem intervence.
Přes již podstatně rozšířené možnosti terapie hyperglykemie není možné pokaždé dosáhnout u pacientů cíle terapie – glykemie v normálním rozmezí bez závažných nežádoucích účinků (zejména hypoglykemie). Pro nové skupiny antidiabetik, které byly vyvinuty, jsou hledány optimální pozice v terapeutickém schématu. Glifloziny jsou novou skupinou antidiabetik, která účinkuje doposud nevyužívaným mechanismem [1]. Cílem tohoto sdělení je zamyšlení nad možnou budoucí pozicí dapagliflozinu ve schématu terapie diabetu 2. typu [2, 3].
Mechanismus účinku gliflozinů
Glukóza, jako malá molekula, prochází přes glomerulární membránu a dostává se do tubulů s ultrafiltrátem v koncentraci shodné s krevní plazmou. V tubulech je vychytávána a transportována zpět do krve. Začátkem devadesátých let minulého století byl objasněn mechanismus zodpovědný za zpětnou resorpci glukózy v proximálnímu tubulu [4]. V epiteliálních buňkách se nalézají dva typy glukózových kotransportérů – přenos glukózy přes membránu z lumen tubulu do nitra epiteliálních buněk probíhá ve spřažení s transportem sodíku ve směru koncentračního gradientu. Na krevním pólu pak je glukóza odsunována z nitra buňky tzv. facilitovanou difuzí prostřednictvím glukózových transportérů GLUT 2.
Sodíko-glukózové kotransportéry v ledvinách jsou dvou typů, označují se zkratkou SGLT1 a SGLT2 (sodium-glucose linked transporter); SGLT1 se nacházejí v části proximálního tubulu vzdálenější od glomerulu, vyznačují se vysokou afinitou a relativně men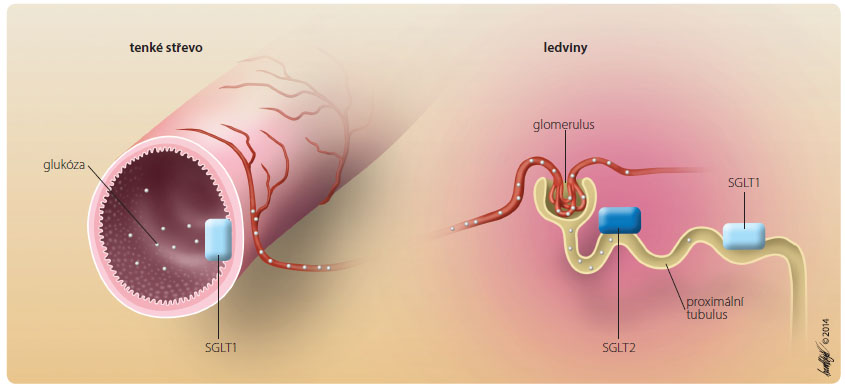 ší kapacitou pro přenos glukózy. Kotransportéry SGLT1 byly prokázány i v jiných tkáních těla, například v myokardu, mozku, zejména však zajišťují vstřebávání glukózy a galaktózy v tenkém střevě. Typ SGLT2 se nachází velmi pravděpodobně pouze v proximálním tubulu, v jiných tkáních těla nebyla doposud jeho přítomnost prokázána. Z hlediska funkce má vysokou kapacitu pro přenos (obr. 1).
ší kapacitou pro přenos glukózy. Kotransportéry SGLT1 byly prokázány i v jiných tkáních těla, například v myokardu, mozku, zejména však zajišťují vstřebávání glukózy a galaktózy v tenkém střevě. Typ SGLT2 se nachází velmi pravděpodobně pouze v proximálním tubulu, v jiných tkáních těla nebyla doposud jeho přítomnost prokázána. Z hlediska funkce má vysokou kapacitu pro přenos (obr. 1).
Uspořádání je celkem logické. Ultrafiltrát s vysokou koncentrací glukózy se dostává nejprve k transportnímu systému, který má vysokou kapacitu pro přenos (SGLT2). V této fázi se zpětně resorbuje až okolo 90 % přefiltrované glukózy. V dalším průběhu proximálního tubulu se nalézá systém (SGLT1) s vysokou afinitou ke glukóze (ta je již z 90 % odčerpána, proto se její koncentrace snižuje), který za normální situace zabezpečí resorpci zbylé glukózy. Oba dva transportní systémy mají (individuálně) definovanou maximální kapacitu, po jejím vysycení se nestačí veškerá glukóza vstřebat, vyvine se glykosurie.
Je prokázáno, že v situaci, kdy je přítomna hyperglykemie (typicky u diabetu), dochází ke zmnožení počtu SGLT2 v epitelech tubulů. Je to důsledek adaptace na zvýšenou nabídku glukózy v primárním ultrafiltrátu. Tento nález vysvětluje, proč u řady pacientů s glykemií okolo 12–15 mmol/l není přítomna glykosurie [5]. Glifloziny inhibují zpětný transport glukózy v ledvinných tubulech, a to cestou inhibice glukózových transportérů SGLT2 (některé glifloziny částečně inhibují i SGLT1) [6]. Důsledkem inhibice SGLT2 je glykosurie. To znamená, že významná část glukózy, která se přefiltruje v glomerulech, se ztrácí močí. Výsledkem je pak snížení glykemie a ztráta energie (ztráta 100 g glukózy denně se promítne do energetické bilance jako úbytek 400 kcal) [7–10].
Dapagliflozin
Dapagliflozin je vysoce selektivní inhibitor SGLT2. Po jeho podání je snížena reabsorpce glukózy v proximálním tubulu, denní ztráty glukózy jsou přímo úměrné dávce dapagliflozinu. Při dávce 10 mg je zpětná reabsorpce glukózy inhibována asi ze 40 %, denní ztráty glukózy močí dosahují průměrně 70 g. Po podání je dapagliflozin rychle absorbován ze zažívacího traktu [11, 12], jeho farmakokinetické parametry umožňují podání jednou denně. Nejčastějšími nežádoucími účinky jsou mykotické infekce genitálu zejména u žen a dále infekce dolních cest močových. Tyto infekce mívají lehčí průběh a obvykle se vícekrát neopakují. Hypoglykemie se mohou vyskytnout, pokud je dapagliflozin kombinován s deriváty sulfonylurey nebo s inzulinem. Běžným nálezem je zvýšení objemu moči (do 400 ml/24 h), v souvislosti se zvýšením diurézy mohou být přítomny mírné známky hemokoncentrace [11].
U osob s diabetem snižuje 12týdenní terapie dapagliflozinem hodnotu glykovaného hemoglobinu o 0,5–0,8 % ve srovnání s placebem [13–18]. Pokles tělesné hmotnosti za 12 týdnů terapie činil ve studiích 2,4 kg až 3,5 kg, což představuje přibližně dvojnásobek poklesu hmotnosti, k němuž docházelo při podávání placeba [19, 20]. V přímém srovnání terapie glipizidem a dapagliflozinem dosahuje rozdíl hmotnosti po 52 týdnech 4,7 kg, tedy hodnoty jistě klinicky významné [18]. Dapagliflozin snižuje obvod pasu, objem viscerálního i podkožního tuku [20], snižuje urikemii, mírně zvyšuje plazmatickou koncentraci HDL cholesterolu a snižuje hladinu triacylglycerolů, snižuje systolický krevní tlak [21]. V odborných časopisech byly publikovány výsledky sledování terapie dapagliflozinem trvající 104 týdnů, na mezinárodních kongresech v roce 2013 se pak objevily první výsledky ze sledování čtyřletého [22]. Metaanalýza studí fáze II a III prokázala kardiovaskulární bezpečnost léčby dapagliflozinem, nicméně výsledky prospektivních studií hodnotících kardiovaskulární riziko nejsou doposud k dispozici Dapagliflozin však pozitivně ovlivňuje i kardiovaskulární rizikové faktory, snižuje tělesnou hmotnost, klinicky významně snižuje krevní tlak [18, 20–24].
V listopadu 2012 byl dapagliflozin registrován v Evropské unii pro terapii pacientů s diabetem 2. typu. Základní terapeutická dávka je 10 mg dapagliflozinu. Je indikován pro monoterapii nebo kombinovanou terapii včetně kombinace s inzulinem [11].
Klinické aspekty použití dapagliflozinu
Účinek dapagliflozinu je závislý na dávce, od té se odvíjí stupeň inhibice SGLT2, míra glykosurie a následně snížení glykemie. Přitom platí, že čím vyšší glykemie, tím více glukózy se v glomerulech filtruje a tím větší účinek bude mít dapagliflozin (u nemocných s hodnotou glykovaného hemoglobinu vyšší než 9 % byl účinek terapie dapagliflozinem velmi dobrý s absolutním poklesem glykovaného hemoglobinu o 2 %) [9]. U pacientů s diabetem je přítomna adaptace na hyperglykemii, kapacita transportérů je zvýšena, renální práh pro glukózu je posunut výše, a proto při zvýšené glykemii není přítomna glykosurie [11]. Z těchto základních vztahů lze odvodit místo v terapii diabetu na jedné straně a limity použití dapagliflozinu na straně druhé.
Účinek dapagliflozinu je nezávislý na inzulinu či na jeho receptoru, proto může být teoreticky použit kdykoliv v průběhu onemocnění diabe![Graf 1 Přehled účinku dapagliflozinu na glykovaný hemoglobin ve čtyřech studiích; podle [14, 16, 27, 28] − Strojek, et al., 2011; Ferrannini, et al., 2010; Bailey, et al., 2010 ; Wilding, et al., 2010. D – dapagliflozin; HbA1C − glykovaný hemoglobin; n – počet pacientů](https://www.remedia.cz/photo-a-29644---.jpg) tem 2. typu, i v pozdních stadiích, kdy je sekrece inzulinu již nízká, anebo v situaci, kdy má pacient příznaky inzulinové rezistence vysokého stupně. Dapagliflozin tedy bude účinkovat i u nedostatečně spolupracujících pacientů. Může být také potenciálně kombinován s jakoukoliv terapií [11]. Dapagliflozin účinně snižuje postprandiální glykemii, jako by vyrovnává glykemický profil, takže snižuje variabilitu glykemie, teoreticky by mohl snížit riziko mikrovaskulárních komplikací více, než by odpovídalo jeho přímému účinku na glykovaný hemoglobin (graf 1).
tem 2. typu, i v pozdních stadiích, kdy je sekrece inzulinu již nízká, anebo v situaci, kdy má pacient příznaky inzulinové rezistence vysokého stupně. Dapagliflozin tedy bude účinkovat i u nedostatečně spolupracujících pacientů. Může být také potenciálně kombinován s jakoukoliv terapií [11]. Dapagliflozin účinně snižuje postprandiální glykemii, jako by vyrovnává glykemický profil, takže snižuje variabilitu glykemie, teoreticky by mohl snížit riziko mikrovaskulárních komplikací více, než by odpovídalo jeho přímému účinku na glykovaný hemoglobin (graf 1).
Dapagliflozin snižuje glykemii tím, že zvyšuje glykosurii. Jeho účinek by se měl proto dostavit u všech pacientů s hyperglykemií, bez ohledu na tělesnou hmotnost. Při snížení glykemie k normálním hodnotám klesá účinek dapagliflozinu, proto sám o sobě nezvyšuje riziko hypoglykemie [18]. Pokud je kombinován se sekretagogy nebo s inzulinem, může se ovšem v důsledku zlepšené kompenzace (snížení glykemie) riziko hypoglykemie zvýšit (efekt sekretagog nebo inzulinu se nesnižuje s normalizací glykemie). V této souvislosti se může objevit otázka, zda snižovat při zahájení léčby dapagliflozinem dávku sulfonylurey či inzulinu. V obecné rovině není třeba, pokud je dapagliflozin správně indikován, je podáván u pacientů se špatnou kompenzací, při současném snížení dávky sekretagog nebo inzulinu by pak zlepšení kompenzace nemuselo být zřetelné. Vždy je však nezbytné vyhodnotit situaci individuálně.
U pacientů, u nichž bude dosaženo zlepšení kompenzace, se vyskytne nový, v klinice neobvyklý fenomén – pacient s glykemiemi blízkými normálním hodnotám bude mít glykosurii. Na tuto skutečnost je třeba upozornit, aby nemocní nebyli zbytečně vyšetřováni. Přítomnost glykosurie také bude možno použít jako orientační test spolupráce pacienta – pokud nebude při léčbě dapagliflozinem přítomna, pacient pravděpodobně nemá dobrou adherenci k terapii.
Jedna z ideálních kombinací, dle mého soudu, je s metforminem a inzulinem [22, 9]. Dapagliflozin omezí vzestup tělesné hmotnosti a účinně zlepší kompenzaci. Vzestupu hmotnosti dapagliflozin také zabrání, pokud bude přidán do kombinace při intenzifikaci terapie, byť jen na krátkou dobu. Dapagliflozin nebude účinný u pacientů se sníženou glomerulární filtrací; u těchto osob se nepřefiltruje tak velké množství glukózy, aby bylo možno vyvolat arteficiální glykosurii v dostatečném objemu. Při snížení glomerulární filtrace pod hodnotu 1 ml/s tedy není indikována léčba dapagliflozinem [11]. Objem moči se zvyšuje v závislosti na glykosurii, obvykle je třeba doplnit denní příjem o přibližně 300 ml tekutin. Opatrnosti je třeba u osob se sníženým pocitem žízně (vyšší věk; zahájení terapie dapagliflozinem není indikováno pro osoby starší 75 let), taktéž za situací, kdy jsou ztráty tekutin vyšší – zejména při horečnatých onemocněních a v teplých dnech. Problematické může být také podání inhibitorů SGTL2 u osob, u nichž je vyvinuta autonomní neuropatie. Tito pacienti mohou mít sklon k hypotenzi při zhoršené schopnosti regulace intravazálního objemu.
„Diuretický“ účinek může být vítán u osob s diastolickou dysfunkcí, dapagliflozin zvyšuje účinek thiazidových diuretik, s nimiž je kombinace povolena a vhodná. Byl by jistě vítán i u pacientů se selhávající funkcí levé komory srdeční, nicméně tito jsou obvykle léčeni kličkovými diuretiky a dapagliflozin není v této situaci doporučován pro zvýšené riziko hypohydratace. O použití dapaglifozinu u pacientů s pokročilým srdečním selháním nejsou k dispozici žádná data, nicméně jeho „diuretický“ efekt by mohl snížit riziko srdečního selhání u pacientů, kteří mají sníženou kardiální rezervu a současně je jejich terapie zintenzivněna. Výsledkem je v tomto případě snížení diuretického účinku glukózy (klesne-li glykemie, snižuje se glykosurie); pokud je terapie vedena velmi intenzivně a necitlivě, u nemocných se manifestují klinické známky selhávání levé komory srdeční.
Uměle vyvolaná glykosurie proti očekávání nezvyšuje významně incidenci bakteriálních uroinfekcí (4,3 % po dapagliflozinu vs. 3,7 % po placebu) [11, 25]. Byla však zaznamenána vyšší incidence mykotických infekcí genitálu [11, 26]. Vulvovaginitida, balanitida a příbuzná infekční onemocnění pohlavních orgánů byly při léčbě dapagliflozinem hlášeny u 4,8 % subjektů, při podávání placeba u 0,9 %. Většina infekcí byla mírných až středně závažných a odpovídala na úvodní standardní léčebné opatření a vzácně došlo k přerušení léčby dapagliflozinem. Infekce byly častěji hlášeny u žen (6,9 % při podávání dapagliflozinu vs. 1,5 % při podávání placeba) a u subjektů s mykotickou infekcí v anamnéze byla vyšší pravděpodobnost rekurence infekce.
Stejně jako v jakékoliv jiné situaci platí, že plný účinek dapagliflozinu se nemůže projevit bez edukace nemocného. V tomto speciálním případě je třeba poučit pacienty o vhodném příjmu tekutin, o tom, že nemohou využít účinku dapagliflozinu k tomu, aby porušovali dietní režim. Taktéž bude asi vhodné rozšířit anamnézu a následně edukaci o problematiku rekurentních mykotických infekcí.
Závěr
Dapagliflozin je prvním registrovaným představitelem nové skupiny inhibitorů SGLT2, nazývaných glifloziny. Jeho účinek je zprostředkován arteficiálním navozením glykosurie. Dapagliflozin je v prvé řadě antidiabetikum, navíc však významně snižuje tělesnou hmotnost a systolický i diastolický krevní tlak. Z klinického hlediska se zdá být největším potenciálním přínosem účinek, který není vázán na inzulin ani na inzulinový receptor, což umožní využít potenciál dapagliflozinu kdykoliv v průběhu onemocnění diabetem 2. typu.
Seznam použité literatury
- [1] Meng W, Ellsworth BA, Nirschi AA, et al. Discovery of dapagliflozin: a potent, selective renal sodium-dependent glucose cotransporter 2 (SGLT2) inhibitor for the treatment of type 2 diabetes. J Med Chem 2008; 51: 1145–1149.
- [2] Kvapil M. Inhibitory SGLT2: Nová cesta k léčbě diabetu. In Kvapil M (eds): Diabetologie 2010. Triton, Praha 2010.
- [3] Kvapil M. Glifloziny: Inhibitory SGLT2. In Kvapil M (eds): Diabetologie 2013. Triton, Praha 2013.
- [4] Wright EM. Renal Na-glucose cotransporters. Am J Physiol 2001; 280: F10–F18.
- [5] Marks J, Carvou NJ, Debnam ES, et al. Diabetes increases facilitative glucose uptake and GLUT2 expression at the rat proximal tubule brush border membrane. J Physiol 2003; 553: 137–145.
- [6] Asano T, Anai M, Sakoda H. SGLT as a therapeutic target. Drugs Fut 2004; 29: 461–466.
- [7] Chao EC. A paradigm shift in diabetes therapy – dapagliflozin and other SGLT2 inhibitors. Discov Med 2011; 11: 255–263.
- [8] Anderson SL, Marrs JC. Dapagliflozin for the treatment of type 2 diabetes. Ann Pharmacother 2012; 46: 590–598.
- [9] Hanefeld M, Forst T. Dapagliflozin, an SGLT2 inhibitor, for diabetes. Lancet 2010; 375: 2196–2198.
- [10] DeFronzo RA, Hompesch M, Kasichayanula S, et al. Characterization of renal glucose reabsorption in response to dapagliflozin in healthy subjects and subjects with type 2 diabetes. Diabetes Care 2013; 36: 3169–3176.
- [11] Souhrn údajů o přípravku Forxiga, dostupné na www.sukl.cz (navštíveno 10. prosince 2013).
- [12] Plosker GL. Dapagliflozin: a review of its use in type 2 diabetes mellitus. Drugs 2012; 72: 2289–2312.
- [13] Vasilakou D, Karagiannis T, Athanasiadou E, et al. Sodium-glucose cotransporter 2 inhibitors for type 2 diabetes: a systematic review and meta-analysis. Ann Intern Med 2013; 159: 262–274.
- [14] Strojek K, Yoon KH, Hruba V, et al. Effect of dapagliflozin in patients with type 2 diabetes who have inadequate glycaemic control with glimepiride: a randomized, 24-week, double-blind, placebo-controlled trial. Diabetes Obes Metab 2011; 13: 928–938.
- [15] Bailey CJ, Iqbal N, T’joen C, List JF. Dapagliflozin monotherapy in drug-naïve patients with diabetes: a randomized-controlled trial of low-dose range. Diabetes Obes Metab 2012 ; 14: 951–959.
- [16] Ferrannini E, Ramos SJ, Salsali A, et al. Dapagliflozin monotherapy in type 2 diabetic patients with inadequate glycemic control by diet and exercise: a randomized, double-blind, placebo-controlled, phase 3 trial. Diabetes Care 2010; 33: 2217–2224.
- [17] Wilding JP, Norwood P, Tjoen C, et al. A study of dapagliflozin in patients with type 2 diabetes receiving high doses of insulin plus insulin sensitizers: applicability of a novel insulin-independent treatment. Diabetes Care 2009; 32: 1656–1662.
- [18] Nauck MA, Del Prato S, Meier JJ, et al. Dapagliflozin versus glipizide as add-on therapy in patients with type 2 diabetes who have inadequate glycemic control with metformin: a randomized, 52-week, double-blind, active-controlled noninferiority trial. Diabetes Care 2011; 34: 2015–2022.
- [19] Rosenstock J, Vieq M, Wei L, et al. Effects of dapagliflozin, an SGLT2 inhibitor, on HbA(1c), body weight, and hypoglycemia risk in patients with type 2 diabetes inadequately controlled on pioglitazone monotherapy. Diabetes Care 2012; 35: 1473–1478.
- [20] Bolinder J, Ljunggren O, Kullberg J, et al. Effects of dapagliflozin on body weight, total fat mass, and regional adipose tissue distribution in patients with type 2 diabetes mellitus with inadequate glycemic control on metformin. J Clin Endocrinol Metab 2012; 97: 1020–1031.
- [21] Foote C, Perkovic V, Neal B. Effects of SGLT2 inhibitors on cardiovascular outcomes. Diab Vasc Dis Res 2012; 9: 117–123.
- [22] Wilding JP, et al. A study of dapagliflozin in patients with type 2 diabetes receiving high doses of insulin plus insulin sensitizers: applicability of a novel insulin-independent treatment. Diabetes Care 2009; 32: 1656–1662.
- [23] Musso G, Gambino R, Cassader M, Pagano G. A novel approach to control hyperglycemia in type 2 diabetes: sodium glucose co-transport (SGLT) inhibitors: systematic review and meta-analysis of randomized trials. Ann Med 2012; 44: 375–393.
- [24] Clar C, Gill JA, Court R, Waugh N. Systematic review of SGLT2 receptor inhibitors in dual or triple therapy in type 2 diabetes. BMJ Open 2012: 18; 2.
- [25] Johnsson KM, Ptaszynska A, Schmitz B, et al. Urinary tract infections in patients with diabetes treated with dapagliflozin. J Diabetes Complications 2013; 27: 473–478.
- [26] Johnsson KM, Ptaszynska A, Schmitz B, et al. Vulvovaginitis and balanitis in patients with diabetes treated with dapagliflozin. J Diabetes Complications 2013; 27: 479–484.
- [27] Bailey CJ, Gross JL, Pieters A, et al. Effect of dapagliflozin in patients with type 2 diabetes who have inadequate glycaemic control with metformin: a randomized, double blind, placebo-controlled study. Lancet 2010; 375: 2223–2233.
- [28] Wilding JP, Woo V, Soler NG, et al. Sustained effectiveness of dapagliflozin over 48 weeks in patients with type 2 diabetes poorly controlled with insulin. Diabetes 2010; 59 (Suppl. 1): A21−A22. Abstract 0078-OR.