Kožní projevy cílené léčby nádorů
Nově zaváděná cílená léčba nádorů je provázena nízkou celkovou toxicitou, ale mezi nežádoucími účinky jsou významnou měrou zastoupeny kožní reakce. Dermatologická toxicita je popisována při podávání inhibitorů tyrozinkináz a proteazomu i při léčbě různými typy monoklonálních protilátek. Nejčastěji je pozorována při terapii látkami inhibujícími aktivitu epidermálního růstového faktoru a jeho receptorů, kde jsou kožní reakce popisovány u více než dvou třetin léčených nemocných, většinou v podobě akneiformního exantému. Vhodná dermatologická terapie dokáže zmírnit projevy kožní toxicity a umožní pokračování cílené onkologické léčby bez zbytečného přerušení.
Úvod
Kůže je orgán, který velmi citlivě reaguje na změny zevního i vnitřního prostředí, a je proto cílovým orgánem toxicity řady léků. Kožní reakce na podávané léky se mohou projevovat jako nespecifické exantémy provázející různé typy léčby nebo jako specifické kožní projevy vázané pouze na určitý léčebný preparát. Neustálé zavádění nových terapeutických postupů vede i k rozšíření spektra lékové kožní toxicity. Typickým příkladem nově pozorovaných nežádoucích účinků léčby jsou kožní reakce provázející cílenou léčbu nádorů zejména monoklonálními protilátkami (MoAb), inhibitory kináz či proteazomu.
Technologie tvorby MoAb byla popsána Milsteinem a Kohlerem již v roce 1975. Zpočátku se využívaly zejména v diagnostice nádorů, ale s rozvojem poznatků molekulární biologie a patogeneze nádorů získaly významné místo i v jejich léčbě. Původní, většinou myší monoklonální protilátky vyvolávaly tvorbu antimyších protilátek (HAMA – human antimouse monoclonal antibody) způsobujících anafylaktický šok či sérovou nemoc. Výroba čistě lidských MoAb je stále ještě obtížná, a tak se v současné době nejvíce využívají méně imunogenní, humanizované nebo chimérické monoklonální protilátky, kde variabilním úsekem kódujícím antigenní specifiku je myší a konstantním úsekem je lidský imunoglobulin, převážně typu IgG1. Hlavní výhodou léčby monoklonálními protilátkami je jejich specificita a cílenost zasahující do nádorového růstu na molekulární úrovni. Účinek MoAb může být zesílen jejich spojením s cytostatiky, radionuklidy nebo enzymy [6, 7].
Cílená léčba v onkologii bývá provázena nízkou celkovou toxicitou. Mezi popisovanými nežádoucími účinky jsou významnou měrou zastoupeny i různé typy kožních reakcí.
Dermatologická toxicita je vázána zejména na monoklonální protilátky inhibující aktivitu epidermálního růstového faktoru a jeho receptorů, ale bývá pozorována i u některých dalších MoAb [3].
Kožní reakce způsobené inhibitory tyrozinkináz
Imatinib je fenylaminopyrimidinový derivát účinně inhibující BCR-abl tyrozin kinázu a receptorové tyrozin kinázy růstového faktoru destiček – platelet-derived growth factor (PDGF) a faktoru kmenových buněk – stem cell factor (SCF). Indikován je k léčbě některých typů chronických myeloidních leukémií a některých gastrointestinálních nádorů. Nejčastějšími kožními projevy nežádoucích účinků léčby jsou makulopapulózní exantémy a periorbitální edémy vyskytující se až u jedné třetiny nemocných. Se stoupající dávkou imatinibu stoupá i četnost a tíže kožních reakcí. Vzácněji jsou při této léčbě popisovány různé typy neutrofilních dermatóz včetně akutní generalizované exantematózní pustulózy, klinicky nejvíce připomínající pustulózní psoriázu. Kožní projevy většinou do 2 týdnů spontánně vymizí, pouze vzácně je nutné přerušení léčby. U několika pacientů byly pozorovány také poruchy pigmentace ve smyslu hypopigmentací i hyperpigmentací včetně ztmavnutí kštice.
Erlotinib a gefitinib jsou nízkomolekulární látky inhibující tyrozinkinázovou aktivitu receptoru pro epidermální růstový faktor (EGFR) kompeticí s adenosintrifosfátem o vazebné místo v intracelulární doméně receptoru. Nadějně se tyto látky jeví především v terapii nemalobuněčného karcinomu plic. Nežádoucí kožní projevy těchto látek jsou podobné jako u monoklonálních protilátek proti EGFR a jsou diskutovány níže v kapitole Monoklonální protilátky proti receptorům epidermálního růstového faktoru.
Kožní projevy způsobené inhibitorem proteazomu
Bortezomib je modifikovaný dipeptidylborát – inhibitor proteazomu, což je enzymový komplex, který má klíčovou roli v řízení proteinů odpovědných za průběh buněčného cyklu. Je využíván zejména v léčbě mnohočetného myelomu. Vzácně jsou popisovány kožní reakce většinou ve formě makulopapulózního exantému. U jednoho pacienta byla pozorována purpura s histologicky potvrzenou leukocytoklastickou vaskulitidou. Kožní projevy odpovídají dobře na léčbu kortikoidy, ale při dalším podání léku se opět vracejí.
Kožní projevy způsobené monoklonálními protilátkami
Chimérická anti-CD-20 monoklonální protilátka rituximab je využívána zejména v terapii nehodgkinských B lymfomů. Kožní reakce se objevují minimálně, u jednoho nemocného byl popsán vznik Stevensova-Johnsonova syndromu v souvislosti s podávanou léčbou. Častěji je popisována sérová nemoc s výskytem morbiliformního exantému, který je nejvýraznější na akrálních partiích končetin. Objevuje se 1 až 2 týdny po zahájení léčby. Hlavní příčinou je pravděpodobně reakce na myší část chimérické protilátky. Po celkovém podání kortikoidů dochází k rychlému ústupu kožních projevů.
Alemtuzumab je humanizovaná MoAb proti povrchovému antigenu CD52, který je exprimován na více než 95 % normálních B i T lymfocytů. Kožní reakce nebyly při podávání tohoto preparátu popsány.
Stejně tak dosud nejsou kožní reakce uváděny po aplikaci gemtuzumabu, monoklonální protilátky namířené proti CD33 antigenu, který je exprimován až u 90 % akutních myeloidních leukémií.
Kožní toxicita nebyla zatím popsána ani při podávání bevacizumabu, monoklonální protilátky proti růstovému faktoru endotelií (VEGF).
Cytotoxické T lymfocyty s antigenem 4 (CTLA-4) jsou odpovědné za toleranci a prevenci autoimunitních reakcí. Potlačení jejich funkce pomocí monoklonální protilátky anti-CTLA-4 (ticilimumab aj.) může pomoci překonat toleranci hostitele vůči nádoru a zesílit imunitní odpověď proti nádorovým buňkám [1, 2]. Léčba je provázena řadou autoimunitních reakcí včetně kožních. Nejčastěji jsou popisovány exantémy tvořené růžovými až červenými drobnými papulemi, někdy i s patrným Koebnerovým fenoménem. Maximum ložisek je na extenzorových partiích končetin, plosky a dlaně nebývají postiženy vůbec. Vzácněji jsou popisovány exantémy charakteru erythema exudativum multiforme nebo Stevensova-Johnsonova syndromu. Z dalších kožních příznaků je možné pozorovat vitiligo nebo generalizovaný pruritus. Léčbu provází často vznik nejizvící alopecie ve kštici, v obočí i v ochlupení na trupu a v oblasti mons pubis. Kožní toxicita dosahuje převážně pouze 1. a 2. stupně a po přerušení léčby dochází ve většině případů k postupnému vymizení kožních projevů.
Monoklonální protilátky proti EGFR
Aktivace receptoru pro epidermální růstový faktor (EGFR) zvyšuje proliferaci nádorových buněk, inhibuje apoptózu, aktivuje angiogenezi, umožňuje metastazování nádoru a zvyšuje jeho rezistenci k protinádorové léčbě. Cílem podávání anti-EGFR protilátek je inhibice aktivity extracelulárních receptorů (EGFR). V současné době se tyto MoAb zkoušejí v léčbě řady solidních nádorů. Trastuzumab, cetuximab a mutuzumab se vážou na extracelulární část EGFR. Hlavní využití trastuzumabu je v léčbě nádorů prsu a nověji se zkouší také u nemalobuněčných plicních nádorů. Váže se převážně na HER2 receptory a jeho podávání nebývá provázeno výraznější kožní toxicitou. Cetuximab je podáván zejména u pokročilých kolorektálních karcinomů a matuzumab u karcinomů pankreatu.
V kůži jsou EGFR exprimovány zejména na proliferujících nediferencovaných keratinocytech bazální vrstvy epidermis a na keratinocytech zevního obalu vlasového folikulu, což je jeden z důvodů, proč je nejvýraznější dermatologická toxicita pozorována právě u těchto monoklonálních protilátek. Blokáda EGFR vyvolává zvýšení apoptózy keratinocytů, zvýšení jejich diferenciace, ztenčení stratum corneum epidermis, zánětlivou infiltraci folikulů a jejich zvětšení a vyplnění velkým množstvím keratinu.
Kožní reakce se vyskytují u více než dvou třetin léčených pacientů. Přehledně jsou uvedeny v tab. 1.
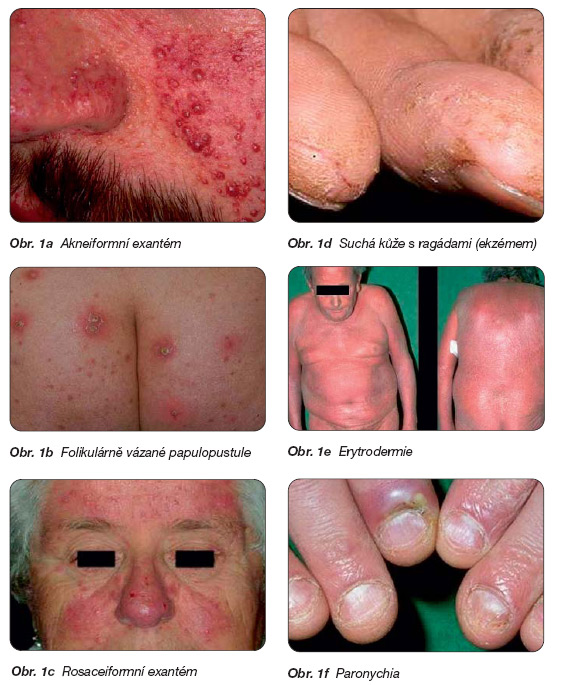
Nejčastějším příznakem kožní toxicity jsou akneiformní erupce, které se objevují již v prvních týdnech po zahájení léčby a postihují 35–90 % nemocných. Typickým projevem jsou folikulárně vázané papulopustuly na obličeji, horních partiích trupu a ve kštici, komedony nebývají zastiženy (obr. 1a). Objevují se již v prvních týdnech léčby a při těžším postižení se postupně šíří i na další partie trupu a končetin (obr. 1b). Kromě kožních lézí napodobujících akné je možné pozorovat i rosaceiformní exantémy nebo projevy napodobující seboroickou dermatitidu obličeje i kštice (obr. 1c). Častým subjektivním příznakem je svědění kůže zejména v místech akneiformního exantému. Jeho vznik bývá považován za projev účinnosti léčby. Tíže postižení dosahuje ale většinou pouze 1. a 2. stupně, velmi vzácně je nutné přerušit podávání monoklonální protilátky kvůli akneiformnímu exantému, spíše dochází i přes pokračující léčbu k jeho ústupu. Spontánně mizí i venektazie, které mohou provázet zejména rosaceiformní exantém.
V delším odstupu od zahájení léčby v průběhu 3–6 týdnů se až u 35 % nemocných objevují ložiska suché, načervenalé a olupující se kůže, převážně na pažích a dolních končetinách a na místech odeznívajícího akneiformního exantému (obr. 1d). Někdy se objevuje i suchost sliznic.V některých případech mohou tato ložiska progredovat za vzniku generalizovaného ekzému až do erytrodermie (obr. 1e).
Z dalších kožních komplikací léčby jsou až u 10 % léčených pacientů popisována bolestivá paronychia postihující zejména palce rukou i nohou, někdy komplikovaná vznikem pyogenního granulomu. Nehtové ploténky bývají výrazně dystrofické (obr. 1f).
Protrahovaná léčba inhibitory EGFR je provázena také změnami kvality vlasů, které jsou tenké, křehké a snadno se lámou. Uvádí se též postižení řas, které jsou naopak prodloužené a vlní se.
Hodnocení nežádoucích kožních projevů a jejich léčba
Kožní toxicita anti-EGFR protilátek je podle intenzity projevů dělena do 4 stupňů (tab. 2).
Hodnocení se týká zejména akneiformního exantému, suchosti kůže a případného vzniku ekzematózních ložisek.
Velmi mírné postižení projevující se drobnými folikulárně vázanými akneiformními eflorescencemi nebo lehce suchou načervenalou kůží bez subjektivních příznaků je hodnoceno stupněm 1.
Výraznější akneiformní exantém nebo ekzematizace ložisek xerózy se současným svěděním kůže různé intenzity jsou považovány za 2. stupeň kožní toxicity. Rozsah postižení v tomto případě nepřesahuje 50 % kožního povrchu.
Stupněm 3 je hodnocen hustý výsev až splývání makulopapulózního akneiformního exantému nebo ekzematózních ložisek. Bývá provázen silným svěděním kůže, vytváří rozsáhlé erytrodermické plochy a postihuje více než 50 % kožního povrchu.
Za nejtěžší 4. stupeň je považován vznik těžkého erytému až edému na téměř celém povrchu kůže. Bývá provázen výrazným olupováním nebo tvorbou rozsáhlých puchýřů a ulcerací. K tomuto postižení může vést zhoršení akneiformního exantému nebo rozšíření a impetiginizace ekzematózních ložisek.
I když u 80–90 % nemocných je popisován pouze 1. a 2. stupeň toxicity, je vhodné kožní projevy léčit.
Léčba akneiformního exantému je podobná jako léčba projevů acne vulgaris nebo rosacey a seboroické dermatitidy a je závislá na stupni postižení. Většinou nevyžaduje ukončit podávání inhibitorů EGFR [5]. U většiny nemocných s postižením stupně 1 a 2 je však vhodná lokální léčba, která dokáže výrazně zmírnit příznaky onemocnění. Akneiformní papulopustule se rychleji hojí při aplikaci roztoků s antibiotiky, například s erythromycinem nebo klindamycinem, dále s obsahem kyseliny salicylové nebo s retinoidy. Při přesušení kůže jsou vhodnější krémy stejného složení. Pokud se kožní projevy blíží více seboroické dermatitidě či rosaceiformnímu exantému, jsou účinné preparáty s obsahem metronidazolu. U 2. stupně kožní toxicity je možné uvažovat o kombinaci lokální a systémové léčby podáváním antibiotik, zejména tetracyklínové řady. Velmi dobrý účinek má také celkově podávaný metronidazol. Pokud dosáhne tíže kožního postižení 3. stupně, je vhodné dočasné přerušení podávání anti-EGFR protilátek se současnou lokální i celkovou léčbou jako u stupně 2 (tab. 3).
Při vzniku xerózy je základním léčebným přístupem dostatečná hydratace kůže a odstranění případných šupin. Prevencí této komplikace může být přechod z gelů a lihových roztoků používaných pro léčbu akneiformního exantému k používání krémů a mastí. U mírných projevů vystačíme s promazáváním indiferentními mastmi, u výraznější xerózy se dobře osvědčují masti a krémy s 2–5 % salicylové kyseliny a dále preparáty obsahující ureu. Při vzniku nánosů hyperkeratóz je vhodné masti aplikovat v okluzivním obvaze. Pro léčbu ekzematizace jsou vhodné lokální kortikosteroidy, minimálně do doby ústupu projevů. Bakteriální superinfekci ložisek ekzému je nezbytné léčit lokálně aplikovanými antibiotiky a virovou superinfekci lokálními antivirotiky. Pokud dochází k dalšímu šíření infekce, je nezbytné i systémové podávání antibiotik nebo antivirových preparátů. Ragády, které se objevují jako častá komplikace přesušené kůže, je vhodné léčit keratolytickými mastmi a možné infekci bránit kombinací se zevně aplikovanými antibiotiky.
Pruritus provázející kožní toxicitu lze tlumit podáváním antihistaminik a ve výjimečných případech i podáváním kortikosteroidů.
Paronychia se léčí velmi obtížně. Nezbytná je prevence prováděním šetrné manikúry nebo nošením volné a vzdušné obuvi. Osvědčuje se zevní aplikace antibiotických a antimykotických preparátů veformě mastí i past v závislosti na charakteru projevů. V některých případech, k potlačení zánětlivé reakce, je vhodná jejich kombinace s kortikosteroidy. Při vzniku pyogenního granulomu se osvědčilo ošetřování nitrátem stříbrným, někdy je však nezbytný i chirurgický zákrok.
Některá pracoviště zkouší potlačit toxicitu anti-EGFR celkovým podáváním kortikosteroidů, určitým rizikem je však nebezpečí vzniku steroidní akné. Stejně tak je v těchto případech sporná léčba akné podáváním retinoidů, protože způsobují suchost kůže i sliznic, a tak mohou potencovat nežádoucí účinky léčby těmito monoklonálními protilátkami.
Dermatologická léčba nemocných s projevy kožní toxicity při terapii monoklonálními protilátkami umožní pokračování onkologické léčby bez přerušení tak, aby pacienti mohli mít z této léčby co největší užitek.
Obr. 1a Akneiformní exantém
Obr. 1b Folikulárně vázané papulopustule
Obr. 1c Rosaceiformní exantém
Obr. 1d Suchá kůže s ragádami (ekzémem)
Obr. 1e Erytrodermie
Obr. 1f Paronychia
Seznam použité literatury
- [1] Reuben JM, Lee BN, Gomez-Navarro J, et al. Biologic and immunomodulatory events after CTLA-4 blockade with ticilimumab in patients with advanced malignant melanoma. Canceor Early View, Articles online in advance of print, 13. April, 2006.
- [2] Jaber SH, Cowen WE, Booher S, et al. Skin reactions in a subset of patients with stage IV melanoma treated with anti-cytotoxic T-lymfocyte antigen 4 monoclonal antibody as a single agent. Arch Dermatol 2006; 142: 166–172.
- [3] Payne AS, James WD, Weiss RB. Dermatologic toxicity of chemoterapeutic agents. Seminars in Oncology 2006; 33: 86–97.
- [4] Lee MW, Seo ChW, Kim SW, et al. Cutaneous side effects in non-small lung cancer patients treated with Iressa an inhibitor of epidermal growth factor. Acta Derm Venereol 2004; 84: 23–26.
- [5] Segaert S, Tabernero J, Chosidow O, et al. The management of skin reactions in cancer patients receiving epidermal growth factor receptor targeted therapies. JDDG 2005; 599–606.
- [6] Booy JP, Johan D, Maddika S, et al. Monoclonal and bispecific antibodies as novel therapeutics. Arch Immunol Ther Exp 2006; 54: 86–101.
- [7] Klener P. Terapeutické cíle na molekulární úrovni. In: Klinická onkologie, Praha, Galén, 2002; 242–245.