Léčba chronické spontánní urtikarie
Souhrn:
Chronická spontánní urtikarie je nejčastějším typem chronických urtikarií. Dříve se označovala jako idiopatická, protože nebyly známy její příčiny. Díky novým poznatkům se situace v posledních letech výrazně změnila, takže podíl skutečně idiopatických případů se odhaduje na polovinu. Zavádění nových antihistaminik a biologik oživilo zájem o problematiku chronické kopřivky jak v oblasti výzkumu, tak klinické praxe. Aktualizované doporučené postupy odborných společností EAACI, GA2LEN, EDF a WAO pro léčbu chronické kopřivky přinášejí lékařům cenné vodítko v diagnostice i v léčbě. Strukturovaná anamnéza představuje nejpřínosnější diagnostický prostředek ke zjištění typu chronické kopřivky. Léky první volby jsou prověřené nesedativní blokátory receptorů H1 (H1 antihistaminika), a to i ve zvýšeném dávkování (ve druhé linii léčby). Jako třetí linie se k nim u refrakterních případů přidávají antileukotrie-ny nebo cyklosporin A anebo omalizumab. Tento první biologický lék pro léčbu chronické urtikarie je po splnění indikačních kritérií nyní hrazen z prostředků veřejného zdravotního pojištění a jeho preskripce je vázána na dermatologická centra biologické léčby. Individuální případy však nadále vyžadují individu-ální přístup, včetně použití méně obvyklých empirických postupů. Pro zvládnutí chronické kopřivky je důležité komplexní pojetí, mezioborová spolupráce a také přiměřená edukace pacienta a psychosomatický přístup.
Key words: chronic spontaneous urticaria – guidelines – omalizumab.
Summary:
Chronic spontaneous urticaria is the most frequent type of chronic urticarias. It was formerly called idiopathic because of its unknown cause. In the last years, the situation changed thanks to the advances in knowledge, so that the real rate of idiopathic cases decreased by about a half. The introduction of new antihistamines and biologics has renewed the interest in chronic urticaria both in investigation and clinical practice. The updated Guidelines of EAACI, GA2LEN, EDF and WAO represent a valuable guide for physicians in diagnostics and therapy. Taking a structured history represents the most beneficial tool to assess the type of chronic urticaria. Non sedating H1 antihistamines are the drugs of first choice, even in updosed regimen. Third line therapy is added on to antihistamines in refractory cases – antileukotrienes, cyclosporine A or omalizumab. Prescription of this first biologic for treatment of chronic urticaria is limited to dermatologic centres of biologic therapy, where – after fulfillment of indication criteria – it is reimbursed by health care insurance authorities. Nevertheless, individual cases need to be solved in an individual way, including the use of less common empirical drugs. For the general management of chronic urticaria, complex understanding, interdisciplinary collaboration and also adequate patient’s education and psychosomatic attitude are important.
Úvod
Chronická spontánní urtikarie (CSU) byla dosud označována jako idiopatická, protože nebyly známy její příčiny. Díky novým poznatkům se situace v posledních letech výrazně změnila, takže podíl skutečně idiopatických případů se odhaduje jen na polovinu. Chronická spontánní urtikarie je nejčastějším typem, představuje tři čtvrtiny chronických urtikarií. Až v polovině případů jsou v pozadí protilátky proti imunoglobulinu E (IgE) a proti receptoru pro IgE (IgER), které vedou k uvolnění histaminu [1,2]. Chronická spontánní urtikarie tedy není projevem alergické reakce, ale především projevem autoreaktivity a autoimunity. Tomu odpovídají i časté komorbidity, tedy asociace s chorobami, jako jsou atopická onemocnění, autoimunitní thyreoiditida, anemie, Sjögrenův syndrom, celiakie, revmatoidní artritida aj. [3]. Z výše uvedených důvodů se pro tuto skupinu používá nově termín chronická spontánní urtikarie – tedy taková urtikarie, kterou nelze na rozdíl od fyzikálních chronických urtikarií cíleně vyvolat [1,4]. Potraviny a léky patří k častým příčinám i spouštěčům CSU, působí různými mechanismy – liberují histamin, snižují funkci diaminooxidázy, blokují diaminooxidázu, zasahují do metabolismu kyseliny arachidonové aj. Také infekce patří mezi časté spouštěcí vlivy [4]. Do pěti let odezní až polovina případů, více než deset let trvá pětina případů CSU [5,6].
Jako prognosticky nepříznivé faktory pro průběh chronické urtikarie se uvádí selhání léčby H1 antihistaminiky v běžném dávkování, její trvání delší než šest měsíců před návštěvou lékaře, přítomnost angioedému, fyzikální urtikarie, průkaz autoprotilátek – štítná žláza, IgE, IgER1, pozitivita ASST (autologous serum skin test, intradermální test s autologním sérem prokazující autoreaktivitu) a BHRT (basophil histamin‑releasing test, test uvolnění histaminu z bazofilů), dále hypertenze, známky aktivace vnější cesty hemokoagulační kaskády (fragmenty protrombinu) nebo fibrinolýzy (D‑dimery) [7].
Chronická kopřivka se objevuje přibližně u 1 % populace, převažují ženy. Na kůži se projevuje jako kopřivkové pomfy (pupeny) anebo angioedém. Podkladem je edém v koriu – edém v horním koriu vede ke vzniku pomfů, hlubší edém ke vzniku angioedému. Za chronickou je kopřivka považována při trvání delším než šest týdnů s denními či s téměř denními výsevy [4,8]. Náhlý vznik a obvykle prchavý charakter kopřivky jsou typické. Angioedém ale odeznívá pomaleji, a to během tří dnů [5,8]. Hlavním mediátorem je především histamin. Kopřivkové projevy však mohou vyvolat i jiné biogenní aminy nebo prozánětlivé mediátory – leukotrieny, faktor aktivující destičky, prostaglandiny, bradykinin, interleukiny, složky komplementu, hemokoagulační faktory aj. [9]. Kopřivka tak může být nazírána jako typ reakce kůže na různé vazoaktivní mediátory, které se uvolňují v důsledku stimulace receptorů mastocytů reagujících na signály nebezpečí z bariérových epiteliálních buněk (keratinocytů).
Doporučené postupy
Diagnostiku a léčbu chronické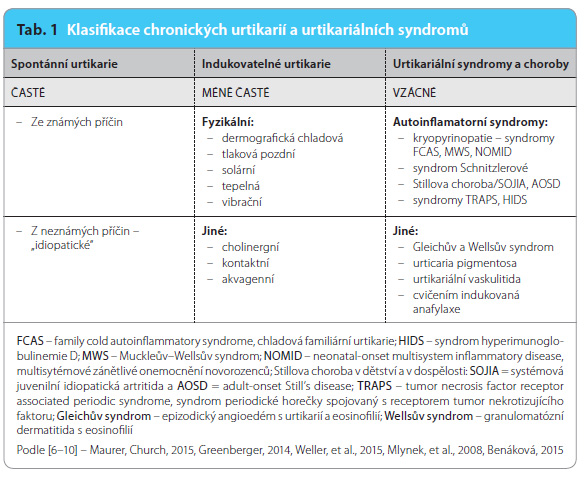 urtikarie posunuly vpřed závěry mezinárodní pracovní skupiny zformulované v dokumentu Doporučené postupy pro diagnostiku a léčbu urtikarie společností EAACI (European Academy of Allergy and Clinical Immunology), EU‑funded Network of Excellence, Global Allergy and Asthma European Network (GA2LEN), European Dermatology Forum (EDF) a World Allergy Organization (WAO), které se objevily v odborném tisku poprvé již v roce 2008. V současnosti je k dispozici již třetí aktualizovaná verze [4]. Dle těchto postupů se chronické kopřivky rozdělují z hlediska vyvolání projevů na spontánní a indukovatelné. Posledně jmenované lze cíleně vyvolat stejným spouštěčem. Jedná se o klasické fyzikální urtikarie, jako jsou dermografická, pozdní tlaková, vibrační, chladová, tepelná a solární a jiné urtikarie – akvagenní, cholinergní a kontaktní. Mediátorem je též histamin, ale mechanismy jeho liberace nejsou dosud známy. Samostatně se řadí urtikariální syndromy a nehistaminové angioedémy (tab. 1).
urtikarie posunuly vpřed závěry mezinárodní pracovní skupiny zformulované v dokumentu Doporučené postupy pro diagnostiku a léčbu urtikarie společností EAACI (European Academy of Allergy and Clinical Immunology), EU‑funded Network of Excellence, Global Allergy and Asthma European Network (GA2LEN), European Dermatology Forum (EDF) a World Allergy Organization (WAO), které se objevily v odborném tisku poprvé již v roce 2008. V současnosti je k dispozici již třetí aktualizovaná verze [4]. Dle těchto postupů se chronické kopřivky rozdělují z hlediska vyvolání projevů na spontánní a indukovatelné. Posledně jmenované lze cíleně vyvolat stejným spouštěčem. Jedná se o klasické fyzikální urtikarie, jako jsou dermografická, pozdní tlaková, vibrační, chladová, tepelná a solární a jiné urtikarie – akvagenní, cholinergní a kontaktní. Mediátorem je též histamin, ale mechanismy jeho liberace nejsou dosud známy. Samostatně se řadí urtikariální syndromy a nehistaminové angioedémy (tab. 1).
Praktický několikastupňový algoritmus dle příznaků vede ke zpřesnění diagnostiky, volby vyšetření a léčby. Doporučené postupy mají lékaři sloužit jako pomoc a vodítko v náročné problematice, jako příručka pro vyšetřování a léčbu pacientů v každodenní praxi. Překlad originálního textu i výkladový článek pro jejich použití v praxi byly letos otištěny v Česko-slovenské dermatologii [10] s praktickými šablonami, tabulkami, schématy a s doprovodným textem. Výbor České dermatologické společnosti ČLS JEP doporučil tyto Doporučené postupy pro praxi v ČR.
Chronické kopřivky se liší průběhem, diagnostikou, prevencí a léčbou. Spontánní i indukovatelné kopřivky lze léčit H1 antihistaminiky, na standardní dávky ale reaguje dostatečně jen polovina nemocných [4,6,7]. Urtikariální syndromy s hlavním mediátorem interleukinem 1 (IL‑1) a angioedémy zprostředkované bradykininem však na léčbu antihistaminiky pochopitelně nereagují [5]. Vyšetřování a léčby chronické kopřivky se primárně ujímá dermatolog, případně alergolog. A samozřejmě i praktický lékař a další odbornosti, pokud se v problematice orientují a sledují ji.
Diagnostika
Diagnosticky je u pacienta přicházejícího k lékaři pro chronickou kopřivku třeba nejdříve vyloučit jiné dermatózy s pomfy (prurigo, ekzémy, parazitózy, pemfigoid aj.) a syndromy s pomfy či s angioedémem (urtikariální autoinflamatorní syndromy a nehistaminové angioedémy). A posléze určit typ a závažnost urtikarie, od čehož se odvíjí volba léčby [4–6]. Základem je pečlivé morfologické vyšetření a cílená anamnéza, případně i cílená laboratorní vyšetření. Ta umožní lékaři zorientovat se a dle toho navrhnout plán vyšetření, preventivních opatření a léčbu. Anamnéza se zaměřuje na nejčastější příčiny a spouštěče. Z léků se často uplatňují nesteroidní antiflogistika, která mohou kopřivku přímo indukovat nebo ji nepřímo exacerbovat [6]. Dále pátráme po vlivech, jako jsou fokální infekce, potraviny, fyzikální vlivy a také komorbidity jako thyreopatie, atopie a další autoimunitní choroby. Mezi kardinální otázky k rozlišení typu chronické urtikarie [4–8,10] patří dotazy na:
- doprovodné příznaky autoinflamatorních a autoimunitních chorob, jako jsou teploty, artralgie, myalgie, únava, cefalea, bolesti břicha. Tyto choroby mají ve svém klinickém obraze urtikarii jako jeden z řady příznaků systémového onemocnění. Nesvědí, jsou bez angioedému a histologicky je často přítomen neutrofilní infiltrát. Jedná se o řídká multisystémová zánětlivá onemocnění, často na podkladě autoinflamace. Léčebně se ukazuje dobrý účinek biologické léčby namířené proti IL‑1;
- trvání jednotlivých projevů déle než 24 hodin, které vyvolávají podezření na urtikariální vaskulitidu. Příznaky se projevují spíše pálením než svěděním, mívají hemoragický charakter, mohou zanechávat pozánětlivé pigmentace. Tato leukocytoklastická vaskulitida může provázet systémový lupus erythematodes, Sjögrenův syndrom, kryoglobulinemii či hypokomplementemii. Léčebně se používají imunosupresiva;
- vyvolání fyzikálními vlivy, jako jsou tlak, teplo, chlad, slunce, voda, pocení, tření, vibrace;
- současný výskyt angioedému – viz dále.
Pokud je na všechny čtyři otázky odpověď negativní, tedy u pacienta se vyskytuje kopřivka a je či není přítomen angioedém, kopřivka nemá doprovodné příznaky autoinflamatorních chorob, projevy nelze opakovaně vyvolat a jednotlivé pomfy netrvají déle než 24 hodin, pak se s velkou pravděpodobností jedná o chronickou spontánní urtikarii. V praxi mohou být posouzení a léčba pacienta s chronickou urtikarií ztíženy např. tehdy, když jde o souběh různých typů urtikarie anebo o souběh kopřivky s jinou chorobou.
Chronický angioedém
Chronický angioedém bez pomfů (tab. 2) nebývá projevem chronické kopřivky, je podezřelý především z působení bradykininu, který na rozdíl od histaminu nezpůsobuje pomfy. Z léků jsou nejčastější příčinou inhibitory angiotensin konvertujícího enzymu (angiotensin converting enzyme, ACE) a n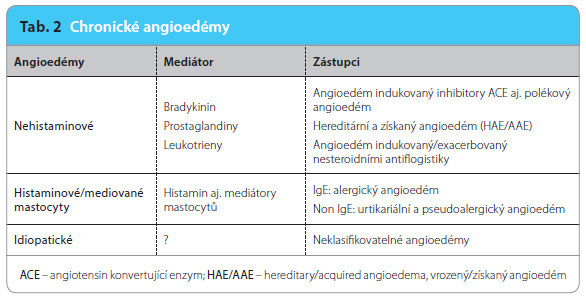 esteroidní antiflogistika [11,12]. Řídce je chronický angioedém projevem hereditárního angioedému, kde se vyskytují abnormality v oblasti komplementového systému (inhibitor C1 složky komplementu) či hemokoagulace (faktor XIII). Anebo může být projevem získaného angioedému, kdy v pozadí bývají lymfoproliferativní onemocnění, resp. monoklonální gamapatie (např. Caldwellův syndrom), autoimunitní choroby (systémový lupus erythematodes) nebo Gleichův syndrom, syndrom kapilárního úniku (capillary leak syndrome) anebo protilátky proti inhibitoru C1, které vedou k jeho konsumpci. Urtikariální angioedém [3,11], tedy izolovaný angioedém bez pomfů jako jediný projev spontánní urtikarie, se vyskytuje řídce – udává se zhruba v 10 % [5,8].
esteroidní antiflogistika [11,12]. Řídce je chronický angioedém projevem hereditárního angioedému, kde se vyskytují abnormality v oblasti komplementového systému (inhibitor C1 složky komplementu) či hemokoagulace (faktor XIII). Anebo může být projevem získaného angioedému, kdy v pozadí bývají lymfoproliferativní onemocnění, resp. monoklonální gamapatie (např. Caldwellův syndrom), autoimunitní choroby (systémový lupus erythematodes) nebo Gleichův syndrom, syndrom kapilárního úniku (capillary leak syndrome) anebo protilátky proti inhibitoru C1, které vedou k jeho konsumpci. Urtikariální angioedém [3,11], tedy izolovaný angioedém bez pomfů jako jediný projev spontánní urtikarie, se vyskytuje řídce – udává se zhruba v 10 % [5,8].
Jiné histaminem zprostředkované chronické angioedémy – alergické a pseudoalergické – se nevyskytují denně či téměř denně, objevují se spíše nárazově, případně intermitentně. Jako idiopatický angioedém se pak označují případy bez rodinné a lékové anamnézy, bez abnormalit v inhibitoru C1, které nereagují na antihistaminika, kortikosteroidy či na adrenalin. Patogeneze je zatím neznámá, mediátorem není ani histamin, ani bradykinin [5,8,11,12].
Diagnostická vyšetření
Laboratorní vyšetření a další testy se provádějí v případech, kdy ze samotné anamnézy a z klinického vyšetření nelze typ urtikarie určit, a v rámci pátrání po příčinách úporného průběhu. Doporučené postupy upřednostňují co nejméně vyšetření [3,4,7,8]. Základem je pátrání po zánětlivých choro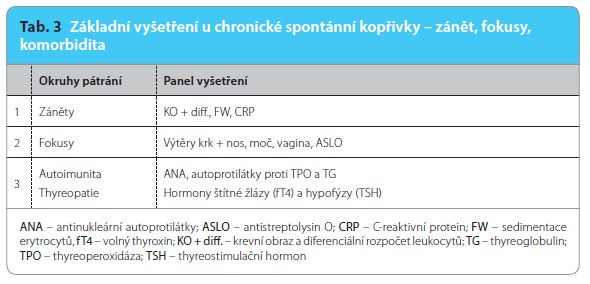 bách, případně je lze rovnou doplnit o základní screening spouštěčů a komorbidit (tab. 3). Další vyšetření jsou prováděna zejména u CSU – cíleně na základě anamnézy, příznaků a s vědomím, co a proč chceme zjistit či vyloučit, ve spolupráci s příslušnými specialisty.
bách, případně je lze rovnou doplnit o základní screening spouštěčů a komorbidit (tab. 3). Další vyšetření jsou prováděna zejména u CSU – cíleně na základě anamnézy, příznaků a s vědomím, co a proč chceme zjistit či vyloučit, ve spolupráci s příslušnými specialisty.
Léčba
Léčba, resp. zvládání CSU klade na lékaře i pacienta značné nároky. Jen zřídka lze příčinu kopřivky odhalit anebo odstranit, proto je pro praxi důležité vyloučit či omezit obecné spouštěcí faktory. Tedy dodržovat určitá režimová opatření, v zásadě obdobná jako u ekzémů – bránit iritaci a pečovat o kůži, vyhýbat se potravinám bohatým na histamin a liberátorům histaminu. Jedná se obecně o vše zrající, kvašené, uzené, marinované. Dále jde o potraviny obsahující konzervační látky, barviva, antioxidanty a také o trvanlivé, rozmrazované skladované potraviny. Dalšími ve výčtu jsou všechny druhy ryb a mořských plodů, alkohol, ovocné šťávy, bylinné čaje, kupované cukrovinky, čokoláda, kakao, některé druhy ovoce a zeleniny atd.
Praktické jsou pro pacienty i písemné edukační materiály a sledování potenciálních spouštěcích vlivů (léky, potraviny, alkohol, fyzikální a kontaktní vlivy, infekce, hormonální i psychické vlivy) formou kalendářního deníčku [4,10].
První linie léčby
Ve farmakoterapii jsou dle současných doporučených postupů léky první volby nesedativní H1 antihistaminika 2. generace v třístupňovém pořadí; cílem této léčebné strategie je naprosté vymizení příznaků. Realistickým cílem je spíše dostat chorobu pod kontrolu, zmírnit příznaky, zabránit vzniku komplikací a snížit dopad na kvalitu života. Proto je pro celkové zvládání kopřivky významná i edukace o nemoci, možnostech a limitacích léčby, o prognóze, preventivních opatřeních a psychosomatický přístup lékaře k pacientovi. Lokální léčba, resp. péče o kůži, má podpůrný význam a je shodná s principy péče o kožní bariéru u ekzémů.
Volba léčby se řídí závažností, resp. dle reakce na léčbu. Závažnost urtikarie se hodnotí jednak dle aktuálního klinického nálezu, ale především dle anamnézy – vzhledem k prchavosti projevů je pacient v ordinaci totiž často asymptomatický. Závažnost se týká intenzity, rozsahu a průběhu kopřivky a rovněž kvality života. K objektivnějšímu hodnocení onemocnění lze použít tzv. skóre UAS7 (Weekly Urticaria Activity Score), kdy záznam průběhu choroby provádí samotný pacient do strukturovaného formuláře a denně v průběhu týdne tak sleduje počet pomfů a intenzitu pruritu [4,8,10].
Dle Doporučených postupů se k léčbě mají v první řadě používat nesedativní antihistaminika 2. generace jako symptomatická léčba snižující uvolňování mediátorů z mastocytů. Jedině při souvislém, denním užívání je možné snížit frekvenci výsevů, rozsah a intenzitu projevů. Vhodné je používat pouze H1 antihistaminika prověřená pro léčbu chronické urtikarie; poněvadž léčba je dlouhodobá, používají se i 2–4krát vyšší dávky, tudíž je třeba mít na paměti i potenciální toxicitu. Jedná se o následující léčiva (řazená abecedně): bilastin, cetirizin/levocetirizin, desloratadin/loratadin, fexofenadin a rupatadin [4,6,7,10,13]. Léčba sedativními antihistaminiky nebo léčba vyššími dávkami neprověřených antihistaminik se tedy z bezpečnostních důvodů u chronické urtikarie nedoporučuje.
Tato doporučení nejsou v praxi stále ještě dostatečně zažitá, přestože se v odborné literatuře objevila již před osmi lety. Při nízké účinnosti antihistaminika v běžném dávkování se používají spíše kombinace různých antihistaminik navzájem, než by se zvyšovala dávka jednoho antihistaminika. Kombinace sice nejsou zapovězeny, ale upřednostňuje se zvyšování dávky prověřeného nesedativního antihistaminika, zejména pro lepší bezpečnost při stejně dobré – ne‑li vyšší – účinnosti [4,6,7,13]. Z hlediska farmakokinetiky totiž při kombinaci různých antihistaminik mezi sebou dochází k blokování či ke snížení metabolizace jednoho či druhého antihistaminika. To s sebou nese i otázky tolerance a bezpečnosti takovéto kombinace.
Druhá linie léčby
Druhou linii léčby v současnosti představuje podání antihistaminika v dávkování zvýšeném na dvojnásobek až čtyřnásobek standardní dávky. Protože výše uvedená antihistaminika netvoří farmakologicky zcela homogenní skupinu (liší se v rychlosti nástupu účinku, v délce doby udržení účinné plazmatické koncentrace, v metabolizaci, ve vlivu na pozornost, v imunomodulačních účincích na cytokiny atd.), nemusí být jejich účinnost a bezpečnost identická, a navíc se může interindividuálně lišit. To odůvodňuje změnu antihistaminika při malé účinnosti za jiné antihistaminikum z této skupiny.
Třetí linie léčby
Pokud ani při zvýšeném dávkování uvedených antihistaminik není kopřivka pod kontrolou, přichází na řadu třetí možnost – přidání imunomodulačních/supresivních přípravků. Jmenovitě se jedná o montelukast nebo o cyklosporin A anebo omalizumab. Systémové kortikosteroidy se doporučují jen k nárazovému podání (7–10 dnů) pro zvládnutí akutní exacerbace. Léčebné schéma je doporučováno jak pro spontánní, tak pro fyzikální a další indukovatelné chronické urtikarie, avšak zde s ohledem na nedostatek studií nepanuje pro volbu dalších léků konsensus [4,6,7]. Antileukotrien montelukast a imunosupresivum cyklosporin A jako léky třetí linie se v indikaci chronické urtikarie v České republice pohybují v kategorii „off label use“, nicméně doporučené postupy na základě četných studií, kasuistik i denní praxe jejich použití jako přídatnou léčbu k antihistaminikům odůvodňují [4]. Jediným přípravkem schváleným v ČR pro léčbu třetí linie při těžké CSU je biologické léčivo omalizumab – viz dále v textu.
Léčba u dětí
Dle aktuálních doporučených postupů se má u dětí s chronickou urtikarií postupovat obdobně jako u dospělých, je třeba respektovat limitaci věkem (tab. 4). Bezpečnost vyššího dáv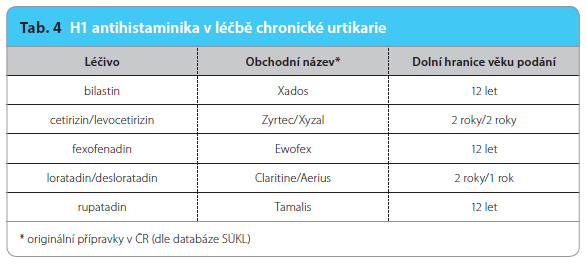 kování v pediatrické populaci je prověřena zatím u dvojic loratadin/desloratadin a cetirizin/levocetirizin [4]. Studie jsou prováděny obvykle s originálními přípravky, takže jak dolní věková hranice, tak bezpečnost vyšších dávek při dlouhodobém používání se mohou u generických antihistaminik výrazně lišit. Montelukast je v ČR schválen pro děti ve věku od šesti měsíců (preskripce je limitována na alergologa), cyklosporin A pro děti ve věku od jednoho roku (viz Souhrn údajů o přípravku, SPC).
kování v pediatrické populaci je prověřena zatím u dvojic loratadin/desloratadin a cetirizin/levocetirizin [4]. Studie jsou prováděny obvykle s originálními přípravky, takže jak dolní věková hranice, tak bezpečnost vyšších dávek při dlouhodobém používání se mohou u generických antihistaminik výrazně lišit. Montelukast je v ČR schválen pro děti ve věku od šesti měsíců (preskripce je limitována na alergologa), cyklosporin A pro děti ve věku od jednoho roku (viz Souhrn údajů o přípravku, SPC).
Léčba v těhotenství a při kojení
U gravidních žen a v laktaci se postupuje z hlediska bezpečnosti obdobně jako u dětí, tedy primárně je podáván loratadin/desloratadin a cetirizin/levocetirizin. Studie hodnotící bezpečnost použití vyšších dávek u gravidních žen nebyly prováděny [4].
Léčba v geriatrii
U starší populace nejsou k dispozici studie s antihistaminiky v léčbě chronické urtikarie. Nesedativní H1 antihistaminika je třeba volit pečlivě a individuálně vzhledem ke snížené jaterní metabolizaci a i s ohledem na snížené vylučování ledvinami [4]. Také lékové interakce mohou mít nežádoucí vliv nejen na účinnost léčby, ale zejména na její bezpečnost. Z tohoto pohledu se jako relativně nejšetrnější pro tuto populaci jeví bilastin, který se nemetabolizuje játry a nemá interakce cestou cytochromu P450 (viz SPC).
Omalizumab
Omalizumab je biologické léčivo, jediný schválený přípravek pro pacienty s těžkou CSU ve třetí linii léčby v ČR. Jedná se o monoklonální humanizovanou protilátku třídy IgG1 proti IgE vyrobenou technologií rekombinantní DNA v buněčné linii získané z vaječníků čínských křečků. Toto léčivo bylo vyvinuto pro léčbu bronchiálního astmatu. Impuls pro použití, resp. iniciování klinických studií pro podávání omalizumabu nemocným s CSU, vyšel od dermatologů, kteří na základě klinického výzkumu upozornili na potenciální roli tohoto léčiva u CSU v souvislosti s přítomností protilátek proti IgE a IgER. Podává se pouze parenterálně, jako přídatná léčba k antihistaminiku.
Preskripce léku je vázána na dermatologická centra biologické léčby. Indikačním kritériem je těžká CSU nereagující dostatečně na předchozí léčbu antihistaminiky podávanou i v dvojnásobně až čtyřnásobně vyšších dávkách, a to u osob starších 12 let. Z hlediska úhradových podmínek je v ČR indikace pouze pro těžkou CSU, kde je závažnost kvantifikována dosažením skóre UAS7 ≥ 28. Dávka a doba předchozího podávání antihistaminik jsou též specifikovány v materiálech Státního ústavu pro kontrolu léčiv: „…nedostatečná odpověď (UAS7 ≥ 28) po předchozí šestitýdenní konsekutivní léčbě H1 antihistaminiky, při které byl minimálně po dobu dvou týdnů podáván minimálně dvojnásobek obvyklé dávky H1 antihistaminik v monoterapii nebo byla podávána kombinace H1 antihistaminik v dávkách, jejichž součet odpovídá minimálně dvojnásobku obvyklé dávky H1 antihistaminik. Anebo nedostatečná odpověď (UAS7 ≥ 28) po předchozí čtyřtýdenní konsekutivní léčbě H1 antihistaminiky ve standardních dávkách v případě, že z důvodů toxicity, intolerance nebo kontraindikací nelze použít zvýšenou dávku antihistaminik podle předchozího kritéria.“
Účinek omalizumabu u CSU není dán přímo snížením hodnot IgE, což v praxi odpovídá faktu, že jak závažnost CSU, tak úspěch léčby nemusí korelovat s celkovou plazmatickou koncentrací IgE. Spíše se jedná o zásah do signálních drah na ose IgE–FcεRI (high‑affinity IgE receptor) a o zvýšení aktivačního prahu mastocytů. To vede ke snížení citlivosti a reaktivity mastocytů na signály a následně ke snížené tvorbě a uvolňování mastocytárních mediátorů. Omalizumab též vede ke sníženému uvolňování zánětlivých mediátorů a cytokinů z bazofilů v cévním řečišti (např. IL‑6, TNFα) a k poklesu atrahování imunitních buněk (jako jsou T-lymfocyty, makrofágy, eosinofily) do místa zánětu [6,14].
Dávkování omalizumabu u CSU se tedy na rozdíl od dávkování u astmatu neodvíjí od celkové plazmatické koncentrace IgE a není ani závislé na tělesné hmotnosti pacienta. Jedna aplikace představuje dvě subkutánní injekce o dávce 150 mg, tedy dávku 300 mg, která se podává ve zdravotnickém zařízení v intervalu čtyř týdnů. Jeden léčebný cyklus je definován jako šest podání dávky 300 mg. Omalizumab má jednak časný terapeutický účinek v řádu hodin/dnů (zhruba 24 hodin, tzv. fast responders), jednak pozdní účinek v řádu dnů/týdnů (zhruba 2–6 týdnů, tzv. slow responders) [6].
Zhodnocení z hlediska pokračování léčby se provádí po třech měsících léčby:
- v léčbě se pokračuje, pokud je účinná – pacient dosáhne snížení hodnoty skóre UAS7 o více než 11 bodů v porovnání s výchozí hodnotou, pak se dokončí šestiměsíční cyklus léčby;
- v léčbě se nepokračuje, pokud je nedostatečně účinná – pacient nedosáhne snížení hodnoty UAS7 skóre o více než 11 bodů v porovnání s výchozí hodnotou;
- v léčbě se nepokračuje, pokud pacient dosáhne kdykoliv po třech měsících i déle kompletního vymizení projevů (UAS7 = 0), tj. léčba je účinná a šestiměsíční cyklus léčby se nedokončí.
Opětovné zahájení léčby se provádí u pacientů, u kterých dojde k relapsu onemocnění, tedy ke zhoršení skóre UAS7 na vstupní indikační hodnoty 28 a více. Optimální by bylo v léčbě pokračovat souvisle, jako je tomu u biologické léčby psoriázy a jiných chronických chorob. Nicméně vzhledem k nákladnosti a také někdy vzhledem k ústupu spontánní urtikarie v průběhu léčby je úhrada nastavena takto. Z praxe či z osobních sdělení zahraničních kolegů s mnohaletou zkušeností s léčbou chronické urtikarie omalizumabem jsou známy případy, kde se díky výbornému účinku léčby omalizumabem snižuje dávka doprovodného antihistaminika na běžné dávkování či ho není vůbec třeba. Nastávají však i opačné situace, kdy je ke zvládnutí choroby zapotřebí dávkování omalizumabu vyššího než 300 mg. Také dávkování v udržovací léčbě může být modifikováno – jednou cestou je snížení dávky na 150 mg/měsíc anebo lze prodloužit interval na 6–8 týdnů (přednáška prof. Any Giménez‑Arnau, CSU Expert Speaker Academy, Kodaň, říjen 2015). Teprve vyhodnocování velkých souborů pacientů v dlouhodobém sledování (databáze, registry) ukáže, jaké další režimy jsou smysluplné z hlediska poměru účinnosti a nákladů i s ohledem na subtypy chronické urtikarie.
Omalizumab je v klinické praxi již od roku 2005, a to v léčbě těžkého astmatu, takže je k dispozici solidní množství bezpečnostních dat o jeho používání. Nejedná se o imunosupresivum, protituberkulózní a protinádorová imunita tedy nejsou dotčeny. Jako i jiné monoklonální protilátky může omalizumab řídce způsobovat reakce I. typu a sérovou nemoc. Častější jsou reakce v místě vpichu, cefalea, artralgie, infekce horních cest dýchacích. Zatím je schválen jen pro léčbu CSU, ve studiích i v kasuistikách se ukazují příznivé léčebné výsledky i v případě těžkých indukovatelných urtikarií [15,16].
Další léčebné možnosti
Tolik současné doporučené postupy. Jakou léčebnou strategii ale zvolit, když je chronická urtikarie rezistentní na antihistaminika i ve vysokých dávkách a další navržená léčiva nelze použít, protože jsou nedostupná, kontraindikovaná, netolerovaná, neúčinná, drahá atd.? Odborná literatura i praxe nabízejí další možnosti, jejich použití je však v kategorii „off label use“, tedy způsobem, který není v souladu s SPC. Uvádějí se antimalarika, sulfony, methotrexat, anticholinergika, kumariny, anti‑TNF a anti‑IL‑1 biologické léky, beta‑blokátory, botulotoxin, danazol, UVA či NBUVB (narrow band UVB) fototerapie, plazmaferéza či intravenózní imunoglobulin (IVIG), systémové kortikosteroidy. Tento výčet svědčí o tom, jak heterogenní skupinu chronické urtikarie představují, a předurčuje nutnost dalšího výzkumu z hlediska podrobnějšího poznání patogeneze, identifikace subtypů a cílené léčby.
Léčba nehistaminových angioedémů
Léčba nehistaminových angioedémů [4,6, 11,12] doznala též pokroku – u angioedémů zprostředkovaných bradykininem – především u angioedému indukovaného inhibitory ACE a u dědičného nebo získaného angioedému – se používá k akutní léčbě i k profylaxi před rizikovými zákroky koncentrát inhibitoru C1, k novým léčivům patří icatibant (antagonista receptoru pro bradykinin) a ekalantid (inhibitor kalikreinu).
Závěr
Léčba chronické spontánní urtikarie je náročná pro pacienta i pro lékaře. Žádný stávající lék není plně uspokojivý, což je dáno heterogenitou příčin, mediátorů, spouštěcích vlivů a omezenou možností zcela tyto vlivy pomocí prevence vyloučit či je léčbou bezpečně zablokovat. Oproti předchozím dobám však již existují doporučené postupy poskytující lékařům objektivně prověřené vodítko pro diagnostiku i léčbu. Každý lékař je v diagnostice i v léčbě individualitou z hlediska znalostí, schopností a přístupu k pacientovi. Používání doporučených postupů však vede jednoznačně ke zlepšení péče o pacienty a jejich léčby.
Léky první volby jsou pro léčbu chronické urtikarie prověřená nesedativní H1 antihistaminika, a to i ve zvýšeném dávkování (druhá linie léčby). Jako třetí linii léčby máme nyní k dispozici biologický lék omalizumab, přípravek, který může zlepšit zvládání choroby u nejtěžších případů. Tam, kde zvolená léčba nevede ke zlepšení (zmírnění) průběhu, je třeba hledat rezervy v diagnostice, v prevenci i v léčbě, pomýšlet i na souběh s jinými chorobami, problém pojímat v širších souvislostech a využívat mezioborové spolupráce. Individuální případy však nadále vyžadují individuální přístup, včetně psychosomatického.
Seznam použité literatury
- [1] Maurer M, Bindslev Jensen C, Gimenez Arnau A, et al. Chronic idiopathic urticaria is no longer idiopathic: time for an update. Br J Dermatol 2013; 168: 445–456.
- [2] Konstantinou GN, Asero R, Ferrer M, et al. EAACI taskforce position paper: evidence for autoimmune urticaria and proposal for defining diagnostic criteria. Allergy 2013; 68: 27–36.
- [3] Magen E, Waitman DA, Dickstein Y, et al. Clinical laboratory characteristics of ANA positive chronic idiopathic urticaria. Allergy Asthma Proc 2015; 36: 138–144.
- [4] Zuberbier T, Aberer W, Asero R, et al. EAACI/GA(2)LEN/EDF/WAO guideline for the definition, classification, diagnosis and management of urticaria: the 2013 revision and update. Allergy 2014; 7: 868–887.
- [5] Maurer M, Magerl M, Metz M, et al. Practical algorithm for diagnosing recurrent wheals or angioedema. Allergy 2013; 68: 816–819.
- [6] Maurer M, Church MK, Gonçalo M, et al. Management and treatment of chronic urticaria. J Eur Acad Dermatol Venereol 2015; 29 (Suppl. 3): 16–32.
- [7] Greenberger PA. Chronic urticaria – new management options. World Allergy Org J 2014; 7: 31.
- [8] Weller K, Zuberbier T, Maurer M. Chronic urticaria: tools to aid the diagnosis and assessment of disease status in daily practice. J Eur Acad Dermatol Venereol 2015; 29 (Suppl. 3): 38–44.
- [9] Mlynek A, Maurer M, Zalewska A. Update of chronic urticaria: focusing on mechanism. Curr Opin Allergy Clin Immunol 2008; 8: 433–437.
- [10] Benáková N. Současné praktické postupy pro vyšetřování a léčbu chronické urtikarie: aktualizovaný přehled a interpretace doporučených postupů pro praxi. Čes slov Derm 2015; 5: 177–224.
- [11] Craig T, et al. WAO guideline for the management of hereditary angioedema. World Allergy Organ J 2012; 5: 182–199.
- [12] Maurer M, Parish LC. The dermatology view of hereditary angiooedema: practical diagnostic and management considerations. J Eur Acad Dermatol Venereol 2013; 27: 133–141.
- [13] Church MK, Maurer M. H1 antihistamines and urticaria – how can we predict the best drug for our patient? Clin Exp Allerg 2012; 42: 1423–1429.
- [14] Chang TW, Chen C, Lin CJ, et al. The potential pharmacologic mechanisms of omalizumab in patients with chronic spontaneous urticaria. J Allergy Clin Immunol 2015; 135: 337–342.
- [15] Metz M, Ohanyan T, Church MK, et al. Omalizumab is an effective and rapidly acting therapy in difficult to treat chronic urticaria: a retrospective clinical analysis. J Dermatol Sci 2014; 11: 57–62.
- [16] Pezzolo O, Peroni A, Gisondi P, et al. Heat urticaria: revision of published cases with and update on classification and management. Br J Dermatol 2016, [Epub ahead of print], doi: 10.1111/bjd.14543.