Lokální terapie v léčbě syndromu diabetické nohy
Terapie syndromu diabetické nohy (SDN) by měla být komplexní a měla by vyžadovat spolupráci celé řady odborníků. Tento článek je zaměřen pouze na část terapie SDN, konkrétně na lokální terapii, se kterou se setkáváme při léčbě akutních či chronických ran, v našem případě diabetických ulcerací. V lokální léčbě diabetických ulcerací můžeme kromě různých forem čištění rány (debridementu) využít celou řadu antiseptik a moderních krytí fungujících na principu vlhké terapie. Lze používat i terapeutické prostředky pracující moderními technologiemi, které dle studií naznačují slibný potenciál v hojení těchto typů ran.
Úvod
Komplexní léčba syndromu diabetické nohy [1], zejména chronických diabetických ulcerací, vyžaduje nejen léčbu infekčních komplikací, adekvátně zvolené metody odlehčení, zhodnocení stavu cévního řečiště včetně stavu mikrocirkulace [2], kontrolu kompenzace diabetu, stavu nutrice a řešení psychosociálních otázek [3], ale i adekvátní lokální terapii.
Lokální léčba diabetických ulcerací má zahrnovat debridement spodiny rány a jejího okolí a ošetření spodiny rány správně zvolenými terapeutickými přípravky, které pomohou:
- nastartovat tvorbu granulací a epitelizace z okrajů rány,
- ochránit ránu před negativními vlivy zevního prostředí,
- optimalizovat vnitřní prostředí rány, např. pH nebo enzymatických procesů,
- podle typu rány snížit nebo zvýšit sekreci, odstranit zápach z rány apod.
Je třeba zdůraznit, že jednotlivé metody a prostředky hojení ran musejí být náležitě indikovány, protože správně fungují jen v určitých fázích hojení ran – např. jiné přípravky je vhodné používat u ran s vysušenou spodinou, jiné u nekrotických ran pacientů s ischemickou chorobou dolních končetin (ICHDK) nebo např. u povleklých silně zapáchajících ran. Při nevhodně zvolené metodě lokální léčby může dojít k progresi lokálního nálezu včetně nekrotizace tkání, prohloubení rány nebo např. k urychlení rozvoje infekce (pomnožení mikrobů pod nevhodně zvoleným krytím).
Lokální terapie
Podle expertní skupiny International Working Group on the Diabetic Foot (IWGDF) [4] a podle odborných prací [5] neexistují studie, které by na základě medicíny založené na důkazech prokázaly s dostatečnou silou efektivitu lokální terapie. Podle studií tvoří výjimku pouze hyperbarická terapie (hyperbaric oxygen therapy, HBOT) a léčba podtlakem (negative-pressure wound therapy, NPWT). Problémy dosud publikovaných studií tkví v tom, že do valné většiny z nich bylo zařazeno malé množství studovaných subjektů, studie byly mnohdy velmi heterogenní, neměly jednotná hodnotící kritéria, probíhaly velmi krátce, nebyly zaslepené a randomizované. Práce obvykle porovnávají pouze účinnost dvou přípravků určených k lokální aplikaci – tj. zkoumaného přípravku a aktivního komparátoru, kterým bývá nedostatečně definovaná „obvyklá léčba“.
Proto se výběr prostředků lokální terapie řídí empirií pramenící z klinických zkušeností jednot![Obr. 1 Systém T.I.M.E. používaný k hodnocení ran posuzuje spodinu ulcerace, množství a typ sekretu, zápach, hloubku ulcerace, přítomnost osteomyelitidy a další; podle [36] – Jeffcoate, et al., 2004. T – tkáň, spodina ulcerace; I – infekce; M – moisture, sekrece; E – epitelizace](https://www.remedia.cz/photo-a-30005---.jpg) livých pracovišť či z mínění expertů na tuto problematiku. Vždy je nutné vzít do úvahy nejen typ rány, konkrétně její vzhled (např. systém T.I.M.E. používaný k hodnocení ran; T – tkáň, spodina ulcerace; I – infekce; M – moisture, sekrece; E – epitelizace) a okolí (např. hyperkeratózy, lokální edém, flegmóna, macerace), ale i systémové faktory, které mohou hojení významně modifikovat (např. ICHDK, otoky dolních končetin, chronická žilní insuficience a další), viz obr. 1 [9].
livých pracovišť či z mínění expertů na tuto problematiku. Vždy je nutné vzít do úvahy nejen typ rány, konkrétně její vzhled (např. systém T.I.M.E. používaný k hodnocení ran; T – tkáň, spodina ulcerace; I – infekce; M – moisture, sekrece; E – epitelizace) a okolí (např. hyperkeratózy, lokální edém, flegmóna, macerace), ale i systémové faktory, které mohou hojení významně modifikovat (např. ICHDK, otoky dolních končetin, chronická žilní insuficience a další), viz obr. 1 [9].
Při lokálním ošetření nejprve provádíme debridement v dostatečném rozsahu na spodině ulcerace a v jejím okolí (odstranění hyperkeratóz). Dále podle typu rány a s přihlédnutím k ostatním faktorům se lokálně aplikují různé typy krytí nebo antiseptické roztoky. K podpoře hojení ran můžeme využít i různé technologie a jiné způsoby léčby, které prozatím označujeme za adjuvantní, neboť jejich účinek nebyl u pacientů se SDN jednoznačně prokázán nebo působí na systémové bázi.
Debridement
Debridement je definován jako odstranění cizího materiálu a nekrotických nebo kontaminovaných tkání z traumatické nebo infikované léze. Debridement tedy slouží zejména k odstranění nekrotické tkáně, která brání růstu granulací a pod níž dochází k pomnožení bakterií a tvorbě hnisu, eventuálně k progresi rány do hlubších etáží kůže, podkoží nebo do hlubších tkáňových struktur (šlachových a kloubních pouzder), v některých případech i k indukci osteomyelitidy. Podobně je vhodné odstranit i fibrinové povlaky. Debridement by měl být dostatečný, tzn. až do zdravé tkáně, kterou by měl odhalit a tím napomoci hojení ran [7]. Cílem správně
- provedeného debridementu je:
- odstranit bakteriální nálož,
- odstranit nekrotickou tkáň,
- zmírnit zánětlivou reakci okolí,
- zredukovat zápach,
- snížit sekreci z rány,
- zlepšit průnik různých působků, léčivých látek a aktivních substancí do tkání [5].
- enzymatický (používají se proteolytické enzymy v gelech, olejích – např. kolagenázy);
- autolytický (hydrogely, hydrokoloidy, hydrofibery – podporují aktivitu vlastního enzymatického systému při čištění rány);
- biologický (aplikace larev – provádějí nejen debridement, ale působí i protiinfekčně svými antimikrobiálními peptidy a podporují tvorbu granulací tím, že stimulují tvorbu růstových faktorů a mechanicky dráždí spodinu rány; obr. 2)[9–11]. Dle metaanalýzy Tiana a kol. larvální terapie zvyšuje počet zhojených ulcerací, snižuje počet amputací a zkracuje dobu hojení i délku antibiotické terapie [12];
- ostrý (chirurgický);
- mechanický (např. metoda wet-to-dry, s použitím gázy, parafínu);
- přímý/nepřímý debridement (pomocí hydroterapie, ultrazvuku nebo léčby řízené podtlakem);
-
ostatní (zahrnuje např. metody absorpční, osmoticky aktivní – medicinální med).
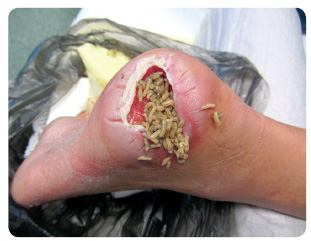
První dva typy debridementu – enzymatický a autolytický – je vhodné provádět za pravidelného sledování odborníky, protože při nich hrozí macerace tkáně a lýza zdravých struktur nebo prohloubení rány do hlubších struktur vlivem přítomné neuropatie (pacient ztrácí citlivost nohou na zevní podněty), především však při poruše bariér hrozí šíření infekce (flegmóna, osteomyelitida).
Léčba řízeným podtlakem
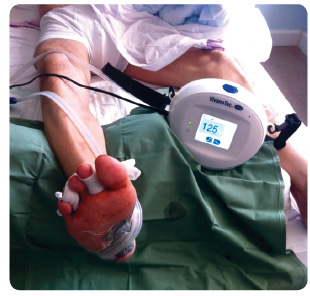
Léčba podtlakem urychluje hojení ran, zejména sekundárních (ran po amputacích, pooperačních) [13]. Jako každá metoda má i NPWT své výhody a nevýhody. Jak již bylo uvedeno, urychluje hojení ran akcelerací růstu granulací, dále napomáhá mechanickému debridementu, odvádí v dostatečné míře exsudát z rány a tím snižuje bakteriální nálož v ráně. Zároveň stimuluje angiogenezi a zlepšuje lokální prokrvení rány, viz obr. 3 [14].
Nevýhodou NPWT je v některých případech přerůstání granulací nad požadovanou úroveň a křehkost novotvořených granulací, které mají větší te![Obr. 3 Léčba řízeným podtlakem u chronických ran; podle [15] – Bém, et al., 2006.](https://www.remedia.cz/photo-a-30007---.jpg) ndenci ke krvácení. NPWT není indikována u pacientů s prokázanou kritickou ICHDK a u ran s hlubokými fistulemi s nejasným vyústěním a/nebo s obnaženými cévami na spodině [14, 15].
ndenci ke krvácení. NPWT není indikována u pacientů s prokázanou kritickou ICHDK a u ran s hlubokými fistulemi s nejasným vyústěním a/nebo s obnaženými cévami na spodině [14, 15].
Existují systémy NPWT, které se běžně používají za hospitalizace, viz obr. 4a, b, nebo ambulantně, viz obr. 5, systémy využívané pouze jednorázově (měly by být stejně efektivní jako ostatní podtlakové systémy) [16] nebo systémy určené pro povrchové rány. Poslední novinkou je využití podtlakových systémů k podpoře hojení autoepidermálními štěpy (vytvářejí se seříznutím částí povrchu kůže, jež jsou za pomoci podtlaku nasáty do speciální komůrky; obr. 6a, b). Ty lze po vygranulování rány použít ke krytí rozsáhlejších povrchových defektů k jejich „doepitelizování“.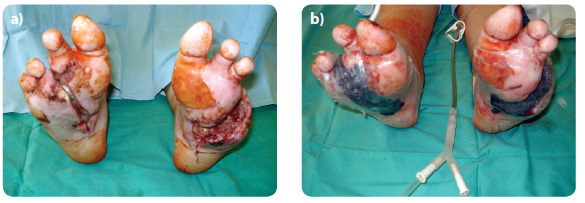
Lokální léčivé přípravky
Lokální přípravky používáme k léčbě SDN v naší klinické praxi poměrně často. Měly by splňovat celou řadu požadavků, např.:
- optimalizovat vnitřní prostředí rány (včetně pH),
- dodávat účinné látky, které mají např. proti-
- infekční účinky,
- zevně krýt ránu a bránit tak jejímu znečištění,
- čistit ránu,
- odvádět exsudát z rány,
-
napomáhat tvorbě granulací či epitelizaci.
Snažíme se využívat metod vlhkého hojení, které jsou schopny optimalizovat vnitřní prostředí a udržet optimální vlhkost rány. Ve vlhkém prostředí dochází rychleji k migraci epidermálních buněk, což urychlí růst epidermis, angiogenezi a syntézu pojivové tkáně. Výběr lokální léčby by se měl řídit přítomností či nepřítomností ischemie, závažností diabetické ulcerace (rozdílným způsobem se léčí povrchové ulcerace a hluboké rány s postižením kloubů, kostí apod.), fází procesu hojení, množstvím exsudátu, umístěním ulcerace a především přítomností infekce atd. [17, 18]. Zde je důležité zdůraznit, že rány diabetiků se chovají jiným způsobem nežli rány pacientů bez diabetu.
Lokální přípravky lze dělit do několika kategorií podle účinné látky, kterou krytí obsahují (např. přípravky se stříbrem, jodem, medicínským medem apod.), podle vehikula, které účinnou látku váže (např. mřížky, pěny apod.), nebo podle typu ran, pro které se používají (krytí pro výrazně secernující rány, k čištění ran apod.). Pokud zvolíme pro nás jednodušší typ dělení, a to posledně zmiňovaný, setkáváme se běžně s přípravky určenými např. k epitelizaci, přípravky podporujícími tvorbu granulací, přípravky k odstranění nekróz apod.
Přípravky k čištění ran ![Obr. 6 a, b Vznik autoepidermálních štěpů pomocí lokálně aplikovaného podtlaku; podle [37] – www.deseretnews.com](https://www.remedia.cz/photo-a-30010---.jpg)
K vyčištění spodiny rány lze používat např. algináty (mají bakteriostatický a hemostatický účinek, podporují autolytický debridement), hydrogely (optimalizují vlhkost rány, odstraňují nekrotické a fibrinové povlaky), hydrokoloidy (podporují autolytický debridement) nebo hydrofibery (absorbují exsudát a také podporují autolytický debridement).
Přípravky určené pro nadměrně secernující rány
Zvýšenou exsudaci lze ovlivnit lokálními přípravky, které mají sklon ránu spíše vysušovat nebo mají schopnost absorbovat nadbytečné množství exsudátu (různé formy aktivního uhlí, přípravky s jodem, algináty, hyperosmolární krytí s obsahem NaCl apod.).
Přípravky s protiinfekčním působením
V této skupině můžeme používat ke krytí ran přípravky s antiinfekčně působícími látkami a antiseptické roztoky. Mezi krytí napomáhající boji proti infekci patří přípravky obsahující např. molekuly stříbra, polyhexamethylen biguanid (PHMB) nebo medicinální med. Některé přípravky jsou dokonce schopny pomocí chemických vazeb vázat bakterie nebo mykotická agens na svůj povrch a při snímání je v podstatě mechanicky odstraňovat.
Antiseptika často využíváme k oplachům nebo k obkladům infikovaných ran. Výhodou antiseptik je také jejich lepší průnik do hlubších struktur, proto je můžeme používat i k léčbě infikovaných kavit nebo fistulí (obdobně jako hydrogely). Nejčastěji používáme ředěné roztoky s jodem, dále antiseptika s chlorhexidinem (účinný vůči grampozitivním a gramnegativním bakteriím), s PHMB (účinný i vůči bakteriím v biofilmech), se superokysličenou vodou (baktericidní, fungicidní, sporicidní, účinná i vůči virům) či s octenidindihydrochloridem (působí na grampozitivní i gramnegativní bakterie, na rezistentní patogeny včetně MRSA – methicilin-rezistentní Staphylococcus aureus, houby a protozoa), fakultativně užíváme i ozonizovanou vodu.
Lokální aplikaci antibiotik spíše nedoporučujeme, jelikož nebyl prokázán jejich klinický účinek [19]. Nutno dodat, že lokální antibiotika mohou snadněji indukovat antibiotickou rezistenci, působí cytotoxicky na rány [7], dokonce mohou alergizovat a iritovat okolí diabetických ulcerací. Výjimkou může být aplikace speciálních hemostaticky působících pěn nebo cementových hmot obohacených gentamicinem, které se používají zejména při chirurgických výkonech u pacientů se SDN, nejčastěji u resekcí a nízkých amputací, kde bylo prokázáno zkrácení doby hojení, ale vždy v návaznosti na pravidelné podiatrické kontroly a kontroly chirurgem [20].
Přípravky podporující tvorbu granulací
Tvorbu granulací podporují např. foamy (vytvářejí vhodné mikroklima, stimulují čištění rány, absorbují nadměrný exsudát a zabraňují průniku patogenů zvenku), hydrofibery, hydrokoloidy, které aplikujeme na vyčištěnou spodinu rány. Tato krytí mají schopnost udržet v ulceraci optimální vlhkost.
Přípravky určené k epitelizaci
Epitelizaci se snažíme zlepšit aplikací mřížek s různými účinnými látkami (jod, chlorhexidin acetát), přípravků s oxidovanou celulózou, foamů apod.
Jiná terapeutika
Další možností lokální terapie, ovšem ekonomicky náročnější, je aplikace náhradních kožních krytů. Principem této metody je uvolňování růstových faktorů z kultivovaných keratinocytů, které podporují granulaci a epitelizaci, protože u diabetických ulcerací se setkáváme s poruchou angiogeneze a produkce růstových faktorů. Náhradní kožní kryty dělíme na epidermální (např. keratinocyty), dermoepidermální a dermální (např. xenografty). Tyto kryty jsou schopny zvyšovat sekreci kolagenu, fibronektinu a růstových faktorů [19]. Xenografty (např. acelulární prasečí dermis (Xe-derma) se používají ke krytí ran, zabraňují průniku infekce, podporují tvorbu granulací a zároveň zamezují jejich nadměrnému vytváření.
Další kapitolu tvoří kolageny, které využíváme ke krytí hlubších ran, včetně pooperačních. Jejich aplikace vyžaduje čistou granulující spodinu. Kolagen absorbuje exsudát z rány a následně vytváří gel na povrchu rány. Podporuje migraci buněk, stimuluje fibroblasty, makrofágy a keratinocyty. Pomocí kolagenu můžeme dosáhnout rychlejšího hojení hlubokých ulcerací nebo operačních ran.
Spíše experimentálně se v lokální terapii dají využívat růstové faktory. Ty mohou na lokální úrovni stimulovat tvorbu granulační tkáně a podpořit epitelizaci [21]. Pozitivní výsledky byly zaznamenány např. po aplikaci destičkového růstového faktoru (platelet derived growth factor, PDGF). V České republice je dostupný rekombinantní PDGF používaný ve formě gelu. Je určen k léčbě chronických ran, ovšem v terénu dobrého cévního zásobení.
Novinkou v lokální léčbě je tzv. leukopatch, přípravek vyráběný z krve pacienta. Centrifugací vzorku dochází k separaci plazmy, erytrocytů a leukocytů s trombocyty. Jmenované skupiny buněk se v podobě tenké gelové vrstvy odnímají ze separátoru a následně se aplikují přímo na ránu.
Adjuvantní terapie
Za adjuvantní terapii považujeme léčbu podporující hojení ran, jejíž výsledky však dosud nebyly jednoznačně prokázány medicínou založenou na důkazech a o jejíž efektivitě jsme spíše přesvědčeni na základě zkušeností z klinické praxe. Některé z metod mají působit přímo na ránu – sem patří např. léčba laserem, ultrazvukem včetně rázové vlny, elektrickým proudem. Systematický přehled Kwana a kol. hodnotil efektivitu terapie diabetických ulcerací elektrickou stimulací, nízkonapěťovým laserem, ultrazvukem (UZ) a elektromagnetickým polem. Metody byly účinné, ale je třeba poznamenat, že studie začleněné do této analýzy zahrnuly malý počet nemocných a měly
nízkou sílu důkazu [22].
Studie DANTE zkoumala fotodynamickou terapii, která je bezpečnou metodou používanou v léčbě diabetických ulcerací, má schopnost snižovat bakteriální nálož a zvyšovat procento zhojených nemocných. V této studii se zkoumal antimikrobiální účinek lokálně aplikovaného fotoaktivního gelu a červeného světla (randomizovaná, dvojitě zaslepená studie kontrolovaná placebem). Studie potvrdila na dávce závislý antibakteriální účinek gelu, ale nebylo jasně deklarováno, vůči kterým mikrobiálním agens je metoda nejúčinnější. Dalším nedostatkem studie Dante bylo krátkodobé působení fotodynamické terapie – po první léčebné aplikaci došlo u nemocných ke zpětnému nárůstu počtu bakterií do 14 dnů) [23, 24].
Jiné metody jsou schopny ovlivňovat hojení ran nepřímo, např. zvýšením koncentrace kyslíku v tkáních. Kyslík je důležitý z hlediska hojení ran – je nutný pro správné fungování např. enzymatických pochodů a podílí se tak na hojení ran přímo (keratinocyty, fibroblasty) nebo nepřímo (aktivace buněk imunitního systému, produkce volných kyslíkových radikálů, produkce růstových faktorů) [25, 26].
Zvýšení dodávky kyslíku do periferních tkání lze docílit několika způsoby – ozonoterapií, hyperbarickou terapií, lokální oxygenoterapií a především 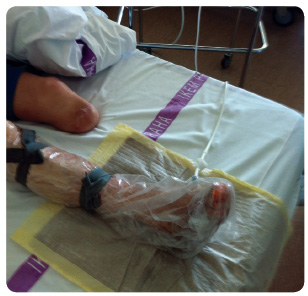 samotnými revaskularizačními metodami.Ozonoterapie – je schopna inaktivovat bakterie, viry a plísně destrukcí jejich buněčných stěn (virových kapsid) vlivem oxidace buněčných partikulí. Ozonoterapie snižuje bakteriální nálož, dokonce je schopna eliminovat i multirezistentní bakterie, viz obr. 7 [25].
samotnými revaskularizačními metodami.Ozonoterapie – je schopna inaktivovat bakterie, viry a plísně destrukcí jejich buněčných stěn (virových kapsid) vlivem oxidace buněčných partikulí. Ozonoterapie snižuje bakteriální nálož, dokonce je schopna eliminovat i multirezistentní bakterie, viz obr. 7 [25].
Hyperbarická terapie (hyperbaric oxygen therapy, HBOT) – zvyšuje koncentraci kyslíku v plazmě vdechováním kyslíku za hyperbarických podmínek [27]. Mimo jiné stimuluje angiogenezi, má antiedematózní i protiinfekční účinky [28, 29]. Účinek HBOT byl potvrzen randomizovanou, dvojitě zaslepenou, placebem kontrolovanou studií HODFU [30]. Tato metoda ale vyžaduje alespoň částečně průchodné cévní řečiště. Je ekonomicky náročnější (nutno absolvovat minimálně 30 sezení) a je spojena s řadou kontraindikací a nežádoucích účinků [31, 32]. HBOT je indikována u nemocných, u nichž je možné danou metodou dostatečně zvýšit tenzi transkutánního kyslíku (TcPO2). Minimální hodnoty TcPO2 v periferní tkáni by měly být alespoň 25 mm Hg [33] a při 2,5 ATA by se měl zvyšovat tlak TcPO2 nad 200 mm Hg.
Lokální oxygenoterapie (topical wound oxygenation) – zvyšuje difuzi molekul kyslíku přes kůži. Tato metoda má i antiedematózní účinek vlivem intermitentně působící komprese na dolní končetinu. Lokální oxygenoterapie působí pouze krátkodobě a do vzdálenosti zhruba 2–5 mm [34]. Proto je tato metoda podle našich zkušeností vhodnější spíše pro povrchové rány. Efektivita lokální oxygenoterapie není doložena výsledky medicíny založené na důkazech (úroveň 1). Další nevýhodou je logistická náročnost aplikací lokální oxygenoterapie (nutno absolvovat minimálně 20 sezení v krátkém časovém horizontu) [35].Samotné revaskularizační metody, jako je PTA (perkutánní transluminální angioplastika) či bypass, pak už představují léčbu intervenční a vyžadují vysoce individualizovaný přístup ke každému nemocnému.
Závěr
V lokální léčbě SDN lze vyžít moderní krytí i technologie, které usnadňují debridement, eliminaci mikrobiálních agens, pomáhají stimulovat tvorbu granulací a přispívají k epitelizaci. Pro objektivní zhodnocení lokální terapie se doporučují randomizované studie jednoznačně potvrzující nejen efektivitu, ale i ekonomický přínos jednotlivých přípravků či metod. Nesmíme však nikdy zapomenout na nezbytnost komplexního přístupu k pacientům se SDN a spokojit se pouze s částí léčebného procesu. Pacienta se syndromem diabetické nohy je třeba odeslat na podiatrickou ambulanci, kde by měl být vypracován plán komplexní terapie včetně odlehčení, léčby infekce, ozřejmení stavu cévního řečiště a eventuálně by mělo být dle potřeby provedeno chirurgické ošetření pacienta.
Práce byla podpořena projektem (Ministerstva zdravotnictví) rozvoje výzkumné organizace 00023001 (IKEM) – Institucionální podpora.
Seznam použité literatury
- [1] Jirkovská A. a spol. Syndrom diabetické nohy, 1. vydání. Jessenius Maxdorf, Praha, 2006.
- [2] Fejfarová V, Jirkovská A. Ischemická choroba dolních končetin u pacientů s diabetes mellitus. Postgraduální medicína 2013; 15: 169–175.
- [3] Fejfarová V, Jirkovská A, Dragomirecká E, et al. Does the diabetic foot have a significant impact on selected psychological or social characteristics of patients with diabetes mellitus? J Diabetes Res 2014: 371938. doi: 10.1155/2014/371938. Epub 2014 Mar 25.
- [4] International Consensus on the Diabetic Foot 2011.
- [5] Gottrup F, Apelqvist J. Present and new techniques and devices in the treatment of DFU: a critical review of evidence. Diabetes Metab Res Rev 2012; 28 (Suppl 1): 64–71.
- [6] Fejfarová V, Jirkovská A, Bém R, et al. Diagnostika a infekce u pacientů se syndromem diabetické nohy. Remedia. 2014; 24: 15–20.
- [7] Stryja H. Repetitorium hojení ran. 1. vydání, Geum, Semily, 2008.
- [8] EWMA Document: Debridement, J Wound Care, 2013.
- [9] Bowling FL, Salgami EV, Boulton AJ. Larval therapy: a novel treatment in eliminating methicillin-resistant Staphylococcus aureus from diabetic foot ulcers. Diabetes Care 2007; 30: 370–371.
- [10] Jaklic D, Lapanje A, Zupancic K, et al. Selective antimicrobial activity of maggots against pathogenic bacteria. J Med Microbiol 2008; 57(Pt 5): 617–625.
- [11] Ceřovský V, Bém R. Lucifensins, the Insect Defensins of Biomedical Importance: The Story behind Maggot Therapy. Pharmaceuticals (Basel) 2014; 7: 251–264.
- [12] Tian X, Liang XM, Song GM, et al. Maggot debridement therapy for the treatment of diabetic foot ulcers: a meta-analysis. J Wound Care 2013; 22: 462–469.
- [13] Armstrong DG, Lavery LA. Negative pressure wound therapy after partial diabetic foot amputation: a multicentre, randomised controlled trial. Lancet 2005; 366: 1704–1710.
- [14] Šimek M, Bém R, et al. Podtlaková léčba ran. 1. vydání, Maxdorf Jesenius, Praha, 2013.
- [15] Bém R, Fejfarová V, Jirkovská A. Terapie syndromu diabetické nohy pomocí řízeného podtlaku (V. A. C. –Vacuum Assisted Closure). Prakt Lek 2006; 86: 268–270.
- [16] Armstrong DG, Marston WA, Reyzelman AM, Kirsner RS. Comparative effectiveness of mechanically and electrically powered negative pressure wound therapy devices: a multicenter randomized controlled trial. Wound Repair Regen 2012; 20: 332–341.
- [17] Millington JT, Norris TW. Effective treatment Strategies for diabetic foot wounds. J Fam Pract 2000; 49 (Suppl): S40–S48.
- [18] Gardiny KG, Jones V, Price P. Topical treatment: which dressing to chaose. Diabetes Metab Res Rev 2000; 16 (Suppl 1): S47–S50.
- [19] Brem H, Sheehan P, Boulton AJM. Protocol for treatment of diabetic foot ulcers. Am J Surg 2004; 187 (Suppl.): 1S–10S.
- [20] Varga M, Sixta B, Bem R, et al. Application of gentamicin-collagen sponge shortened wound healing time after minor amputations in diabetic patients – a prospective, randomised trial. Arch Med Sci 2014; 10: 283–287.
- [21] Steed DL. The role of growth factors in wound healing. Surg Clin North Am 1997; 77: 575–586.
- [22] Kwan RL, Cheing GL, Vong SK, Lo SK. Electrophysical therapy for managing diabetic foot ulcers: a systematic review. Int Wound J 2013; 10: 121–131.
- [23] Morley S, Griffiths J, Philips G, et al. Phase IIa randomized, placebo-controlled study of antimicrobial photodynamic therapy in bacterially colonized, chronic leg ulcers and diabetic foot ulcers: a new approach to antimicrobial therapy. Br J Dermatol 2013; 168: 617–624.
- [24] Mannucci E, Genovese S, Monami M, et al. Photodynamic topical antimicrobial therapy for infected foot ulcers in patients with diabetes: a randomized, double-blind, placebo-controlled study – the D.A.N.T.E (Diabetic ulcer Antimicrobial New Topical treatment Evaluation) study. Acta Diabetol 2014; 51: 435–440.
- [25] Elvis AM, Ekta JS. Ozone therapy: A clinical review. J Nat Sci Biol Med 2011; 2: 66–70.
- [26] Blackman E, Moore C, Hyatt J, et al. Topical wound oxygen therapy in the treatment of severe diabetic foot ulcers: a prospective controlled study. Ostomy Wound Manage 2010; 56: 24–31.
- [27] Fejfarová V, Jirkovská A. Hyperbarická oxygenoterapie podporuje hojení chronických diabetických ulcerací. Kazuistiky v diabetologii 2011; 9: 32–34.
- [28] Caravaggi C. Role of HBO in the management of infected ulcers of ischemic diabetic foot. Abstrakt v EWMA Abstract Book 2007, str. 97.
- [29] Almzaiel A, Smerdon G, Billington R, et al. Mechanisms by which hyperbaric oxygen therapy may resole inflammation. Abstrakt v EWMA Abstract Book 2011, str. 66.
- [30] Löndahl M, Katzman P, Nilsson A, Hammarlund C. Hyperbaric oxygen therapy facilitates healing of chronic foot ulcers in patients with diabetes. Diabetes Care 2010; 33: 998–1003.
- [31] Fagher K, Landin-Olsson I, Katzman L, et al. Improved survival in patients with diabetes and chronic foot ulcers after Hyperbaric Oxygen Therapy. Outcome of a randomized double-blind placebo controlled study. Abstrakt v Abstract Book Diabetic foot 2011: 179–180.
- [32] Gore A, Muralidhar M, Espey MG, et al. Hyperoxia sensing: from molecular mechanisms to significance in disease. J Immunotoxicol 2010; 7: 239–254.
- [33] Löndahl M, Katzman P, Hammarlund C, et al. Relationship between ulcer healing after hyperbaric oxygen therapy and transcutaneous oximetry, toe blood pressure and ankle-brachial index in patients with diabetes and chronic foot ulcers. Diabetologia 2011; 54: 65–68.
- [34] Cronjé FJ. Oxygen therapy and wound healing – topical oxygen is not hyperbaric oxygen therapy. S Afr Med J 2005; 95: 840.
- [35] Howard MA, Asmis R, Evans KK, Mustoe TA. Oxygen and wound care: a review of current therapeutic modalities and future direction. Wound Repair Regen 2013; 21: 503–511.
- [36] Jeffcoate WJ, Price P, Gardiny KG. Wound healing and treatments for people with diabetic foot ulcers. Diabetes Metab Res Rev 2004; 20 (Suppl 1): S78–S89.
- [37] http://www.deseretnews.com/article/865586792/New-skin-graft-method-in-use-at-Provo-hospital.html?pg=all; Navštíveno 7. 10. 2014.