Novinky v léčbě pacientů s pokročilým maligním melanomem
Maligní melanom je nejagresivnější kožní nádor s dramaticky rostoucí incidencí. Pacienti s pokročilým onemocněním mají velmi špatnou prognózu. Dosud standardní léčba spočívající v chemoterapii nebo biochemoterapii nedokázala zásadně ovlivnit přežití pacientů. Pokroky v oblasti imunologie a molekulární biologie umožnily vývoj nových léků, založených na stimulaci imunitního systému (moderní imunoterapie) nebo přímo namířených proti nádoru (cílená léčba). Jak ipilimumab (protilátka proti cytotoxickému T lymfocytárnímu antigenu 4, CTLA-4), tak vemurafenib (inhibitor BRAF kinázy) dokázaly prodloužit celkové přežití ve velkých randomizovaných klinických studiích III. fáze. Tyto léky se stávají novým standardem v léčbě pacientů s melanomem v pokročilém stadiu. K dalším velmi nadějným přípravkům z oblasti cílené léčby patří dabrafenib (selektivní BRAF inhibitor) a trametinib (MEK inhibitor).
Úvod
Incidence maligního melanomu celosvětově dramaticky narůstá. Za posledních třicet let se v České republice znásobila téměř 5krát; v roce 2010 bylo zachyceno 24 nových případů na 100 000 obyvatel. Problematický je stále rostoucí výskyt maligního melanomu u mladých lidí. Příčiny jsou pravděpodobně multifaktoriální, velkou roli zřejmě hraje změna životního stylu. Přibližně 80–85 % pacientů je dnes diagnostikováno s lokalizovaným onemocněním, 10–15 % s postižením regionálních lymfatických uzlin a zhruba 5 % se vzdálenými metastázami [1].
Prognóza pacientů s diseminovaným maligním melanomem je stále velmi nepříznivá. Medián přežití se pohybuje mezi 6–9 měsíci [2]. Délka života pacientů s pokročilým melanomem je do velké míry určována místem a rozsahem metastatického postižení.
Melanom patří k nádorům s primární rezistencí k chemoterapii a radioterapii. Za posledních třicet let proběhlo mnoho klinických studií III. fáze, ve kterých byla zkoušena různá cytostatika a jejich kombinace s imunoterapií (interleukin-2, interferon alfa, protinádorové vakcíny), bohužel bez zásadního ovlivnění přežití [3–5]. Velké naděje jsou dnes vkládány do moderní imunoterapie a cílené léčby.
Pro rychlejší orientaci v následujícím textu jsou vysvětleny základní termíny, které mají vztah k hodnocení efektu léčby:
- CR (complete response) – kompletní léčebná odpověď, vymizení všech měřitelných i případně neměřitelných známek onemocnění;
- PR (partial response) – částečná léčebná odpověď (dle kritérií WHO zmenšení měřitelných lézí o 50 % a více, dle kritérií RECIST zmenšení o 30 % a více)*;
- SD (stable disease) – stabilizace onemocnění (dle kritérií WHO zmenšení měřitelných lézí do 50 % nebo zvětšení do 25 %, dle kritérií RECIST zmenšení do 30 % nebo zvětšení do 20 %)*;
- PD (progressive disease) – progrese onemocnění (vznik nového ložiska nebo dle kritérií WHO zvětšení měřitelných lézí nad 25 %, dle kritérií RECIST zvětšení nad 20 %)*;
- RR (response rate) – počet léčebných odpovědí (CR + PR), udává se často v procentech;
- PFS (progression free survival) – čas bez progrese onemocnění;
- OS (overall survival) – celkové přežití;
- linie léčby – fáze léčby, během níž je podáván lék nebo kombinace léků. Její trvání je limitováno účinností a toxicitou léčby. Pokud léčba selže, dochází k její změně a pak mluvíme o další linii léčby. Pacient tak podstupuje první linii léčby, druhou linii léčby, případně další linie; záleží na diagnóze, léčebných možnostech, cílech a celkovém stavu pacienta.
Moderní imunoterapie
Jednou z příčin vzniku nádorového onemocnění je selhání funkcí imunitního systému. Základním úkolem imunoterapie je proto obnovení a stimulace protinádorové imunity. Rozsáhlý výzkum v oblasti protinádorových vakcín, cytokinů (interferony, interleukiny) a adoptivních buněčných terapií (tumor infiltrující lymfocyty – TIL) zatím nepřinesl velký průlom. Problémem bývá nedostatečná účinnost léčby. V případě TIL, i přes slibné léčebné výsledky, je překážkou technicky a finančně náročná příprava buněk. Větších úspěchů na poli imunoterapie bylo nedávno dosaženo pomocí blokády tzv. negativních regulačních molekul, jako je CTLA-4 (cytotoxický T lymfocytární antigen 4) a PD-1 (programmed death-1) receptor na T lymfocytech nebo PD-L1 (programmed death-1 ligand) na nádorových buňkách. Vyřazení těchto molekul cílenými protilátkami (anti-CTLA-4, anti-PD-1, anti-PD-L1) může vést k vyšší aktivitě T lymfocytů a imunitního systému jako celku [6].
Ipilimumab
 Ipilimumab je IgG1 lidská monoklonální protilátka proti receptoru CTLA-4. Přestože je její účinnost zkoušena u mnoha malignit, zatím nejlepších výsledků dosáhl výzkum právě při léčbě maligního melanomu. Proběhla řada klinických studií fáze II, kde byl ipilimumab zkoušen v různých léčebných režimech (monoterapie, kombinace s vakcínami nebo chemoterapií) a v různých dávkách (0,3 mg/kg, 3 mg/kg, 10 mg/kg) [7, 8].
Ipilimumab je IgG1 lidská monoklonální protilátka proti receptoru CTLA-4. Přestože je její účinnost zkoušena u mnoha malignit, zatím nejlepších výsledků dosáhl výzkum právě při léčbě maligního melanomu. Proběhla řada klinických studií fáze II, kde byl ipilimumab zkoušen v různých léčebných režimech (monoterapie, kombinace s vakcínami nebo chemoterapií) a v různých dávkách (0,3 mg/kg, 3 mg/kg, 10 mg/kg) [7, 8].
V roce 2010 byly publikovány výsledky první velké randomizované multicentrické studie fáze III u pacientů s neresekabilním melanomem III. a IV. klinického stadia předléčených chemoterapií. Pacienti byli randomizováni do tří ramen, v nichž nemocní dostávali ipilimumab, ipilimumab v kombinaci s vakcínou gp100 nebo samotnou vakcínu gp100. Ipilimum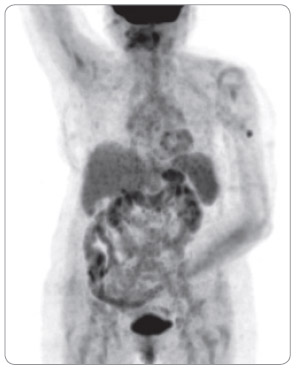 ab byl podáván v dávce 3 mg/kg v 90minutové nitrožilní infuzi každé tři týdny, celkem čtyřikrát. Medián OS v rameni s ipilimumabem v kombinaci s vakcínou gp100 byl 10,0 měsíce, v rameni se samotným ipilimumabem 10,1 měsíce a se samotnou vakcínou gp100 pak 6,4 měsíce.
ab byl podáván v dávce 3 mg/kg v 90minutové nitrožilní infuzi každé tři týdny, celkem čtyřikrát. Medián OS v rameni s ipilimumabem v kombinaci s vakcínou gp100 byl 10,0 měsíce, v rameni se samotným ipilimumabem 10,1 měsíce a se samotnou vakcínou gp100 pak 6,4 měsíce.
Rozdíly v přežití mezi pacienty léčenými samotným ipilimumabem a vakcínou byly statisticky signifikantní (p = 0,003). Léčebná odpověď (CR a PR) v rameni se samotným ipilimumabem byla zaznamenána u 10,9 %. U dalších 17,5 % pacientů bylo dosaženo stabilizace onemocnění. Většina nežádoucích účinků studiové léčby byla způsobena nadměrnou aktivitou imunitního systému. K nejčastěji postiženým orgánům patřila kůže a gastrointestinální trakt. Nejčastějším imunitně podmíněným 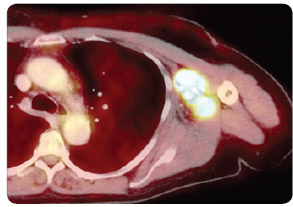 nežádoucím účinkem byl průjem (až 30 % pacientů). Při rozvoji vážnější toxicity (stupeň 3 a 4) je doporučeno okamžitě začít podávat vysoké dávky kortikosteroidů, eventuálně, v případě jejich neúčinnosti, pacienty zavčas převést na jinou imunosupresivní léčbu (infliximab, mykofenolát mofetil) [9].
nežádoucím účinkem byl průjem (až 30 % pacientů). Při rozvoji vážnější toxicity (stupeň 3 a 4) je doporučeno okamžitě začít podávat vysoké dávky kortikosteroidů, eventuálně, v případě jejich neúčinnosti, pacienty zavčas převést na jinou imunosupresivní léčbu (infliximab, mykofenolát mofetil) [9].
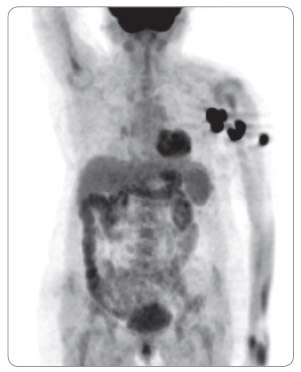
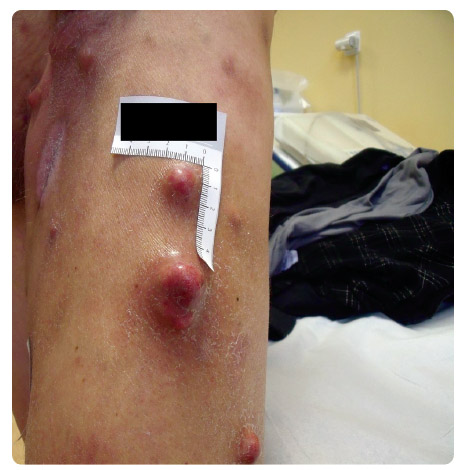
Výsledky druhé velké klinické studie fáze III u pokročilého melanomu byly prezentovány a publikovány v roce 2011. Tato klinická studie byla zaměřena 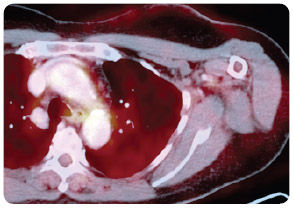 na chemoterapií nepředléčené pacienty (první linie paliativní systémové léčby). Ipilimumab zde byl podáván ve vyšší dávce, a sice 10 mg/kg. Pacienti byli randomizováni do dvou ramen. V prvním rameni studie byl podáván ipilimumab 10 mg/kg (4krát á 3 týdny) v kombinaci s dakarbazinem (850 mg/m2), ve druhém rameni dostávali nemocní dakarbazin v monoterapii (850 mg/m2). Mediány OS v ramenech s léčebnou kombinací ipilimumab-dakarbazin byly 11,2 měsíce oproti 9,1 měsíce v rameni s dakarbazinem, jednoleté přežití 47,3 % vs. 36,3 %, dvouleté 28,5 % vs. 17,9 %, tříleté 20,8 % vs. 12,2 % a čtyřleté přežití 19 % vs. 9,6 % (p < 0,001). Četnost léčebných odpovědí (CR + PR) byla v rameni s kombinací ipilimumab-dakarbazin 15,2 %, v rameni s dakarbazinem samotným 10,3 % (p = 0,09). Trvání léčebné odpovědi bylo ale při monoterapii ipilimumabem signifikantně delší (19,3 vs. 8,1 měsíce; p = 0,03). Nejčastějším imunitně podmíněným nežádoucím účinkem stupně 3 a 4 byla v rameni s ipilimumabem překvapivě hepatitida, která se vyskytla v 31,6 %, zatímco v rameni s dakarbazinem se objevila pouze ve 2,4 %. Příčinou byla pravděpodobně potenciace této toxicity dakarbazinem [10]. Naše vlastní zkušenosti s léčbou ipilimumabem ukazují obr. 1, 2, 3, 4.
na chemoterapií nepředléčené pacienty (první linie paliativní systémové léčby). Ipilimumab zde byl podáván ve vyšší dávce, a sice 10 mg/kg. Pacienti byli randomizováni do dvou ramen. V prvním rameni studie byl podáván ipilimumab 10 mg/kg (4krát á 3 týdny) v kombinaci s dakarbazinem (850 mg/m2), ve druhém rameni dostávali nemocní dakarbazin v monoterapii (850 mg/m2). Mediány OS v ramenech s léčebnou kombinací ipilimumab-dakarbazin byly 11,2 měsíce oproti 9,1 měsíce v rameni s dakarbazinem, jednoleté přežití 47,3 % vs. 36,3 %, dvouleté 28,5 % vs. 17,9 %, tříleté 20,8 % vs. 12,2 % a čtyřleté přežití 19 % vs. 9,6 % (p < 0,001). Četnost léčebných odpovědí (CR + PR) byla v rameni s kombinací ipilimumab-dakarbazin 15,2 %, v rameni s dakarbazinem samotným 10,3 % (p = 0,09). Trvání léčebné odpovědi bylo ale při monoterapii ipilimumabem signifikantně delší (19,3 vs. 8,1 měsíce; p = 0,03). Nejčastějším imunitně podmíněným nežádoucím účinkem stupně 3 a 4 byla v rameni s ipilimumabem překvapivě hepatitida, která se vyskytla v 31,6 %, zatímco v rameni s dakarbazinem se objevila pouze ve 2,4 %. Příčinou byla pravděpodobně potenciace této toxicity dakarbazinem [10]. Naše vlastní zkušenosti s léčbou ipilimumabem ukazují obr. 1, 2, 3, 4.
Cílená léčba
Klinický výzkum na genové a molekulární úrovni umožnil vývoj nových léků, které známe pod pojmem cílená léčba. Dnes se do této oblasti řadí především tzv. malé molekuly (nejčastěji tyrozinkinázové inhibitory). Obecným principem této léčby je cílený zásah do patologicky aktivované signální dráhy, která je příčinou maligního chování takto postižené buňky. Nejvíce prozkoumány jsou zatím inhibitory mutovaných proteinových kináz BRAF, MEK (mitogeny aktivovaná kináza) a c-kit.
Inhibitory BRAF
Vemurafenib
Prvním průlomovým přípravkem z oblasti cílené léčby u diseminovaného maligního melanomu je vemurafenib (PLX4032). Jedná se inhibitor BRAF kinázy, která je důležitou součástí komplexu RAS-RAF-MEK-ERK nebo také MAPK (mitogeny aktivovaná proteinkináza) signální cesty. Jeho inhibiční efekt se projeví jen u mutované formy BRAF (v 75–90 % mutace V600E, substituce valinu kyselinou glutamovou na 600. aminokyselině; v 10–25 % mutace V600K, náhrada valinu lysinem). Výše zmíněné mutace V600 způsobují trvalou aktivaci BRAF kinázy, což vede k nekontrolovanému množení maligně transformovaných buněk.
Vemurafenib je schopen vysoce specificky inhibovat mutovanou BRAF, čímž se liší od jiných nespecifických inhibitorů BRAF (sorafenib). Léčba tímto kinázovým inhibitorem má však některá nově zjištěná úskalí. Prvním je růst keratoakantomů a spinocelulárních karcinomů kůže, jejichž výskyt se pohybuje v rozmezí 12–31 %
dle údajů různých studií. Vyskytují se nejčastěji během prvních osmi týdnů léčby [11–14]. Dalším problémem je vznik rezistence na tento přípravek, a to nejčastěji reaktivací MAPK signální dráhy nebo poruchami v jiných signálních kaskádách (zvýšená aktivita kinázy PDGFR-β, IGF-1R/PI3K) [15–17].
První významnou klinickou studií, ve které se podával vemurafenib pacientům s maligním melanomem, byla multicentrická studie fáze I (BRIM-1). Četnost léčebných odpovědí byla zaznamenána u dosud nevídaného počtu pacientů: jednalo se o 81 % z celého souboru a medián OS pacientů dosáhl 14,5 měsíce. Druhou větší studií zkoumající bezpečnost a účinnost vemurafenibu u pacientů s diseminovaným maligním melanomem byla studie fáze II (BRIM-2). I zde byla zjištěna vysoká četnost léčebných odpovědí (52 %) a prodloužení mediánu OS činilo 15,9 měsíce. Výskyt kožního spinocelulárního karcinomu byl zaznamenán ve 26 % [12].
Příznivé výsledky z předchozích studií byly potvrzeny multicentrickou studií fáze III (BRIM-3), která porovnávala léčbu vemurafenibem v dávce 960 mg per os (p.o.) 2krát denně s dakarbazinem v dávce 1000 mg/m2 aplikované i.v. každé 3 týdny u nepředléčených pacientů s metastatickým či lokálně pokročilým maligním melanomem s mutací BRAF V600E. Výsledky byly následující: počet léčebných odpovědí (CR a PR) v rameni s vemurafenibem byl 53 %, v rameni s dakarbazinem 8 %, medián času PFS byl 6,9 vs. 1,6 měsíce a medián OS 13,6 vs. 10 měsíců (p < 0,001). Retrospektivně byla potvrzena účinnost vemurafenibu i u pacientů s mutací BRAF V600K, ale četnost léčebných odpovědí byla nižší než v případě mutace BRAF V600E. Výskyt kožního spinocelulárního karcinomu byl zachycen u 12 % pacientů, všechny tyto léze se vyřešily jednoduchou excizí bez nutnosti modifikovat dávky vemurafenibu [13, 14]. Vemurafenib je účinný i u mozkových metastáz, k dispozici jsou zatím jen výsledky studie fáze I, studie fáze II stále probíhá [18].
Vlastní zkušenosti s vemurafenibem jsme měli možnost získat v rámci programu „expanded access study“, nábor byl ukončen v prosinci roku 2012.
Dabrafenib (GSK2118436)
Dabrafenib je podobně jako vemurafenib selektivním inhibitorem BRAF V600E/K. V roce 2012 byly prezentovány výsledky multicentrické studie fáze III (BREAK-3). Cílovou skupinou byli nepředléčení pacienti s neresekovatelným melanomem stadia III a IV s přítomnou mutací BRAF V600E. Dabrafenib byl podáván v dávce 150 mg p.o. 2krát denně, srovnávací léčbou byl dakarbazin 1000 mg/m2 podávaný i.v. každé tři týdny. V rameni s dabrafenibem byl zaznamenán signifikantně vyšší počet léčebných odpovědí (RR dle investigátorů 53 % vs. 19 % u dakarbazinu, dle nezávislé komise 50 % vs. 6 %) i signifikantně delší medián PFS (dle investigátorů 5,1 vs. 2,1 měsíce u dakarbazinu, dle nezávislé komise 6,7 vs. 2,9 měsíce). Údaje o mediánu OS zatím nejsou známy, ale jsou očekávány podobné výsledky jako u vemurafenibu. Medián času do léčebné odpovědi byl 6,3 týdne.
K nejčastějším nežádoucím účinkům patřily bolesti hlavy, bolesti kloubů, únava, kožní hyperkeratóza, papilomatóza, u 6 % pacientů se objevil spinocelulární karcinom kůže. Na rozdíl od vemurafenibu byl pozorován nižší výskyt kožní fotosenzitivity (40–50 % vs. 3 %), nebyla zde zjištěna ani hepatotoxicita. Nově se objevují teploty, jejichž etiologie není jasná [19, 20].
Podobně jako vemurafenib prokázal účinnost u pacientů s mozkovými metastázami (předléčení i nepředléčení) také dabrafenib, a to ve studii fáze II (BREAK-MB). Byli zde léčeni pacienti s mutací BRAF V600E a BRAF V600K. Dle výsledků je zřejmé, že léčebný přínos je u pacientů s mutací BRAF V600E vyšší než u těch, kteří trpí mutací BRAF V600K (RR 31–39 % vs. 7–22 %, medián OS 31–33 týdnů vs. 16–22 týdnů) [21].
Inhibitory MEK
Trametinib (GSK1120212)
Trametinib je reverzibilní selektivní inhibitor kinázy MEK 1 a 2. Stejně jako u předchozích léčivých přípravků máme i u tohoto léčiva k dispozici předběžné výsledky ze studie III. fáze (METRIC). Zkoumanou skupinou byli opět nepředléčení pacienti s neresekovatelným melanomem stadia III a IV a přítomnou mutací BRAF V600E/K. Trametinib byl podáván v dávce 2 mg p.o. 1krát denně, ve srovnávacím rameni této studie byl podáván dakarbazin nebo paklitaxel. V rameni s trametinibem byl zaznamenán také signifikantně vyšší počet léčebných odpovědí ve srovnání s chemoterapií (RR 22 % vs. 8 %) i signifikantně delší medián PFS (4,8 měsíce vs.1,5 měsíce u chemoterapie); údaje o mediánu OS zatím nejsou známy. K nejčastějším nežádoucím účinkům patřily vyrážka, průjem, hypertenze, periferní otoky a únava. Nově byly pozorovány chorioretinopatie (1 %) a přechodný mírný pokles ejekční frakce levé komory (7 %) [22].
Kombinace inhibitorů BRAF a MEK
Kombinace dabrafenib-trametinib
Vyšší účinnost, oddálení vzniku rezistence a snížení výskytu proliferujících kožních lézí při léčbě inhibitorem BRAF v monoterapii na preklinických modelech bylo impulsem ke klinickým hodnocením kombinace inhibitorů BRAF a MEK. Dosud byly prezentovány výsledky klinické studie fáze I a II. Kombinace dabrafenibu v dávce 150 mg podávané p.o. 2krát denně a trametinibu v dávce 2 mg p.o. podávané 1krát denně je účinnější než dabrafenib v monoterapii, což ukazují jak hodnoty RR (76 % vs. 54 %), tak mediánu PFS (9,4 vs. 5,8 měsíce) s přijatelným profilem toxicity. Oproti monoterapii dabrafenibem či trametinibem byl u této kombinace léčiv zaznamenán nižší výskyt kožní toxicity (rash, hyperkeratóza, keratoakantomy, spinocelulární karcinomy kůže), hypertenze a průjmů. Naopak došlo k častějšímu výskytu teplot (až u 70 % pacientů) [23]. Nyní probíhá studie III. fáze.
Inhibitory c-kit
Aktivační mutace c-kit se nachází jen asi u 3 % všech melanomů. Je však ve vyšším procentu zastoupena u melanomů slizničních (sinonazální 10 %, anální 25 %, vulvovaginální 35 %) a akrálních (10–15 %), což je podstatné vzhledem k vysoké incidenci těchto typů především u asijské populace (až 70 % všech melanomů vs. 6–7 % u bílé rasy) [24, 25]. Vyšší četnost mutací c-kit byla zjištěna také u melanomů vznikajících v kůži chronicky exponované slunečnímu záření. Nejznámějším zástupcem inhibitorů c-kit je imatinib mesylát, k dalším patří nilotinib, masitinib, dasatinib. Četnost léčebných odpovědí ze studií II. fáze se pohybuje mezi 16–23 %, PFS 3–4 měsíce [26].
Strategie léčby u pacientů s pokročilým maligním melanomem
 Bez ohledu na stanovenou úhradu je mezi onkology široce diskutován možný léčebný algoritmus terapie melanomu se zapojením moderní imunoterapie a cílené léčby. Většina onkologů se dnes kloní k názoru, že před léčbou bychom měli znát minimálně stav mutace BRAF V600, případně mutace c-kit (slizniční a akrální melanomy). U cílené léčby víme, že nástup účinku je relativně rychlý (cca do 6 týdnů), a je tudíž vhodná, za podmínky přítomné mutace, k primárnímu podávání u pacientů s pokročilým nádorem, vysokou hladinou LDH (laktát dehydrogenáza) a symptomy onemocnění, obr. 5 a 6.
Bez ohledu na stanovenou úhradu je mezi onkology široce diskutován možný léčebný algoritmus terapie melanomu se zapojením moderní imunoterapie a cílené léčby. Většina onkologů se dnes kloní k názoru, že před léčbou bychom měli znát minimálně stav mutace BRAF V600, případně mutace c-kit (slizniční a akrální melanomy). U cílené léčby víme, že nástup účinku je relativně rychlý (cca do 6 týdnů), a je tudíž vhodná, za podmínky přítomné mutace, k primárnímu podávání u pacientů s pokročilým nádorem, vysokou hladinou LDH (laktát dehydrogenáza) a symptomy onemocnění, obr. 5 a 6.
Nevýhodou cílené léčby může být její dočasná účinnost a rychlý vznik sekundární rez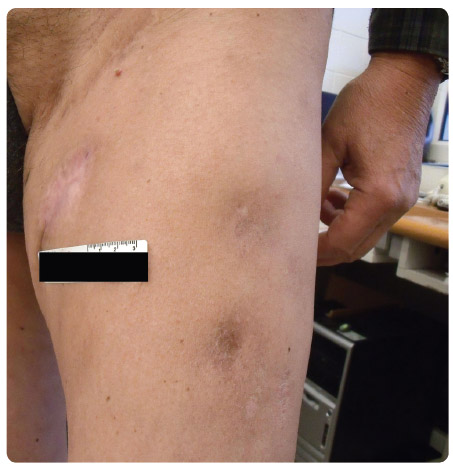 istence (nejčastěji reaktivací MAPK signální dráhy). Imunoterapie typu ipilimumabu je schopná aktivovat imunitní systém řádově v měsících. Proto je vhodná pro pacienty s méně agresivním onemocněním a nepříliš rozsáhlou nádorovou masou. Výhodou je v případě léčebné odpovědi její dlouhodobé trvání. Jeden z možných algoritmů je uveden na obr. 7.
istence (nejčastěji reaktivací MAPK signální dráhy). Imunoterapie typu ipilimumabu je schopná aktivovat imunitní systém řádově v měsících. Proto je vhodná pro pacienty s méně agresivním onemocněním a nepříliš rozsáhlou nádorovou masou. Výhodou je v případě léčebné odpovědi její dlouhodobé trvání. Jeden z možných algoritmů je uveden na obr. 7.
Závěr
Pokročilý maligní melanom stále patří k diagnózám s velmi vážnou prognózou a omezenými léčebnými možnostmi. Standardní léčba představovaná chemoterapií, případně v kombinaci s interferonem alfa nebo interleukinem-2, významně neprodlužuje přežití. Intenzivní výzkum umožnil vývoj nových léků z obla![Obr. 7 Léčebný algoritmus u pokročilého maligního melanomu; podle [27] – Wolchok, 2012.](https://www.remedia.cz/photo-a-29339---.jpg) sti imunoterapie a cílené léčby. Z moderní imunoterapie zatím nejvýznamnějších výsledků dosáhl ipilimumab (protilátka anti-CTLA-4), velký potenciál má nivolumab (protilátka
sti imunoterapie a cílené léčby. Z moderní imunoterapie zatím nejvýznamnějších výsledků dosáhl ipilimumab (protilátka anti-CTLA-4), velký potenciál má nivolumab (protilátka
anti-PD-1) a protilátky anti-PD-L1. Ze skupiny cílených léčiv se zatím ukazují jako perspektivní inhibitory mutované BRAF kinázy (vemurafenib a dabrafenib) a inhibitor MEK trametinib. V případě slizničních a akrálních melanomů s mutací c-kit najdou pravděpodobně své uplatnění inhibitory c-kit, jako je imatinib, nilotinib a další. Výsledky aktuálních klinických studií jsou povzbudivé. Stále však není dořešena řada zásadních otázek. V každém případě lze říci, že dochází k významnému pokroku v léčbě tohoto závažného onemocnění.
Seznam použité literatury
- [1] Dusek L, Muzik J, Kubasek M, et al. Epidemiology of malignant tumours in the Czech Republic [online]. Masaryk University, 2005. Available from: http://www.svod.cz.
- [2] Korn EL, Liu PY, Lee SJ, et al. Meta-analysis of phase II cooperatice group trials in metastatic stage IV melanoma to determine progression-free and overall survival benchmarks for future phase II trials. J Clin Oncol 2008; 26: 527–534.
- [3] Serrone L, Zeuli M, Sega FM, et al. Dacarbazine-based chemotherapy for metastatic melanoma: thirty-year experience overview. J Exp Clin Cancer Res 2000; 19: 21–34.
- [4] Eggermont AM, Kirkwood JM. Re-evaluating the role of dacarbazine in metastatic melanoma: what have learned in 30 years? Eur J Cancer 2004; 40: 1825–1836.
- [5] Atkins MB, Lotze MT, Dutcher JP, et al. High-dose recombinant interleukin 2 therapy for patients with metastatic melanoma: analysis of 270 patients treated between 1985 and 1993. J Clin Oncol 1999; 17: 2105–2116.
- [6] Kirkwood JM, Tarhini AA, Panelli MC, et al. Next generation of immunotherapy for melanoma. J Clin Oncol 2008; 26: 3445–3455.
- [7] O´Day SJ, Maio M, Chiarion-Sileni V, et al. Efficacy and safety of ipilimumab monotherapy in patients with previously treated, advanced melanoma: a multicenter single-arm phase II study. Ann Oncol 2010; 21: 1712–1717.
- [8] Weber J, Thompson JA, Hamid O, et al. A randomized, double-blind, placebo controlled, phase II study comparing the tolerability and efficacy of ipilimumab administered with or without prophylactic budesonide in patients with unresectable stage III or IV melanoma. Clin Cancer Res 2009; 15: 5591–5598.
- [9] Hodi FS, O´Day SJ, McDermott DF, et al. Improved survival with ipilimumab in patients with metastatic melanoma. N Engl J Med 2010; 363: 711–723.
- [10] Robert C, Thomas L, Bondarenko I, et al. Ipilimumab plus dacarbazine for previously untreated metastatic melanoma. N Engl J Med 2011; 364: 2517–2526.
- [11] Flaherty KT, Puzanov I, Kim KB, et al. Inhibition of mutated, activated BRAF in metastatic melanoma. N Engl J Med 2010; 363: 809–819.
- [12] Ribas A, Kim KB, Schuchter LM, et al., BRIM-2: An open-label, multicenter phase II study of vemurafenib in previously treated patients with BRAF V600E mutation-positive metastatic melanoma. J Clin Oncol 2011; 29 (15 Suppl): Abstract 8509.
- [13] Chapman PB, Hauschild A, Robert C, et al. BRIM-3 Study Group. Improved survival with vemurafenib in melanoma with BRAF V600E mutation. N Engl J Med 2011; 364: 2507–2516.
- [14] Chapman PB, Hauschild A, Robert C, et al. Updated overall survival (OS) results for BRIM-3, a phase III randomized, open-label, multicenter trial comparing BRAF inhibitor vemurafenib (vem) with dacarbazine (DTIC) in previously untreated patients with BRAFV600E-mutated melanoma [abstract]. J Clin Oncol 2012; 30 (15 Suppl): Abstract 8502.
- [15] Heidorn SJ, Milagre C, Whittaker S, et al. Kinase-Dead BRAF and Oncogenic RAS Cooperate to Drive Tumor Progression through CRAF. Cell 2010; 140: 209–221.
- [16] Johannessen CM, Boehm JS, Kim SY, et al. COT drives resistance to RAF inhibition through MAP kinase pathway reactivation. Nature 2010; 468: 968–972.
- [17] Heneberg P. Advances in clinical treatment of malignant melanoma: B-RAF kinase inhibition. Klin Onkol 2011; 24: 256–264.
- [18] Dummer R, Goldinger SM, Turtschi CP, et al. Open-label pilot study of vemurafenib in previously treated metastatic melanoma (mM) patients (pts) with symptomatic brain metastases (BM) [abstract] Ann Oncol 2012; 23: ix366, Abstract 1125P.
- [19] Menzies AM, Long GV, Murali R. Dabrafenib and its potential for the treatment of metastatic melanoma. Drug Des Devel Ther 2012; 6: 391–405.
- [20] Hauschild A, Grob JJ, Demidov LV, et al. Dabrafenib in BRAF-mutated metastatic melanoma: a multicentre, open-label, phase 3 randomised controlled trial. Lancet 2012; 380: 358–365.
- [21] Long GV, Trefzer U, Davies MA, et al. Dabrafenib in patients with Val600Glu or Val600Lys BRAF-mutant melanoma metastatic to the brain (BREAK-MB): a multicentre, open-label, phase 2 study. Lancet Oncol 2012; 13: 1087–1095.
- [22] Flaherty KT, Robert C, Hersey P, et al. METRIC Study Group. Improved survival with MEK inhibition in BRAF-mutated melanoma. N Engl J Med 2012; 367: 107–114.
- [23] Flaherty KT, Infante JR, Daud A, et al. Combined BRAF and MEK inhibition in melanoma with BRAF V600 mutations. N Engl J Med 2012; 367: 1694–1703.
- [24] Schoenewolf NL, Bull C, Belloni B, et al. Sinonasal, genital and acrolentiginous melanomas show distinct characteristics of KIT expression and mutations. Eur J Cancer 2012; 48: 1842–1852.
- [25] Guo J, Si L, Kong Y, et al. Phase II, Open-Label, Single-Arm Trial of Imatinib Mesylate in Patients With Metastatic Melanoma Harboring c-KIT Mutation or Amplification. J Clin Oncol 2011; 29: 2904–2909.
- [26] Guo J, Si L, Kong Y, et al. A phase II study of imatinib for advanced melanoma patients with KIT aberrations. J Clin Oncol 2010; 28 (15 Suppl): Abstract 8527.
- [27] Wolchok J. How recent advances in immunotherapy are changing the standard of care for patients with metastatic melanoma. Ann Oncol 2012; 23 (8 Suppl): viii15-viii21.