Novinky v terapii chronické infekce virem hepatitidy C
Formou přehledného článku jsou probrány základní informace o polymorfismech genu IL28B. Haplotyp CC SNP rs12979860 je významně asociován s dosažením setrvalé virologické odpovědi. Jeho výskyt vykazuje geografickou rozdílnost. Ve druhé části článku je uveden přehled pěti rozsáhlých klinických studií, které poskytly registrační data pro užití bocepreviru (BOC) a telapreviru (TVR) v indikaci chronické HCV (hepatitis C virus) infekce u dosud neléčených osob i osob infikovaných genotypem HCV 1, které byly v minulosti léčeny neúspěšně. V první skupině je při použití bocepreviru nebo telapreviru dosahováno setrvalé virologické odpovědi v přibližně 65–75 % případů, ve druhé skupině pak v přibližně 60–65 %.
Úvod
Virová hepatitida C, jejíž původce byl poprvé popsán v roce 1989, představuje i ve druhém desetiletí 21. století významný celosvětový zdravotní problém. Virem je podle současných odhadů infikováno kolem 170 milionů osob na celém světě. Incidence infekce ve vyspělých zemích světa klesá, nicméně stále není nulová. Dle aktuálních prognóz bude nadále narůstat počet nově odhalených případů infekce, která vznikla v minulých desetiletích. Je pravděpodobné, že se mezi těmito nově diagnostikovanými osobami bude zvyšovat podíl osob trpících pokročilou jaterní chorobou, či dokonce jaterní cirhózou a hepatocelulárním karcinomem (HCC).
Terapie HCV (hepatitis C virus) infekce se v současné době nachází na začátku zcela nové éry. Období, do něhož právě vstupujeme, bude nepochybně charakterizováno dvěma objevy. Tím prvním je objev polymorfismů genu kódujících jeden z interferonů typu 3 (IL28B) a jejich vztahu k průběhu HCV infekce a především k účinku protivirové léčby. Druhým zlomovým momentem je objev přímo působících virostatik (directly acting antivirals, DAA) a jejich postupné pronikání do léčby, které představuje zásadní zlom v dosavadní protivirové léčbě založené na podávání interferonu v nejrůznějších modifikacích a schématech.
Polymorfismy genu IL28B
IL28B je gen kódující interferon typu III, IFN-lambda3 (interferon-lambda3), který je lokalizován na 19. chromozomu. Objev polymorfismů tohoto genu je produktem tzv. genome-wide association studies (GWAS). V oblasti genu IL28B bylo dosud identifikováno několik jednonukleotidových polymorfismů (single nucleotide polymorphism, SNP) s úzkým vztahem k nejrůznějším parametrům HCV infekce. Mechanismus, jakým je pozitivní efekt příznivého genotypu zprostředkován, nebyl dosud objasněn.
Prvním SNP popsaným v oblasti genu IL28B byl SNP rs12979860 [1]. Tento SNP je v silném vztahu k účinnosti protivirové léčby. Haplotyp CC v této poloze je asociován s 2,5krát vyšší účinností terapie nežli haplotypy TT a CT [1]. Různý výskyt tohoto výhodného haplotypu v různých geografických oblastech a populacích vysvětluje do velké míry různou účinnost protivirové léčby v různých etnikách. Asociace haplotypu CC rs12979860 s dosažením setrvalé virologické odpovědi (SVR, sustained viral response) představuje dosud nejpřesnější prediktivní faktor účinku léčby. Polymorfismy genu IL28B se proto staly dalším, vcelku standardním, kritériem, podle kterého jsou stratifikováni pacienti s chronickou HCV infekcí ve všech klinických studiích s moderními variantami protivirové léčby.
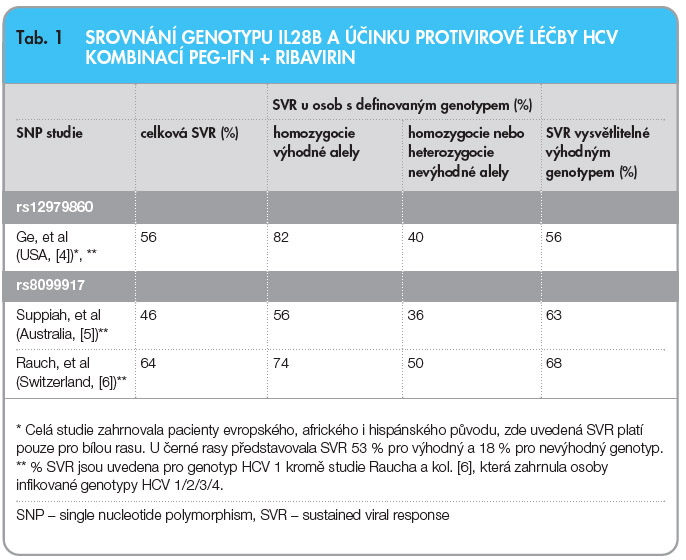 Kromě již zmíněného polymorfismu bylo popsáno dalších 6 SNP v této oblasti se vztahem k HCV, rs12979860 je z nich jednoznačně nejvýznamnější. Jako druhý nejsilněji asociovaný SNP byl identifikován polymorfismus rs8099917 [2]. V tomto druhém polymorfismu je nejvýhodnější alela T. TT homozygocie v pozici rs8099917 byla např. identifikována jako jediný nezávislý prediktor času do spontánní eliminace viru při akutní HCV infekci [3]. Haplotyp CC rs12979860 je dále asociován se spontánní eliminací HCV (OR 0,33; p < 10–12) [1]. Srovnání významnosti obou polymorfismů z pohledu asociace se SVR ukazuje tab. 1. Z ní je dobře patrno, že například mezi americkými bělochy infikovanými genotypem HCV 1 je celková úspěšnost léčby 56 %, ale u osob s haplotypem rs12979860 CC je SVR dosaženo až v 82 %. Další dva polymorfismy byly popsány v pozicích rs8103142 a rs28416813. Tyto dva poslední SNP jsou těsně asociovány s polymorfismy rs12979860, a tudíž se zatím nepodařilo jednoznačně charakterizovat jejich vlivy na HCV infekci.
Kromě již zmíněného polymorfismu bylo popsáno dalších 6 SNP v této oblasti se vztahem k HCV, rs12979860 je z nich jednoznačně nejvýznamnější. Jako druhý nejsilněji asociovaný SNP byl identifikován polymorfismus rs8099917 [2]. V tomto druhém polymorfismu je nejvýhodnější alela T. TT homozygocie v pozici rs8099917 byla např. identifikována jako jediný nezávislý prediktor času do spontánní eliminace viru při akutní HCV infekci [3]. Haplotyp CC rs12979860 je dále asociován se spontánní eliminací HCV (OR 0,33; p < 10–12) [1]. Srovnání významnosti obou polymorfismů z pohledu asociace se SVR ukazuje tab. 1. Z ní je dobře patrno, že například mezi americkými bělochy infikovanými genotypem HCV 1 je celková úspěšnost léčby 56 %, ale u osob s haplotypem rs12979860 CC je SVR dosaženo až v 82 %. Další dva polymorfismy byly popsány v pozicích rs8103142 a rs28416813. Tyto dva poslední SNP jsou těsně asociovány s polymorfismy rs12979860, a tudíž se zatím nepodařilo jednoznačně charakterizovat jejich vlivy na HCV infekci.
Klinický význam polymorfismů
Znalost haplotypů IL28B poskytuje důležitou informaci o pravděpodobnosti dosažení SVR. Od roku 2010 jsou dostupné komerční kity k vyšetřování příslušných polymorfismů. Výsledky tohoto vyšetření spolu s dalšími predikčními faktory, jako je genotyp viru, viremie a virová kinetika sledovaná v počátcích léčby, umožní ve vazbě na pravděpodobnost dosažení SVR rozhodovat, zda je pacient indikován například k opakování standardní protivirové léčby, či zda je lepší vyčkat do doby, kdy budou dostupná přímo působící virostatika (viz dále).
Bohužel ani genotypy IL28B nemají pozitivní prediktivní hodnotu 100 %. Rozhodování o léčbě tudíž ani nadále nemůže být založeno pouze na znalosti a výsledku analýzy SNP IL28B. Pozitivní prediktivní hodnota je navíc ovlivněna obecnou pravděpodobností dosažení SVR v dané populaci, takže extrapolace výsledků z klinických studií do populací jiných částí světa není zjevně zcela správným krokem.
Znalost SNP může ale velmi dobře ovlivnit rozhodování o zahájení, odložení či nezahájení protivirové terapie v případech akutní HCV infekce. Osoby s příznivými haplotypy asociovanými se spontánní eliminací mohou být zřejmě sledovány a neléčeny déle, jejich léčba může být odložena, protože mají vyšší pravděpodobnost dosažení spontánní eliminace viru. A naopak. Kombinace příznivých haplotypů IL28B a příznivé virové kinetiky v počátcích léčby (např. RVR, rapid virological response – rychlá virologická odpověď) může být vodítkem pro identifikaci osob, u kterých je možné podávání protivirové léčby významně zkrátit. V tomto ohledu je však třeba vyčkat na výsledky klinických studií.
Stejně tak asociace SNP IL28B a senzitivity na IFN může napomoci identifikovat osoby, které by spíše mohly mít prospěch z podání DAA v režimech obsahujících tzv. leadin fázi, viz dále. U těchto osob je větší riziko rozvoje virologické rezistence na DAA.
Přímo působící virostatika (DAA)
V posledních letech jsme zaplavováni výsledky velkého množství klinických studií s tzv. přímo působícími virostatiky (DAA). V léčbě HCV infekce jde o zcela novou skupinu léčivých látek ve smyslu mechanismu účinku. Látky této skupiny přímo inhibují některý z enzymů uplatňujících se v průběhu replikačního cyklu HCV. Jejich místo účinku je tudíž přesně definováno a známo. V rámci replikace HCV dochází k syntéze jediného polyproteinu, který je translačním produktem celého virového genomu. Jeho následné štěpení zahajuje virová proteáza, která postupně 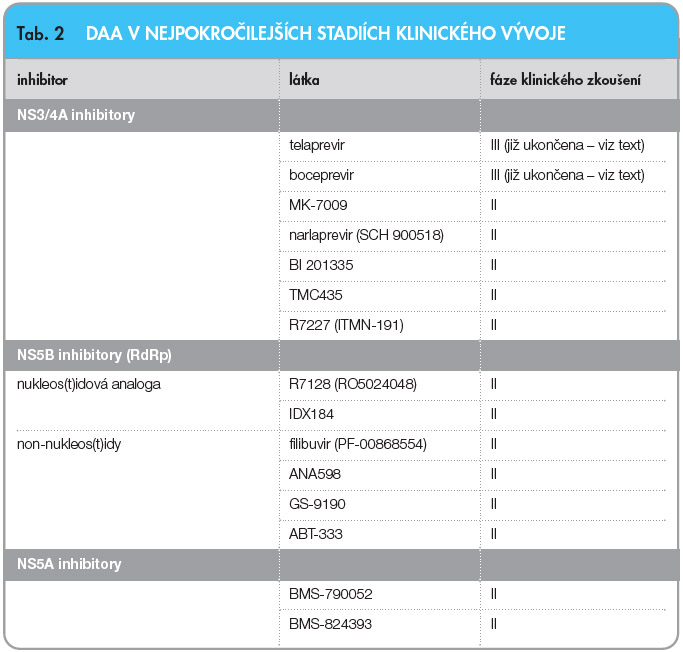 uvolňuje jednotlivé strukturální i nestrukturální proteiny. Posledním krokem procesu je uvolnění RNA polymerázy, která představuje klíčový enzym celé replikace. DAA jsou látky inhibující nejčastěji buď právě proteázu (produkt NS3/4 oblasti virového genomu) či RNA polymerázu (produkt NS5B). Je známo i několik látek, které inhibují produkt oblasti genomu HCV značené jako NS5A, jehož přesný význam a aktivita v rámci replikačního cyklu nejsou dosud známy. Tab. 2 ukazuje přehled DAA v nejpokročilejších stadiích klinického vývoje. FDA a EMEA v průběhu roku 2011 schválily k užití v indikaci chronické HCV infekce preparáty boceprevir (BOC) a telaprevir (TVR). Proto si těchto dvou preparátů všimneme trochu podrobněji. DAA dosud ale nejsou standardní součástí protivirové léčby chronické HCV infekce, z tohoto důvodu nejdříve stručně probereme aktuálně platná standardní doporučení.
uvolňuje jednotlivé strukturální i nestrukturální proteiny. Posledním krokem procesu je uvolnění RNA polymerázy, která představuje klíčový enzym celé replikace. DAA jsou látky inhibující nejčastěji buď právě proteázu (produkt NS3/4 oblasti virového genomu) či RNA polymerázu (produkt NS5B). Je známo i několik látek, které inhibují produkt oblasti genomu HCV značené jako NS5A, jehož přesný význam a aktivita v rámci replikačního cyklu nejsou dosud známy. Tab. 2 ukazuje přehled DAA v nejpokročilejších stadiích klinického vývoje. FDA a EMEA v průběhu roku 2011 schválily k užití v indikaci chronické HCV infekce preparáty boceprevir (BOC) a telaprevir (TVR). Proto si těchto dvou preparátů všimneme trochu podrobněji. DAA dosud ale nejsou standardní součástí protivirové léčby chronické HCV infekce, z tohoto důvodu nejdříve stručně probereme aktuálně platná standardní doporučení.
Standardní terapeutický postup
Poslední verze standardních terapeutických postupů byla vydána Evropskou asociací pro studium jater v červnu 2011 [7]. Tyto standardy již respektují vývoj posledních několika let, kdy bylo zřejmé, že od původních striktních schémat založených na rigidně definovaných dávkách a délkách léčby nastává příklon k větší individualizaci léčby. Individualizace spočívá především v určení celkové doby léčby podle odpovědi na protivirovou léčbu v jejích prvních fázích, týdnech až měsících.
Standardním terapeutickým postupem v případech chronické HCV infekce je v současné době podání kombinace pegylovaného interferonu α (PEG-IFN) a ribavirinu (RBV). Na trhu jsou dostupné dva preparáty PEG-IFN, pegylovaný interferon a-2a a pegylovaný interferon a-2b. PEG-IFNa-2a je doporučován ve fixním dávkování 180 mg s.c. 1krát týdně, PEG-IFNa-2b se dávkuje podle tělesné hmotnosti, 1,5 mg/kg s.c. 1krát týdně. Dávkování ribavirinu závisí na genotypu HCV. Pacienti infikovaní genotypem 1 (a 4–6) by měli být léčeni dávkou dle tělesné hmotnosti: 15 mg/kg tělesné hmotnosti denně. Pacienti infikovaní genotypem 2 a 3 mohou být léčeni fixní dávkou 800 mg denně. Osoby, které mají BMI > 25 nebo rizikové faktory asociované s nižší šancí na SVR (inzulinová rezistence, metabolický syndrom, těžká fibróza či cirhóza, vyšší věk), by měly být léčeny stejným dávkovacím schématem jako osoby infikované genotypem HCV 1.
Délka léčby PEG-IFN + RBV může být upravována podle odpovědi během terapie. Během léčby by měla být HCV RNA vyšetřována ve třech časových bodech: před zahájením léčby, v týdnu 4 a 12. Vyšetření v týdnu 24 je přínosné u vybrané skupiny osob. Délka léčby by se měla řídit následujícími pravidly:
- Pacienti infikovaní genotypem HCV 1, kteří mají RVR, by měli být léčeni 24 týdnů, pokud mají nízkou výchozí viremii (zde není absolutní shoda, ale pozitivních výsledků je dosahováno pro pacienty s viremií 400 000–800 000 IU/ml). U pacientů s výchozí viremií vyšší než 800 000 IU/ml je jednoznačně indikována léčba trvající 24 týdnů.
- Pacienti infikovaní genotypem HCV 1, kteří dosáhnou časné virologické odpovědi (early viral response, EVR), by měli být léčeni 48 týdnů.
- Pacienti infikovaní genotypem HCV 1, kteří dosáhnou pomalé virologické odpovědi, mohou být léčeni 72 týdnů.
- Pacienti infikovaní genotypem 2 a 3, kteří dosáhnou RVR a mají nízkou výchozí viremii (400 000–800 000 IU/ml), mohou být léčeni pouze 16 týdnů. Riziko relapsu infekce je v tomto případě lehce vyšší.
- Pacienti infikovaní genotypem HCV 2 a HCV 3, kteří mají pokročilou fibrózu, cirhózu nebo faktory negativně ovlivňující šanci na SVR, by neměli být léčeni pouze 16 týdnů v žádném případě.
- Pacienti s genotypy HCV 2 a 3 a buď s EVR nebo s pomalou odpovědí nebo bez negativních predikčních faktorů by měli být léčeni 48 týdnů, respektive 72 týdnů.
Přehled dosavadních klinických studií s přímo působícími virostatiky (DAA)
Uspořádání následujících studií je poněkud složité, nicméně reflektuje moderní přístup, tzv. Response Guided Therapy (RGT). Volně se tento termín překládá jako léčba vedená podle dosažené odpovědi. Obecně se jedná o postup, kdy osoby, které dosáhnou rychleji negativní sérové HCV RNA, jsou léčeny kratší dobu a naopak osoby s pomalejší odpovědí jsou léčeny déle. Účelem tohoto přístupu je definovat pacienty, u nichž je indikována léčba pouze na relativně krátkou dobu (např. 12–24 týdnů), a naopak určit osoby, které skutečně nezbytně nutně potřebují léčbu dlouhodobou (nejčastěji 48 týdnů, ale i déle). Důvodem je přirozeně snaha o snížení expozice léčivým látkám majícím nejrůznější nežádoucí účinky a také snaha o snížení nákladů na léčbu, které zavedením DAA velmi výrazně narůstají.
Dalším znakem dosud publikovaných studií s DAA je neutříděná terminologie. Ve studiích jsou používány rozdílné termíny a definice vstupních kritérií, různě bývají označovány i jednotlivé typy protivirové odpovědi. Tato nejednotnost potom může vést k určitým zavádějícím hodnocením při srovnávání výsledků jednotlivých studií. Většina dosud publikovaných studií s DAA se zaměřila na pacienty infikované genotypem HCV 1 a jsou dostupné studie pro osoby dosud neléčené – naivní, ale i pro osoby v minulosti již neúspěšně léčené.
Osoby infikované genotypem HCV 1, které nebyly dosud léčeny – naivní
Telaprevir
![Obr. 1 Schéma studie ADVANCE – dosud neléčené osoby s genotypem HCV 1; PEG-IFN – peginterferon a-2b, TVR – telaprevir, RBV – ribavirin, eEVR – extended early virological response = prodloužená časná virologická odpověď, SOC – kontrolní větev; podle [8] – Jacobson, et al., 2011.](https://www.remedia.cz/photo-a-28615---.jpg) Studie ADVANCE [8]: schéma organizace studie ukazuje obr. 1. Osoby, které dosáhly ve studii tzv. eEVR (extended Early Virological Response, prodloužená časná virologická odpověď = negativní sérová HCV RNA ve 4. a 12. týdnu léčby), byly VŽDY léčeny 24 týdnů. Část osob ze skupiny s eEVR byla léčena trojkombinací s
Studie ADVANCE [8]: schéma organizace studie ukazuje obr. 1. Osoby, které dosáhly ve studii tzv. eEVR (extended Early Virological Response, prodloužená časná virologická odpověď = negativní sérová HCV RNA ve 4. a 12. týdnu léčby), byly VŽDY léčeny 24 týdnů. Část osob ze skupiny s eEVR byla léčena trojkombinací s ![Graf 1 Výsledky studie ADVANCE – RVR a SVR (ITT analýza); RVR – rychlá virologická odpověď (rapid virological response), SVR – setrvalá virologická odpověď (sustained viral response), PEG-IFN – peginterferon a-2b, TVR – telaprevir, RBV – ribavirin, HCV – virus hepatitidy C, TVR12/PEG-IFN + RBV48 – léčba 12 týdnů telaprevirem a peginterferonem a-2a v kombinaci s ribavirinem po dobu 48 týdnů, TVR8/PEG-IFN + RBV48 – léčba 8 týdnů telaprevirem a peginterferonem a-2a s ribavirinem po dobu 48 týdnů, SOC – Standard of Care, tzn. kontrolní větev; podle [8] – Jacobson, et al., 2011.](https://www.remedia.cz/photo-a-28616---.jpg) telaprevirem po dobu 8 týdnů a část 12 týdnů. Osoby bez eEVR byly vždy léčeny 48 týdnů, telaprevir užívaly rovněž 8 týdnů či 12 týdnů. Kontrolní větví byla skupina léčená standardní dvojkombinací PEG-IFN + ribavirin. Výsledky ITT analýzy studie ukazuje graf 1. Je patrno, že větve obsahující telaprevir se nelišily ve smyslu dosažení RVR a SVR, ale významně častěji bylo dosaženo RVR i SVR ve srovnání se standardní léčbou.
telaprevirem po dobu 8 týdnů a část 12 týdnů. Osoby bez eEVR byly vždy léčeny 48 týdnů, telaprevir užívaly rovněž 8 týdnů či 12 týdnů. Kontrolní větví byla skupina léčená standardní dvojkombinací PEG-IFN + ribavirin. Výsledky ITT analýzy studie ukazuje graf 1. Je patrno, že větve obsahující telaprevir se nelišily ve smyslu dosažení RVR a SVR, ale významně častěji bylo dosaženo RVR i SVR ve srovnání se standardní léčbou.
![Obr. 2 Schéma studie ILLUMINATE; PEG-IFN – peginterferon a-2b, RBV – ribavirin, eEVR – extended early virological response = prodloužená časná virologická odpověď; podle [9] – Sherman, et al., 2011.](https://www.remedia.cz/photo-a-28617---.jpg) Studie ILLUMINATE [9]: studie byla uspořádána na základě znalostí výsledků studie ADVANCE, její schéma ukazuje obr. 2. Graf 2 pak ukazuje výsledky. Je patrno, že celková účinnost ve smyslu
Studie ILLUMINATE [9]: studie byla uspořádána na základě znalostí výsledků studie ADVANCE, její schéma ukazuje obr. 2. Graf 2 pak ukazuje výsledky. Je patrno, že celková účinnost ve smyslu ![Graf 2 Výsledky studie ILLUMINATE v jednotlivých skupinách; SVR – setrvalá virologická odpověď (sustained viral response); podle [9] – Sherman, et al., 2011.](https://www.remedia.cz/photo-a-28618---.jpg) dosažení SVR byla 72 %. Prakticky stejnou účinnost 24týdenní a 48týdenní léčby pak lze interpretovat tak, že pro osoby, které dosáhnou eEVR při použití trojkombinační léčby, je dostačující léčba trvající 24 týdnů, naopak pro osoby, které eEVR nedosáhnou, je indikována léčba na dobu 48 týdnů.
dosažení SVR byla 72 %. Prakticky stejnou účinnost 24týdenní a 48týdenní léčby pak lze interpretovat tak, že pro osoby, které dosáhnou eEVR při použití trojkombinační léčby, je dostačující léčba trvající 24 týdnů, naopak pro osoby, které eEVR nedosáhnou, je indikována léčba na dobu 48 týdnů.
Boceprevir
![Obr. 3 Schéma studie SPRINT-2; PEG-IFN – peginterferon a-2b, BOC – boceprevir, RBV – ribavirin; podle [10] – Poordad, et al., 2011.](https://www.remedia.cz/photo-a-28619---.jpg) Studie SPRINT-2 [10]: schéma studie fáze III s boceprevirem ukazuje obr. 3. Proti studiím s telaprevirem je zde zásadní rozdíl. Boceprevir není podáván od počátku protivirové léčby, ale až po 4týdenní tzv. lead in fázi vedené kombinací PEG-IFN + ribavirin. Podkladem pro toto uspořádání byly studie nižších fází a analýzy vzniku rezistencí na boceprevir. Pokud byl podáván boceprevir od počátku léčby, docházelo k rozvoji virologické rezistence a k prolomení příznivého efektu léčby. Kontrolní větev označená jako PEG-
Studie SPRINT-2 [10]: schéma studie fáze III s boceprevirem ukazuje obr. 3. Proti studiím s telaprevirem je zde zásadní rozdíl. Boceprevir není podáván od počátku protivirové léčby, ale až po 4týdenní tzv. lead in fázi vedené kombinací PEG-IFN + ribavirin. Podkladem pro toto uspořádání byly studie nižších fází a analýzy vzniku rezistencí na boceprevir. Pokud byl podáván boceprevir od počátku léčby, docházelo k rozvoji virologické rezistence a k prolomení příznivého efektu léčby. Kontrolní větev označená jako PEG-![Graf 3 Výsledky studie SPRINT-2 podle rasy; ve všech skupinách byla podávána kombinace PEG-IFN/RBV po dobu 4 týdnů, dále skupina 1 užívala kombinaci BOC/PEG-IFN/RBV po dobu 24 týdnů, skupina 2 byla léčena kombinací BOC/PEG-IFN/RBV po dobu 44 týdnů, skupina 3 (kontrolní skupina) dostávala placebo a PEG-IFN/RBV po dobu 44 týdnů; BOC – boceprevir, PEG-IFN – peginterferon a-2b, RBV – ribavirin; podle [10] – Poordad, et al., 2011.](https://www.remedia.cz/photo-a-28620---.jpg) IFN/RBV 48 týdnů představuje standardní dvojkombinační léčbu. Výsledky studie rozdělené podle rasy ukazuje graf 3. Samostatná analýza černé rasy reflektuje již znalosti o polymorfismech IL28B tak, jak byly probrány výše. I v této studii je patrno značné navýšení SVR ve větvích s boceprevirem proti standardní léčbě, a to i v tak obtížně léčitelné skupině osob, jako jsou Afroameričané.
IFN/RBV 48 týdnů představuje standardní dvojkombinační léčbu. Výsledky studie rozdělené podle rasy ukazuje graf 3. Samostatná analýza černé rasy reflektuje již znalosti o polymorfismech IL28B tak, jak byly probrány výše. I v této studii je patrno značné navýšení SVR ve větvích s boceprevirem proti standardní léčbě, a to i v tak obtížně léčitelné skupině osob, jako jsou Afroameričané.
Osoby infikované genotypem HCV 1, předchozí neúspěšná léčba
Telaprevir
Studie![Obr. 4 Schéma studie REALIZE: telaprevir u non-responderů na předchozí protivirovou léčbu; PEG-IFN – peginterferon a-2b, RBV – ribavirin, TVR – telaprevir; podle [11] – Zeuzem, et al., 2011.](https://www.remedia.cz/photo-a-28621---.jpg) REALIZE [11]: schéma studie ukazuje obr. 4. Při hodnocení všech skupin pacientů bylo dosaženo SVR v 65 % při použití trojkombinace PEG-IFN/RBV + TVR. V kontrolní větvi (Standard of Care, SOC) bylo SVR dosaženo pouze v 17 % případů. Zajímavější jsou přirozeně výsledky v jednotlivých
REALIZE [11]: schéma studie ukazuje obr. 4. Při hodnocení všech skupin pacientů bylo dosaženo SVR v 65 % při použití trojkombinace PEG-IFN/RBV + TVR. V kontrolní větvi (Standard of Care, SOC) bylo SVR dosaženo pouze v 17 % případů. Zajímavější jsou přirozeně výsledky v jednotlivých ![Graf 4 SVR ve studii REALIZE ve skupinách podle účinku předchozí protivirové léčby; PEG-IFN – peginterferon a-2b, RBV – ribavirin, TVR – telaprevir, SVR – setrvalá virologická odpověď (sustained viral response); podle [11] – Zeuzem, et al., 2011.](https://www.remedia.cz/photo-a-28622---.jpg) skupinách podle odpovědi na předchozí protivirovou léčbu, což ukazuje graf 4. Je patrno, že i ve skupině osob rezistentních na předchozí léčbu (null response) je dosahováno přibližně 6krát vyššího procenta SVR než při použití opakované standardní léčby kombinací PEG-IFN a RBV.
skupinách podle odpovědi na předchozí protivirovou léčbu, což ukazuje graf 4. Je patrno, že i ve skupině osob rezistentních na předchozí léčbu (null response) je dosahováno přibližně 6krát vyššího procenta SVR než při použití opakované standardní léčby kombinací PEG-IFN a RBV.
Boceprevir
![Obr. 5 Schéma studie RESPOND-2: boceprevir u osob dříve léčených kombinací PEG-IFN + RBV; BOC – boceprevir, PEG-IFN – peginterferon a-2b, RBV – ribavirin; podle [12] – Bacon, et al., 2011.](https://www.remedia.cz/photo-a-28623---.jpg) Studie RESPOND-2 [12]: schéma studie ukazuje obr. 5 a její výsledky graf 5. Pro srovnání s předchozí studií je nutné si uvědomit, že skupina zde označená jako předchozí „non-responders“ byla definována jako skupina osob, u nichž při předchozí terapii došlo ve 12. týdnu léčby k poklesu HCV RNA ≥ 2 log oproti výchozím hodnotám,
Studie RESPOND-2 [12]: schéma studie ukazuje obr. 5 a její výsledky graf 5. Pro srovnání s předchozí studií je nutné si uvědomit, že skupina zde označená jako předchozí „non-responders“ byla definována jako skupina osob, u nichž při předchozí terapii došlo ve 12. týdnu léčby k poklesu HCV RNA ≥ 2 log oproti výchozím hodnotám, ![Graf 5 Výsledky studie RESPOND-2: podíl SVR podle terapeutické větve a účinnosti předchozí léčby; BOC – boceprevir, PEG-IFN – peginterferon a-2b, RBV – ribavirin; podle [12] – Bacon, et al., 2011.](https://www.remedia.cz/photo-a-28624---.jpg) ale nikdy nebyla HCV RNA negativní. Z pohledu definicí užitých ve studii REALIZE jde tedy spíše o osoby s částečnou odpovědí. I tak je patrno významné navýšení odpovědi ve smyslu SVR u obou skupin pacientů při použití fixního léčebného trojkombinačního schématu s boceprevirem ve srovnání s odpovědí při opakování standardní protivirové léčby PEG-IFN + RBV.
ale nikdy nebyla HCV RNA negativní. Z pohledu definicí užitých ve studii REALIZE jde tedy spíše o osoby s částečnou odpovědí. I tak je patrno významné navýšení odpovědi ve smyslu SVR u obou skupin pacientů při použití fixního léčebného trojkombinačního schématu s boceprevirem ve srovnání s odpovědí při opakování standardní protivirové léčby PEG-IFN + RBV.
Závěr
V současné době stojíme na prahu nové éry léčby chronické (i akutní?) HCV infekce. Období, které máme před sebou, bude nepochybně érou přímo působících virostatik a farmokogenomiky. V nejbližších letech lze očekávat další záplavu informací o významu polymorfismů genu IL28B pro HCV infekci. Pravděpodobně bude postupně objasněn i mechanismus tohoto vlivu. V příštím roce jsou očekávány výsledky prvních studií s podáváním přímo „ideálního“ IFN-l. Další vývoj v oblasti přímo působících virostatik je obtížně odhadnutelný. V posledním roce se ukázalo, že několik molekul s velmi dobrým protivirovým efektem vede u člověka k rozvoji závažných nežádoucích účinků. Výzkum řady z těchto nadějných látek byl proto zastaven. Pravděpodobný vývoj bude zřejmě směřovat k tomu, aby se virostatika stala dominantní lékovou skupinou používanou k terapii HCV infekce. Ze současného portfolia zřejmě jako první zmizí pegylovaný interferon, naopak ribavirin bude pravděpodobně užíván ještě řadu let.
V ČR v současné době probíhá na specializovaných pracovištích řada klinických studií fází II či III s novými molekulami z třídy přímo působících virostatik. Boceprevir je na přibližně 12 pracovištích v republice dostupný díky specifickému léčebnému programu, analogické kroky podniká Česká hepatologická společnost a Společnost infekčního lékařství ČLS JEP i k zajištění brzké dostupnosti telapreviru.
Seznam použité literatury
- [1] Thomas DL, Thio CL, Martin MP, et al. Genetic variation in IL28B and spontaneous clearance of hepatitis C virus. Nature 2009; 461: 798–801.
- [2] Balagopal A, Thommas DL, Thio LC. IL28B and the control of Hepatitis C virus infection. Gastroenterology 2010; 139: 1865–1876.
- [3] Grebely J, Petoumenos K, Hellard M, et al. Potential role for interleukin-28B genotype in treatment decision-making in recent hepatitis C virus infection. Hepatology 2010; 52: 1216–1224.
- [4] Ge D, Fellay J, Thompson AJ, et al. Genetic variation in IL28B predicts hepatitis C treatment-induced viral clearance. Nature 2009; 461: 399–401.
- [5] Suppiah V, Moldovan M, Ahlenstiel G, et al. IL28B is associated with response to chronic hepatitis C interferon-alpha and ribavirin therapy. Nat Genet 2009; 41: 1100–1104.
- [6] Rauch A, Kutalik Z, Descombes P, et al. Genetic variation in IL28B is associated with chronic hepatitis C and treatment failure: a genome-wide association study. Gastroenterology 2010; 138: 1338–1345.
- [7] European Association for the Study of the Liver. EASL Clinical Practice Guidelines: management of hepatitis C virus infection. J Hepatol 2011; 55: 245–264.
- [8] Jacobson IM, McHutchison JG, Dusheiko G, et al. Telaprevir for previously untreated chronic hepatitis C virus infection. N Engl J Med 2011; 364: 2405–2416.
- [9] Sherman KE, Flamm SL, Afdhal NH, et al. Response-guided telaprevir combination treatment for hepatitis C virus infection. N Engl J Med 2011; 365: 1014–1024.
- [10] Poordad F, McCone J Jr, Bacon BR, et al. Boceprevir for untreated chronic HCV genotype 1 infection. N Engl J Med 2011; 364: 1195–1206.
- [11] Zeuzem S, Andreone P, Pol S, et al. Telaprevir for retreatment of HCV infection. N Engl J Med 2011; 364: 2417–2428.
- [12] Bacon BR, Gordon SC, Lawitz E, et al. Boceprevir for previously treated chronic HCV genotype 1 infection. N Engl J Med 2011; 364: 1207–1217.