Osteonekrózy čelistí u onkologicky nemocných
Článek se zabývá problematikou osteonekróz čelistních kostí u onkologicky léčených pacientů. Pozornost je soustředěna především na osteoradionekrózy vzniklé po radioterapii a na kostní nekrózy, které mohou provázet léčbu bisfosfonáty. Autoři popisují možné teorie a příčiny jejich vzniku a zamýšlejí se nad velmi obtížnou léčbou, farmakologickou i chirurgickou. Důraz kladou na prevenci těchto komplikací, která je v obou případech založena na pečlivé sanaci chrupu s extrakcí nevyhovujících zubů před zahájením léčby.
Úvod
Léčba pacientů s onkologickým onemocněním je bezesporu komplikovaná a těžká, podílí se na ní celá řada odborností. Pacient od okamžiku, kdy je obeznámen s diagnózou, zahajuje pouť vedoucí, v tom lepším případě, k uzdravení, nebo alespoň k prodloužení života. Na této cestě se potkává s různými lékaři, léčebnými postupy, které jej svým vlastním způsobem ovlivňují. Přinášejí mu úlevu, zdárné řešení jeho onemocnění, nebo také další problémy s léčbou spojené.
V naší stomatochirurgické praxi vidíme, jak může ústní dutina změnit vnímání kvality života k horšímu. Mezi komplikující záležitosti jistě patří bolest zubu, bolestivá léze sliznice, nebo dokonce nekróza alveolu či čelisti. Toto vše nutí pacienta vyhledat specializovanou pomoc. Ze stomatologického pohledu je dále patrné, že některým situacím je možno s velkou pravděpodobností předejít, nebo alespoň udělat vše pro to, aby nevznikly. Hlavní náplní našeho sdělení bude problematika nekróz čelistních kostí neboli osteonekrózy čelistí. Pokládáme toto téma za důležité nejen kvůli vzrůstajícímu počtu postižených, ale také kvůli velmi problematické léčbě.
Osteonekróza čelistí
Jedná se o nozologickou jednotku známou přes 150 let. Byla definována jako nekrotická kost vzniklá na podkladě příčin, které omezují krevní zásobení kosti. Možné příčiny byly hledány a postupně definovány a nakonec rozděleny na lokální a systémové. Mezi lokální patří například infekce v okolí kosti, ostitida, osteomyelitida, dále úrazy, zlomeniny a v neposlední řadě také radioterapie zaměřená na oblast čelistních kostí z důvodu léčby maligního onemocnění hlavy a krku.
Další příčiny jsou systémové a patří mezi ně například stavy po otravách, komplikace onemocnění cukrovkou, léčba revmatických onemocnění kortikoidy nebo jinou imunosupresivní terapií, možný důsledek léčby malignit chemoterapií a především v posledních několika letech diskutované podávání bisfosfonátů. Máme-li se věnovat osteonekrózám čelistí u onkologických pacientů, zaměřme se hlavně na osteoradionekrózu, tedy nekrózu kosti vzniklou na podkladě ozáření, a dále na osteonekrózu vzniklou po nebo při léčbě bisfosfonáty. Klinický projev těchto nekróz čelistí je stejný, bez ohledu na vyvolávající příčinu. Může probíhat po mnoho let asymptomaticky, později se může objevit bolest čelisti, parestezie, následně lze vidět kostní defekt alveolu s projevy zánětu na okolní sliznici nebo přilehlé kůži. Může být přítomna i extraorální kožní píštěl. Proces postihující dolní čelist může dospět až k patologické zlomenině s posunem úlomků.
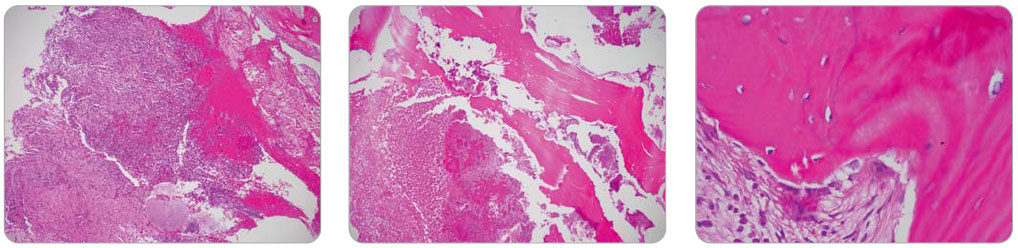 Také histomorfologický obraz osteonekrózy vzniklé v průběhu užívání bisfosfonátů je víceméně identický s osteoradionekrózou. V preparátech osteoradionekrózy byl ojediněle zachycen osteoklast. Histologické vyšetření je podstatné k vyloučení přítomnosti maligních buněk. Nekrotická kostní tkáň částečně sekvestruje, což umožňuje vznik sekundární infekce, zánětlivé infiltrace. Ve většině případů mikroskopický obraz dále ukazuje rozsáhlé saprofytické kolonizace vláknitými mikroorganismy. Histologický obraz jako takový nic neříká o možné příčině nekrózy.
Také histomorfologický obraz osteonekrózy vzniklé v průběhu užívání bisfosfonátů je víceméně identický s osteoradionekrózou. V preparátech osteoradionekrózy byl ojediněle zachycen osteoklast. Histologické vyšetření je podstatné k vyloučení přítomnosti maligních buněk. Nekrotická kostní tkáň částečně sekvestruje, což umožňuje vznik sekundární infekce, zánětlivé infiltrace. Ve většině případů mikroskopický obraz dále ukazuje rozsáhlé saprofytické kolonizace vláknitými mikroorganismy. Histologický obraz jako takový nic neříká o možné příčině nekrózy.
Osteoradionekróza
Literatura nabízí celou řadu definic osteoradionekrózy. Mezi ustálené definice lze zařadit i tuto: jedná se o kostní lézi s porušeným slizničním nebo kožním krytem vzniklou ozářením, která trvá déle než 3 měsíce a je bez prokázané přítomnosti recidivy nádoru [1].
Poprvé popsal osteoradionekrózu čelisti snad Claude Regaud (1870–1940) v roce 1922. Jednalo se v té době o významného francouzského lékaře, univerzitního profesora a průkopníka v léčbě malignit pomocí záření izotopem radia [2]. Osteoradionekróza postihuje mnohem častěji čelist dolní než horní, poměr se udává 24 : 1. Důvodem je rozdílné cévní zásobení čelistí. Horní čelist je mnohem více cévně zásobena než čelist dolní.
Dalším faktorem je způsob radioterapie, v souborech se popisuje jako riziková dávka vyšší než 60 Gy, použití brachyterapie a konkomitantní radiochemoterapie. Důležitá je také frakcionace, horší následky mohou být spojeny s hypofrakcionací. Zásadní je rovněž velikost a umístění nádoru, což rozhoduje také o směru paprsků. Nejvíce osteoradionekróz je popisováno po ozáření pro karcinom tonzily nebo retromolární oblasti. Velmi důležitým předpokladem ke zvýšení rizika osteoradionekrózy je přítomnost zubů. Udává se, že v ozubené čelisti vzniká poradiační nekróza 3krát častěji ve srovnání s čelistí bezzubou. Se zuby úzce souvisí chirurgický výkon na ozářené čelisti, tedy extrakce zubu, porušení slizničního krytu, deperiostace kosti apod. Mezi doplňkové faktory patří dále malnutrice, často doprovázená chronickým alkoholismem a nikotinismem, to vše ruku v ruce s nedostatečnou hygienou ústní dutiny.
Teorie vzniku
Během let byly formulovány celkem tři teorie vzniku osteoradionekrózy čelisti. Následné teorie vytvořené na podkladě nových vědomostí postupem času pozměnily ty předchozí. Nicméně neubraly nic na jejich platnosti, neboť příčina je s velkou pravděpodobností multifaktoriální. První teorie byla vytvořena v roce 1938. Za základ se považoval průnik infekce z dutiny ústní do radiací změněné kosti po poranění sliznice. Vysvětluje vysoce pravděpodobný vznik po extrakci zubu, ale nevysvětluje spontánní vznik nekrózy po ozáření [3]. Další na řadě je teorie definovaná roku 1983. Připouští, že se již primárně nemusí jednat o infekci, ale o soubor následných iradiačních změn tkáňového a humorálního metabolismu. Zavádí pojmy jako hypoxie, hypovaskularita a hypocelularita v ozářené kosti [4].
 Zatím poslední teorie zabývající se osteoradionekrózou pochází z roku 2004: klade důraz na imunologické pochody v kosti nastartované ozářením, které vedou k fibrotizaci a atrofii tkáně s následnou resorpcí [5]. Pouze pro ilustraci se pokusíme stručně popsat možný mechanismus. Iniciátorem všech změn je ionizující záření a vzniklé volné kyslíkové radikály, které vedou k poškození endotelu kapilár, k jejich trombóze a následné hypoxii kostní tkáně. Tento stav rozproudí imunitní reakci, zánět s výraznou produkcí cytokinů (IL-1, IL-4, IL-6, FGF, TNF-a), a tím stimulaci fibroblastů a myofibroblastů, což vede k fibrotizaci tkáně. Zároveň hypoxie vede také k destrukci osteoblastů, osteocytů a osteoklastů. Výsledkem tohoto děje je vznik hypocelulární, hypoxické a fibrotické tkáně. Časem dochází k odumření fibroblastů, rozvoji jizvení tkáně a dále, což je podstatné, ke vzniku osteoklastů z makrofágů, které vcestovaly do takto změněné tkáně z krevního řečiště. Osteoklasty tímto způsobují resorpci kosti, demineralizaci. V ozářené kosti neexistuje, v důsledku nepřítomnosti osteoblastů, protichůdný metabolický děj, osteogeneze. Dochází tedy ke vzniku osteolytických defektů a vzniku osteoradionekrózy. Takto postižená kost je otevřena do dutiny ústní plné různých mikroorganismů včetně bakterií, kvasinek a plísní, které velmi rychle nekrotickou kost osidlují a dále destruují.
Zatím poslední teorie zabývající se osteoradionekrózou pochází z roku 2004: klade důraz na imunologické pochody v kosti nastartované ozářením, které vedou k fibrotizaci a atrofii tkáně s následnou resorpcí [5]. Pouze pro ilustraci se pokusíme stručně popsat možný mechanismus. Iniciátorem všech změn je ionizující záření a vzniklé volné kyslíkové radikály, které vedou k poškození endotelu kapilár, k jejich trombóze a následné hypoxii kostní tkáně. Tento stav rozproudí imunitní reakci, zánět s výraznou produkcí cytokinů (IL-1, IL-4, IL-6, FGF, TNF-a), a tím stimulaci fibroblastů a myofibroblastů, což vede k fibrotizaci tkáně. Zároveň hypoxie vede také k destrukci osteoblastů, osteocytů a osteoklastů. Výsledkem tohoto děje je vznik hypocelulární, hypoxické a fibrotické tkáně. Časem dochází k odumření fibroblastů, rozvoji jizvení tkáně a dále, což je podstatné, ke vzniku osteoklastů z makrofágů, které vcestovaly do takto změněné tkáně z krevního řečiště. Osteoklasty tímto způsobují resorpci kosti, demineralizaci. V ozářené kosti neexistuje, v důsledku nepřítomnosti osteoblastů, protichůdný metabolický děj, osteogeneze. Dochází tedy ke vzniku osteolytických defektů a vzniku osteoradionekrózy. Takto postižená kost je otevřena do dutiny ústní plné různých mikroorganismů včetně bakterií, kvasinek a plísní, které velmi rychle nekrotickou kost osidlují a dále destruují.
Léčba osteoradionekrózy
Terapie osteoradionekrózy bývá velmi obtížná. Spočívá hlavně v šetrné a opakované toaletě defektů a v dlouhodobém podávání antibiotik; z naší zkušenosti se nejlépe osvědčil klindamycin 300 mg 3krát denně dlouhodobě, dále chinolony (ciprofloxacin) nebo betalaktamová antibiotika – peniciliny, cefalosporiny (aztreonam, meropenem).
Snahou je minimalizovat chirurgickou léčbu, neboť každým větším výkonem může dojít ke zhoršení, zvětšení rozsahu osteonekrózy. Bývá omezena na šetrnou nekrektomii, při větších defektech a jejich ohraničení se provádí sekvestrotomie a ve výjimečných případech je indikována resekce čelisti. Další možností v léčbě je hyperbarická oxygenoterapie. Byly publikovány práce, které popírají přínos hyperbarické oxygenoterapie v léčbě osteoradionekrózy [6]. Nicméně existuje celá řada dalších, ukazujících na vhodnost této léčby, přinejmenším jako doplňku k chirurgické léčbě s rekonstrukcí defektu [7, 8].
Co nás čeká v budoucnu?
Existují práce, které se zabývají preventivně léčebnou možností ovlivnění osteoradionekrózy pomocí kombinace pentoxifylinu a tokoferolu. Hlavním přínosem pentoxifylinu je snížení viskozity krve, zvýšení elasticity erytrocytů, dilatace cév, útlum zánětlivé reakce a snížení proliferace fibroblastů. Tokoferol působí jako antioxidační látka, ochrana enzymů a membrán [9]. Využívá se kombinace účinku těchto léčiv. Je známo několik dávkovacích schémat, v jednom z nich se podává pentoxifylin v dávce 800 mg/den a tokoferol v dávce 1000 IU nebo 600 mg/den [10]. Podávání této kombinace s sebou přináší další otázky ve smyslu: Kdy začít tuto kombinaci podávat, stačí například od dávky 30 Gy, nebo je podávání nutné od začátku radioterapie? Nenaruší nám tyto účinné látky citlivost nádorových buněk k ionizujícímu záření? Má smysl tyto léky podávat jako prevenci osteonekrózy čelisti, když k ní může dojít dle statistiky přibližně u 6 % ozařovaných pacientů? Odpovědi na tyto otázky nám jistě přinese budoucí vývoj.
Jako další farmakologická léčba je popisována terapie osteoradionekrózy pomocí bisfosfonátů. Přesněji pomocí klodronátu, který patří mezi nedusíkaté bisfosfonáty. Odůvodnění tohoto použití bisfosfonátu plyne z logiky výše uvedené teorie o resorpci kostní jizvy pomocí osteoklastů. Bisfosfonát tlumí funkci osteoklastů, takže může zabránit rozvoji defektu a urychlit jeho zhojení. Při potvrzení kostního defektu se podává v dávce 1600 mg/den, a to 5 dní v týdnu po dobu 3 měsíců, nejlépe v kombinaci s pentoxifylinem a tokoferolem [10].
Osteonekróza při léčbě bisfosfonáty
Bisfosfonáty jsou syntetická analoga pyrofosfátu, jež se vážou na hydroxyapatit kostní hmoty, vedou k inhibici osteoklastů, čímž brání resorpci kosti. Díky těmto vlastnostem se používají v léčbě osteoporózy či Pagetovy choroby, v onkologii k léčbě mnohočetného myelomu, osteolytických metastáz nádorů prsu, prostaty, ledvin aj. Prokazatelně zlepšují kvalitu přežívání, mírní bolest, snižují riziko patologických zlomenin a hyperkalcemie. Bisfosfonáty se rozdělují na nedusíkaté, které byly vyrobeny nejdříve (klodronát, etidronát), a dále na dusíkaté (pamidronát, alendronát, ibandronát, zoledronát, risedronát). Dusíkatá sloučenina mění mechanismus účinku na osteoklasty a dle dostupných zdrojů také zvyšuje schopnost ovlivnit resorpci kosti [11].
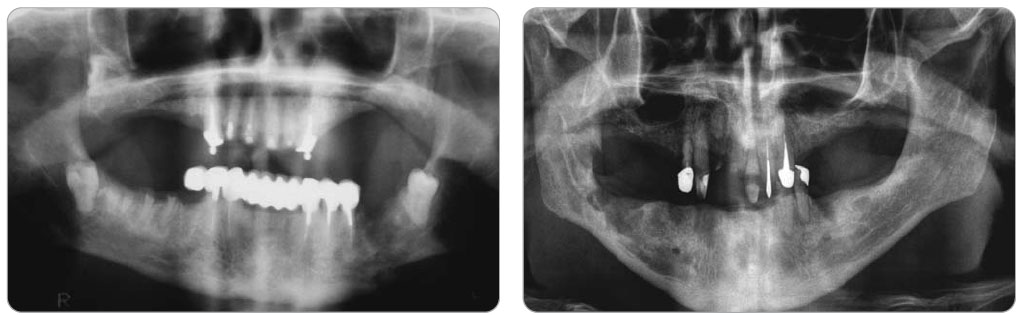 Definice osteonekrózy při léčbě bisfosfonáty (Bisphosphonate-Related OsteoNecrosis of the Jaw, BRONJ) je stanovena AAOMS (American Association of Oral and Maxillofacial Surgeons) jako nekrotická kost vzniklá při nebo po používání bisfosfonátů, bez předchozího ozáření čelistí nebo bez dřívější přítomnosti kostní metastázy, přičemž se kostní defekt nehojí déle než 8 týdnů [12]. Snad první zmínka o nekróze čelistní kosti po léčbě bisfosfonáty byla publikována v roce 2003 [13]. Od té doby je možno najít celou řadu článků. Dokonce existují statistické soubory s vyjádřenou možnou mírou rizika vzniku této komplikace. Například při intravenózním podávání je riziko vzniku BRONJ 0,8–12 %, při dlouhodobém, déle než 3 roky trvajícím perorálním podávání je riziko rozdílné u onkologických pacientů, kde činí 0,06 %, a u pacientů léčených pro
Definice osteonekrózy při léčbě bisfosfonáty (Bisphosphonate-Related OsteoNecrosis of the Jaw, BRONJ) je stanovena AAOMS (American Association of Oral and Maxillofacial Surgeons) jako nekrotická kost vzniklá při nebo po používání bisfosfonátů, bez předchozího ozáření čelistí nebo bez dřívější přítomnosti kostní metastázy, přičemž se kostní defekt nehojí déle než 8 týdnů [12]. Snad první zmínka o nekróze čelistní kosti po léčbě bisfosfonáty byla publikována v roce 2003 [13]. Od té doby je možno najít celou řadu článků. Dokonce existují statistické soubory s vyjádřenou možnou mírou rizika vzniku této komplikace. Například při intravenózním podávání je riziko vzniku BRONJ 0,8–12 %, při dlouhodobém, déle než 3 roky trvajícím perorálním podávání je riziko rozdílné u onkologických pacientů, kde činí 0,06 %, a u pacientů léčených pro 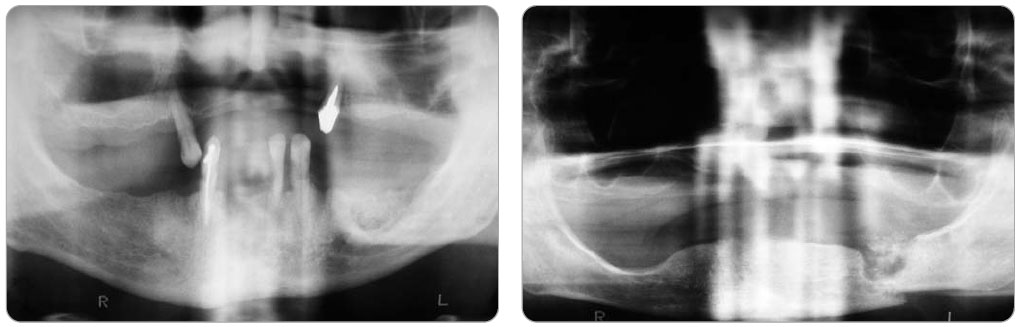 osteoporózu, kde činí pouze 0,00038 %. Existuje také míra rizika u jednotlivých onkologických nemocí, při nichž se bisfosfonáty podávají. Mnohočetný myelom představuje 44% riziko vzniku čelistní nekrózy, metastatický karcinom plic 32% a pokročilý karcinom prostaty 5% riziko. Dále je zjištěn poměr mezi postižením dolní a horní čelisti, dolní čelist je postižena pouze 2krát častěji než horní. Znamená to tedy, že je horní čelist postižena mnohonásobně více, než je tomu například u osteoradionekrózy [14, 15].
osteoporózu, kde činí pouze 0,00038 %. Existuje také míra rizika u jednotlivých onkologických nemocí, při nichž se bisfosfonáty podávají. Mnohočetný myelom představuje 44% riziko vzniku čelistní nekrózy, metastatický karcinom plic 32% a pokročilý karcinom prostaty 5% riziko. Dále je zjištěn poměr mezi postižením dolní a horní čelisti, dolní čelist je postižena pouze 2krát častěji než horní. Znamená to tedy, že je horní čelist postižena mnohonásobně více, než je tomu například u osteoradionekrózy [14, 15].
Možný mechanismus vzniku
Přesný mechanismus vzniku osteonekrózy po podání bisfosfonátů není dosud znám. Selektivní vliv na osteoklasty je dán vazbou bisfosfonátů na hydroxyapatit kosti. Nedusíkaté bisfosfonáty pravděpodobně působí až po pohlcení osteoklastem a po proniknutí do jeho cytoplazmy na metabolismus ATP a tím blokují metabolismus buňky jako celku a způsobují smrt osteoklastu. Zato dusíkaté bisfosfonáty proniknou do metabolismu prekurzorů cholesterolu, do řetězce mevalonátového cyklu; omezí tak metabolismus drobných proteinů nutných pro složení a funkci buněčné membrány, což vede také k odumření buňky. Díky mnohaleté akumulaci v kosti působí bisfosfonáty nejen na osteoklasty, ale v závislosti na koncentraci také na celou řadu dalších buněk. Potlačují mimo jiné angiogenezi, proliferaci cév a při vysoké místní koncentraci mohou vést k destrukci membrán všech okolních buněk. Čelistní kosti mají fyziologicky intenzivnější kostní metabolismus. Díky žvýkání jsou velmi zatěžovány, a proto dochází k rychlejší remodelaci kosti. Tato vystupňovaná aktivita má za následek větší kumulaci bisfosfonátů v oblasti obličejového skeletu. Tímto lze vysvětlit větší podíl postižení maxilly, neboť maxilla je více prokrvena, takže se k ní dostane více molekul bisfosfonátu, které se navážou do kosti. Zatěžování čelistí žvýkáním může vést při omezené kostní remodelaci ke vzniku drobných kostních mikrotraumat. Samotná vysoká koncentrace bisfosfonátů v čelisti může způsobit dokonce i nekrózu slizničního krytu. Celý tento mechanismus je navíc zasazen do dutiny ústní, plné různých druhů ústních bakterií [16].
Shrneme-li tedy doposud zjištěné poznatky, dostaneme možnou teorii vzniku bisfosfonátové nekrózy: inhibice remodelace kosti, porucha mikrocirkulace, možné porušení slizničního krytu, případná drobná mikrotraumata kosti, ústní bakterie, přidružená imunosuprese po chemoterapii, eventuálně po léčbě kortikoidy. Nutno připojit i další doplňkové, pomocné faktory, kterými jsou: stav chrupu, kazy, periapikální chronické záněty, stav parodontu, obvykle špatná ústní hygiena, přidružená onemocnění (diabetes mellitus, hyperkoagulace, stav kostní denzity), podávané léky, kouření, alkoholismus a v neposlední řadě stomatochirurgický výkon – například jednoduchá extrakce zubu ve výše zmíněných podmínkách. Právě stomatochirurgický výkon, extrakce zubu z důvodu bolesti, je příčinou podstatné většiny vzniklých bisfosfonátových osteonekróz.
Proč záleží na typu bisfosfonátu?
Pomineme-li rozdělení bisfosfonátů na dusíkaté a nedusíkaté, můžeme je rozdělit podle intenzity účinku, relativní síly, s jakou jsou schopny ovlivnit osteoklasty a zabránit resorpci kosti. Skórování vychází z charakteristiky klodronátu, který má hodnotu relativní síly 1, alendronát například 150, ibandronát 860, pamidronát 100 a zoledronát 10 000 [11].
Tento systém úzce souvisí se statistickými daty vzniklých osteonekróz a dává předpoklad ke vzniku teorie „rizikové kumulační dávky v čelisti“, tedy vytvoření míry rizika, pravděpodobnosti vzniku nekrózy pro daný typ bisfosfonátu po určitém čase.
Při léčbě pamidronátem, který má relativní potenci 100, je pravděpodobnost vzniku nekrózy 0 % za dobu užívání 1 roku, ale už 4 % po 3 letech užívání. Zoledronát s relativní silou 10 000 má pravděpodobnost vytvoření rizikové kumulační dávky, tedy možného vzniku osteonekrózy, po 1 roce užívání 1 %, po 3 letech však tato pravděpodobnost stoupá na 21 % [17]. AAOMS stanovila na základě těchto poznatků určitá pravidla formulovaná jako existence přímé úměry mezi silou bisfosfonátu a rizikem vzniku BRONJ. Dále určila nepřímou úměru mezi silou bisfosfonátu a délkou jeho užívání před vznikem BRONJ. A do třetice definovala přímou úměru mezi délkou užívání bisfosfonátu a vznikem BRONJ [15].
Léčba BRONJ
Pokud dojde k vytvoření bisfosfonátové osteonekrózy, je její léčba velmi problematická. Základ léčby tvoří lokální toaleta defektu spolu se šetrným odstraňováním nekrotických hmot, výplachy úst lokálními dezinfekčními roztoky. Při projevech zánětu se podávají dlouhodobě antibiotika (peniciliny, klindamycin, erythromycin, tetracykliny). Dojde-li k ohraničení nekrózy, je indikováno odstranění sekvestru. Pokud vznikne v důsledku nekrózy kosti patologická zlomenina čelisti doprovázená bolestí s obtížným příjmem potravy, je možno provést resekci postižené čelisti s rekonstrukcí defektu. Chirurgicky velmi obtížně řešitelné jsou nekrózy alveolu v postranních úsecích horní čelisti, kde kvůli přítomnosti čelistní dutiny obvykle dojde u rozsáhlých nekróz k vytvoření oroantrální píštěle se všemi následky: prouděním vzduchu při mluvení nebo výtokem tekutin z nosu při jídle [18, 19]. Cíl léčby je stanoven velmi realisticky. Není zaměřen na vyléčení nekrózy, ale na prostý a pro pacienta důležitý záměr – odstranit bolest. Dále má léčba směřovat k zabránění rozvoje základního onkologického onemocnění a zamezit rozšiřování nekrózy. Vzhledem k nutnosti mezioborového přístupu k řešení zhoubného onemocnění je i léčba osteonekrózy po terapii bisfosfonáty mezioborová. Podílí se na ní stomatolog, eventuálně stomatochirurg spolu s onkologem. Při léčbě nekrózy vyvstává pro ošetřujícího onkologa otázka, zda ukončit nebo přerušit terapii bisfosfonáty. Bohužel chybí dostatek informací, které by rozhodly o vhodném postupu. Existují práce, které přerušení či ukončení léčby bisfosfonáty odmítají, argumentují dlouhým poločasem vyloučení z kosti, díky němuž nemá takovýto postup zásadní vliv na zlepšení osteonekrózy. Další popisují ana případech dokazují zlepšení stavu nemocných po přerušení léčby bisfosfonátem na dobu 6–12 měsíců.
Nabízí se několik možných řešení. Jde však o řešení kompromisní, léčba musí být „šitá na míru“ konkrétní situaci. Doporučuje se před chirurgickým výkonem na čelistech přerušit léčbu bisfosfonátem na 3 měsíce, provést výkon a po zhojení extrakčních ran léčbu opět zahájit. Dalším řešením je změnit typ bisfosfonátu, vzhledem k výrazné síle dusíkatých bisfosfonátů se nabízí záměna za nedusíkatý typ. Rovněž je možno například prodloužit interval mezi infuzemi a tím oddálit vytvoření rizikové kumulační dávky tak, jak to bylo popsáno výše. Musíme však zdůraznit, že přerušení nebo změna bisfosfonátové léčby je plně v rukou onkologů, kteří přesně vědí, jaký je zdravotní stav pacienta, stav jeho základního onemocnění, a dovedou tak nejlépe určit rizika a efektivitu změny bisfosfonátové léčby.
Osteonekrózy – srovnání
Hlavní náplní tohoto sdělení bylo ukázat a připomenout výskyt nekrózy čelistních kostí u pacientů léčených pro onkologické onemocnění. V širším slova smyslu není důležité, jakým mechanismem k nekróze dojde, ale to, že k ní vůbec dojde a že podstatným způsobem zasahuje do života onkologicky nemocných.
Rádi bychom se zamysleli nad rozdíly a podobností těchto výše popsaných nekróz.
Mezi základní rozdíly patří jistě mechanismus vzniku. Histologicky lze nalézt pouze drobné rozdíly, a to spíše v přítomnosti osteoklastů. Kde se rozdíl naprosto stírá, je klinický vzhled dané léze. Obě nekrózy bolí, pacienta obtěžují a znesnadňují mu příjem potravy. Žalostné je také, že obě vznikají jako nechtěný výsledek onkologické léčby v souvislosti s provedeným stomatochirurgickým výkonem.
Alarmující je rostoucí incidence bisfosfonátové nekrózy, která se začíná vyskytovat nejen u onkologicky nemocných, ale také u pacientů léčených pro jiná kostní onemocnění, např. pro osteoporózu. Naštěstí incidence osteoradionekrózy má klesající tendenci. Z téměř 16 % postižených pacientů před 30 lety klesla nyní na úroveň kolem 6 %.
Dalším neméně důležitým faktem je, jak se na vznik osteonekrózy čelistí pohlíží. Zda se jedná o nevyhnutelnost spojenou s léčbou nutnou pro prodloužení přežití – v případě lokální radioterapie, nebo se jedná o následek preventivní systémové léčby, u které je prokázán výrazný efekt na kvalitu života, ale ne na délku přežití.
Zmiňované nekrózy čelistí jsou obecně velmi obtížně řešitelné, vzhledem k tomuto poznatku se v první řadě neusiluje o vyléčení, ale pouze o odstranění bolesti a okolního zánětu. Léčebné schéma, jemuž dominuje konzervativní a šetrný přístup, je také víceméně stejné.
Prevence
Prevence osteonekróz čelistí je sice organizačně náročnější, ale vzhledem k obtížnosti léčby by měla být základní a klíčová. Vyžaduje od onkologů, aby se aktivně zajímali o stav dutiny ústní svých pacientů a posílali je před zahájením léčby k ošetřujícímu stomatologovi. Ten by měl udělat RTG snímek chrupu (ortopantomogram), důkladně chrup vyšetřit a provést pečlivou sanaci, případně extrakci nevyhovujících zubů. Cílem tohoto postupu před zahájením léčby je dosáhnout takového stavu chrupu, aby po dobu léčby, předpokládá se několik let, nebylo nutné žádný zub extrahovat.
Závěr
Osteonekrózy u onkologických pacientů nevznikají ve velké většině případů hned, ale nejčastěji až po určitém čase. Po radioterapii se již s možností čelistní nekrózy částečně počítá, jedná se o komplikaci s historickými kořeny a pacient je o této možné nežádoucí komplikaci ošetřujícím onkologem jistě informován. Navíc je velmi povzbudivé, že množství osteoradionekróz klesá, právě možná díky již zavedeným preventivním opatřením před zahájením a během léčby ionizujícím zářením.
Opačně je tomu u osteonekróz po nebo při terapii bisfosfonáty. Jedná se o komplikaci popisovanou teprve v nedávné době, která se navíc projeví až po několika letech podávání. Je pacient s touto komplikací vůbec seznámen? Je poučen, aby svému stomatologovi při ošetření oznámil, že užívá bisfosfonáty? Je pacient informován natolik, aby věděl, že dostává pravidelně v infuzi nebo v tabletách léky, které mu mohou způsobit nějaké komplikace?
Představíme-li si, kolik pacientů nyní bisfosfonáty užívá nebo začne užívat, můžeme si být jisti, že se ve svých praxích s tímto problémem jistě setkáme.
Seznam použité literatury
- [1] Harris M. The conservative management of osteoradionecrosis of the mandible with ultrasound therapy. Br J Oral Maxillofac Surg 1992; 30: 313–318.
- [2] Regaud C. Sur la necrose des os attentē par un processus cancereux et traites par les radiaions. Compt Rend Soc Biol 1922; 87: 629.
- [3] Watson WL, Scarborough JE. Osteoradionecrosis in intraoral cancer. Am J Roentgenol 1938; 40: 524–534.
- [4] Marx R. Osteoradionecrosis: a new concept of its pathophysiology. J Oral Maxillofac Surg 1983; 41: 283–288.
- [5] Delanian S, Lefaix JL. The radiation-induced fibroatrophic process: therapeutic perspective via the antioxidant pathway. Radiother Oncol 2004; 73: 119–131.
- [6] Annane D, Depondt J, Aubert P, et al. Hyperbaric oxygen therapy for radionecrosis of the jaw: A randomized, placebo-controlled, double-blind trial from the ORN96 Study Group. J Clin Oncol 2004; 22: 4893–4900.
- [7] Brown DH, Evans AW, Sandor GKB. Hyperbaric oxygen therapy in the management of osteoradionecrosis of the mandible. Adv Otorhinolaryngol 1998; 54: 14–32.
- [8] Mansfield MJ, Sanders DW, Heimbach RD, Marx RE. Hyperbaric oxygen as an adjunct in the treatment of osteoradionecrosis of the mandible. J Oral Surg 1981; 39: 585–589.
- [9] Delanian S, Depondt J, Lefaix JL. Major healing of refractory mandible osteoradionecrosis after treatment combining pentoxifylline and tocopherol: a phase II trial. Head Neck 2005; 27: 114–123.
- [10] Lyons A, Ghazali N. Osteoradionecrosis of the jaws: current understanding of its pathophysiology and treatment, British Journal of Oral and Maxillofacial Surgery 2008; 46: 653–660.
- [11] Carol D M, Thomas AE. Bisphosphonates in orthopaedic surgery. Journal of Bone and Joint Surgery 2005; 87: 7; ProQuest Medical Library, pg. 1609.
- [12] American Association of Oral and Maxillofacial Surgeons, Position Paper on Bisphosphonate-Related Osteonecrosis of the Jaw-Approved by the Board of Trustees September 25, 2006.
- [13] Marx RE, et al. Pamidronate (Aredia) and zoledronate (Zometa) induced avascular necrosis of the jaws: a growing epidemic. J Oral Maxillofac Surg 2003; 61: 1115–1117.
- [14] Bartl R, Mast G. Bisphosphonate-associated osteonecrosis of the jaw: A pathophysiologic approach, Bone, Volume 42, Issue null, S92–S92.
- [15] American Association of Oral and Maxillofacial Surgeons, Position Paper on Bisphosphonate-Related Osteonecrosis of the Jaw-2009 Update.
- [16] Mehrotra B, Ruggiero S. Bisphosphonate Complications Including Osteonecrosis of the Jaw. Hematology Am Soc Hematol Educ Program 2006: 356–360, 515.
- [17] Mariotti A. Bisphosphonates and Osteonecrosis of the Jaws. J Dent Educ 2008; 72: 919–929.
- [18] Bulik O, Machálka M. Využití tukového tvářového laloku. Čes Stomat 2007; 107: 149–152.
- [19] Machálka M, Adam Z, Bulik O, Kozumplíková M. Osteonekróza čelistí při léčbě bisfosfonáty. Čes Stomat 2006; 106: 136–139.