Pethidin slaví 70 let
Pethidin (nazývaný také meperidin) patří mezi opioidní analgetika. Je to syntetický opioidní agonista, který kromě silného analgetického účinku působí mimo jiné také anticholinergně a má lokálně anestetické účinky. Pethidin je indikován k léčbě silné akutní bolesti po těžkých úrazech, operacích a k léčbě chronické bolesti při maligních tumorech. Nejčastěji je aplikován intramuskulárně k potlačení pooperační bolesti. Pethidin je více rozpustný v tucích než morfin, což je důvodem rychlejšího nástupu účinku. Při silných bolestech je ale pethidin méně účinný než morfin, nevýhodou je také toxicita jeho metabolitu norpethidinu. Je pozoruhodné, že aplikace pethidinu pokračuje již 70 let.
V tomto roce slaví pethidin 70 let od syntézy. V roce 1939 jej připravili němečtí chemici O. Eisleb a O. Schaumann z firmy Bayer. Šlo vlastně o objev téměř náhodný, protože pethidin byl syntetizován jako antimuskarinová látka (obr. 1). Pethidin (meperidin) má strukturální příbuznost podobnou atropinu a ostatním tropanovým alkaloidům a také s nimi má společné některé jejich účinky. Mechanismy účinků pethidinu jsou velmi zajímavé. Především patří mezi m-agonisty opioidního receptoru podobně jako morfin. Mechanismus jeho analgetického účinku je tedy dán 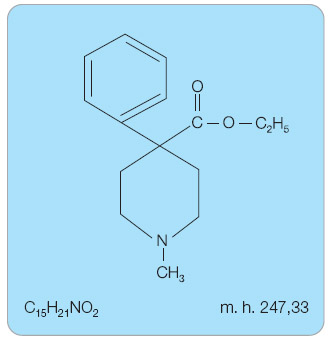 interakcí s opioidními receptory. Kromě silných analgetických a anticholinergních účinků má také lokálně anestetické účinky, které jsou ve vztahu k interakci se sodíkovým kanálem [1]. In vitro má pethidin zjevný spasmolytický efekt, který je způsoben jeho lokálními anestetickými účinky. V rozporu s obecným míněním však nebylo možno spolehlivě prokázat spasmolytické účinky in vivo. Pethidin má také stimulační účinky, které jsou zprostředkovány inhibicí transportu dopaminu a noradrenalinu do nervového zakončení – účinek podobný kokainu [2]. Pro tento svůj inhibiční účinek může pethidin v pokusech na zvířatech nahradit kokain při tréninku rozlišování kokainových a fyziologických roztoků. Podání pethidinu je také spojováno v některých případech se serotoninovým syndromem, což dokazuje jeho interakci se serotoninergními neurony. Definitivně to však nebylo prokázáno. Pethidin je s úspěchem používán k tlumení svalového třesu po celkové anestezii. Mechanismus účinku však nebyl do nedávné doby znám, protože ultrapotentní opioid, jako je např. sufentanil, nebyl tak úspěšný při potlačování svalového třesu jako pethidin. Na protitřesovém účinku se navíc nepodílejí opioidní receptory, protože naloxon neinhibuje účinky pethidinu na svalové chvění. Takada a kol. prokázali v roce 2002 v pokusech in vitro i in vivo, že pethidin se váže na α2-adrenergní receptory, a sice na populaci α2B-adrenergních receptorů [3]. Mechanismus je tedy stejný jako při podání α2-agonistů, např. klonidinu nebo dexmedetomidinu.
interakcí s opioidními receptory. Kromě silných analgetických a anticholinergních účinků má také lokálně anestetické účinky, které jsou ve vztahu k interakci se sodíkovým kanálem [1]. In vitro má pethidin zjevný spasmolytický efekt, který je způsoben jeho lokálními anestetickými účinky. V rozporu s obecným míněním však nebylo možno spolehlivě prokázat spasmolytické účinky in vivo. Pethidin má také stimulační účinky, které jsou zprostředkovány inhibicí transportu dopaminu a noradrenalinu do nervového zakončení – účinek podobný kokainu [2]. Pro tento svůj inhibiční účinek může pethidin v pokusech na zvířatech nahradit kokain při tréninku rozlišování kokainových a fyziologických roztoků. Podání pethidinu je také spojováno v některých případech se serotoninovým syndromem, což dokazuje jeho interakci se serotoninergními neurony. Definitivně to však nebylo prokázáno. Pethidin je s úspěchem používán k tlumení svalového třesu po celkové anestezii. Mechanismus účinku však nebyl do nedávné doby znám, protože ultrapotentní opioid, jako je např. sufentanil, nebyl tak úspěšný při potlačování svalového třesu jako pethidin. Na protitřesovém účinku se navíc nepodílejí opioidní receptory, protože naloxon neinhibuje účinky pethidinu na svalové chvění. Takada a kol. prokázali v roce 2002 v pokusech in vitro i in vivo, že pethidin se váže na α2-adrenergní receptory, a sice na populaci α2B-adrenergních receptorů [3]. Mechanismus je tedy stejný jako při podání α2-agonistů, např. klonidinu nebo dexmedetomidinu.
Pethidin je více rozpustný v tucích než morfin. To vede k rychlejšímu nástupu účinku. Délka klinického účinku je 120–150 minut. Přestože analgezie trvá většinou pouze 2–3 hodiny, pethidin je podáván k tlumení pooperační bolesti nejčastěji ve 4–6hodinových intervalech, což je pro zmírnění pooperačních bolestí většinou nedostatečné. Pethidin je také méně účinný než morfin při silných bolestech nebo při bolestech spojených s pohybem nebo kašláním. Jeho analgetický účinek představuje asi 1/10 analgetického účinku morfinu. Podobně jako ostatní opioidy může pethidin způsobit fyzickou nebo psychickou závislost. Podle některých autorů vzniká závislost rychleji než po podání ostatních opioidů, protože pethidin se vyznačuje rychlým nástupem účinku a stimulačním efektem podobným kokainu. Ve srovnání s oxykodonem, hydromorfonem a placebem je podávání pethidinu spojeno s větší euforií, s potížemi v koncentraci a se zhoršením psychomotorických a kognitivních funkcí [4]. Případné nežádoucí účinky doprovázející podávání pethidinu, jako jsou křeče, dysforie nebo tremor, jsou primárně spojeny s účinkem jeho metabolitu norpethidinu.
Pethidin je rychle hydrolyzován v játrech na kyselinu pethidinovou a také demetylován na norpethidin, který má asi polovinu analgetické aktivity pethidinu, ale delší biologický poločas 8–12 hodin. Při opakovaném podávání nebo při renálním selhání se může v organismu kumulovat. Norpethidin je toxický a má konvulzivní a halucinogenní účinky. Toxické účinky zprostředkované metabolity nemohou být antagonizovány antagonisty opioidních receptorů, jako je naloxon nebo naltrexon, a jsou pravděpodobně výsledkem anticholinergní aktivity norpethidinu. Neurotoxicita metabolitu pethidinu je unikátním rysem tohoto opioidu ve srovnání s ostatními. Metabolity pethidinu jsou dále konjugovány s kyselinou glukuronovou a vylučovány do moče.
Zcela zvláštní úlohu hraje metabolismus pethidinu u rodiček, které ho dostávají k tlumení bolesti při porodu. Pethidin rychle prostupuje placentou, a proto již za 6 minut od aplikace se ustanoví rovnováha mezi fetální a mateřskou plazmatickou koncentrací. Plazmatická koncentrace u plodu dále stoupá a je vyšší než u matky již po 2 hodinách od aplikace. Maximální koncentrace v tkáních plodu je dosaženo teprve po 2–3 hodinách od aplikace. U novorozence činí biologický poločas pethidinu 23 hodiny, což je více než 7krát déle ve srovnání s dospělým. Nedostatečně vyvinutá glukuronidizace přispívá dále k tomu, že uplyne ještě 6 dní, než je pethidin vyloučen z organismu. Samozřejmě hlavní metabolit pethidinu norpethidin hraje také důležitou roli. Zatímco dochází k postupnému klesání jeho plazmatické koncentrace v mateřské krvi, u novorozence stoupá plazmatická hladina norpethidinu až do 8 hodin po porodu. Kardiopulmonální funkce novorozence a skóre dle Apgarové nejsou nízkými dávkami pethidinu významně změněny. Ale po podání tohoto analgetika v dávce 50 mg rodičce bylo pozorováno změněné neurofyziologické chování novorozence trvající až tři dny po porodu. Není vyloučeno, že změněné neurofyziologické chování novorozence se přes jemné ovlivnění emocí matky může negativně projevit na jeho bezprostředním dalším vývoji [5].
Mezi nežádoucí účinky pethidinu patří účinky společné s ostatními opioidy, jako je zácpa, nauzea nebo zvracení, kromě toho se však vyskytují anticholinergní účinky, např. sucho v dutině ústní. Relativně kontraindikováno je podávání pethidinu u pacientů s těžkými jaterními chorobami nebo s chorobami ledvin s historií křečí v anamnéze nebo u pacientů s epilepsií, dále pak u nemocných se zvětšenou prostatou nebo s retencí moče, u pacientů s hypertyreózou, astmatem nebo s Addisonovou nemocí. Podání pethidinu může vyvolat vážné komplikace. Při kombinaci s antidepresivy může nastat delirium, výrazná agitace, křeče a hypertermie. Byly popsány rovněž fatální komplikace. Je to pravděpodobně způsobeno zvýšením hladiny serotoninu v mozku. Byly popsány také interakce pethidinu se svalovými relaxancii, antidepresivy, benzodiazepiny a s alkoholem. Opakované podávání pethidinu může mít neurotoxické účinky.
Pethidin je nejčastěji aplikován intramuskulárně k potlačení pooperační bolesti. V kombinaci s midazolamem je podáván při nepříjemných diagnostických výkonech, např. při kolonoskopii, buď titračně i.v., nebo i.m. Intravenózní cesta však není doporučována pro vážné riziko uvolnění histaminu. Po perorální aplikaci má relativně vysokou biologickou dostupnost 50–60 %. Pethidin je indikován k léčbě silné akutní bolesti po těžkých úrazech, operacích a k léčbě chronické bolesti při maligních tumorech. Ve 20. století byl mnohými lékaři považován za lék volby pro dosažení analgezie, v roce 1983 ho předepisovalo při akutní bolesti 60 % lékařů a při chronické bolesti 22 % lékařů. Ve srovnání s morfinem je stále stejně oblíben při léčení bolestí spojených s biliárními spasmy nebo s renální kolikou pro své možné antispasmolytické účinky. V porodnictví je pethidin oblíben k tlumení bolesti v otevírací době. Je však třeba mít na paměti, že již jediná dávka pethidinu může ovlivnit plod a vylučování tohoto opioidu a jeho metabolitu norpethidinu může trvat až jeden týden. Je pozoruhodné, že aplikace pethidinu pokračuje již 70 let a mnozí lékaři používají pethidin přednostně jako silné analgetikum při akutních bolestech. I když je v některých zemích, jako např. v Austrálii, jeho podávání silně omezeno a vyhrazeno jen pro určité indikace, má dosud v Evropě velkou popularitu.
Práce vznikla za podpory grantu IGA MZČR NR 9369-3.
Seznam použité literatury
- [1] Wagner LE II, Eaton M, Sabnis SS, Gingrich KJ. Meperidine and lidocaine block of recombinant voltage-dependent Na+ channels: evidence that meperidine is a local anesthetic. Anesthesiology 1999; 91: 1481–1490.
- [2] Izenwasser S, Newman AH, Cox BM, Katz JL. The cocaine-like behavioral effects of meperidine are mediated by activity at the dopamine transporter. Eur J Pharm 1996; 297: 9–17.
- [3] Takada K, Clark DJ, Davies MF, et al. Meperidine exerts agonist activity at the a2B-adrenoceptor subtype. Anesthesiology 2002; 96: 1420–1426.
- [4] Walker DJ, Zacny JP. Subjective, psychomotor, and physiological effects of cumulative doses of opioid m agonists in healthy volunteers. J Pharmacol Exp Ther 1999; 289: 1454–1464.
- [5] Hess L, Mühlbachová E, Fischerová D, Pařízek A. Sedace a analgezie u porodu. In Pařízek A. a kol.: Porodnická analgezie a anestezie. Praha, Grada Publishing 2002; 223–229.