Postavení bariatrie v léčbě diabetu 2. typu
Článek rozebírá principy jednotlivých v současnosti běžně prováděných bariatrických operací (bandáž žaludku, sleeve gastrektomie, plikace žaludku, gastrický bypass a biliopankreatická diverze) a zabývá se jejich vlivem na dosažení remise diabetu 2. typu nebo na zlepšení jeho kompenzace. Je navržen jednoduchý algoritmus výběru vhodného typu zákroku založený na délce trvání diabetu a přítomnosti komplikací, s přihlédnutím k náročnosti operace, její reverzibilitě a očekávanému účinku.
Úvod
Od počátku tohoto tisíciletí, paralelně s rozvojem farmakologických možností terapie diabetu mellitu 2. typu (DM2T), se také díky zvyšující se popularitě bariatrických výkonů rozvíjely chirurgické možnosti ovlivnění DM2T. Tyto výkony zlepšují nejen kompenzaci diabetu, ale mohou, pokud jsou správně indikovány a načasovány, dle mezinárodních doporučení za splnění základní podmínky BMI vyššího než 35, vést k vymizení nejen hyperglykemie, ale také inzulinové rezistence (IR) jako jednoho ze základních kamenů DM2T. Meta-analýzy sérií případů a kontrolovaných studií potvrzují, že všechny metody bariatrické chirurgie vedou k redukci nadváhy minimálně ze 60 % (excess weight loss, EWL) a k remisi již rozvinutého diabetu ve více než 75 % případů [1].
Díky tomuto specifickému působení se dnes proto v diabetologických indikacích mluví o metabolické chirurgii a postupně se odhalují mechanismy, jakými vedou změny v toku nutrientů trávicím traktem k ovlivnění patofyziologie diabetu. Je však třeba poznamenat, že většina poznatků je stále na úrovni hypotéz, jen částečně ověřených na malých souborech, a kvalitní randomizovaná prospektivní data jsou vzácná. Také se teprve nedávno začaly objevovat prospektivní komparativní chirurgické studie porovnávající efekt jednotlivých typů zákroků. Posledním úskalím při hodnocení vlivu bariatrie na diabetes je nejednotnost operační techniky, jakási chirurgická umělecká tvořivost, projevující se nejvíce u gastrického bypassu, a nejednotnost sledovaných parametrů, podle kterých se hodnotí úspěšnost výkonu – např. chirurgické studie v naprosté většině případů uvádějí jako parametr redukce hmotnosti pro internisty téměř neznámou procentuál-ní redukci nadváhy (excess weight loss, EWL). V tomto článku je používán původní anglický termín, aby nedocházelo k záměně s naším vnímáním nadváhy jako dia-gnózy.
I přes tyto výhrady se ale pojďme podívat, jaké jsou typy v současnosti prová-děných metabolických operací, co víme o jejich účinku na glukózovou homeostázu a jaké postavení by metabolická chirurgie měla zaujímat v armamentariu diabetologa.
Rozdělení výkonů
Možnosti ovlivnění obezity a diabetu chirurgickou cestou se dají rozdělit na dvě skupiny: výkony restrikční, založené převážně na omezení objemu přijímané potravy, a výkony malabsorpční, spočívající ve vyloučení části trávicího traktu z činnosti, vedoucí k různému stupni nedokonalosti vstřebávání živin.
Restrikční výkony, u nás představující cca 90 % všech prováděných výkonů, zahrnují bandáž žaludku (laparoscopic adjustable gastric band, LAGB), laparoskopickou gastroplikaci (laparoscopic gastric curvature plication, LGCP) a tubulizaci žaludku (rukávová gastrektomie, sleeve gastrectomy, SG). Většinou jako terapie druhé linie jsou pak k dispozici Roux-en-Y gastrický bypass (RYGB), který je přechodem mezi restrikčním a malabsorpčním výkonem, a biliopankreatická diverze (BPD) jako čistý malabsorpční výkon.
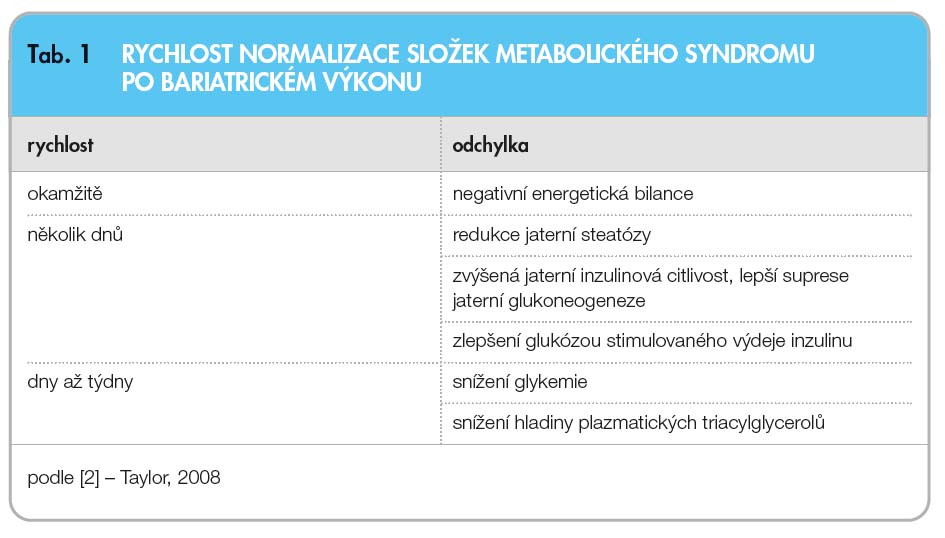 Z klinické zkušenosti se ukázalo, že zákroky na trávicím traktu ovlivňují IR a kompenzaci diabetu již během několika dnů až týdnů – ještě předtím, než dojde k signifikantním úbytkům hmotnosti. Taylor [2] postuluje sekvenci normalizace jednotlivých odchylek tvořících metabolický syndrom po bariatrickém zákroku (tab. 1). Gumbs a spoluautoři [3] shrnuli dostupné poznatky o účincích bariatrie do 2 hypotéz:
Z klinické zkušenosti se ukázalo, že zákroky na trávicím traktu ovlivňují IR a kompenzaci diabetu již během několika dnů až týdnů – ještě předtím, než dojde k signifikantním úbytkům hmotnosti. Taylor [2] postuluje sekvenci normalizace jednotlivých odchylek tvořících metabolický syndrom po bariatrickém zákroku (tab. 1). Gumbs a spoluautoři [3] shrnuli dostupné poznatky o účincích bariatrie do 2 hypotéz:
- Akutní kalorická restrikce téměř okamžitě, po odeznění operačního stresu, zlepšuje IR a glukózový metabolismus cestou modifikace hladin hormonů enteroinzulární osy, především GLP-1 (gluca-gon-like peptide-1), GIP (glukózo-dependentní inzulinotropní polypeptid) a ghrelinu. Toto je nejvíce patrné po gastrickém bypassu a biliopankreatické diverzi, částečně také po sleeve gastrektomii.
- Dlouhodobé zlepšení IR a glukózového metabolismu je důsledkem redukce množství tukové tkáně, hlavně viscerální a hepatální, jež se projeví ve změnách hladin adipokinů, jako je leptin, rezistin, adiponektin a pravděpodobně další. Tímto způsobem účinkují převážně restrikční operace typu bandáže, plikace a možná i sleeve gastrektomie.
Intenzivně se v chirurgických kruzích diskutuje relativní význam zásahu do funkce proximálního a distálního tenkého střeva (tzv. foregut a hindgut hypotéza) [4].
Restrikční operace
Gastrická bandáž
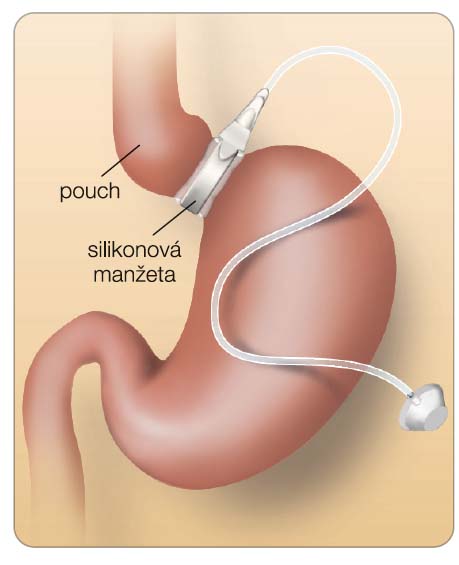 Gastrická bandáž (LAGB) spočívá v umístění silikonové manžety na žaludek, která vede k vytvoření tzv. pouche (minižaludku) s objemem cca 20–30 ml (obr. 1). Naplnění žaludku potravou o objemu cca 100–150 ml umožňuje dosáhnout dobrého pocitu sytosti trvajícího cca 3 hodiny, během kterých je pouch postupně vyprazdňován. Mediátorem pocitu sytosti je pravděpodobně trvalý tlak na vlákna n. vagus inervující fundus (který se po najedení ještě zvětšuje) vysílající signály do centra sytosti. Svou roli hraje také zpomalení evakuace žaludku. Při zachování odstupů mezi jídly a dodržení doporučeného množství je tak pacient schopen za den přijmout pouze cca 750 ml potravy a necítit přitom hlad. Pokud je strava dobře vybrána, dochází nejdříve k razantnímu a později k pozvolnému úbytku hmotnosti, který se celkově pohybuje od 20 % vstupní hmotnosti [5], nebo od 40 % redukce EWL [6].
Gastrická bandáž (LAGB) spočívá v umístění silikonové manžety na žaludek, která vede k vytvoření tzv. pouche (minižaludku) s objemem cca 20–30 ml (obr. 1). Naplnění žaludku potravou o objemu cca 100–150 ml umožňuje dosáhnout dobrého pocitu sytosti trvajícího cca 3 hodiny, během kterých je pouch postupně vyprazdňován. Mediátorem pocitu sytosti je pravděpodobně trvalý tlak na vlákna n. vagus inervující fundus (který se po najedení ještě zvětšuje) vysílající signály do centra sytosti. Svou roli hraje také zpomalení evakuace žaludku. Při zachování odstupů mezi jídly a dodržení doporučeného množství je tak pacient schopen za den přijmout pouze cca 750 ml potravy a necítit přitom hlad. Pokud je strava dobře vybrána, dochází nejdříve k razantnímu a později k pozvolnému úbytku hmotnosti, který se celkově pohybuje od 20 % vstupní hmotnosti [5], nebo od 40 % redukce EWL [6].
Implantovaná bandáž je adjustabilní, tj. na jejím vnitřním průměru je integrovaný balónek, který je spojen s portem vyvedeným do podkoží, většinou podél levého žeberního oblouku. Napíchnutím portu je možné přidávat či ubírat tekutinu v balónku, regulovat tím vnitřní průměr bandáže a tím rychlost, s jakou se horní část žaludku vyprazdňuje. Nespornou výhodou bandáže je její reverzibilita – pokud je bandáž odstraněna, dojde k restituci stavu GIT ad integrum. Ztrácí se tím však funkce a prakticky vždy dochází k postupnému návratu k původní hmotnosti a k návratu k progresi prediabetu.
Efekt LAGB na rozvoj a kompenzaci DM2T je nejlépe vyjádřen u obézního pa-cienta ještě před manifestací diabetu nebo velmi časně na začátku jeho diabetické „kariéry”, s vyjádřenou IR a s pouze relativním nedostatkem inzulinu. Redukce tu-kové tkáně a zlepšení v hladinách adipoki-nů a v poměrech mezi nimi umožní zlepšit působení inzulinu a přispěje k vymizení známek rezistence, jak bylo dokumentováno v četných studiích [7–9]. Kromě souhrnu observačních a retrospektivních studií [10] jsou dnes k dispozici také studie prospektivní [11] a také randomizovaná kontrolovaná studie stejných autorů [5]. První studie [11] demonstrovala 1 rok po implantaci LAGB u 50 po sobě jdoucích pacientů s DM2T remisi diabetu v 64 % případů, zásadní vylepšení kontroly glykemie u dalších 26 % a mírné vylepšení kontroly diabetu u zbylých 10 % pacientů. Zlepšení IR bylo dáno především rozsahem redukce hmotnosti, zlepšení funkce b-buněk pak bylo nepřímo úměrné délce trvání poruchy glukózové tolerance, např. 95 % všech pacientů s porušenou glykemií nalačno dosáhlo setrvalé normoglykemie a během dalších 4 let sledování nedošlo u nikoho z této skupiny k progresi do DM2T.
Delší doba nutná ke zlepšení parametrů IR po LAGB je také potvrzena dalšími studiemi, např. IR měřená pomocí HOMA-IR (homeostasis model assessment-insulin resistance) se neměnila 3 měsíce po operaci, ale zlepšila se až 12 měsíců poté a pozitivně korelovala s redukcí nitrobřišní a jaterní tukové tkáně měřené magnetickou rezonancí [12].
Laparoskopická tubulizace žaludku
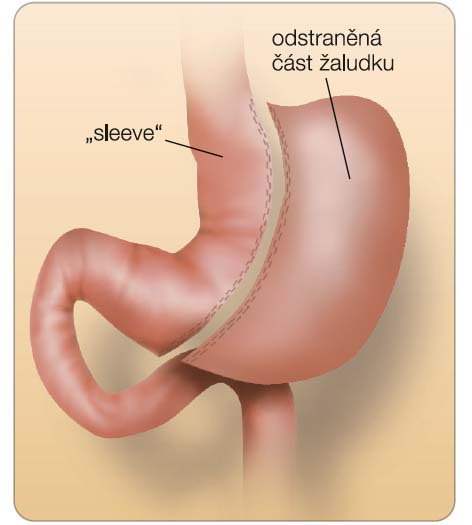 Princip operace spočívá v uvolnění velkého zakřivení žaludku a po kalibraci na bužii, nejčastěji rozměru 32–35 F v sutuře žaludeční stěny, v odstranění velké části jinak zdravé žaludeční tkáně (obr. 2). Je zachováno cca 5 cm pyloru. Původně byla tato operace myšlena jako předstupeň dosažení definitivního výsledku formou gastrického bypassu nebo BPD u super-obézních lidí (BMI > 50).
Princip operace spočívá v uvolnění velkého zakřivení žaludku a po kalibraci na bužii, nejčastěji rozměru 32–35 F v sutuře žaludeční stěny, v odstranění velké části jinak zdravé žaludeční tkáně (obr. 2). Je zachováno cca 5 cm pyloru. Původně byla tato operace myšlena jako předstupeň dosažení definitivního výsledku formou gastrického bypassu nebo BPD u super-obézních lidí (BMI > 50).
Dostatečný efekt sleeve gastrektomie jako samostatné operace byl zhodnocen před 3 lety [13] na základě metaanalýzy publikovaných výsledků u 14 776 pacientů:
• 86,3 % bylo zamýšleno jako samostatná operace;
• EWL představovala za 1 rok v průměru 60,7 %, za 2 roky 64,7 %, za 3 roky 61,7 %, za 4 roky 64,6 % a za 5 let 48,5 %.
Efekt sleeve gastrektomie na IR či prediabetes se také blíží spíše efektu kombinovaných výkonů, jako je gastrický bypass, než účinku bandáže žaludku [14]. Vidal [15] porovnával v prospektivní studii 39 pacientů s LSG s 52 pacienty s RYGB a došel ke stejnému výsledku ve vymizení diabetu jeden rok po zákroku – v 85 % případů u obou typů operace – jako Silecchia [16], který popisuje vymizení diabetu za jeden rok po výkonu u 69,2 % a zlepšení kompenzace u dalších 15,4 %.
Retrospektivní Rosenthalova studie [17] ukazuje dosažení remise u 27 % pacientů již za 2 měsíce po operaci a u 63 % po 6 měsících od operace. Průměrná hladina HbA1c dosáhla normálních hodnot za rok po operaci. Hodnota BMI klesla během 6 měsíců po operaci ze 46,1 ± 10,8 kg/m2 na 35,8 ± 5,1 kg/m2. Stejně jako je tomu u LAGB, pacienti s kratším trváním diabetu a větší hmotnostní redukcí dosáhli remise diabetu mnohem častěji.
Je nutné upozornit také na technická úskalí sleeve gastrektomie; ta spočívají především v odstranění dvou ze tří antire-fluxních mechanismů (žaludeční bubliny a Hissova úhlu) [13], a proto je nutná velká opatrnost v zachování intaktního jícnu. Také je potřeba zachovat dostatečnou část pyloru, aby bylo umožněno vstřebávání vitaminu B12 díky vnitřnímu faktoru.
Stále se však pátrá po vysvětlení vynikajících výsledků sleeve gastrektomie. Velké naděje se vkládaly do ghrelinu, orexigenního peptidu tvořeného v žaludku. Resekce velké části žaludku měla vést ke snížení hladin ghrelinu, což např. výzkumy skupiny prof. Haluzíka [18] u pacientů po LSG potvrdily. Otázkou zůstává, jak vysvětlit již sníženou hladinu ghrelinu u obézních před chirurgickým zákrokem a v odstupu více let od operace tendenci ghrelinu opět narůstat, a to při zachování dobrého efektu operace na hmotnost a diabetes.
Laparoskopická gastroplikace
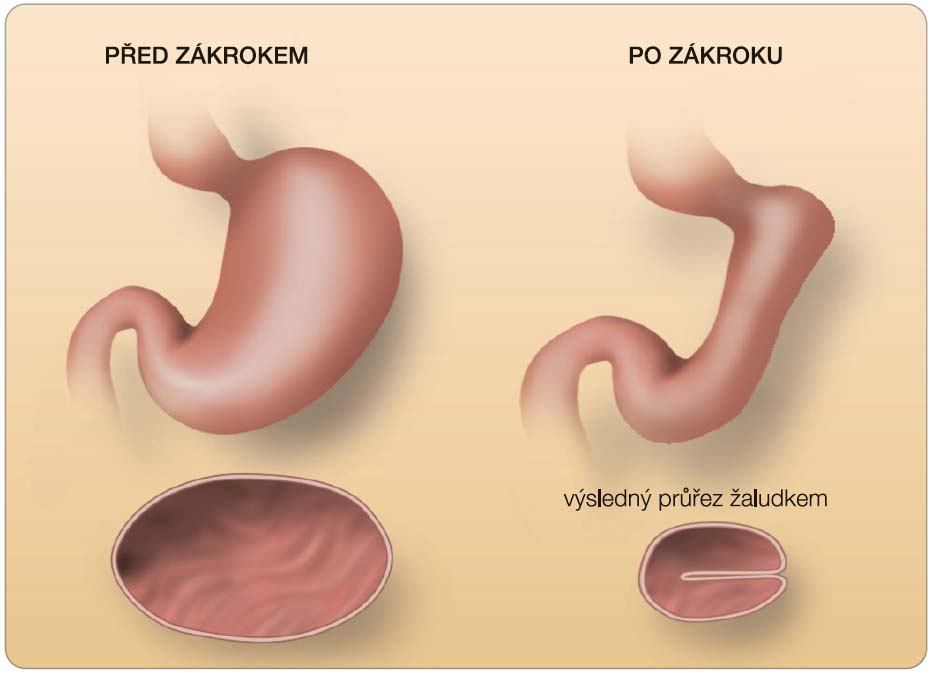 Tato operace je nejnovějším restrikčním výkonem, systematicky prováděným teprve od října 2009 na 3 pracovištích v celém světě: v Clevelandu v USA, v Sao Paulu v Brazílii a v Praze na pracovišti prof. Frieda. Operace byla vyvinuta jako levnější a jednodušší alternativa k LAGB, jelikož nepo-užívá žádný implantovaný materiál. Zároveň má vlastnosti sleeve gastrektomie, ale neodstraňuje se část normálního a zdravého orgánu – je tedy, na rozdíl od LSG, potenciálně vratným výkonem. Operace spočívá v invaginaci žaludku za gastroskopické asistence a v prošití serózy žaludku pokračujícím stehem v jedné nebo ve dvou vrstvách (obr. 3). Reálná kapacita vzniklého žaludku je 80–100 ml v klidovém stavu.
Tato operace je nejnovějším restrikčním výkonem, systematicky prováděným teprve od října 2009 na 3 pracovištích v celém světě: v Clevelandu v USA, v Sao Paulu v Brazílii a v Praze na pracovišti prof. Frieda. Operace byla vyvinuta jako levnější a jednodušší alternativa k LAGB, jelikož nepo-užívá žádný implantovaný materiál. Zároveň má vlastnosti sleeve gastrektomie, ale neodstraňuje se část normálního a zdravého orgánu – je tedy, na rozdíl od LSG, potenciálně vratným výkonem. Operace spočívá v invaginaci žaludku za gastroskopické asistence a v prošití serózy žaludku pokračujícím stehem v jedné nebo ve dvou vrstvách (obr. 3). Reálná kapacita vzniklého žaludku je 80–100 ml v klidovém stavu.
Iniciální publikované výsledky s plikací žaludku jsou více než povzbudivé. Ramos [19] uvádí výsledky 18měsíčního sledování svých prozatím operovaných pacientů (více než 100): průměrnou operační dobu 50 minut (40–100 minut) – tj. mnohem méně než u sleeve gastrektomie, pacienti opouštějí nemocnici po průměrně 36 hodinách (rozsah 24–96 hod.). Nebyly přítomny žádné intraoperační komplikace a EWL dosahovala minimálně 20 % během jednoho měsíce od operace. Za 18 měsíců po operaci byla průměrná EWL 62 % (45–77 %) u 9 pacientů s takto dlouhou dobou sledování.
Technicky velmi podobnou operaci prováděl Talebpour [20] v Íránu mezi roky 2005–2007. Výsledky sledování více než stovky pacientů (průměrný BMI 47) ukazují EWL dosahující 60 % za 24 měsíců.
Roux-en-Y gastrický bypass
Gastrický bypass byl v podstatě prvním bariatrickým výkonem, provádí se od roku 1966. Je to dnes celosvětově nejčastější bariatrická operace, ale je to také zákrok, kde se nejčastěji projevuje lidová tvořivost operujících chirurgů, takže literární údaje o účincích těchto operací jsou často velmi odlišné – porovnávají se totiž často velmi odlišné operace. Gastrický bypass je přechodem mezi restrikčními a malabsorp-čními operacemi: není ovlivněno vstřebávání makronutrientů, ale hlavním účinkem se zdá být komplexní ovlivnění hormonálních regulací v kombinaci s určitým stupněm restrikce příjmu potravy.
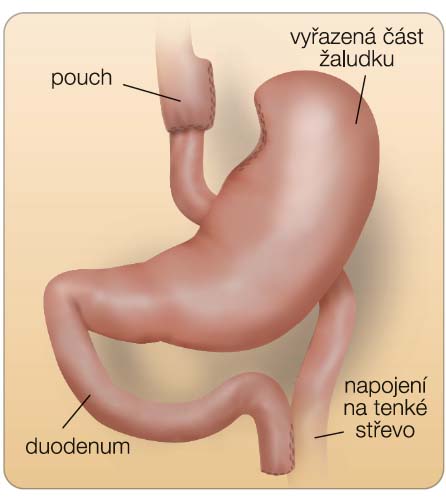 Operace spočívá ve vytvoření malého žaludečního pouche, velikostí podobného jako u nenaplněné bandáže, který je plně oddělen od zbývajícího žaludku. Zbývající tělo žaludku zůstává spojeno s biliopankreatickou kličkou o délce 50–100 cm (dle chirurga); ve zvolené délce je jejunum přerušeno a aborální část je použita jako alimentární klička k vytvoření „side-to-end“ gastro-jejuno anastomózy. Spojení alimentární a biliopankreatické kličky je prováděno po 100–150 cm délky alimentární kličky, opět dle zkušeností operatéra a s přihlédnutím k BMI; doporučuje se obě kličky prodlužovat se zvyšujícím se BMI (obr. 4). Diabetičtí pacienti podstupující RYGB hubnou signifikantně méně než pa-cienti bez diabetu, také ostatní parametry metabolického syndromu se zlepšují méně často než u nediabetiků. Carbonell [21] popisuje 655 pacientů s DM2T (věk 45,8 ± 10,4 let) v porovnání s nediabetickou populací (n = 2538) se stejným vstupním BMI (tab. 2). Remise diabetu bylo v případě nemocných kontrolovaných předoperačně dietou dosaženo u 89,8 %, u pacientů léčených předoperačně perorálními antidiabetiky u 82,7 % a u diabetiků vyžadujících předoperačně k dosažení dobré kontroly inzulinoterapii v 53,3 % případů.
Operace spočívá ve vytvoření malého žaludečního pouche, velikostí podobného jako u nenaplněné bandáže, který je plně oddělen od zbývajícího žaludku. Zbývající tělo žaludku zůstává spojeno s biliopankreatickou kličkou o délce 50–100 cm (dle chirurga); ve zvolené délce je jejunum přerušeno a aborální část je použita jako alimentární klička k vytvoření „side-to-end“ gastro-jejuno anastomózy. Spojení alimentární a biliopankreatické kličky je prováděno po 100–150 cm délky alimentární kličky, opět dle zkušeností operatéra a s přihlédnutím k BMI; doporučuje se obě kličky prodlužovat se zvyšujícím se BMI (obr. 4). Diabetičtí pacienti podstupující RYGB hubnou signifikantně méně než pa-cienti bez diabetu, také ostatní parametry metabolického syndromu se zlepšují méně často než u nediabetiků. Carbonell [21] popisuje 655 pacientů s DM2T (věk 45,8 ± 10,4 let) v porovnání s nediabetickou populací (n = 2538) se stejným vstupním BMI (tab. 2). Remise diabetu bylo v případě nemocných kontrolovaných předoperačně dietou dosaženo u 89,8 %, u pacientů léčených předoperačně perorálními antidiabetiky u 82,7 % a u diabetiků vyžadujících předoperačně k dosažení dobré kontroly inzulinoterapii v 53,3 % případů.
Účinky gastrického bypassu na kompenzaci diabetu jsou téměř okamžité, ukazující na disociaci role hormonálních regulací a hmotnostní redukce. Dobře dokumentován je například vliv na GLP-1, jehož tvorba je v odpovědi na příjem potravy u diabetiků snížena, po RYGB se díky přítomnosti nenatrávené potravy v distálním ileu z vyšuje a dosahuje velmi rychle normálních hodnot jako u zdravé populace. RYGB vede k rychlé stimulaci tvorby GLP-1 se všemi pozitivními důsledky, které známe při terapii analogy GLP-1 nebo inhibitory DPP-4 [22]. RYGB tedy v časné fázi po operaci vede ke zvýšení hladin inzulinu a ke zlepšení parametrů glukózového metabolismu [23]. Jako jediný mechanismus remise diabetu by však zvýšení inzulinemie nestačilo a musí se kombinovat např. se zlepšením senzitivity díky kalorické restrikci.
vyšuje a dosahuje velmi rychle normálních hodnot jako u zdravé populace. RYGB vede k rychlé stimulaci tvorby GLP-1 se všemi pozitivními důsledky, které známe při terapii analogy GLP-1 nebo inhibitory DPP-4 [22]. RYGB tedy v časné fázi po operaci vede ke zvýšení hladin inzulinu a ke zlepšení parametrů glukózového metabolismu [23]. Jako jediný mechanismus remise diabetu by však zvýšení inzulinemie nestačilo a musí se kombinovat např. se zlepšením senzitivity díky kalorické restrikci.
Biliopankreatická diverze
Biliopankreatická diverze (BPD) je jednoznačně nejagresivnějším výkonem metabolické chirurgie. Vede k zásadnímu stupni malabsorpce všech makronutrientů a je indikována pouze u pacientů, kteří jsou schopni dlouhodobé spolupráce v oblasti kontrol nutričního stavu a doplňování mikroprvků a vitaminů. Na druhou stranu je to výkon, který v téměř 100 % případů vede k dlouhodobé remisi diabetu, podle nejdelších studií až v délce 10 a více let [24]. Příčinou je pravděpodobně multifaktoriální působení na inzulinovou senzitivitu – vyloučením kontaktu potravy s duodenem a proximálním jejunem, jako je tomu u RYGB, zásadní malabsorpce lipidů a prokázané nebo spekulované modifikace hormonálních hladin (GLP-1, ghrelin, jiné působky). Jednoznačně je ale prokázáno, že zlepšení až vymizení IR je po této operaci nejvýraznější. Princip operace je podobný žaludečnímu bypassu, s větším žaludečním pouchem a s odlišnými délkami kliček.
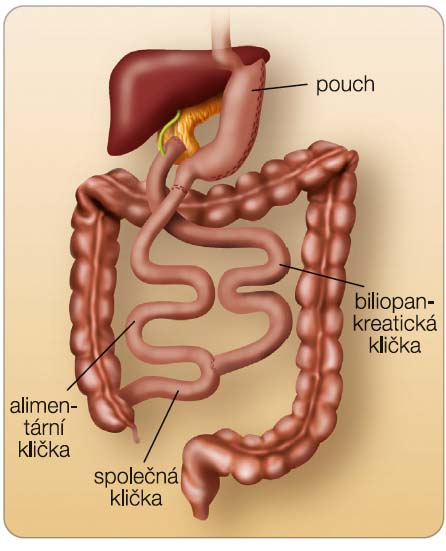 Aby byl výkon čistě malabsorpční, spočívá v distální gastrektomii, se zachovaným objemem žaludku 200–500 ml. Ponechává se dlouhá biliopankreatická klička – délka společné kličky od ileocékální chlopně je cca 50–100 cm; délka alimentární kličky je přibližně 200 cm (obr. 5).
Aby byl výkon čistě malabsorpční, spočívá v distální gastrektomii, se zachovaným objemem žaludku 200–500 ml. Ponechává se dlouhá biliopankreatická klička – délka společné kličky od ileocékální chlopně je cca 50–100 cm; délka alimentární kličky je přibližně 200 cm (obr. 5).
Zmenšení žaludku je nedostatečné k to-mu, aby vedlo k významné restrikci objemu potravy, a provádí se spíše k redukci incidence vředů v gastroenteroanastomóze a prekancerózních lézí ve stejné lokalizaci [25]. Výsledná malabsorpce je výrazná. Ve studii 15 pacientů 2–3 roky po BPD v době stabilizované hmotnosti se absorpce přijaté energie (průměr 3070 kcal denně, rozmezí 1840–4060 kcal) pohybovala v rozmezí 32–71 %. Se stupněm malabsorpce po BPD souvisí také nutnost substituce hlavně mikronutrienty – železem v kombinaci s folátem a vitaminem B12, kalciem spolu s vitaminem D – a zdá se i jinými vitaminy a minerály dle aktuálních hodnot, a to celoživotně.
Hlavním efektem BPD je právě multifaktoriální modifikace IR. Její dramatické snížení do normálních až podnormálních hodnot bylo popsáno v prospektivní studii u 107 pacientů (z toho 35 diabetiků) sledovaných před operací a 2 roky po ní [26], zatímco hmotnost stále zůstávala v pásmu 1. stupně obezity (BMI 30–35 kg/m2). Návrat k normální inzulinové senzitivitě v hyperinzulinemickém, euglykemickém clampu byl v jiné studii popsán již 10. p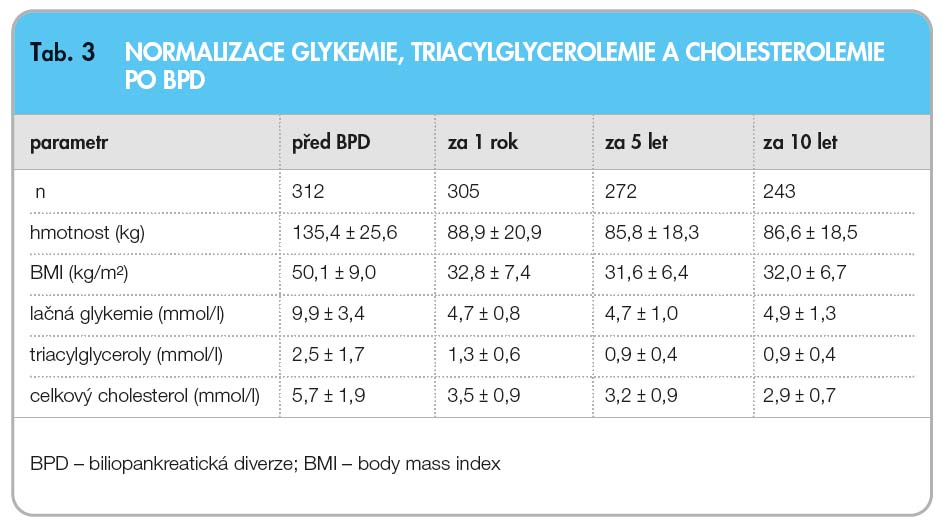 o-operační den [27]. Dále se ukazuje, že malabsorpce lipidů vede k depleci orgánových a intramyocelulárních tukových zásob. Tím se opět zvyšuje účinek inzulinu na celotělovou utilizaci glukózy, intrace-lulární signalizaci po navázání inzulinu na receptor a je ovlivněna hladina cirkulujícího leptinu. Snížení celotělové IR tedy vede k rychlému snížení inzulinemie, na rozdíl od RYGB [23]. Snížené hladiny lipidů v oběhu budou také snižovat lipotoxicitu zhoršující funkci b-buněk [28] (tab. 3).
o-operační den [27]. Dále se ukazuje, že malabsorpce lipidů vede k depleci orgánových a intramyocelulárních tukových zásob. Tím se opět zvyšuje účinek inzulinu na celotělovou utilizaci glukózy, intrace-lulární signalizaci po navázání inzulinu na receptor a je ovlivněna hladina cirkulujícího leptinu. Snížení celotělové IR tedy vede k rychlému snížení inzulinemie, na rozdíl od RYGB [23]. Snížené hladiny lipidů v oběhu budou také snižovat lipotoxicitu zhoršující funkci b-buněk [28] (tab. 3).
Diskuse
Dosažení remise diabetu, nebo alespoň dramatického zlepšení jeho kompenzace po bariatrickém/metabolickém zákroku je do velké míry závislé na spolupráci pacienta po operaci, a proto je nutné, aby pacienti byli pod zkušeným odborným dohledem. Všichni potenciální zájemci o chirurgické řešení diabetu by proto měli být indikováni specializovanými bariatrickými centry, kde je k dispozici nejen bariatrický chirurg s dostatečnou praxí, ale také specializovaný internista, diabetolog nebo endokrinolog, a také zkušený psycholog zabývající se touto problematikou. Jedině tak bude zaručeno, že jsou vyloučeny všechny kontraindikace a pacient bude podrobně seznámen s režimem po operaci, a bude tedy schopen informovaně se zákrokem souhlasit.
Pokud je tato podmínka splněna, pak se z dostupných dat zdá, že metabolická chirurgie by měla být aktivně nabízena všem obézním diabetikům jako jedna z terapeutických možností ke zvážení, s respektováním preferencí pacienta. Potenciál dosažení remise diabetu se zvyšuje s rostoucí agresivitou zákroku, a tak by měly také být jednotlivé zákroky nabízeny.
Bandáž žaludku je v rukou zkušeného bariatrického chirurga operací nejbezpečnější, a to nejen díky samotné technice operace, ale také díky mnohaletým zkušenostem s potenciálními komplikacemi a jejich řešením. Z hlediska schopnosti dosáhnout remise diabetu je ovšem účinná nejméně. Přesto však literární údaje dokumentují dosažení remise ve 40–80 % případů, s dalšími cca 20 % dosažení zlepšené kompenzace při stávající nebo redukované farmakologické léčbě. Procento dosažení remise bylo vždy vyšší s větší redukcí hmotnosti a s kratší dobou trvání diabetu. Gastrická bandáž je tedy vhodná pro obézní pacienty s vyjádřenou IR, porušenou glykemií nalačno, porušenou glukózovou tolerancí nebo v prvních několika málo letech od stanovení diagnózy DM2T [5, 6, 29–31].
Plikace žaludku jako naopak nejnovější typ operace s pravděpodobně velmi podobným účinkem na DM2T jako LAGB si zatím své místo v léčbě pacientů s diabetem hledá. Jednou z jejích jasných výhod je absence cizího materiálu v těle, což může být pro některé pacienty důležité. Nevýhodou oproti LAGB je nemožnost adjustace a absence dlouhodobých dat.
Sleeve gastrektomie je ve zlepšení kompenzace diabetu velmi pravděpodobně účinnější než předchozí restrikční výkony – zároveň ale také s větší technickou náročností operace, která navíc vede k odstranění části úplně zdravého orgánu, bez možnosti náhrady. Podle některých studií se zdá být stejně účinná na dosažení remise diabetu měřené hyper-inzulinemickým clampem jako gastrický bypass – za 36 měsíců sledování 80,9 % vs. 81,2 % léčených [14].
Roux-en-Y gastrický bypass je celosvětově přijímán jako vysoce účinná chirurgická léčba DM2T. K dispozici je nejvíce studií dokumentujících dosažení remise diabetu v 75–90 %, bez zásadní závislosti na délce trvání diabetu či na dosažené redukci hmotnosti [9, 14, 30, 31]. Na druhou stranu je třeba si uvědomit, že se již jedná o zákrok velmi agresivní, s mnohočetnými suturami trávicího traktu, nevratný a s řádově vyšší frekvencí perioperačních, časných pooperačních a dlouhodobých komplikací. Měl by být tedy rezervován pro diabetiky s pokročilejším onemocněním, kde je riziko operace alespoň vyváženo potenciálním přínosem v podobě kompenzace diabetu a ostatních metabolických odchylek, čehož nelze jinými prostředky dosáhnout.
Totéž platí i pro BPD. I když se jedná o operaci ve světě méně častou (z velké části pro její původ v Itálii a rivalitu mezi americkými a evropskými chirurgy), v dosažení opravdu dlouhodobé remise diabetu je ještě účinnější než bypassové operace – úspěchu bývá dosaženo až v 95 % případů [24]. Technická náročnost této operace není větší než u RYGB, možná díky zachování větší porce žaludku je gastroenteroanastomóza dokonce jednodušší, dochází však k rozvoji malabsorpce mikro- a makronutrientů, a je proto nezbytná doživotní pravidelná kontrola jejich hladin a substituce mikroprvky a vitaminy. Pro mnoho pacientů je to však jediná cesta, jak dosáhnout dramaticky lepší kompenzace diabetu a odvrátit tak rozvoj invalidizujících mikro- a makrovaskulárních komplikací. Posledních několik let se dokonce skupina profesora Scopinara intenzivně věnuje využití BPD u diabetiků, kteří nesplňují základní indikační kritérium bariatric-ké operace, tj. BMI > 35, s velmi zajímavými výsledky [33, 34].
Závěr
Metabolická chirurgie si postupně získává své místo nejen v léčbě obezity, ale i jejích komplikací, především DM2T. Je potřeba pohlížet na její postupy ne jako na soupeře farmakologické terapie, ale jako na vhodné doplnění léčby u pacientů nedosahujících kritéria dostatečné kompenzace farmakologickými a režimovými opatřeními. V začátcích onemocnění diabetem volíme restrikční operace s malým operačním rizikem, potenciálně reverzibilní a v podstatě fyziologicky fungující zákroky s představou dosažení remise diabetu na mnoho let. U pokročilejších stadií diabetu pak musíme přistoupit k agresivnějším zákrokům s větším rizikem operace, ale s vědomím, že žádným jiným zákrokem nemůžeme dát pacientovi tak dobrou šanci na dosažení výborné kompenzace. Zároveň je potřeba si uvědomit, že žádná operace nebude mít očekávaný úspěch bez alespoň minimální spolupráce pacienta a bez dostatečné erudice ošetřujícího lékaře.
Seznam použité literatury
- [1] Levy P, Fried M, Santini F, Finer N. The comparative effects of bariatric surgery on weight and type 2 diabetes. Obes Surg 2007; 17: 1248–1256.
- [2] Taylor R. Pathogenesis of Type 2 diabetes: tracing the reverse route from cure to cause. Diabetologia 2008; 51: 1781–1789.
- [3] Gumbs AA, Modlin IM, Ballantyne GH. Changes in insulin resistance following bariatric surgery: role of caloric restriction and weight loss. Obes Surg 2005; 15: 462–473.
- [4] Mason EE. The mechanism of surgical treatment of type 2 diabetes. Obes Surg 2005; 15: 459–461.
- [5] Dixon JB, O’Brien PE, Playfair J, et al. Adjustable gastric banding and conventional therapy for type 2 diabetes. JAMA 2008; 299: 316–323.
- [6] Brancatisano A, Wahlroos S, Metthews S, Brancatisano R. Gastric banding for the treatment of type 2 diabetes mellitus in morbidly obese. Surg Obes Relat Dis 2008; 4: 423–429.
- [7] Trakhtenbroit MA, Leichman JG, Algahim MF, et al. Body weight, insulin resistance, and serum adipokine levels 2 years after 2 types of bariatric surgery. Am J Med 2009; 122: 435–442.
- [8] Ballantyne GH, Gumbs A, Modlin IM. Changes in insulin resistance following bariatric surgery and the adipoinsular axis: role of the adipocytokines, leptin, adiponectin, and resistin. Obes Surg 2005; 15: 692–699.
- [9] Angrisani L, Lorenzo M, Borrelli V. Laparoscopic adjustable gastric banding versus Roux-en-Y bypass: 5-year results of a prospective randomized trial. Surg Obes Relat Dis 2007; 3: 127–132.
- [10] Maggard MA, Shugarman LR, Suttorp M, et al. Meta-analysis: surgical treatment of obesity. Ann Intern Med 2005; 142: 547–559.
- [11] Dixon JB, O’Brien PE. Health outcomes of severely obese type 2 diabetic subjects 1 year after laparoscopic gastric banding. Diabetes Care 2002; 25: 358–363.
- [12] Heath ML, Kow L, Slavotinek JP, et al. Abdominal adiposity and liver fat content 3 and 12 month after gastric banding surgery. Metabolism 2009; 58: 753–758.
- [13] Gagner M, Deitel M, Kalberer TL, et al. The Second International Consensus Summit for Sleeve Gastrectomy, March 19–21, 2009. Surg Obes Relat Dis 2009; 5: 476–485.
- [14] Abbatini F, Rizzello M, Casella G, et al. Long-term effects of laparoscopic sleeve gastrectomy, gastric bypass and adjustable gastric banding on type 2 diabetes. Surg Endosc 2010; 24: 1005–1010.
- [15] Vidal J, Ibarzabal A, Romero F, et al. Type 2 diabetes mellitus and the metabolic syndrome following sleeve gastrectomy in severely obese subjects. Obes Surg 2008; 18: 1077–1082.
- [16] Silecchia G, Boru C, Pecchia A, et al. Effectiveness of laparoscopic sleeve gastrectomy (first stage of biliopancreatic diversion with duodenal switch) on co-morbidities in super-obese high-risk patients. Obes Surg 2006; 16 : 1138–1144.
- [17] Rosenthal R, Li X, Samuel S, et al. Effect of slee-ve gastrectomy on patients with diabetes mellitus. Surg Obes Relat Dis 2009; 5: 429–434.
- [18] Dostálová I, Haluzík M. The role of ghrelin in the regulation of food intake in patients with obesity and anorexia nervosa. Physiol Res 2009; 58: 159–170.
- [19] Ramos A, Galvao NM, Galvao M, et al. Laparoscopic greater curvature plication: initial results of an alternative restrictive bariatric procedure. Obes Surg 2010; 20: 913–918.
- [20] Talebpour M, Amoli BS. Laparoscopic total gastric vertical plication in morbid obesity. Laparoendosc Adv Surg Tech A 2007; 17: 793–798.
- [21] Carbonell AM, Wolfe LG, Meador JG, et al. Does diabetes affect weight loss after gastric bypass? Surg Obes Relat Dis 2008; 4: 441–444.
- [22] Patriti, A, Facchiano, E, Sanna A, et al. The enteroinsular axis and the recovery from type 2 diabetes after bariatric surgery. Obes Surg 2004; 14: 840–848.
- [23] Mingrone G, Castagneto-Gisey L. Mechanisms of early improvement/resolution of type 2 diabetes after bariatric surgery. Diabetes Metab 2009; 35: 518–523.
- [24] Scopinaro N, Marinari GM, Camerini GB, et al. Specific effects of biliopancreatic diversion on the major components of metabolic syndrome: a long-term follow-up study. Diabetes Care 2005; 28: 2406–2411.
- [25] Scopinaro N, Adami GF, Marinari GM, et al. Bilio-pancreatic diversion. World J Surg 1998; 22: 936–946.
- [26] Valera-Mora ME, Simeoni B, Gagliardi L, et al. Predictors of weight loss and reversal of comorbidities in malabsorptive bariatric surgery. Am J Clin Nutr 2005; 81: 1292–1297.
- [27] Mari A, Manco M, Guidone C, et al. Restoration of normal glucose tolerance in severely obese patients after bilio-pancreatic diversion: role of insulin sensitivity and beta cell function. Diabetologia 2006; 49: 2136–2143.
- [28] Unger RH. Lipotoxicity in the pathogenesis of obesity-dependent NIDDM. Genetic and clinical implications. Diabetes 1995; 44: 863–870.
- [29] Ponce J, Haynes B, Paynter S, et al. Effect of Lap-Band-induced weight loss on type 2 diabetes mellitus and hypertension. Obes Surg 2004; 14: 1335–1342.
- [30] Buchwald H, Avidor Y, Braunwald E, et al. Bariat-ric surgery: a systematic review and meta-analysis. JAMA 2004; 292: 1724–1737.
- [31] Ballantyne GH, Wasielewski A, Saunders JK. The surgical treatment of type II diabetes mellitus: changes in HOMA insulin resistance in the first year following laparoscopic Roux-en-Y gastric bypass (LRYGB) and laparoscopic adjustable gastric banding (LAGB). Obes Surg 2009; 19: 1297–1303.
- [32] Ferrannini E, Mingrone G. Impact of different ba-riatric surgical procedures on insulin action and beta-cell function in type 2 diabetes. Diabetes Care 2009; 32: 514–520.
- [33] Scopinaro N, Adami GF, Papadia FS, et al. The effects of biliopancreatic diversion on type 2 diabetes mellitus in patients with mild obesity (BMI 30–35 kg/m2) and simple overweight (BMI 25–30 kg/m2): a prospective controlled study. Obes Surg 2011; 21: 880–888.
- [34] Fried M, Ribaric G, Buchwald JN, et al. Metabolic surgery for the treatment of type 2 diabetes in patients with BMI < 35 kg/m2: an integrative review of early studies. Obes Surg 2010; 20: 776–790.