Postavení farmakoterapie v léčbě ženské močové inkontinence
Konzervativní terapie ženské stresové inkontinence nedosahuje efektivity chirurgické terapie, ale v indikovaných případech je její úspěšnost vysoká. Mezi možnosti konzervativní léčby patří rehabilitace svalů pánevního dna, farmakoterapie (a-sympatomimetika, duloxetin, tricyklická antidepresiva, estrogeny) a pesaroterapie. Farmakoterapie urgentní inkontinence je na rozdíl od léčby stresové inkontinence metodou volby. Základem terapie jsou léky s anticholinergním působením, jejichž efektivita je vysoká, ale s užíváním jsou často spojeny významné nežádoucí účinky (xerostomie, xeroftalmie, poruchy akomodace, obstipace), které představují hlavní důvody přerušení léčby. V postmenopauze jsou součástí této terapie vaginálně aplikované estrogeny, které umožňují snížit dávky anticholinergik při zachování vysoké účinnosti léčby. Farmakoterapie močové inkontinence obvykle nedosahuje stoprocentní efektivity, přesto však napomáhá významně zvýšit kvalitu života trpících žen.
Úvod
Močová inkontinence je definována jako nechtěný únik moči, který způsobuje sociální a hygienický problém [1]. Její prevalence stoupá s věkem, ve věkové skupině nad 65 let se u obou pohlaví vyskytuje v rozmezí 15–35 %. U osob žijících v domech s ústavní péčí stoupá tento podíl až na 50 %. Močová inkontinence ovšem není typická jen pro období stáří. Epidemiologické studie tvrdí, že například výskyt stresové inkontinence se ve věku mezi 30 a 60 lety pohybuje na úrovni 30 % [2]. Podle některých studií se tato inkontinence vyskytuje i u dvacetiletých vrcholových sportovkyň během sportovního výkonu, a to až ve 28 % [3].
Výskyt močové inkontinence je v populaci dospělých žen velmi vysoký. S tím ovšem kontrastuje alarmující nízký zájem o léčbu. Podle studií hodnotících prevalenci a incidenci močové inkontinence hledá lékařskou pomoc pouze 1,5–6 % trpících žen [4–7]. Pacientky s urgentní inkontinencí, pro něž je vhodná efektivní farmakoterapie, hledají pomoc častěji než ženy stresově inkontinentní [8].
Konzervativní léčba stresové inkontinence
Stresová inkontinence představuje nechtěný únik moči v situaci, kdy intravezikální tlak převýší maximální uzavírací uretrální tlak, a to bez současné kontrakce detruzoru. Moč tedy uniká při fyzické aktivitě, sportu, běhu, kašli, při kýchání apod.
V terapii ženské stresové inkontinence platí základní zásada: využití všech efektivních možností nechirurgické léčby před indikací k chirurgickému výkonu. Léčba konkrétní pacientky by měla být navržena až po stanovení přesné příčiny potíží a měla by být vždy individuálně upravena. Často se využívá kombinace jednotlivých léčebných metod, přičemž základem úspěchu je dokonale poučená a spolupracující pacientka. Farmakoterapie má v konzervativní léčbě stresové inkontinence obvykle podpůrný charakter, dominantní je cvičení pánevních svalů [9].
Rehabilitace svalů pánevního dna
Insuficience svalů pánevního dna má při vzniku stresové inkontinence zásadní vliv. Spontánní porod většího plodu, rozsáhlejší porodní poranění, těžká fyzická práce a u žen obvyklá obstipace představují rizikové faktory poškození pánevního dna. Soustava cviků slouží k rehabilitaci svalstva pánevního dna, zejména ke zvýšení jeho kontrakčních schopností a bazálního tonu. Předpokládá se, že následkem cvičení se zvyšuje klidový uretrální uzavírací tlak a zlepšuje se koordinace při reflexních kontrakcích svalů pánevního dna v průběhu stresových manévrů (např. kašel, smích, kýchání). Pro rehabilitační cvičení je velmi důležitá správně směřovaná motivace pacientky a její schopnost absolvovat celý program fyzioterapie [10]. Tato poznámka k léčebné taktice je poměrně důležitá, v současnosti je totiž oblíbenější pasivní přístup pacienta, který si představuje spíše polykání tablet či operaci, která je následována rychlým vyléčením, než aktivní spolupráci na léčebném procesu.
K rehabilitačním metodám patří Kegelovy cviky, používání vaginálních konusů nebo elektrostimulace.
Kegelovy cviky
Kegel prezentoval speciální program cvičení svalů pánevního dna již před více než půl stoletím. Pravidelné cvičení se doporučuje až třikrát denně po dobu přibližně 20 minut. Většinou dočasné zmírnění příznaků inkontinence je zaznamenáno asi u 75 % pacientek [10]. Pro dosažení trvalé efektivity je nutné pravidelné cvičení a dlouhodobý aktivní přístup. Pokud se léčebný efekt nedostaví do několika měsíců, další cvičení postrádá na významu.
Vaginální konusy
Jedná se o cvičení svalstva pánevního dna pomocí intravaginálně umístěných předmětů různé hmotnosti ve tvaru konusu. Když je konus po určité době tréninku pacientkou bez problémů v pochvě udržen, mění se za další o větší hmotnosti. Toto cvičení se provádí denně po dobu 20 minut. Příznivé výsledky léčby jsou udávány asi v 50 % případů.
Elektrostimulace
V léčbě močové inkontinence se využívá nepřímá elektrostimulace nervosvalových struktur pánevního dna, uretry a detruzoru pomocí intravaginálně umístěné sondy přijímající elektrické impulzy z externího zdroje. V případě stresové inkontinence se většinou využívá frekvence 50 Hz, která způsobuje kontrakce příčně pruhovaného svalu. Terapeutický význam má stimulace trvající 30 minut denně po dobu třiceti dnů. Dočasný příznivý efekt této léčby se dostavuje až v 60 %. Při odeznívajícím účinku lze elektrostimulaci kdykoli opakovat.
Farmakoterapie stresové inkontinence
Žádná světově doporučená farmakoterapie pro léčbu stresové inkontinence v současnosti neexistuje. Ve farmakologické léčbě stresové inkontinence se využívají zejména léky zvyšující uretrální uzavírací tlak (a-sympatomimetika, tricyklická antidepresiva a estrogeny).
a-sympatomimetika
V hrdle močového měchýře a v proximální uretře se vyskytují a-adrenergní receptory, jejichž stimulace sympatomimetiky vede ke zvýšení uretrálního tlaku [11]. V současné době se ovšem tyto léky pro jejich nežádoucí účinky (zvýšení krevního tlaku, nespavost, bolesti hlavy, třes, tachykardie, palpitace a srdeční arytmie) v praxi téměř nepoužívají. K dispozici je pouze midodrin, který se používá zejména v léčbě ortostatické hypotenze a jehož vedlejší účinky jsou výrazně redukovány.
Duloxetin
Ve farmakoterapii stresové inkontinence byly v poslední době učiněny významné kroky, a to zejména díky průkazu serotoninu a noradrenalinu jako mediátorů přenosu vzruchu v urogenitální oblasti. Byla vyvinuta nová účinná látka – duloxetin, která snižuje zpětné vychytávání serotoninu a noradrenalinu, což zintenzivňuje aktivitu a-adrenergních nervových zakončení a zvyšuje napětí uretrální stěny [12, 13]. Stimulací somatických nervových zakončení se zvyšuje i tonus příčně pruhovaného svalstva pánevního dna, což vede k dalšímu zmírnění příznaků stresové inkontinence [14, 15]. Duloxetin vede ke zvýšení bazálního tonu svěrače a k jeho silnějším kontrakcím v průběhu plnění močového měchýře. Závěry starší studie [16] tvrdí, že noradrenalin a serotonin nemají přímý vliv na motorické neurony, ale facilitují efekt neurotransmiteru glutamátu, který sám působí na motorické neurony a je účinný při plnění močového měchýře. Ve fázi vyprazdňování při naplněném měchýři jsou motorické neurony inhibovány, což je způsobeno absencí glutamátu, který je nezbytný pro jejich aktivaci. Podávání duloxetinu tudíž nevede k retenci moči a k poruchám vyprazdňování.
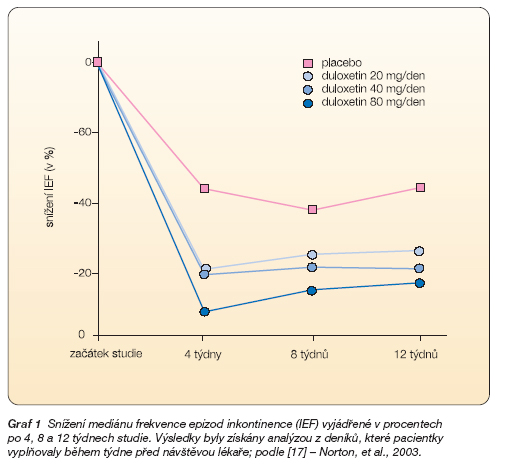
Rozsáhlá dvojitě slepá randomizovaná placebem kontrolovaná studie publikovaná před několika lety [17] posuzovala efektivitu a bezpečnost podávání duloxetinu v různých dávkách (20–80 mg denně). Ve studii byly sledovány zejména dva parametry: frekvence epizod inkontinence (IEF) a specifický dotazník hodnotící kvalitu života inkontinentních (I-QOL). Medián frekvence epizod inkontinence poklesl ve skupině duloxetinu ve srovnání s placebem statisticky signifikantně o 64 % ve skupině léčené duloxetinem 80 mg denně oproti 41% poklesu v placebové větvi (graf 1). Duloxetin byl prokazatelně efektivní nejen u lehčích forem, ale i v případech těžké inkontinence. Zlepšení kvality života korespondovalo s poklesem frekvence epizod inkontinence. Nejčastějším nežádoucím účinkem byla nauzea.
Duloxetin se podává 2x denně v obvyklé dávce 40 mg a po perorálním požití se dobře vstřebává a dosahuje cmax za 6 hodin po podání. Z 96 % se váže na plazmatické bílkoviny, jeho metabolity jsou vylučovány převážně močí a poločas eliminace se pohybuje okolo 12 hodin.
Nežádoucí účinky léčby (nauzea, xerostomie, nespavost, obstipace, únava, závratě) jsou podle krátkodobého sledování signifikantně častější ve skupině duloxetinu (24,1 %) ve srovnání s placebem (4,1 %), ale na zhodnocení jejich výskytu na základě dlouhodobého používání si musíme ještě počkat [18].
Terapie duloxetinem se v současnosti jeví jako jediná perspektivní a efektivní možnost farmakologické léčby stresové inkontinence [19] a postupné rozšiřování tohoto léku na světové trhy právě probíhá.
Tricyklická antidepresiva
Anticholinergního působení (snížení kontraktility močového měchýře) těchto léků se využívá při léčbě urgentní inkontinence. V terapii stresové inkontinence je možné využít efektu na adrenergní stimulaci hladkých svalových vláken v močové trubici, což vede ke zvýšení uzavíracího tlaku uretry [11]. K praktickému použití je k dispozici imipramin v běžné dávce 2 x 1 tableta denně. Potenciální anticholinergní účinky (zácpa, sucho v ústech, poruchy akomodace), sedativní vliv a případné abstinenční příznaky po vysazení však představují základní limity terapie tricyklickými antidepresivy u žen trpících pravou stresovou inkontinencí. Výhodnější se jeví využití imipraminu v léčbě smíšené inkontinence u žen trpících stresovou i urgentní symptomatologií.
Estrogeny
Terapie estrogeny v postmenopauze zlepšuje prokrvení pochvy a zvyšuje tvorbu vaginálního sekretu. Pochva i uretra mají společný embryonální základ, a proto se při léčbě estrogeny zlepšuje prokrvení v kapilárních plexech močové trubice a zvyšuje se vrstva urotelu. To by mělo vést k vzestupu uretrálního uzavíracího tlaku a ke zmírnění příznaků zejména stresové inkontinence. Subjektivní efektivita této léčby je studiemi opakovaně prokázána, ale jednoznačné objektivní kritérium hodnocení úspěchu pomocí některé vyšetřovací metody (urodynamika, ultrasonografie apod.) dosud neexistuje [20]. Vaginální estrogeny jsou v mnoha studiích podávány v kombinaci s a-sympatomimetiky. Význam této kombinace je rovněž diskutabilní [19]. Estrogeny mohou zvýšit efektivitu působení sympatomimetik cestou zvýšení počtu a senzitivity a-adrenergních receptorů [21]. Lokální aplikace estrogenů je bezpečná [22] a měla by být v zájmu zlepšení trofiky urogenitálního traktu u žen v postmenopauze podávána i před chirurgickou terapií stresové inkontinence. Dávkování je individuální (1krát denně až 2krát týdně). Podávání lokálních vaginálních estrogenů vede postupně ke snížení poševního pH, což má zásadní význam v prevenci recidivujících uroinfekcí, jejichž prevalence je v postmenopauze a v seniu významně vyšší [23].
Vaginální pesary
Vaginální pesary redukují symptomy stresové inkontinence tím, že upravují porušené anatomické poměry a zvyšují výtokový odpor uretry. V současnosti prochází tato léčebná metoda určitou renesancí. K dispozici je totiž řada moderních pesarů různých velikostí a tvarů, které jsou vyrobeny z měkčích plastů než v minulosti. Mechanismus působení pesaru je velmi podobný principům chirurgické léčby stresové inkontinence. Z tohoto důvodu bývá pesaroterapie alternativou k operaci. Pesary je možné používat intermitentně, například při občasném sportu, ale také dlouhodobě, a to zejména u starších pacientek, u nichž není operační léčba z různých, zejména zdravotních důvodů proveditelná [24].
Konzervativní léčba urgentní inkontinence
Urgentní inkontinence (hyperaktivní měchýř) představuje nechtěný únik často většího množství moči v důsledku silného a neovladatelného nucení k mikci. Dělí se na formu motorickou, která je spojena s hyperreflexií detruzoru, a senzorickou, pro kterou je typická zvýšená senzitivita močového měchýře. V klinickém obraze urgentní inkontinence se vedle urgencí vyskytuje i polakisurie a nykturie. Tento typ inkontinence se vyskytuje častěji u žen v postmenopauze a v seniu.
Pokud se zjistí konkrétní příčina urgentní mikční symptomatologie (např. recidivující infekce dolních močových cest, stenóza uretry, divertikl, tumor měchýře), samozřejmou podmínkou vyléčení je její odstranění [25]. V ostatních případech je metodou léčby urgentní inkontinence moderní farmakoterapie, která je charakterizována zejména vysokou účinností a pohodlnou aplikací při přiměřených nárocích na spolupráci pacientky. Podmínkou úspěšné léčby je diagnostický proces, při kterém se nesmí zapomenout na velký význam získání kvalitní anamnézy a na mikční deník se záznamem epizod spojených s urgencí, únikem moči či s močením. Záznam o množství a distribuci příjmu tekutin by měl být jeho nedílnou součástí.
Mezi metody konzervativní léčby urgentní inkontinence patří:
– Modifikace životního stylu
Pacientka s urgentní inkontinencí by měla být v úvodu léčebného procesu poučena o nutnosti příjmu dostatečného množství tekutin během celého dne, o příčině mikčních potíží a o maximální možné efektivitě terapie. Správná motivace a trpělivost každé inkontinentní ženy je pro dosažení dlouhodobé účinnosti léčby rozhodující.
– Reedukace močového měchýře
Tato léčebná metoda je založena na postupném prodlužování intervalů mezi mikcemi. K prodloužení může dojít až po dostatečné fixaci intervalu předchozího.
– Elektrostimulace
Obdobně jako v případě stresové inkontinence se i v terapii urgentní symptomatologie používá nepřímá intravaginální elektrostimulace. Léčba obvykle trvá 30 dnů, ale frekvence proudu jsou nižší a pohybují se mezi 10 a 20 Hz.
– Farmakoterapie urgentní inkontinence
Historie farmakoterapie hyperaktivního měchýře je dlouhá. V průběhu vývoje novějších preparátů již mnohá léčiva ztratila na svém původním významu. Cílem medikamentózní léčby je snížení nadměrné aktivity detruzoru a zvýšení funkční kapacity močového měchýře včetně zvětšení objemu při prvním nucení k mikci.
Látky blokující muskarinové receptory
Látky s antimuskarinovým účinkem kompetitivně blokují působení acetylcholinu na muskarinových receptorech nervosvalové ploténky. Nejedná se o zcela kompletní blokádu vzhledem k tomu, že inervace části vláken hladké svaloviny je noncholinergní a nonadrenergní. Z těchto důvodů se v terapii často kombinují látky s různým mechanismem působení.
Muskarinové receptory jsou tvořeny subtypy M1–M5. V močovém měchýři se nacházejí receptory M2 a M3. Receptorová selektivita má zásadní význam v terapii urgentní inkontinence, a to jak v maximálním využití anticholinergního efektu, tak v minimalizaci nežádoucích účinků léčby [26].
Základní kontraindikací léčby anticholinergiky je glaukom. Některé pacientky s tímto onemocněním však tyto léky mohou užívat, a proto je vhodné odeslat pacientku s urgentní inkontinencí a glaukomem ke konzultaci o možnosti léčby k oftalmologovi [27]. Mezi léky s antimuskarinovým účinkem v současnosti u nás používané patří trospium, tolterodin a solifenacin.
Trospium je kvarterní amoniová sloučenina se spasmolytickým účinkem, jejíž biologický poločas se pohybuje mezi 6–15 hodinami a maximální sérové koncentrace dosahuje za 4–6 hodin po požití. Užívá se obvykle dvakrát denně v dávce 15 mg a léčba se upravuje podle výskytu nežádoucích účinků [28].
Tolterodin je antimuskarinový lék působící zejména na receptory M3. Jeho hlavní výhodou ve srovnání s oxybutininem je menší afinita k muskarinovým receptorům v slinných žlázách, přičemž efektivita obou léků je podle komparativních studií srovnatelná [29]. Recentně publikovaná komparativní studie uživatelek tolterodinu a propiverinu dokumentuje srovnatelnou účinnost a výskyt nežádoucích účinků u obou těchto léčebných přípravků [30].
Solifenacin je novým lékem doporučeným k terapii urgentní inkontinence, který se náš trh dostal v minulém roce. Jeho efektivita je vysoká a studiemi opakovaně prokázaná [31, 32]. Doporučená denní terapeutická dávka se pohybuje mezi 5 a 10 mg jednou denně. Rozsáhlá klinická komparativní studie hodnotící efektivitu a toleranci solifenacinu a tolterodinu s pomalým uvolňováním účinné látky dokumentovala vyšší efektivitu ve skupině solifenacinu, přičemž nežádoucí účinky byly v obou sledovaných souborech srovnatelné [33].
Látky se smíšeným antimuskarinovým a spasmolytickým působením
Látky se smíšeným působením anticholinergním a spasmolytickým dosahují léčebného efektu různými mechanismy, ale mají zejména antimuskarinovou aktivitu, která je velmi pravděpodobně dominantně zodpovědná za klinickou účinnost. Do této skupiny patří zejména oxybutinin a propiverin.
Historicky nejstarším účinným lékem na současném trhu je oxybutinin. Užívá se běžně v dávce 2 x 5 mg denně. Jeho forma s okamžitým uvolňováním účinné látky disponuje mezi používanými léky nejvyšším výskytem nežádoucích účinků, přičemž efektivita léčby posuzovaná podle redukce epizod urgence a urgentní inkontinence je vysoká [34]. Novější lékové formy oxybutininu – tablety s pomalým uvolňováním účinné látky a forma transdermální – mají vyšší biologickou dostupnost, lépe redukují frekvenci epizod inkontinence a poněkud snižují anticholinergní nežádoucí účinky s léčbou spojené [35].
V některých evropských zemích je oblíbeným přípravkem tlumícím symptomy hyperaktivního měchýře propiverin. Užívá se v dávce 2 x 15 mg denně. Propiverin signifikantně zvyšuje funkční kapacitu močového měchýře, ale má i řadu typických anticholinergních nežádoucích účinků [30]. Jeho tolerance je ovšem ve srovnání s oxybutininem lepší a příčinou toho je zejména nižší frekvence výskytu suchosti v ústech během terapie [36].
Limitujícím faktorem farmakoterapie urgentní inkontinence pomocí léčiv obou výše uvedených skupin jsou jejich nežádoucí účinky. Mezi nejčastější a nejnepříjemnější patří suchost sliznic (xerostomie, xeroftalmie), poruchy zažívání, obstipace a poruchy akomodace. Taktika léčby není všeobecně stanovena [37]. V zájmu dosažení co nejlepší tolerance a efektivity terapie se obvykle začíná oxybutininem či propiverinem. Léčba pomocí těchto léků se individuálně upravuje tak, aby bylo dosaženo maximálního tlumivého efektu na detruzor při minimu nežádoucích účinků. Terapie obvykle začíná doporučenými denními dávkami, například 2 x 1 tableta oxybutininu či propiverinu, při výrazných vedlejších obtížích se dávka redukuje na takovou, která je pacientkou dlouhodobě tolerována. Pokud jsou nežádoucí účinky výrazné či efektivita nedostatečná, přistupuje se ke změně terapie a volí se léčiva ze skupiny antimuskarinových preparátů, v našich podmínkách obvykle solifenacin či tolterodin, jejichž působení je mnohem selektivnější a podle publikovaných studií mají ve srovnání s léky první volby redukované nežádoucí účinky (zejména sucho v ústech) [26]. Tato terapie je zpravidla dlouhodobě dobře tolerována, její nevýhodou je pouze vyšší cena. Pokud pacientka v minulosti užívala oxybutinin či propiverin s minimálním efektem nebo měla při této léčbě významné nežádoucí účinky, terapie začíná přímo podáváním solifenacinu či tolterodinu.
Na současném trhu jsou spolu s léky s okamžitým uvolňováním účinné látky (immediate-release) k dispozici i formy s pomalým uvolňováním účinné látky (extended-release), které zajišťují 24hodinový efekt v jedné denní dávce. Tato léková forma významně zvyšuje compliance pacientek, potencuje efektivitu a parciálně redukuje nežádoucí účinky s léčbou spojené, což zdůvodňuje současnou preferenci těchto lékových forem před léky s okamžitým uvolňováním účinné látky.
Tricyklická antidepresiva
Tricyklická antidepresiva zlepšují jímací funkci močového měchýře. Tohoto efektu je dosaženo kombinací relaxačního vlivu na detruzor a tonizace hladké svaloviny močové trubice. Zlepšení terapeutického efektu je možné dosáhnout kombinací s menší dávkou anticholinergika. V současné praxi se používá imipramin [38].
Hormonální terapie
Estrogeny byly popsány již v kapitole o konzervativní léčbě stresové inkontinence. Pro léčbu urgentní inkontinence platí všechny popsané možnosti působení. Při respektování všech kontraindikací je tato léčba vhodná v kombinaci s anticholinergiky u mnoha postmenopauzálních žen s urgentní inkontinencí [39, 40]. Kombinovaná terapie dosahuje často podstatně vyššího efektu a umožňuje redukci dávek anticholinergik, což vede ke zmírnění výskytu jejich nežádoucích účinků.
Závěr
V medikamentózní léčbě stresové i urgentní inkontinence u žen v postmenopauze lze využít příznivého efektu lokální estrogenní terapie. Velmi očekávanou možnost konzervativní léčby lehčí formy stresové inkontinence přináší nedávno představený inhibitor zpětného vychytávání serotoninu a noradrenalinu – duloxetin.
V léčbě urgentní inkontinence se obvykle využívá anticholinergního působení oxybutininu či propiverinu. Pokud je efektivita této terapie nedostatečná a nežádoucí účinky jsou výrazné, doporučuje se výměna za solifenacin či tolterodin, jejichž anticholinergní účinky, zejména sucho v ústech, jsou významně redukovány.
Seznam použité literatury
- [1] Abrams P, Cardozo L, Fall M, et al. The standardisation of terminology of lower urinary tract function: Report from the Standardisation Sub-committee of the International Continence Society. Neurourol Urodyn 2002; 21: 167–178.
- [2] Burgio KL, Matthews KA, Engel BT. Prevalence, incidence and correlates of urinary incontinence in healthy, middle-aged women. J Urol 1991; 146: 1255–1259.
- [3] Nygaard IE, Thompson FL, Svengalis SL, Albright JP. Urinary incontinence in elite nulliparous athletes. Obstet Gynecol 1994; 84: 183–187.
- [4] Hording U, Pedersen KH, Sidenius K, Hedegaard L. Urinary incontinence in 45-year-old women. An epidemiological survey. Scand J Urol Nephrol 1986; 20: 183–186.
- [5] Ushiroyama T, Ikeda A, Ueki M. Prevalence, incidence, and awareness in the treatment of menopausal urinary incontinence. Maturitas 1999; 33: 127–132.
- [6] Samuelsson EC, Victor AFT, Svärdsudd KF. Five-year incidence and remission rates of female urinary incontinence in a Swedish population less than 65 years old. Am J Obstet Gynecol 2000; 183: 568–574.
- [7] Simeonova Z, Milsom I, Kűllendorff AM, et al. The prevalence of urinary incontinence and its influence on the quality of life in women from an urban Swedish population. Acta Obstet Gynecol Scand 1999; 78: 546–551.
- [8] Hagglund D, Walker-Engstrom ML, Larsson G, Leppert J. Quality of life and seeking help in women with urinary incontinence. Acta Obstet Gynecol Scand 2001; 80: 1051–1055.
- [9] Hanuš T. Stresová inkontinence moči. Postgrad Med 2001; 3: 279–284.
- [10] Feyereisl J. Terapie stresové inkontinence moče. Moderní gynekologie a porodnictví 1999; 8: 37–44.
- [11] Martan A. Nové možnosti v medikamentózní léčbě urgentní inkontinence moči u žen. Čes Gynek 2005; 1: 3–8.
- [12] Fraser MO, Chancellor MB. Neural control of the urethra and development of pharmacotherapy for stress urinary incontinence. BJU Int 2003; 91: 743–748.
- [13] Thor KB. Serotonin and norepinephrine involment in afferent pathways to the uretral rhabdosphincter: implications for treating stress urinary incontinence. Urology 2003; 62: 3–9.
- [14] van Kerrebroeck P. Duloxetine: an innovative ap-proach for treating stress urinary incontinence. BJU Int 2004; 92: 31–37.
- [15] Oelke M, Roovers JP, Michel MC. Safety and tolerability of duloxetine in women with stress urinary incontinence. BJOG 2006; 113 (Suppl 1): 22–26.
- [16] Thor KB, Katofiasc MA. Effects of duloxetine, a combined serotonin and norepinephrine reuptake inhibitor, on central neural control of lower urinary tract function in the chloralose-anesthetized female cats. J Pharmacol Exp Ther 1995; 274: 1014–1024.
- [17] Norton PA, Zinner NR, Yalcin I, et al. Duloxetine versus placebo in the treatment of stres urinary incontinence. Am J Obstet Gynecol 2002;187: 40–48.
- [18] Dmochowski RR, Miklos JR, Bortin PA, et al. Duloxetine versus placebo for the treatment of North American women with stress urinary incontinence. J Urol 2003; 170: 1259–1263.
- [19] Schuessler B, Baessler K. Pharmacologic treatment of stress urinary incontinence: expectations for outcome. Urology 2003; 62: 31–38.
- [20] Horčička L, Chmel R. Využití lokálně aplikovaných estrogenů v léčbě urogenitálních potíží. Gynekolog 1997; 6: 73–74.
- [21] Larsson B, Anderson KE, Batra S, et al. Effects of estradiol on norepinephrine-induced contraction, alpha adrenoceptor number and norepinephrine content in the female rabbit urethra. J Pharmacol Exp Ther 1984; 229: 557–563.
- [22] Weisberg E, Ayton R, Darling G, et al. Endometrial and vaginal effects of low-dose estradiol delivered by vaginal ring or vaginal tablet. Climacteric 2005; 8: 83–92.
- [23] Palacios S, Castelo-Branco C, Cancelo MJ, Vasquez F. Low-dose, vaginally administered estrogens may enhance local benefits of systemic therapy in the treatment of urogenital atrophy in postmenopausal women on hormone therapy. Maturitas 2005; 14: 98–104.
- [24] Horčička L. Pesary v urogynekologii. Praktická gynekologie 2002; 5: 6–7.
- [25] Chmel R, Kawaciuk I. Divertikl ženské močové trubice – stále aktuální problém v urogynekologii. Čes Gynek 2002; 67; 152–157.
- [26] Hegde SS. Muscarinic receptors in the bladder: from basic research to therapeutics. Br J Pharmacol 2006; 147 Suppl 2: S80–S87.
- [27] Altan-Yaycioglu R, Yaycioglu O, Aydin Akova Y, et al. Ocular side-effects of tolterodine and oxybutynin, a single-blind prospective randomized trial. Br J Clin Pharmacol 2005; 59: 588–592.
- [28] Rovner ES. Trospium chloride in the management of overactive bladder. Drugs 2004; 64: 2433–2446.
- [29] Nitti VW, Dmochowski R, Appell RA, et al. Efficacy and tolerability of tolterodine extended-release in continent patients with overactive bladder and nyocturia. BJU Int 2006; 97: 1262–1266.
- [30] Junemann KP, Halaska M, Rittstein T, et al. Propiverine versus tolterodine: efficacy and tolerability in patients with overactive bladder. Eur Urol 2005; 48: 478–482.
- [31] Staskin DR, Te AE. Short- and long-term efficacy of solifenacin treatment in patients with symptoms of mixed urinary incontinence. BJU Int 2006; 97: 1256–1261.
- [32] Cardozo L, Lisec M, Miliard R, et al. Randomized, double-blind placebo controlled trial of the once daily antimuscarinic agent solifenacin succinate in patients with overactive bladder. J Urol 2004; 172: 1919–1924.
- [33] Chapple CR, Martinez-Garcia R, Selvaggi L, et al. A comparison of the efficacy and tolerability of solifenacin succinate and extended release tolterodine at treating overactive bladder syndrome: results of the STAR trial. Eur Urol 2005; 48: 464–470.
- [34] Holmes DM, Montz FJ, Stanton SL. Oxybutinin versus propantheline in the management of detrusor instability. A patient-regulated variable dose trial. Br J Obstet Gynaecol 1989; 96: 607–612.
- [35] Siddiqui MA, Perry CM, Scott LJ. Oxybutynin extended-release: a review of its use in the management of overactive bladder. Drugs 2004; 64: 885–912.
- [36] Madersbacher H, Mürtz G. Efficacy, tolerability and safety profile of propiverine in the treatment of the overactive bladder (non-neurogenic and neurogenic). World J Urol 2001; 19: 324–335.
- [37] Erdem N, Chu FM. Management of overactive bladder and urge urinary incontinence in the elderly patient. Am J Med 2006; 119: 29–36.
- [38] Lin HH, Sheu BC, Lo MC, Huang SC. Comparison of treatment outcomes for imipramine for female genuine stress incontinence. Br J Obstet Gynaecol 1999; 106: 1089–1092.
- [39] Cardozo L, Lose G, McClish D, Versi E. A systematic review of the effects of estrogens for symptoms suggestive of overactive bladder. Acta Obstet Gynecol Scand 2004; 83: 892–897.
- [40] Cardozo L, Rekers H, Tapp A, et al. Oestriol in the treatment of postmenopausal urgency: a multicenter study. Maturitas 1993; 18: 47–53.