Selektivní ovlivnění srdeční frekvence – nový fenomén v kardiovaskulární farmakoterapii
Velké epidemiologické studie jasně ukázaly, že zvýšená klidová srdeční frekvence (SF) je nezávislým rizikovým faktorem morbidity a mortality u zdravých osob, hypertoniků, nemocných s ischemickou chorobou srdeční, po prodělaném infarktu myokardu a s chronickým srdečním selháním. Na zvýšenou klidovou SF by proto mělo být pohlíženo stejně jako na ostatní klasické rizikové faktory, jako jsou hypertenze, hypercholesterolémie, kouření či diabetes mellitus. Je velmi dobře dokumentováno, že úspěšná intervence těchto rizikových faktorů zlepšuje prognózu jak v primární, tak i v sekundární prevenci. Několik velkých, placebem kontrolovaných klinických studií u nemocných po prodělaném akutním infarktu myokardu nebo s chronickým srdečním selháním přesvědčivě prokázalo, že b-blokátory významně snižují u těchto nemocných morbiditu i mortalitu. Zdá se, že tyto příznivé účinky jsou zřetelnější u nemocných s vyšší výchozí klidovou SF, u těchto nemocných je také při léčbě výraznější snížení SF. Existuje řada dokladů, které opravňují hypotézu, že hlavním mechanismem, kterým b-blokátory zlepšují prognózu, je snížení SF jako takové. Také při léčbě bradykardizujícími blokátory kalciových kanálů bylo u nemocných po prodělaném infarktu myokardu dokumentováno zlepšení prognózy. Nicméně, jak b-blokátory, tak i bradykardizující blokátory kalciových kanálů mají vedle bradykardizujícího ještě řadu dalších účinků na hemodynamiku, které se mohou na zlepšení prognózy podílet, ale také mohou mít vliv oslabující. Ivabradin – nový selektivní blokátor kanálů If v pacemakerových buňkách sinoatriálního uzlu specificky snižuje SF, jiné účinky nemá. Nedávno byla ukončena velká morbiditní a mortalitní studie BEAUTIFUL, ve které je účinnost ivabradinu testována oproti placebu u nemocných se stabilní ischemickou chorobou srdeční a se systolickou dysfunkcí levé komory. Výsledky této studie budou zveřejněny v průběhu letošního roku. Další klinická studie SHIFT zkouší ivabradin, opět proti placebu, u nemocných s chronickým systolickým srdečním selháním. Teprve výsledky těchto dvou studií přinesou odpověď na otázku, jaký je dopad zpomalení SF na prognózu nemocných s kardiovaskulárními chorobami, tedy v sekundární prevenci. Odpověď na to, zda by měla být zvýšená klidová SF u jinak zdravých osob farmakologicky snižována – podobně jako snižujeme zvýšený krevní tlak, tedy v primární prevenci – však od těchto studií očekávat nemůžeme.
Úvod
Klidová srdeční frekvence (SF) je jedním z nejjednodušších kardiovaskulárních parametrů. Její prognostický význam však není zcela jasný. Sice tušíme a věříme, že klidová tachykardie je prognosticky nepříznivá, ale jako nezávislý prognostický faktor není klidová SF formálně přijímána. Také farmakologické snížení SF jako takové není v současnosti léčebným cílem ve snaze ovlivnit příznivě dlouhodobou prognózu nemocného.
Epidemiologická data z dlouhodobých sledování zdravých osob ukázala, že existuje nezávislý vztah mezi klidovou SF a kardiovaskulární morbiditou a mortalitou. Publikované studie z všeobecné populace a velkých souborů hypertoniků, které zahrnují přibližně 180 000 individuí, ukazují, že kardiovaskulární, ale i celková mortalita významně stoupá se zvyšující se klidovou SF [1–3]. V dnes již klasické Framinghamské studii byla po dobu 30 let sledována kohorta 5070 zdravých mužů a žen. Vztah mezi zvýšenou klidovou SF a celkovou mortalitou byl zjištěn jak u mladších, tak u starších osob, u mužů byl tento vztah výraznější, ale i u žen byl statisticky významný [4]. V jiné americké studii u 5995 zdravých osob ve věku 25–74 let, které byly sledovány po dobu 6–13 let, byla zvýšená klidová SF identifikována jako nezávislý rizikový faktor koronární morbidity i mortality u obou pohlaví, a to jak u bělochů, tak i u černochů [5]. V jiné studii u zdravých mužů a žen bylo zjištěno, že zvýšená klidová SF je nejenom prediktorem celkové i kardiovaskulární mortality, ale také nezávislým prediktorem náhlé srdeční smrti [6].
Pakliže vysoká klidová SF zhoršuje prognózu a zkracuje život, je namístě položit si otázku, zda naopak snížení klidové SF (ať již farmakologické nebo nefarmakologické) prognózu zlepší a život prodlouží. Pojďme se podívat, zda a jaké důkazy jsou pro podporu této lákavé hypotézy k dispozici. U některých divoce žijících zvířat, která podléhají hibernaci, je vztah mezi SF a délkou života těsný a jasně prokazatelný. Například u hibernujících netopýrů se snižuje klidová SF 45krát, na 10–20 tepů/min. Hibernující netopýři žijí o 70 % déle (39 vs. 23 roků) než nehibernující druhy netopýrů [7]. U lidí je však dlouhodobá hibernace představitelná jen v oblasti románů science fiction. Známou a velmi dobře dostupnou intervencí, která snižuje SF a prodlužuje život, je fyzické cvičení. Dlouhodobý vytrvalostní trénink zvyšuje u člověka tonus parasympatiku a naopak snižuje tonus sympatiku. Výsledkem těchto změn vegetativního nervového systému je snížení klidové SF. Je zajímavé, že pravidelná tělesná aktivita a klidová SF těsně korelovaly s dlouhodobým přežíváním starších nemocných ve francouzské studii IPC [8].
U nemocných s ischemickou chorobou srdeční je snížení SF obecně považováno za prospěšný léčebný efekt. Snižuje spotřebu kyslíku v myokardu a současně prodloužením diastoly a zlepšením subendokardiální perfuze zvyšuje jeho nabídku. Navíc snížení klidové SF také snižuje riziko ruptury aterosklerotického plátu [9] a u nemocných po prodělaném infarktu myokardu významně redukuje riziko náhlé smrti. Jak u experimentálních zvířat, tak u lidí může být prospěšný antiischemický účinek snížení SF zrušen síňovou kardiostimulací [10, 11]. To ukazuje na význam snížení SF v pozitivním účinku bradykardizujících léčiv, jako jsou b-blokátory nebo bradykardizující blokátory kalciových kanálů.
b -blokátory snižují klidovou SF i mortalitu
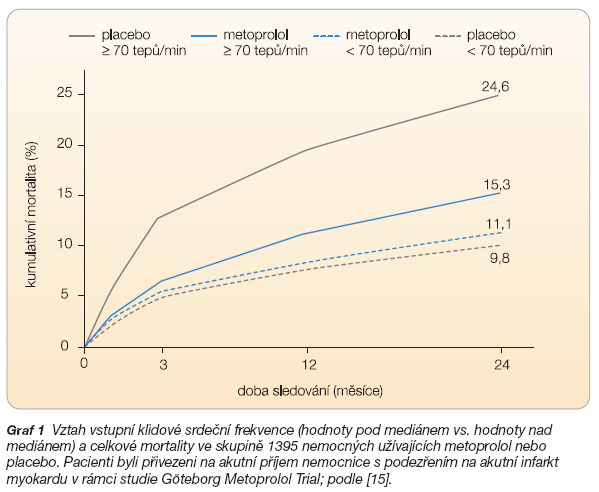
Začátkem osmdesátých let byly publikovány první studie s b-blokátory v sekundární prevenci. Již první tři z těchto velkých klinických studií konzistentně a přesvědčivě ukázaly, že b-blokátory, konkrétně timolol, metoprolol a propranolol významně snižují u nemocných po prodělaném infarktu myokardu celkovou i kardiovaskulární mortalitu, výskyt náhlé srdeční smrti a počet hospitalizací [12–14]. V těchto studiích se také ukázalo, že nemocní se vstupní klidovou SF vyšší než medián měli v průběhu studie vyšší mortalitu a také že příznivý účinek b-blokátorů byl nejzřetelnější u nemocných s nejvyšší vstupní klidovou SF. Výsledky studie Göteborg Metoprolol Trial šly dokonce ještě dál. Ukázaly, že veškeré prospěšné účinky b-blokátoru metoprololu (snížení celkové mortality, náhlé srdeční smrti, výskytu fibrilace komor, výskytu reinfarktů a velikosti infarktového ložiska odhadnuté pomocí enzymů) byly mnohonásobně výraznější u nemocných, kteří měli vstupní klidovou SF nad mediánem hodnot (> 70 tepů/min) než u nemocných, kteří měli vstupní klidovou SF pod tímto mediánem [15] (graf 1).
Ve studii Norwegian Timolol Multicenter Study byla léčba timololem spojena s poklesem mortality o 41,6 % [12]. Klidová SF byla v této studii významným prediktorem celkové mortality, přitom ale mortalita při určité SF byla podobná jak při podávání timololu, tak placeba. V logistické regresní analýze zůstala klidová SF významným prediktorem mortality, ale druh léčby (placebo nebo aktivní léčba) nikoliv. To znamená, že většina příznivého vlivu timololu na snížení mortality může být přičtena na vrub snížení klidové SF. Naproti tomu studie APSI (Acebutolol et Prévention Secondaire de l Infarctus) u vysoce rizikových nemocných po prodělaném infarktu myokardu ukázala velký pokles celkové i kardiovaskulární mortality (o 48 % a 58 %) při léčbě acebutololem, přestože acebutolol snížil klidovou SF jen mírně [16].
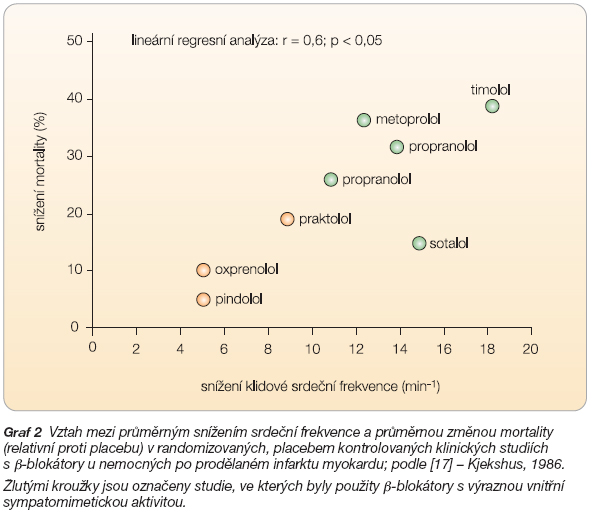
Kjekshus analyzoval všechny placebem kontrolované klinické studie s dlouhodobým podáváním b-blokátorů u nemocných po akutním infarktu myokardu [17]. Na výsledcích 11 klinických studií, které zahrnuly více než 16 000 nemocných, ukázal, že existuje statisticky významná korelace mezi snížením klidové SF a poklesem celkové mortality (graf 2).
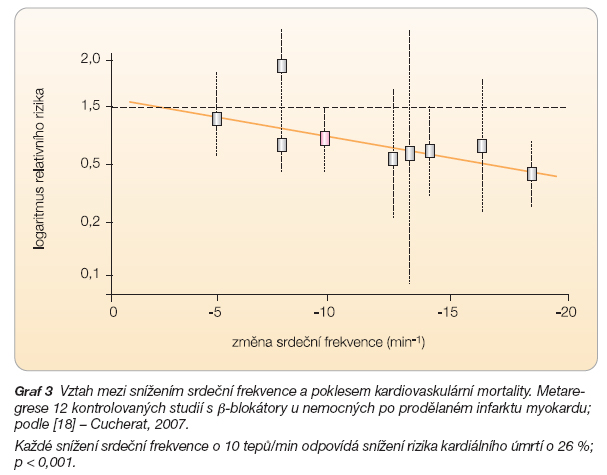
Nedávno byla publikována metaregresní analýza 12 randomizovaných, placebem kontrolovaných studií s b-blokátory u nemocných po prodělaném infarktu myokardu, která ukázala velmi podobné snížení relativního rizika kardiovaskulárního úmrtí (p = 0,02) (graf 3), náhlého srdečního úmrtí (p < 0,01) a reinfarktů (p < 0,01) [18].
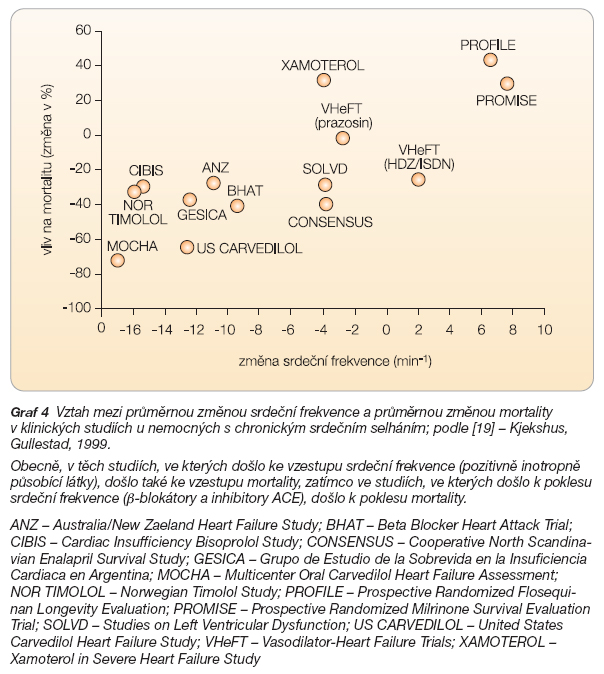
Kjekshus a Gullestad analyzovali u nemocných s chronickým srdečním selháním vztah mezi léčbou, klidovou SF a prognózou [19]. Podobně jako u nemocných po infarktu myokardu nalezli korelaci mezi snížením klidové SF a mortalitou – léčiva, která snížila klidovou SF, také snížila mortalitu, zatímco léčiva, která ji zvýšila, měla trend mortalitu zvyšovat (graf 4).
Výsledky velkých klinických studií s b-blokátory u srdečního selhání jsou s touto korelací v souladu. Například ve studii CIBIS (Cardiac Insufficiency Bisoprolol Study) snížila léčba bisoprololem ve srovnání s placebem klidovou SF přibližně o 15 tepů/min. Snížení SF bylo v multivariační analýze v této studii nejmohutnějším prediktorem přežití [20]. Korelace mezi logaritmem rizika mortality a změnou SF byla v rozmezí -40 až +10 tepů/min takřka lineární. V navazující a větší studii CIBIS II byly bazální klidová SF a změna SF při léčbě významnými prediktory mortality [21]. Nejlepší prognózu měli nemocní s nejnižší bazální klidovou SF a s nejvyšším poklesem SF při léčbě. Také při analýze dat ze studie COMET (Carvedilol or Metoprolol European Trial) byla SF dosažená při léčbě významným a nezávislým prediktorem mortality, přestože SF neovlivnila delší přežívání při léčbě karvedilolem ve srovnání s metoprololem [22]. Nicméně, ve studii MERIT-HF (Metoprolol CR/XL Randomized Intervention Trial in Congestive Heart Failure) byl příznivý účinek metoprololu na mortalitu a morbiditu nezávislý na dosažené SF [23], což naznačuje, že snížení klidové SF není jediným mechanismem, kterým se realizují příznivé účinky b-blokátorů u nemocných se srdečním selháním.
Vedle b-blokátorů snižují výrazně SF také některé nedihydropyridinové blokátory kalciových kanálů, především verapamil a diltiazem. Podobně jako b-blokátory, také bradykardizující blokátory kalciových kanálů snižují riziko reinfarktů [24] a u nemocných po infarktu myokardu, kteří nemají známky srdečního selhání, i mortalitu [25].
Měli bychom lidem s vysokou klidovou SF předepisovat bradykardizující léky?
Z epidemiologických studií víme, že vysoká klidová SF je prognosticky nevýhodná a představuje nezávislý rizikový faktor [1, 26]. Klidová SF > 90 tepů/min může být u jinak zdravého člověka škodlivá. Měli bychom tedy léčit vysokou klidovou SF se stejným úsilím, s jakým léčíme ostatní hlavní rizikové faktory kardiovaskulárních onemocnění, jako jsou hypertenze, diabetes mellitus, dyslipidémie nebo abdominální obezita? Nutno konstatovat, že zatím neexistuje u lidí žádná studie, která by u zdravých osob prokázala, že dlouhodobá bradykardizující léčba je prospěšná, zlepšuje prognózu, přináší přijatelný poměr rizika a prospěchu a je také cenově přijatelná. Existují však některé důkazy z experimentů na zvířatech. U opic vede zpomalení SF ablací sinoatriálního uzlu nebo dlouhodobé podávání b-blokátoru propranololu k zřetelnému snížení výskytu aterosklerózy a ke zpomalení jejího rozvoje [27]. Podávání digoxinu myším jim zpomaluje SF a prodlužuje délku života [28].
Co bychom tedy v současnosti měli dělat s nemocným, který má vysokou klidovou SF? Především bychom měli vyšetřit a eventuálně léčit odstranitelné příčiny tachykardie, jako jsou anémie, hypoxémie, hypertyreóza, alkoholismus, chronický stres nebo deprese, a vyloučit, že vysoká klidová SF je důsledkem podávaných léků (hormony štítné žlázy, katecholaminy, aminofylin a další). Pokud je toto vše vyloučeno, pak by osobě s vysokou klidovou SF měly být doporučeny změny životního stylu, především odstranění abúzu toxických látek (kofein, alkohol, nikotin, amfetaminy, kokain) a pravidelná fyzická aktivita. Užitečné mohou být také různé relaxační techniky, které odstraňují nebo snižují úzkost a stres. V případě nutnosti není důvod vyhýbat se farmakoterapii antidepresivy nebo jinými psychofarmaky s tlumivými účinky.
Betablokátory snižují jak klidovou SF, tak i reakci SF na zátěž. Jak již bylo uvedeno výše, snižují u nemocných po prodělaném infarktu myokardu, stejně jako u nemocných s chronickým srdečním selháním konzistentně celkovou i kardiovaskulární mortalitu, výskyt náhlé srdeční smrti a výskyt reinfarktů. Snížení SF b-blokátory je však doprovázeno mnohými dalšími účinky: b-blokátory snižují systémový krevní tlak, snižují kontraktilitu myokardu, prodlužují diastolu, zvyšují koronární průtok, zejména v subendokardiálních vrstvách. To vše vede na jedné straně ke snížení spotřeby kyslíku v myokardu, na straně druhé ke zvýšení jeho dodávky. Podobně i bradykardizující blokátory kalciových kanálů verapamil a diltiazem vedle snížení SF působí také jako periferní vazodilatancia, snižují systémový krevní tlak a působí negativně inotropně. Nelze proto s jistotou zjistit, nakolik je za účinnost b-blokátorů a bradykardizujících blokátorů kalciových kanálů zodpovědné prosté snížení SF a nakolik jejich další účinky. Může to být i opačně – příznivé účinky snížení SF mohou být u těchto léčiv oslabovány jejich jinými účinky, např. efektem negativně inotropním.
Odpovědi zřejmě přinesou výsledky studií s ivabradinem
Srdeční frekvence je primárně určována sinoatriálním uzlem v pravé síni. V buňkách tohoto uzlu specializované převodní tkáně je celá řada kationtových kanálů aktivovaných hyperpolarizací, jejichž vzájemná souhra řídí rychlost diastolické depolarizace, a tím srdeční frekvenci. Je proto přirozené, že se na tyto kanály a jejich ovlivnění zaměřil farmakologický výzkum. Jeden z těchto kanálů se označuje If a jeho blokátory se jmenují bradiny. Z několika zkoušených bradinů se ukázal jako nejnadějnější specifický blokátor kanálů If ivabradin. Ivabradin blokuje specificky kanály If v pacemakerových buňkách sinoatriálního uzlu, aniž ovlivňuje ostatní iontové kanály. Vykazuje unikátní farmakodynamické vlastnosti, protože zpomaluje SF, aniž má vazodilatační, negativně inotropní, negativně dromotropní či negativně lusitropní* účinky.
Protože ivabradin selektivně snižuje SF, v závislosti na dávce v průměru o 10–15 tepů/min, je velmi účinným antianginózním léčivem. V závislosti na podané dávce vede ke zvýšení tolerance zátěže a zabraňuje vzniku ischémie vyvolané zátěží [29]. Jeho antianginózní a antiischemické účinky jsou naprosto srovnatelné s atenololem i amlodipinem. Ivabradin je velmi dobře tolerován, vůbec neovlivňuje síňokomorové vedení nebo interval QT, nemá negativně inotropní účinky a nesnižuje krevní tlak. Může být proto bezpečně používán v kombinaci se všemi běžně používanými kardiovaskulárními léčivy včetně b-blokátorů. V současnosti je ivabradin registrován v celé řadě zemí pro léčbu stabilní anginy pectoris u nemocných se sinusovým rytmem. Od roku 2007 je ve stejné indikaci registrován a kategorizován i v ČR.
V pilotních studiích u nemocných s ischemickou chorobou srdeční a systolickou dysfunkcí levé komory zvýšil ivabradin tolerovanou zátěž měřenou 6minutovým testem chůzí a vedl ke zmenšení jak diastolického, tak systolického objemu levé komory. To bylo podnětem k provedení velkých mortalitních a morbiditních studií u nemocných se stabilní ischemickou chorobou srdeční, sinusovým rytmem a systolickou dysfunkcí levé komory (studie BEAUTIFUL) a u nemocných s chronickým systolickým srdečním selháním ischemické etiologie (studie SHIFT).
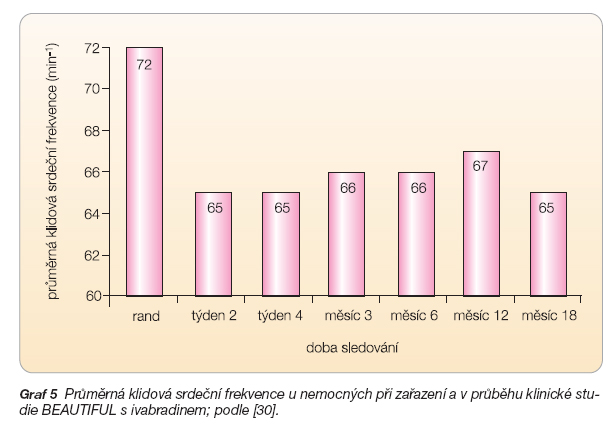
Ve studii BEAUTIFUL bylo randomizováno 10 917 nemocných s průměrným věkem 65 Î 9 roků, s průměrnou hodnotou ejekční frakce 32 6 6 % [30]. Z toho 600 nemocných bylo do studie zařazeno v ČR. Primárním sledovaným klinickým ukazatelem je kombinace kardiovaskulární mortality a závažné kardiovaskulární morbidity (hospitalizace pro infarkt myokardu nebo pro nové či zhoršené srdeční selhání). Průměrná SF při zařazení do studie byla 72 tepů/min, po randomizaci na zaslepenou léčbu (ivabradin dvakrát denně 5–7,5 mg vs. placebo) klesla na 65 tepů/min, tedy v průměru o 7 tepů/min (graf 5).
Je přitom zajímavé, že 87 % nemocných ve studii užívalo b-blokátory. Ivabradin přitom byl velmi dobře tolerován. Nejčastějším nežádoucím účinkem byla bradykardie (< 60 tepů/min), která se vyskytla u 6 % nemocných, symptomatická byla u 4,5 % a k ukončení léčby studovanou medikací vedla jen u 2,4 % nemocných. Dalším častějším nežádoucím účinkem byly oční fosfeny (zrakové vjemy typu záblesků či zářivých kontur v periferii zorného pole), které se vyskytly u 4,5 %, k ukončení studované léčby ale vedly jen u 0,36 % nemocných. Studie BEAUTIFUL (The morBidity-mortality EvAlUaTion of the I(f) inhibitor ivabradine in patients with stable coronary artery disease and left ventricULar dysfunction) byla nedávno ukončena, v současnosti se analyzují výsledky a jejich první prezentaci můžeme očekávat v září 2008 na Evropském kardiologickém kongresu v Mnichově. Do studie SHIFT (The Systolic Heart failure treatment with the I(f) inhibitor ivabradine Trial) má být zařazeno 5500 nemocných s hodnotou ejekční frakce < 30 % a klidovou SF ≥ 70 tepů/min. Primárním sledovaným klinickým ukazatelem je kombinace kardiovaskulární mortality a hospitalizací pro nové nebo zhoršené srdeční selhání. Příjem nemocných do této studie stále ještě probíhá.
Vzhledem ke specifickému mechanismu účinku ivabradinu, který selektivně snižuje SF, budou výsledky těchto dvou velkých mortalitních studií prvním přímým testem významu snížení SF v sekundární prevenci kardiovaskulárních příhod a dají konečně odpověď na otázku, zda prosté zpomalení SF zlepší prognózu kardiovaskulárních nemocných. Zatím prakticky všechny důkazy o vztahu mezi klidovou SF a kardiovaskulární prognózou pocházejí z observačních studií. Ani tyto studie však nepřinesou odpověď na otázku, zda prosté zpomalení SF může prodloužit život i zdravým osobám.
Seznam použité literatury
- [1] Hradec J. Jaká je optimální srdeční frekvence? Cor Vasa 2007; 49: 163–165.
- [2] Palatini P, Benetos A, Grassi G, Julius S, et al. Identification and management of the hypertensive patient with elevated heart rate: statement of a European Society of Hypertension Consensus Meeting. J Hypert 2006; 24: 603–610.
- [3] Jouven X, Empana JP, Buyck JF, et al. Resting heart rate and its changes over years as a risk factor for mortality in the general population: the Paris Prospective Study I. Eur Heart J 2006; 27 (Abstract Suppl.), Abstract 303.
- [4] Kannel WB, Kannel C, Paffenberger RS Jr, Cupples LA. Heart rate and cardiovascular mortality: the Framingham Study. Am Heart J 1987; 1113: 1489–1494.
- [5] Gillum RF, Makuc DM, Feldman JJ. Pulse rate, coronary heart disease, and death: the NHANES I Epidemiological Follow-up Study. Am Heart J 1991; 121: 172–177.
- [6] Jouven X, Empona JP, Schwartz PJ, et al. Heart rate profile during exercise as a predictor of sudden death. N Engl J Med 2005; 352: 1951–1958.
- [7] Wilkinson GS, South JM. Life expectancy, ecology and longevity in bats. Aging Cell 2002; 1: 124–131.
- [8] Benetos A, Thomas F, Bean KE, et al. Role of modifiable risk factors in life expectancy in the elderly. J Hypertens 2005; 23: 1803–1808.
- [9] Heidland UE, Strauer BE. Left ventricular muscle mass and elevated heart rate are associated with coronary plaque disruption. Circulation 2001; 104: 1477–1482.
- [10] Guth BD, Heusch G, Seitelberger R, Ross J Jr. Mechanism of beneficial effect of beta-adrenergic blockade on exercise-induced myocardial ischemia in conscious dog. Circ Res 1987; 60: 738–746.
- [11] Simonsen S, Ihlen H, Kjekshus JK. Haemodynamic and metabolic effects of timolol (Blocadren) on ischaemic myocardium. Acta Med Scand 1983; 213: 393–398.
- [12] The Norwegian Multicenter Study Group. Timolol-induced reduction in mortality and reinfarction in patients surviving acute myocardial infarction. N Engl J Med 1981; 304: 801–807.
- [13] Hjalmarson A, Elmfeldt D, Herlitz J, et al. Effect on mortality of metoprolol in acute myocardial infarction. A double-blind randomised trial. Lancet 1981; 2: 823–827.
- [14] The Beta-Blocker Heart Attack Study Group. The Beta-Blocker Heart Attack Trial preliminary report. JAMA 1981; 246: 2073–2074.
- [15] The Göteborg Metoprolol Trial in acute myocardial infarction. Am J Cardiol 1984; 53: 1D–50D.
- [16] Boissel JP, Leizorovicz A, Picolet H, Peyrieux JC. Secondary prevention after high-risk acute myocardial infarction with low-dose acebutolol. Am J Cardiol 1990; 66: 251–260.
- [17] Kjekshus JK. Importance of heart rate in determining beta-blocker efficacy in acute and long-term acute myocardial infarction intervention trials. Am J Cardiol 1986; 57: 43F–49F.
- [18] Cucherat M. Quantitative relationship between resting heart rate reduction and magnitude of clinical benefits in post-myocardial infarction. A meta-regression of randomized clinical trials. Eur Heart J 2007; 28: 3012–3019.
- [19] Kjekshus J, Gullestad L. Heart rate as a therapeutic target in heart failure. Eur Heart J 1999; 1 (Suppl H): H64–H69.
- [20] Lechat P, Escolano S, Golmard JL, et al. Prognostic value of bisoprolol-induced hemodynamic effects in heart failure during the Cardiac Insufficiency Bisoprolol Study (CIBIS). Circulation 1997; 96: 2197–2205.
- [21] Lechat P, Hulot LS, Escolano S, et al. Heart rate and cardiac rhythm relationship with bisoprolol benefit in chronic heart failure in CIBIS II trial. Circulation 2001; 103: 1428–1433.
- [22] Metra M, Torp-Pedersen C, Swedberg K, et al. Influence of heart rate, blood presssure, and beta-blocker dose on outcome and the difference in outcome between carvedilol and metoprolol tartarate in patients with chronic heart failure: results from the COMET trial. Eur Heart J 2005; 26: 2259–2268.
- [23] Gullestad L, Wikstrand J, Deedwania P, et al. What resting heart rate should one aim for when treating patients with heart failure with a beta-blocker? Experiences from the Metoprolol Controlled Release/Extended Release Randomized Intervention Trial in Chronic Heart Failure (MERIT-HF). J Am Coll Cardiol 2005; 45: 252–259.
- [24] The Multicenter Diltiazem postinfarction Trial Research Group. The effect of diltiazem on mortality and reinfarction after myocardial infarction. N Engl J Med 1988; 319: 385–392.
- [25] The Danish Study Group on Verapamil in Myocardial Infarction. Effect of verapamil on mortality and major events after acute myocardial infarction (The Danish Verapamil Infarction Trial II – DAVIT II). Am J Cardiol 1990; 66: 779–785.
- [26] Hradec J. Can we define an optimal heart rate for all patients? Medicographia 2006; 262–263.
- [27] Beere PA, Glagov S, Zarins CK. Retarding effect of lowered heart rate on coronary atherosclerosis. Science 1984; 226: 180–182.
- [28] Coburn AF, Grey RM, Rivera SM. Observations on the relation of heart rate, life span, weight and mineralization in the digoxin-treated A-J mouse. Johns Hopkins Med J 1971; 128: 169–193.
- [29] Borer JS, Fox K, Jaillon P, Lerebours G. Ivabradine Investigators Group. Antianginal and antiischemic effects of ivabradine, an I(f) inhibitor, in stable angina: randomized, double-blind, multicentered, placebo-controlled trial. Circulation 2003; 107: 817–823.
- [30] The BEAUTIFUL Study Group. The BEAUTIFUL Study: Randomized trial of ivabradine in patients with stable coronary artery disease and left ventricular systolic dysfunction – Baseline characteristics of the study population. Cardiology 2008; 110: 271–282.