Stimulancia užívaná v České republice
Článek je přehledem terapeutických možností v České republice v současné době. Popisuje podrobně farmakologii a klinickou problematiku aplikace metylphenidatu. Zabývá se rovněž problematikou návyku u vybraných stimulancií.
Úvod
Stimulancia mají zásadní význam v psychofarmakologii dětí a dorostu, kde jsou užívána od roku 1937, kdy Bradley publikoval poznatky o pozitivním účinku stimulancií u hyperaktivních dětí s poruchou pozornosti (ADHD). V posledních 20–30 letech je léčba ADHD stimulancii postupně akceptována i u dospělých. Dále jsou stimulancia indikována také u narkolepsie a hypersomnie (léčba je vyhrazena neurologům) (tab. 1).
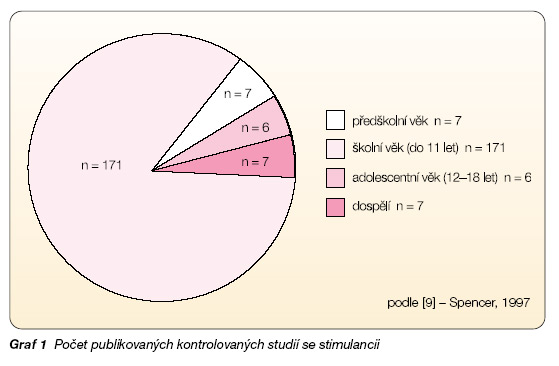
Stimulancia se stala léky první volby u hyperkinetické poruchy (ADHD) dětského i dospělého věku. Tato indikace není v našich zemích dosud zcela známá, jedná se o léčbu bez rizika závislosti vzhledem k biologické odlišnosti jedinců s hyperkinetickou poruchou. Studie z poslední doby prokázaly, že riziko závislosti na běžně zneužívaných drogách u jedinců s ADHD léčených methylphenidatem výrazně klesá. Rozhodující je správná indikace, kterou má vždy provádět psychiatr s erudicí v dané problematice, v dětském věku vždy pedopsychiatr. Graf 1 z roku 1997 dokumentuje výbornou podloženost uvedených tvrzení kontrolovanými klinickými studiemi. Od roku 1997 byla publikována ještě řada dalších klinicky doložených studií.
Stimulancia mohou být výjimečně použita u pacientů se závažným organickým psychosyndromem (např. po proběhlém úrazu hlavy, po zánětlivém onemocnění), ale také u dětí s infantilním autismem ke zlepšení pozornosti a výbavnosti. V americké literatuře je methylphenidat používán v nízkých dávkách jako součást farmakoterapie u některých pacientů se stavy vyčerpání symptomatického původu (např. po závažném somatickém onemocnění).
Stimulancia ovlivňují jak psychické interakce, tak také funkce motorické. Při pokusech se zvířaty jsou výraznější motorické účinky, u člověka ovlivnění psychiky.
Stimulancia jsou převážně sympatomimetické léky. Kromě uváděného methylphenidatu jsou v zahraničí užívány také amphetamin, dexamphetamin. Psychostimulancia spadají mezi psychotropní látky, jejichž distribuce je omezena konvencí OSN skupina II.
Mechanismus účinku
Stimulancia blokují zpětné vychytávání reuptake dopaminu a noradrenalinu na presynaptických neuronech a zvyšují míru uvolňování těchto neurotransmiterů do synaptické štěrbiny. Blokují dopaminový transportér, který je odpovědný za transport dopaminu zpět přes presynaptickou membránu. Psychostimulancia jsou také popisována jako nekatecholaminová sympatomimetika. Mají agonizující efekt na a-adrenergní a b-adrenergní receptory. Tyto látky zde působí jako přímí a nepřímí agonisté. Presynapticky způsobují stimulancia stochiometrické přemístění norepinephrinu ze zásobních depot na presynaptické zakončení [10]. Psychostimulancia působí dopaminergně v nucleus accumbens, kde způsobují oddálení odpovědi, ovlivňují pracovní paměť a ovlivňují rovněž noradrenergní aferentaci z locus coeruleus do prefrontálního kortexu. Některé hypotézy účinku předpokládají, že stimulancia působí stimulačně v prefrontální oblasti a inhibičně v oblasti striatální. D-izomer methylphenidatu má větší účinek na loko-motorickou aktivitu a inhibici reuptake než l-izomer. Methylphenidat má dva asymetrické atomy uhlíku, a proto 4 optické izomery (d- a l-izomer, threo- a erythroizomery. Threoizomer má vyšší potenciál účinku než erythroizomer. Téměř 60° zakřivení mezi terciárními aminy a karbometoxylovými skupinami u threoizomeru je stejné jako u kokainu [3]. U erythroformy je jen slabá vazba mezi dusíkem a karboxylovými atomy [3]. Komerčně vyráběné methylphenidaty mají pouze d-, l-threomethylphenidaty-racemáty. Tím je patrně zčásti vysvětlen rozdíl mezi rizikem vzniku závislosti u kokainu a methylphenidatu. (U kokainu je riziko vysoké, u methylphenidatu velmi malé.)
Absorpce a metabolismus stimulancií
Methylphenidat se váže jen z 15 % na bílkoviny plazmy, velmi snadno proniká hematoencefalickou bariérou a vyskytuje se ve větší koncentraci v CNS než v plazmě. Účinek léku na chování se projeví již v průběhu absorpce, tj. 30 min. po požití. A trvá 3–4 hod. Účinek na chování klesá dříve, než poklesne hladina methylphenidatu v plazmě, a souvisí s poklesem dopaminu v extracelulárním prostoru, který je zřetelně rychlejší než pokles methylphenidatu v plazmě (clockwise hystersis – [4]). Methylphenidat se vylučuje rychle a úplně a není shromažďován v tukových depozitech. Peak methylphenidatu v plazmě vzniká poprvé po půl hodině, tmax se objevuje za 2,5 hodiny. Průměrný poločas vylučování se pohybuje v rozmezí 2–7 hodin (průměrně 3 hodiny). Lék je metabolizován hydrolýzou esterové skupiny za vzniku ritalininové kyseliny. Přibližně 20 % je oxidováno a konjugováno v játrech. Většina pacientů vykazuje lineární vztah mezi dávkou a individuální behaviorální odpovědí. Mohou však vznikat i jiné vztahy mezi dávkou a odpovědí (např. kvadratický vztah mezi dávkou a účinkem). V roce 1977 byla ustanovena optimální dávka 0,3 mg/kg, avšak další výzkumné skupiny tento závěr nepotvrdily.
Lze předpokládat, že i v naší republice bude perspektivně registrován methylphenidat s prodlouženou dobou vylučování (SR), jehož poločas vylučování je 2–6 hod., a klinický účinek je prodloužen až na 8 hodin. Methylphenidat vykazuje široké terapeutické okno. Vztah mezi terapeutickou a letální dávkou v experimentech na zvířeti představuje poměr 1 : 100.
Riziko závislosti
Methylphenidat má malý návykový potenciál, což patrně souvisí také s rozdíly ve farmakokinetice (clockwise hystersis – [4]), dále pak s tím, že v komerčně vyráběném methylphenidatu se nevyskytuje threoforma. Methylphenidat má při perorálním použití minimální schopnost vyvolat euforii [6]. Tento lék není používán jako rekreační droga [5]. V průběhu léčby není potřeba zvyšovat dávku. Po jeho vysazení v průběhu léčby se neobjevují žádné abstinenční příznaky. Riziko závislosti u neléčených hyperkinetických dětí je 10–16 %. Děti s ADHD, které se stanou později závislými, nezneužívají stimulancia. Prospektivní studie ukázaly, že dlouhodobá léčba stimulancii (methylphenidatem) nezvyšuje, ale snižuje riziko závislosti. U závislých pacientů, kteří jsou primárně postiženi ADHD, je k léčbě užíván methylphenidat. Výjimečně se u dospělých toxikomanů v USA vyskytuje intravenózní aplikace methylphenidatu (rozdrcené tablety) a tato forma závislosti může být komplikována pulmonální hypertenzí nebo očními lézemi u zneužívajících pacientů.
Při zneužívání ostatních stimulancií (pervitin, extase apod.) u zdravých osob dochází postupně ke zvyšování tolerance, ta vede ke zvyšování dávky a vysoká dávka relativně může způsobit toxickou psychózu s paranoidními halucinatorními příznaky, které napodobují schizofrenii. Po vysazení dlouhodobě zneužívaných stimulancií se dostaví zvýšená potřeba spánku, zvýšená chuť k jídlu, dysforie a zvýšené snění. U pacientů léčených stimulancii pro hyperkinetický syndrom riziko závislosti na stimulanciích po jejich vysazení nestoupá.
Kognitivní účinky stimulancií
Methylphenidat zvyšuje exekutivní kontrolní procesy, zlepšuje inhibiční kontrolu a funkci provozní paměti u dětí s ADHD. Stimulancia zlepšují kvalitu pozornosti, upravují reakční čas, zlepšují krátkodobou paměť a proces učení. Stimulancia výrazně snižují nepozornost a těkavost, zvyšují akademickou produktivitu a výkonnost.
Důležitá je otázka dávkování stimulancií. Dávkování je nutno upravit vždy zcela individuálně s ohledem na jednotlivé příznaky a školní výsledky dětí a adolescentů a pracovní výsledky dospělých. Řada výzkumů prokázala, že léčba dětí, dorostu i dospělých stimulancii má kladný vliv na vztahy v rodině a celkovou rodinnou interakci. Děti pak spíše vyhoví příkazům a matky jsou zase méně kritické a vřelejší. Totéž platí pro komunikaci s vrstevníky u dětí i dospělých.
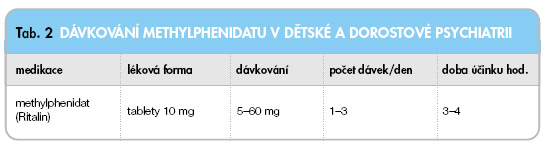
Dávkování stimulancií v dětské psychiatrii
V současné době je v ČR užíván pouze methylphenidat (tab. 2).
Dávkování stimulancií v psychiatrii dospělých
Standardní dávkování u dospělých pacientů s ADHD není dosud stanoveno. Bylo však již publikováno více než 10 dvojitě slepých placebem kontrolovaných studií a větší počet studií otevřených, takže s touto terapií je dostatek zkušeností. Začíná se nejnižší dávkou 10 mg 1–3krát denně u methylphenidatu. Tato dávka se jedenkrát týdně zvyšuje až do dosažení žádaného účinku. Methylphenidat je podáván v dávce 10–90 mg denně. Preparát je v zahraničí často podáván také ve formě retardovaných tablet. Krátký poločas vylučování může způsobit rebound fenomén. Tomu lze odpomoci podáváním léku vícekrát denně. Pokud se účinek nedostaví do dvou týdnů po optimalizaci dávky, je podávání léku bezpředmětné. Při indikaci stimulancií (methylphenidatu) v dospělosti je třeba přesně stanovit diagnózu. Je nutné prokázat léčenou nebo neléčenou hyperkinetickou poruchu ve školním věku (mezi 6.–10. rokem) pomocí osobní anamnézy. V rodině pacienta se často vyskytuje hyperkinetická porucha u rodičů, event. u prarodičů nebo sourozenců. Diagnózu doplňujeme škálovacími postupy, např. škálou Wenderovou. Překlad škály jsme publikovali v Remediích [7]. V jednotlivých případech bývá medikace methylphenidatem výhodná u dospělých pacientů s organickým psychosyndromem různé etiologie a u pacientů s exhaustivními syndromy po závažných somatických onemocněních.
Dlouhodobé terapeutické účinky stimulancií
Podrobné studie ukazují, že perspektiva dětí a adolescentů s ADHD se výrazně zlepšuje, u dospělých s ADHD ubývá morozity, vznětlivosti, v některých případech i agresivity. U dětí se výrazně zlepšuje soustředění a tím i výkonnost ve škole, u adolescentů a dospělých se zlepšují výsledky ve studiu a v zaměstnání. Sekundárně se zlepšují i perspektivy ve vztazích s ostatními lidmi, ve vztazích s rodiči a učiteli, u adolescentů a dospělých ve vztazích partnerských a profesionálních. Úbytek hyperaktivity a impulzivity výrazně snižuje rizika konfliktů a nedorozumění. Zlepšuje se i perspektiva léčby komorbidních poruch, např. deprese, úzkosti apod.
Nežádoucí účinky stimulancií
Krátkodobé nežádoucí účinky závisí u jednotlivých pacientů na dávce a jejich intenzita je u většiny dětí jen mírná. Ze 4200 pacientů ve 110 studiích sumarizovaných Barkleyem a kol. v roce 1990 musela jen 4 % předčasně ukončit léčbu kvůli nežádoucím účinkům medikace. K nejběžnějším patří nespavost, snížená chuť k jídlu, úbytek hmotnosti, bolesti břicha, hlavy, dráždivost a zvýšená plačtivost. Mírně může stoupnout i tepová frekvence a výjimečně i krevní tlak. V některých studiích bývá doporučován ke korekci nespavosti diphenhydramin, gastrointestinálním symptomům lze předejít podáváním léku mezi jídlem.
Časté nejsou ani tiky, které vzniknou u 1 % dětí léčených stimulancii. U 13 % se zhorší tiky již existující, z toho důvodu nepovažujeme za vhodné podávání stimulancií dětem, u kterých se tiky již vyskytují. U některých dětí se po vyloučení léku (poločas vylučování je 2,5–3 hodiny) může projevit opětovné mírné nebo výraznější zhoršení hyperkinetického syndromu. Tomu lze zabránit úpravou frekvence podávání léku.
Psychotické komplikace po podání stimulancií pro ADHD jsou naprosto raritní a rychle se upraví po vysazení léku a podání antipsychotika.
Zcela ojediněle se může objevit vypadávání vlasů, leukocytóza, pruritus, kožní vyrážky, event. zvýšená teplota. U dětí se sníženým záchvatovým prahem, pokud je to nutné, je vhodné podávat stimulancia v kombinaci s antikonvulzivy.
Dlouhodobé nežádoucí účinky stimulancií
Sem patří především účinky stimulancií na výšku a hmotnost dětí, ty jsou však klinicky jen málo významné. Stimulancia snižují poněkud chuť k jídlu, což je u většiny pacientů vzhledem k časté obezitě dětí i dospělých spíše výhodou. Je proto vhodné sledovat při kontrolách také hmotnost dítěte. Jen někdy je žádoucí, aby dítě, event. i dospělý, zařadili terapeutické prázdniny v délce jednoho až dvou měsíců za rok, event. vynechali methylphenidat jeden den v týdnu (o víkendu), tím ještě klesá možnost lékového ovlivnění hmotnosti léčeného pacienta.
Lékové interakce
Souhrnně platí, že kombinace stimulancií s jinými léky se většinou nedoporučuje. Kombinace s blokátory MAO mohou způsobit prudké zvýšení krevního tlaku s rizikem vážných komplikací. Nevhodná je kombinace s kofeinem a centrálními analeptiky. Stimulancia potencují účinek warfarinu. Kombinace s antiastmatiky může vést k závratím, tachykardii, palpitaci a agitovanosti. Stimulancia mohou také interferovat s tricyklickými antidepresivy, a proto je jejich kombinace až na zcela ojedinělé výjimky nevhodná. Stimulancia mohou rovněž blokovat antihypertenzní působení guanethidinu.
Methylphenidat inhibuje izoenzym P-450 2D6, a proto může zvyšovat sérové hladiny léků, které jsou tímto cytochromem metabolizovány. Podávání stimulancií v kombinaci s anxiolytiky je nevhodné vzhledem k možné paradoxní reakci na tuto kombinaci (potenciace úzkosti a neklidu).
Kontraindikace
Stimulancia jsou kontraindikována ke zvyšování psychické výkonnosti nebo pro zlepšení soustředění u zdravých jedinců. Vzniká riziko závislosti (u methylphenidatu je nevýznamné).
Stimulancia jsou kontraindikována u středně těžké nebo těžké depresivní poruchy pro riziko potenciace suicidiálního chování, psychotických stavů, mánie, mentální anorexie, schizotypálních osobností. Stimulancia rovněž nepodáváme u pacientů, v jejichž osobní a rodinné anamnéze se vyskytovaly psychózy.
V somatické medicíně nelze podávat stimulancia při hypertenzi, tyreotoxikóze, tachyarytmii, angině pectoris a ischemické chorobě srdeční, u kardiomyopatií a infarktu myokardu.
Závěrečné poznámky, stimulancia v ambulantní praxi
Stimulancia představují bezpečnou léčbu v případě správné indikace, která přísluší dětskému psychiatrovi, psychiatrovi pro dospělé a u narkolepsie neurologovi.
Výhledově lze předpokládat i v České republice zavedení methylphenidatu s prodlouženým uvolňováním, který zlepšuje účinnost a uživatelský komfort u ADHD.
Podávání methylphenidatu nevede u pacientů s ADHD v dětském a dospělém věku k závislosti, pokud je diagnóza správně stanovena. Naopak, podávání methylphenidatu u těchto pacientů riziko závislosti snižuje.
Seznam použité literatury
- [1] Barkley R, McMurray M, Edelbrock C, Robbins K. Side effects of MPH in children with attention deficit hyperactivity disorder: A systematic placebo-controlled evaluation. Pediatrics 1990; 86: 184–192.
- [2] Bradley C. The Behavior of Children Receiving Benzedrine. Am J Psychiatry 1937; 94: 577–585.
- [3] Buckner CK, Patil PN, Tye A, Malspeis L. Steric aspects of adrenergic drugs. XII. Some peripheral effect of (+/-) – erythro-and (+/-)-threo-methylphenidate. Journal of Pharmacology and Experimental Therapeutics 1969; 166: 308–319.
- [4] Cox BM. Drug tolerance and physical dependence. In W. B. Pratt, P. Taylor (Eds.) Principles of drug action: The basis of pharmacology. New York, Churchil Livingstone, 1990.
- [5] Gittelman R, Mannuza S. Hyperactive boys almost grown up: III. Methylphenidate effects on ultimate height. Archives of General Psychiatry 1988; 45: 1131–1134.
- [6] Klein D. Treatment of anxiety, personality, somatoform and factitious disorders. In: D. Klein, R. Gittelman, F. Quitkin, A. Rifkin (Eds.) Diagnosis and drug tratment of psychiatric disorders: Adults and children. Baltimore, Williams and Wilkins, 1980.
- [7] Paclt I. Hyperkinetický syndrom v dospělosti. Remedia 2001; 11: 401–411.
- [8] Raboch J, Jirák R, Paclt I. Psychofarmakologie pro praxi. Praha, Triton, 2005.
- [9] Spencer TJ. Summary of medication trials of ADHD adults at Mass. general hospital. Dopaminergic disorders II. Ritz-Carlton, Boston-Boston, 28.–30. 4.1997.
- [10] Weiner N. Drugs that inhibit adrenergic nerves and block adrenergic receptors. In A. Gilman, L. Goodman (Eds.). Norepinephrine, epinephrine and the sympathomimetic amines. New York: Pharmacological Basis of Therapeutics, 1991.