Technologické novinky v diabetologii
Diabetes mellitus je celosvětově rozšířené chronické onemocnění se značným dopadem na morbiditu a mortalitu pacientů. Rychle se rozvíjející technologie pomáhají pacientům dosáhnout optimální kompenzace diabetu a tím oddálit a omezit rozvoj pozdních komplikací. Mezi hlavní technologické milníky v diabetologii patří vývoj senzorů pro kontinuální měření glykemie a systémy pro kontinuální aplikaci inzulinu. Ideálem by bylo vytvoření tzv. uzavřeného okruhu pacient-senzor-pumpa s automatickou regulací dodávky inzulinu bez nutnosti zásahu pacienta. Následující článek se zabývá přehledem technologií používaných v současné diabetologii a výhledem do budoucnosti.
Úvod
Diabetes mellitus je celosvětově rozšířené onemocnění s potenciálně závažnými komplikacemi. Jediným dosud prokázaným faktorem snížení rizika rozvoje makro- i mikrovaskulárních komplikací je dosažení co nejtěsnější kompenzace v podobě téměř normální hladiny glykovaného hemoglobinu [1, 2]. Nicméně dosažení a udržení těsné kompenzace je spojeno s vyšším rizikem vzniku hypoglykemií, které, jak bylo prokázáno řadou studií, zvyšují morbiditu a mortalitu ve všech věkových skupinách a morbiditu u malých dětí [3]. Dalším faktorem, který se zřejmě může podílet na morbiditě a mortalitě diabetiků, je glykemická variabilita. Je prokázána asociace glykemické variability s oxidačním stresem, endoteliální dysfunkcí a hypoglykemií [4]. Ideální léčba diabetika by měla vést k dosažení normálních glykemií bez výskytu jejich velkých vzestupů a poklesů.
Podmínkou dosažení těsné kompenzace diabetu je častý selfmonitoring (samostatné měření glykemie), kvalitní léky s nízkým rizikem vzniku hypoglykemií, inzuliny s vyrovnanými profily a nástroje k aplikaci inzulinu. K tomu všemu nám pomáhají dostupné technologie, které můžeme rozdělit na dvě skupiny: systémy pro měření glykemie (selfmonitoring) a systémy umožňující aplikaci inzulinu.
Systémy pro měření glykemie
Glukometry jsou přístroje sloužící k měření glykemie z kapilární krve v ambulantních podmínkách. V současné době stačí ke změření glykemie jen minimální objem krve, 0,3–1,5 µl dle typu glukometru a k vlastnímu stanovení využívají glukózo-oxidázové nebo glukózo-dehydrogenázové reakce. Ačkoli je k měření používána plná krev, jsou výstupy glukometru většinou kalibrovány na hodnoty korelující s plazmatickou koncentrací glukózy. Aktuálně je na trhu přítomna celá škála glukometrů různých výrobců. Rozdíly mezi jednotlivými glukometry spočívají v jejich odolnosti vůči měření v teplotních extrémech či v nadmořské výšce. Dále se liší v obohacení měřicích proužků pomocnými substancemi, které eliminují vliv např. maltózy, askorbátu a aceteminofenu na přesnost měření. A v neposlední řadě se tyto výrobky liší nabídkou dalších funkcí umožňujících hlubší analýzu naměřených hodnot glykemie. Všechny schválené glukometry ovšem splňují odchylku naměřených hodnot v normálním rozmezí do 15–20 % od laboratorně stanovené plazmatické glykemie [5]. Speciální funkcí je např. možnost zadávání poměru inzulin/karbohydráty, korekčního faktoru (citlivosti na inzulin) a cílové glykemie. Glukometr pak na podkladě zadaných hodnot dokáže vypočítat odhad bolusové dávky inzulinu nutné k pokrytí požitých sacharidů a k dosažení cílové glykemie. Technologicky vyspělé glukometry dále umožňují radiofrekvenční komunikaci s inzulinovými pumpami a tím automatický přenos změřených glykemií do „chytrých“ inzulinových pump k výpočtu individuálních dávek inzulinu. Nejmodernější inzulinové pumpy komunikují přímo se spárovanými senzory pro kontinuální měření glykemie a zobrazují naměřené hodnoty glykemie přímo na displeji pumpy.
Důležitým faktorem výběru glukometru je jeho schopnost nahrávat naměřená data přes USB konektory počítače do databází umožňujících jejich další hlubší analýzu. Takovými systémy jsou například Carelink, Diasend a Diabass. Některé glukometry jsou schopny propojit se s online databázemi pomocí mobilních telefonů (LG) nebo dokáží přeměnit „chytrý telefon“ (iPhone, iTouch) v glukometr (systém iBG Star Blood Glucose Meter). Online databáze slouží v rámci tzv. telemedicíny k telefonickým nebo mailovým konzultacím pacienta a jeho ošetřujícího lékaře (pacient nahraje doma data z glukometru do databáze a lékař po jejich zhodnocení kontaktuje pacienta s návrhem dalšího postupu).
Systémy pro kontinuální měření glykemie (CGMS) umožňují téměř v reálném čase měřit a zobrazovat hodnoty koncentrace glukózy v intersticiální tekutině. Vlastní měření probíhá malým, do podkoží zavedeným senzorem potaženým glukózooxidázovým enzymem. Elektrochemický signál je radiofrekvenčně přenášen do příjímače, kde je následně převeden na hodnotu glykemie. Přijímačem může být samostatná jednotka (DexCom, Freestyle Navigator, Medtronic Guardian, iPro), nebo inzulinová pumpa (MiniMed/Medtronic, Animas). Zavedené senzory v podkožní tkáni jsou schopny měřit v 1–5minutových intervalech po dobu 3 až 10 dnů [6]. K zajištění dostatečné přesnosti jsou nutné pravidelné kalibrace CGMS glykemiemi z glukometru. Přesnost CGMS se obecně pohybuje v rozmezí ±20 % aktuální glykemie z glukometru [7]. Jednou z překážek dosažení lepší přesnosti je časové zpoždění koncentrace glukózy mezi arteriální krví a intersticiální tekutinou (tzv. lag-time). Zpoždění je dáno jednak dobou nutnou k vyrovnání koncentrací glukózy v krvi a intersticiální tekutině a jednak technologickým zpožděním během zpracování signálu elektronikou senzoru. Lag-time se dle typu senzoru pohybuje mezi 8–20 minutami, přičemž se prodlužuje při rychlých změnách glykemie [8].
Výhody CGMS s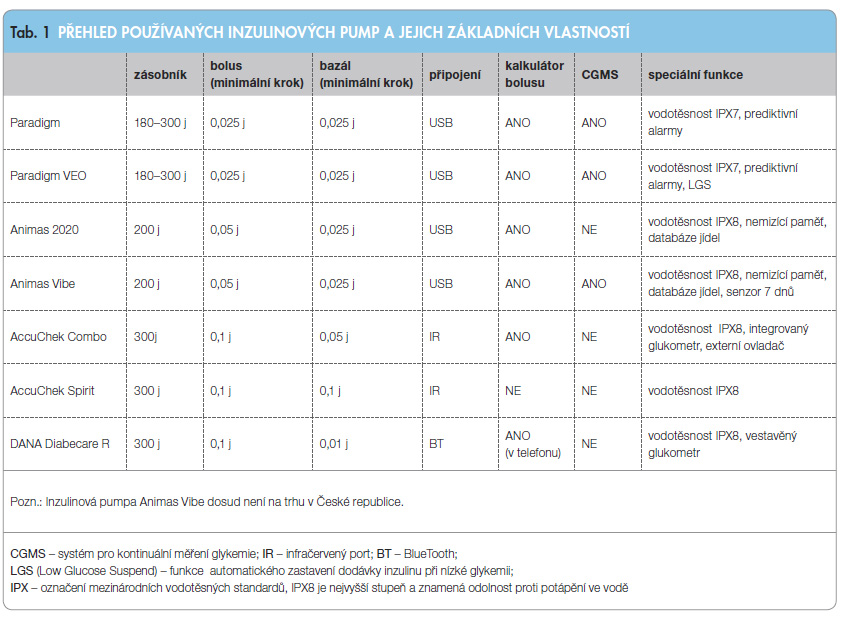 počívají v kontinuálním záznamu glykemií umožňujícím identifikaci postprandiálních hyperglykemií, nočních nebo nerozpoznaných hypoglykemií, analýzu a zobrazení trendů a predikci dalšího vývoje glykemií, což pacientovi umožňuje reagovat dříve, než nastane nežádoucí situace. Nevýhodou je nutnost pravidelného a častého „nošení“ senzoru pacientem – studie prokazují efekt CGMS až tehdy, je-li používán minimálně 60–70 % času (tzn. minimálně 5 dnů v týdnu); další nevýhodou je stále ještě poměrně vysoká cena tohoto zařízení [9].
počívají v kontinuálním záznamu glykemií umožňujícím identifikaci postprandiálních hyperglykemií, nočních nebo nerozpoznaných hypoglykemií, analýzu a zobrazení trendů a predikci dalšího vývoje glykemií, což pacientovi umožňuje reagovat dříve, než nastane nežádoucí situace. Nevýhodou je nutnost pravidelného a častého „nošení“ senzoru pacientem – studie prokazují efekt CGMS až tehdy, je-li používán minimálně 60–70 % času (tzn. minimálně 5 dnů v týdnu); další nevýhodou je stále ještě poměrně vysoká cena tohoto zařízení [9].
Systémy pro aplikaci inzulinu
 Nejstarším zařízením pro aplikaci inzulinu jsou inzulinové stříkačky, tzv. inzulinky. V současné době jsou jimi pacienti vybavováni k podání inzulinu v případě selhání sofistikovanějších aplikačních systémů. Nejrozšířenějším aplikačním systémem jsou inzulinová pera, zařízení, která umožňují po vložení inzulinové cartridge přesné a pohodlné dávkování inzulinu. Některá inzulinová pera jsou vybavena elektronikou zaznamenávající datum, čas a velikost poslední dávky inzulinu. Aktuálním trendem je ale odklon od sofistikovaných inzulinových per k jednoduchým předplněným dávkovačům – pacient jej po využití vyhodí a použije nový.
Nejstarším zařízením pro aplikaci inzulinu jsou inzulinové stříkačky, tzv. inzulinky. V současné době jsou jimi pacienti vybavováni k podání inzulinu v případě selhání sofistikovanějších aplikačních systémů. Nejrozšířenějším aplikačním systémem jsou inzulinová pera, zařízení, která umožňují po vložení inzulinové cartridge přesné a pohodlné dávkování inzulinu. Některá inzulinová pera jsou vybavena elektronikou zaznamenávající datum, čas a velikost poslední dávky inzulinu. Aktuálním trendem je ale odklon od sofistikovaných inzulinových per k jednoduchým předplněným dávkovačům – pacient jej po využití vyhodí a použije nový.
 Nejfyziologičtější aplikaci inzulinu představují inzulinové pumpy, které umožňují aplikaci bazální dávky inzulinu po krocích o velikosti 0,025 IU a bolusů po krocích od 0,05 IU (tab. 1). K vlastní aplikaci inzulinu používají buď tenké kanyly s katétrem zavedeným do podkoží, nebo jsou připojeny přímo na povrch těla a katétr je na spodní straně (patch) pumpy [10]. Současné pumpy jsou schopny kalkulovat doporučenou dávku bolusu inzulinu na podkladě vložených informací o množství požitých sacharidů, aktuální glykemii a poměru inzulin/karbohydráty. Pumpy MiniMed/Medtronic a Animas (obr. 1 a obr. 2) přímo komunikují se svými senzory pro kontinuální měření glykemie, čímž spojují výhody inzulinové pumpy a CGMS.
Nejfyziologičtější aplikaci inzulinu představují inzulinové pumpy, které umožňují aplikaci bazální dávky inzulinu po krocích o velikosti 0,025 IU a bolusů po krocích od 0,05 IU (tab. 1). K vlastní aplikaci inzulinu používají buď tenké kanyly s katétrem zavedeným do podkoží, nebo jsou připojeny přímo na povrch těla a katétr je na spodní straně (patch) pumpy [10]. Současné pumpy jsou schopny kalkulovat doporučenou dávku bolusu inzulinu na podkladě vložených informací o množství požitých sacharidů, aktuální glykemii a poměru inzulin/karbohydráty. Pumpy MiniMed/Medtronic a Animas (obr. 1 a obr. 2) přímo komunikují se svými senzory pro kontinuální měření glykemie, čímž spojují výhody inzulinové pumpy a CGMS.
 Přes všechny technologie, které máme v současné době k dispozici, se stále nedaří dosáhnout optimální kompenzace u většiny diabetiků. CGMS vede ke zlepšení hodnot glykovaného hemoglobinu, a to hlavně ve spojení s inzulinovou pumpou, kdy zlepšení činí až 0,5 % (5 mmol/mol dle aktuální normy platné v ČR) a sníží glykemickou variabilitu [11]. Dále mají z používání CGMS prospěch hlavně diabetici starší 25 let, u mladší generace
Přes všechny technologie, které máme v současné době k dispozici, se stále nedaří dosáhnout optimální kompenzace u většiny diabetiků. CGMS vede ke zlepšení hodnot glykovaného hemoglobinu, a to hlavně ve spojení s inzulinovou pumpou, kdy zlepšení činí až 0,5 % (5 mmol/mol dle aktuální normy platné v ČR) a sníží glykemickou variabilitu [11]. Dále mají z používání CGMS prospěch hlavně diabetici starší 25 let, u mladší generace 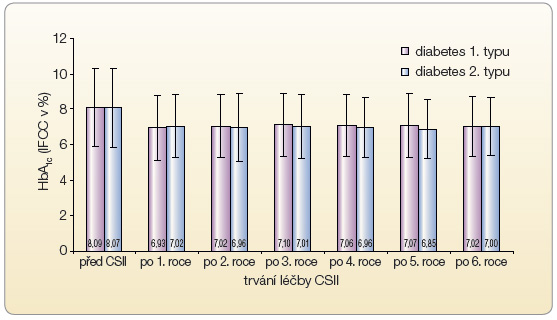 jsou dosavadní výsledky studií rozporuplné a odráží je i platné doporučení Americké diabetologické společnosti [12]. CGMS na druhou stranu zatím neprokázal efekt na snížení incidence těžkých hypoglykemií [13].
jsou dosavadní výsledky studií rozporuplné a odráží je i platné doporučení Americké diabetologické společnosti [12]. CGMS na druhou stranu zatím neprokázal efekt na snížení incidence těžkých hypoglykemií [13].
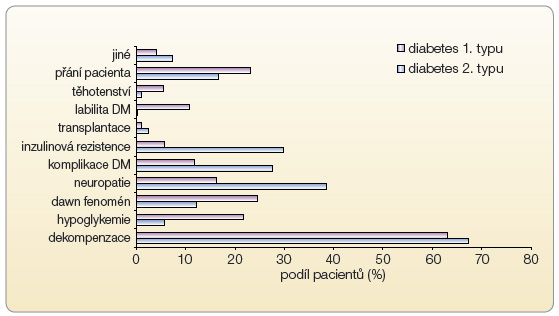
V České republice funguje od roku 1998 Národní registr pacientů léčených inzulinovou pumpou, který sbírá jak demografická data zařazených pacientů, tak i údaje o jejich kompenzaci a výskytu komplikací. Aktuálně jsou v registru data od 4500 diabetiků (celkový odhadovaný počet diabetiků léčených pomocí inzulinové pumpy je cca 6000), přičemž zhruba 89 % diabetiků je 1. typu a 9 % tvoří pacienti s diabetem 2. typu. Na podkladě údajů z Registru jsme schopni říci, že pacienti využívající inzulinovou pumpu zlepší kompenzaci průměrně o 1 % (10 mmol/mol) glykovaného hemoglobinu a tuto kompenzaci jsou schopni udržet v čase (graf 1 a graf 2) [14].
Budoucnost na závěr
Existující modely inzulinových pump jsou neustále zdokonalovány, technicky propracovávány a obohacovány o další funkce, které by měly napomoci zvýšení jejich bezpečnosti a funkčnosti. Např. inzulinová pumpa MiniMed/Medtronic VEO ve spojení s CGMS zastavuje na přechodnou dobu dodávku inzulinu při dosažení hypoglykemie, na kterou pacient nereaguje [15]. Pozornost zasluhuje i vylepšené hodnocení a zobrazení dat senzoru CGMS u inzulinové pumpy Animas Vibe se senzorem Dexcom G4. Implementace sofistikovaných funkcí do inzulinových pump, včetně samostatné reakce na naměřené glykemie, je předstupněm uzavření okruhu pumpa-senzor-pacient. Dokončení uzavřeného okruhu automatického řízení glykemie bez nutnosti zásahu pacienta je v posledním desetiletí cílem úsilí řady odborníků po celém světě. Dokončení plně funkčního uzavřeného okruhu brání i přes vyvinuté sofistikované řídicí algoritmy mimo jiné i zatím ještě relativně nízká přesnost kontinuálních senzorů a dlouhý biologický poločas používaných inzulinových analog [16].
Probíhá vývoj senzorů pro kontinuální monitorování glykemie ve snaze o jejich miniaturizaci a neinvazivnost. Naděje jsou vkládány do vývoje transdermálního optického systému, který využívá fluorescence flouroforem značeného glukózu vázajícího proteinu (Symphony tCGM), nebo do vývoje neenzymatických senzorů založených na nanočásticích vzácných kovů a hydrogelech [17, 18].
„Hudbou budoucnosti“ už není ani „chytrý“ inzulin, který se uvolňuje v závislosti na koncentraci glukózy v organismu. Společnost Biodel vyvíjí bazální inzulin, který se uvolňuje proporcionálně ke koncentraci glukózy v intersticiální tekutině a tím zlepšuje dosažení fyziologické koncentrace glukózy [19].
Podpořeno projektem Ministerstva zdravotnictví koncepčního rozvoje výzkumné organizace 00669806 – FN Plzeň.
Seznam použité literatury
- [1] Pop-Busui R, Herman WH, Feldman EL, et al. DCCT/EDIC Research Group DCCT and EDIC studies in type 1 diabetes: lessons for diabetic neuropathy regarding metabolic memory and natural history. Curr Diab Rep 2010; 10: 276–282.
- [2] White NH, Sun W, Cleary PA, et al. DCCT-EDIC Research Group Effect of prior intensive therapy in type 1 diabetes on 10-year progression of retinopathy in the DCCT/EDIC: comparison of adults and adolescents. Diabetes 2010; 59: 1244–1253.
- [3] Bloomfield HE, Greer N, Newman D, et. al. Predictors and Consequences of Severe Hypoglycemia in Adults with Diabetes – A Systematic Review of the Evidence [Internet]. Washington (DC): Department of Veterans Affairs; 2012 Apr.
- [4] Ceriello A, Esposito K, Piconi L, et. al. Glucose “peak” and glucose “spike”: Impact on endothelial function and oxidative stress. Diabetes Res Clin Pract 2008; 82: 262–267.
- [5] Heinemann L. Quality of glucose measurement with blood glucose meters at the point-of-care: relevance of interfering factors. Diabetes Technol Ther 2010; 12: 847–857.
- [6] Mamkin I, Ten S, Bhandari S, Ramchandani N. Real-time continuous glucose monitoring in the clinical setting: the good, the bad, and the practical. J Diabetes Sci Technol 2008, 2: 882–889.
- [7] Kovatchev BP, Gonder-Frederick LA, Cox DJ, Clarke WL. Evaluating the accuracy of continuous glucose-monitoring sensors: continuous glucoseerror grid analysis illustrated by TheraSense Freestyle Navigator data. Diabetes Care 2004; 27: 1922–1928.
- [8] Keenan DB, Mastrototaro JJ, Voskanyan G, Steil GM. Delays in minimally invasive continuous glucose monitoring devices: A review of current technology. J Diabetes Sci Technol 2009; 3: 1207–1214.
- [9] Bergenstal RM, Tamborlane WV, Ahmann A, et. al. Effectiveness of sensor-augmented insulin-pump therapy in type 1 diabetes. N Engl J Med 2010; 363: 311–320.
- [10] Anhalt H, Bohannon NJ. Insulin patch pumps: their development and future in closed-loop systems. Diabetes Technol Ther 2010; 12 (Suppl 1): S51–S58.
- [11] Misso ML, Egberts KJ, Page M, et al. Continuous subcutaneous insulin infusion (CSII) versus multiple insulin injections for type 1 diabetes mellitus. Cochrane Database of Systematic Reviews 2010, Issue 1. Art. No.: CD005103. DOI:10.1002/14651858.CD005103.pub2.
- [12] American Diabetes Association, Standards of Medical Care in Diabetes – 2013, Diabetes Care 2013; 36: S11-S66; doi:10.2337/dc13-S011.
- [13] Langendam M, Luijf YM, Hooft L, et al. Continuous glucose monitoring systems for type 1 diabetes mellitus. Cochrane Database Syst Rev 2012 Jan 18; 1:CD008101. doi: 10.1002/14651858.CD008101.pub2. Review.
- [14] Jankovec Z, et al. Analysis of continuous patient data from the Czech National Register of patients with type 1 and type 2 diabetes using insulin pump therapy. Diab Res Clin Pract 2009, doi:10.1016/j.diabres.2009.09.028.
- [15] Jankovec Z. Možnosti léčby inzulinovými pumpami. Interní Med 2012; 14: 116–118.
- [16] Weinstock RS. Closing the Loop: Another Step Forward. Diabetes Care 2011; 34: 2136–2137.
- [17] Saxl T, Khan F, Ferla M, et al. A fluorescence lifetime-based fibre-optic glucose sensor using glucose/galactose-binding protein. Analyst 2011; 136: 968–972.
- [18] Nie H, Yao Z, Zhou X, et al. Nonenzymatic electrochemical detection of glucose using well-distributed nickel nanoparticles on straight multi-walled carbon nanotubes. Biosens Bioelectron 2011; 30: 28–34.
- [19] http://www.biodel.com/content/pipeline/biod-smartbasal.htm