Dupilumab
Souhrn:
Středně těžká až těžká atopická dermatitida (atopický ekzém, AE) představuje významnou fyzickou a psychologickou zátěž pro pacienty v mnoha směrech, dále je také nezanedbatelný ekonomický dopad na pečovatele a plátce. Za posledních 15 let od schválení dvou lokálních inhibitorů kalcineurinu (takrolimu a pimekrolimu) nebyly schváleny žádné nové terapie zaměřené na léčbu AE, což pro pacienty, u nichž stávající dostupná léčebná strategie nebyla úspěšná, bylo velmi traumatické. První nově dostupnou látkou v této oblasti je dupilumab, který se vyznačuje cíleným mechanismem účinku, takže na rozdíl od existujících nespecifických imunosupresivních látek, které mají nepříznivé vedlejší účinky, může být používán dlouhodobě. Dupilumab je lidská monoklonální protilátka třídy IgG4, která se specificky váže na podjednotku receptoru IL‑4Ra a přerušuje signalizační kaskádu zprostředkovanou cytokiny IL‑4 a IL‑13. Dupilumab tak účinně blokuje specificky tento úsek Th2 řízené imunitní odpovědi. Léčba dupilumabem vede k potlačení aberantního zánětu a k částečné normalizaci profilu genové exprese kůže AE. Dupilumab zlepšuje kožní bariéru díky up‑regulaci genů kódujících proteiny, které se podílejí na epidermální struktuře, a také díky svému účinku na snížení intenzity svrbění. Stejně tak terapie dupilumabem vede i k redukci rizika kožní infekce. Klinické studie ukázaly, že terapie dupilumabem výrazně zmírňuje symptomy AE (včetně pruritu a vlivu na spánek), což následně způsobilo klinicky významný pokles výskytu úzkosti a deprese a tím také celkové zlepšení kvality života.
Summary:
Atopic dermatitis (AD) is a chronic, systemic immune‑mediated disease marked by persistent underlying inflammation. Patients with AD experience extensive eczematous skin lesions and debilitating symptoms, including intense pruritus, pain & discomfort, and significant sleep disruption. Patients with AD often experience symptoms of anxiety and/or depression. The disease is associated with higher health care resource utilization and productivity loss than in less severe forms of the disease. In the last 15 years, since the approval of two local calcineurin inihibitors (tacrolimus and pimecrolimus), no new therapies for AE treatment were approved which was very frustrating for patients in whom no available therapy was successful. Dupilumab is a novel recombinant human immunoglobulin IgG4 monoclonal antibody that inhibits interleukin‑4 (IL‑4) and interleukin‑13 (IL‑13) signaling by specifically binding to the IL‑4Rα subunit shared by the IL‑4 and IL‑13 receptor complexes and is the first treatment to target the underlying type 2 (including Th2) inflammation associated with AD. In adults with moderate to severe AD, in combination with topical corticosteroids or in monotherapy, dupilumab provides rapid and sustained improvements in lesion extent and severity, pruritus and sleep disturbance. Treatment with Dupixent® leads to a reversal in both the gene expression profile of atopic dermatitis, and specific markers of inflammation and reduces the frequency of exacerbations and skin infections. Clinical studies have shown that the therapy with dupilumab significantly lowers AE symptoms (including pruritus and sleep disturbances) that leads to clinically pronounced decrease in depression and anxiety and the overall quality of life.
Key words: atopic dermatitis, systemic treatment, dupilumab.
Patofyziologie atopické dermatitidy
Atopická dermatitida (AD) je silně svědivé chronicky recidivující neinfekční zánětlivé kožní onemocnění charakteristické variabilitou morfologie i průběhu. Jedná se o chorobu multifaktoriální – genetická dispozice vede k dysfunkci kožní bariéry a k imunologické dysbalanci, jež jsou navzájem provázané a vyvolávají hyperreaktivitu kůže [1,2]. Zhruba u 80 % pacientů je AD spojena se zvýšeným rizikem vzniku dalších atopických onemocnění (např. alergické rinokonjunktivitidy, bronchiálního astmatu) a alergie na potraviny a na aerogenní alergeny [3,4]. Atopická dermatitida se nejčastěji vyvíjí v průběhu kojení a raného dětství, ale u některých pacientů může přetrvávat i v dospělosti. Přibližně 70–85 % dospělých pacientů udává vznik onemocnění v kojeneckém věku nebo v dětství [5–7]. Atopická dermatitida se však může poprvé vyskytnout až v dospělém věku („late onset AD“); obvykle více svědí, je chroničtější a závažnější [8,9].
Atopická dermatitida je onemocnění způsobené CD4+ pomocnými T lymfocyty (Th2). Th2 lymfocyty tvoří cytokiny interleukin 4 (IL 4) a interleukin 13 (IL 13), které jsou klíčovými mediátory AD a dalších atopických onemocnění [10]. Nitrobuněčné signalizační kaskády aktivované prostřednictvím IL 4 a IL 13 vedou ke zvýšené expresi jiných cytokinů a chemokinů typu 2 a následně k aktivaci dalších typů zánětlivých buněk (lymfocytů B a T, monocytů, eozinofilů), což výrazně ovlivňuje funkci epidermální bariéry [1–3]. Porucha kožní bariéry s sebou nese poruchy hydratace kůže. U atopiků abnormity extracelulárních lipidů ve stratum corneum, hlavně deficience ceramidů, výrazně přispívají k poruše bariérové funkce [11].
V důsledku toho, že si kůže pacienta s AD není schopna zachovat hydrataci, se voda odpařuje, kůže se svrašťuje, praská, a ještě více se vysuší. Ztráta ochranné bariéry kůže mimo jiné vede ke zvýšenému riziku infekce [12]. Přítomnost mikroskopických trhlin v kůži umožňuje snadný průnik mikrobů, které mohou způsobit houbovou, virovou a bakteriální kožní infekci (např. S. aureus nebo streptokoky), což téměř vždy podněcuje exacerbaci onemocnění [13]. Svědění kůže (pruritus) spojené s výraznými poruchami spánku patří mezi hlavní symptomy u dospělých se středně těžkou až těžkou formou AD [14].
Léčba atopické dermatitidy
Léčebná strategie AD u dospělých se odvíjí především od závažnosti onemocnění, která je dána nejen jeho rozsahem a intenzitou, ale i průběhem, reakcí na léčbu, tolerancí léčby, komplikacemi, intenzitou exacerbace a vlivem na kvalitu života. Léčba AD u dospělých je kombinovaná a je zaměřena na jednotlivé složky onemocnění, jako je zklidnění zánětu, obnova kožní bariéry, prevence či eliminace sekundární infekce, snížení pruritu a ovlivnění imunologické dysbalance. K dosažení těchto cílů u dospělých se středně těžkou až závažnou AD, kteří neprokázali dostatečnou odpověď na lokální terapii, se obecně vyžaduje systémová léčba. Žádná z nyní dostupných systémových terapií ale nemá dostatečně příznivý poměr přínosu a rizik, což znemožňuje její dlouhodobé použití u pacientů se středně závažnou až těžkou chorobou, kteří nevykazují dostatečnou klinickou odpověď, nebo u pacientů, kteří lokální terapii netolerují nebo u kterých je lokální terapie kontraindikována.
Cyklosporin A představuje zlatý standard léčby těžké chronické AD a je jedinou imunosupresivní léčbou, kromě systémových kortikoidů, s indikací pro těžké formy AD schválenou v několika zemích Evropské unie [15]. Potenciální toxicita cyklosporinu zahrnuje nefrotoxicitu, hypertenzi, třes, hypertrichózu, bolest hlavy a gingivální hyperplazii. Varování uvádí vzácný výskyt lymfomů a jiné malignity, infekce, renální toxicitu, hepatotoxicitu a hypertenzi [16,17]. Kvůli nežádoucím účinkům je použití cyklosporinu omezeno na jeden rok s průběžným monitoringem funkce ledvin a jater [16]. Terapie cyklosporinem A pomáhá překonat nejhorší období nemoci, ale bohužel nevede k definitivnímu uzdravení [17,18].
Dupilumab
Dupilumab je lidská monoklonální
protilátka třídy IgG4, která
se specificky váže na podjednotku receptoru IL 4Ra
a přerušuje signalizační kaskádu zprostředkovanou cytokiny
IL 4 a IL 13 [10] (obr. 1). Dupilumab tak účinně blokuje specificky tento úsek
Th2 řízené imunitní odpovědi. Léčba dupilumabem vede
k potlačení aberantního zánětu a k částečné
normalizaci profilu genové exprese kůže AD [18]. Dupilumab
zlepšuje kožní bariéru díky up regulaci
genů kódujících proteiny, které se podílejí na epidermální
struktuře, a také zmírněním svrbění. Stejně tak terapie
dupilumabem vede i ke snížení rizika kožní infekce
[19,20].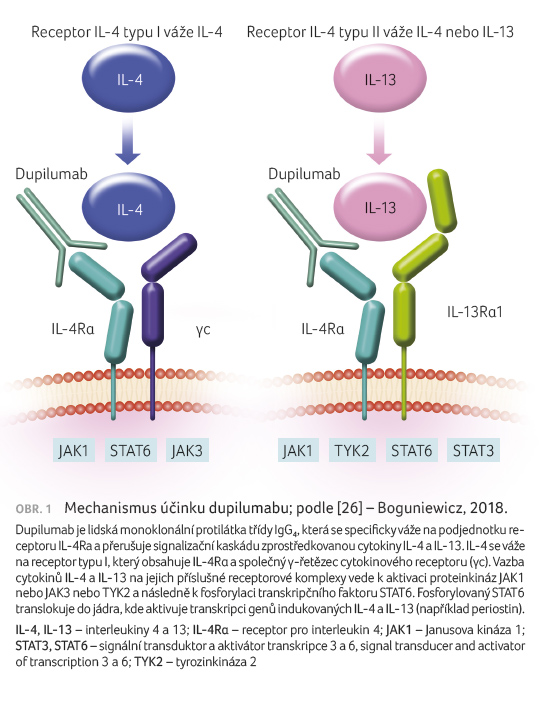
Klinické zkušenosti
Čtyři randomizované, dvojitě
zaslepené, placebem kontrolované studie fáze III byly provedeny
s cílem zhodnotit účinnost a bezpečnost dupilumabu
u dospělých jedinců se středně těžkou až těžkou AD.
Studie SOLO 1 a SOLO 2 hodnotily účinnost dupilumabu jako
monoterapii [21], studie CHRONOS posuzovala účinnost dupilumabu
v kombinaci s topickými kortikosteroidy [22], studie CAFÉ
se zaměřila na účinnost dupilumabu v kombinaci
s topickými kortikosteroidy u dospělých s anamnézou
nedostatečné odpovědi na léčbu cyklosporinem A nebo
s intolerancí této léčby [23] (obr. 2).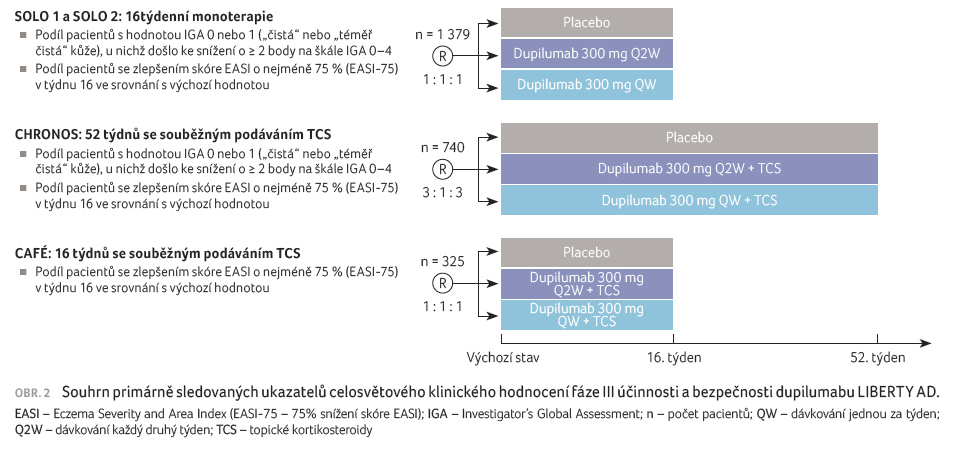
SOLO 1 (n = 671) a SOLO
2 (n = 708) byly multicentrické, randomizované, placebem
kontrolované studie s identickým uspořádáním, do kterých
byli zařazeni pacienti se středně těžkou až těžkou AD
nedostatečně kontrolovanou pomocí lokální léčby. Pacienti byli
randomizováni k terapii dupilumabem v dávce 300 mg
podávané subkutánně (s.c.) týdně (D QW), k léčbě
dupilumabem v dávce 300 mg s.c. každý druhý týden (D
Q2W), nebo k podávání placeba. Primárním sledovaným
ukazatelem byl podíl pacientů se skóre IGA (Investigator’s Global
Assessment) 0 nebo 1, resp. s poklesem skóre IGA o ≥ 2
body v 16. týdnu (graf 1A). Tohoto parametru dosáhlo ve studii SOLO 1 při
léčbě dupilumabem 37 % (D QW), resp. 38 % pacientů (D
Q2W), při podávání placeba 10 % (p < 0,001).
Ve studii SOLO 2 byly výsledky podobné (36 %, resp. 36 %,
vs. 8 %; p < 0,001).
Také podíl pacientů s nejméně 75% snížením skóre EASI
(Eczema Severity and Area Index – EASI 75) byl v obou
studiích signifikantně vyšší při terapii dupilumabem než při
podávání placeba (p < 0,001)
(graf 1B).
Léčba dupilumabem byla spojena také se zlepšením dalších
sledovaných ukazatelů, včetně zmírnění pruritu či symptomů
úzkosti a deprese a zvýšení kvality života. Co se týká
nežádoucích účinků, ve skupinách s dupilumabem byly
v porovnání s placebovými skupinami častěji
zaznamenány reakce v místě vpichu a konjunktivitida.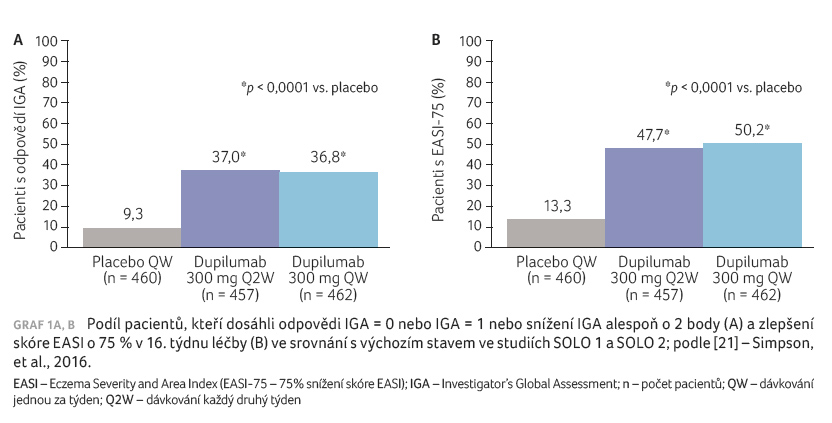
LIBERTY AD CHRONOS (n = 740)
byla multicentrická, randomizovaná, placebem kontrolovaná, dvojitě
zaslepená studie trvající 52 týdnů, které se zúčastnili
pacienti se středně těžkou až těžkou AD a s nedostatečnou
odpovědí na léčbu topickými kortikosteroidy [22]. Ti byli
randomizováni k léčbě dupilumabem v dávce 300 mg
s.c. týdně, k terapii dupilumabem v dávce 300 mg s.c.
podávané každý druhý týden, nebo k podávání placeba,
zároveň byli léčeni (slabými či středně silnými) topickými
kortikosteroidy v kombinaci s kalcineurinovými inhibitory,
či bez nich. Primárním sledovaným ukazatelem byl podíl pacientů
se skóre IGA 0 nebo 1 a s poklesem skóre IGA o ≥ 2
body a podíl nemocných s EASI 75 v 16. týdnu.
Obou těchto parametrů bylo dosaženo signifikantně častěji
u pacientů léčených dupilumabem v porovnání
s placebem – četnost IGA 0 nebo 1 činila 39 % (D QW),
resp. 39 % (D Q2W) vs. 12 % (placebo) a četnost EASI 75
64 %, resp. 69 % vs. 23 % (v obou případech p < 0,0001)
(graf 2).
Výsledky v 52. týdnu sledování, které bylo možno
vyhodnotit u 623 nemocných, byly obdobné (odpovídající
podíly pacientů činily 40 %, resp. 36 %, vs. 13 % a 64 %,
resp. 65 %, vs. 22 %; v obou případech p < 0,0001)
(graf 2).
Terapie dupilumabem vedla rovněž k výraznějšímu snížení
četnosti vzplanutí AD, ke zmírnění pruritu a dalších
symptomů AD, ke zmírnění deprese či úzkosti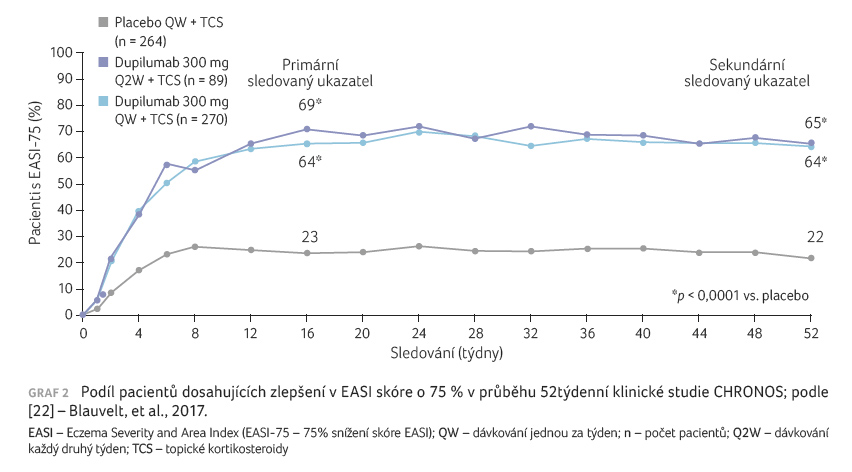 a ke zlepšení
kvality života.
a ke zlepšení
kvality života.
Výskyt nežádoucích účinků byl ve všech ramenech srovnatelný (83 %, resp. 88 %, vs. 84 %), podobně jako výskyt závažných nežádoucích účinků (3 %, resp. 4 %, vs. 5 %). U pacientů léčených dupilumabem byl dokumentován vyšší výskyt reakcí v místě aplikace, konjunktivitidy a lokálních herpetických infekcí; při této terapii nebyly zjištěny žádné významné laboratorní abnormality. Studie potvrdila, že dupilumab vede k setrvalému zmírnění známek a příznaků AD, přičemž jeho dlouhodobý bezpečnostní profil je přijatelný.
Provedena byla rovněž 16týdenní multicentrická, randomizovaná, dvojitě zaslepená, placebem kontrolovaná studie fáze III LIBERTY AD CAFÉ (n = 325), jejímž cílem bylo posoudit účinnost a bezpečnost dupilumabu v kombinaci s topickými kortikosteroidy u nemocných s nedostatečnou odpovědí na léčbu cyklosporinem či s nesnášenlivostí této léčby. Pacienti byli náhodně přiřazeni k léčbě dupilumabem v dávce 300 mg QW, dupilumabem v dávce 300 mg Q2W, nebo k aplikaci placeba, zároveň byli léčeni (středně silnými) topickými kortikosteroidy [23].
Primárního sledovaného parametru,
tj. EASI 75 v 16. týdnu, dosáhlo signifikantně
více pacientů léčených dupilumabem v porovnání
s placebem – 59,1 % (D QW), resp. 62,6 % (D Q2W), vs.
29,6 % (placebo) (graf 3).
Ve skupinách léčených dupilumabem došlo rovněž
ke statisticky významnému zlepšení ostatních klinických
parametrů a ke zmírnění symptomů AD, včetně pruritu
a bolesti, poruch spánku a symptomů úzkosti či deprese,
i ke zlepšení kvality života. Výskyt nežádoucích
účinků byl ve všech skupinách srovnatelný, 69,1 % (D
QW), resp. 72,0 % (D Q2W), vs. 69,4 % (placebo), podobně jako
výskyt závažných nežádoucích účinků (1,8 %, resp. 1,9 %,
vs. 1,9 %). Při terapii dupilumabem byla častěji hlášena
konjunktivitida, při podávání placeba kožní infekce.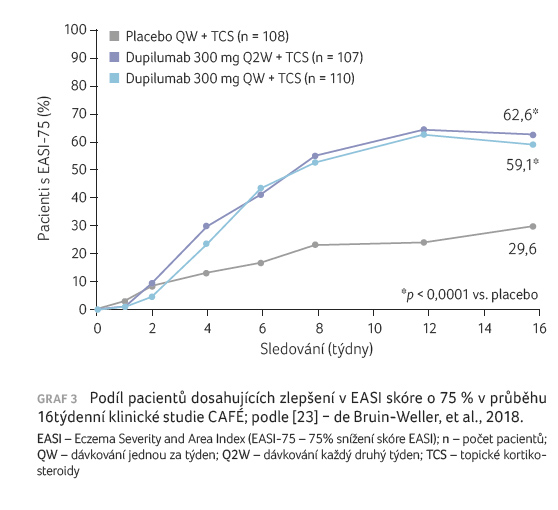
Dupilumab v léčbě atopické
dermatitidy
Populace, pro kterou by dupilumab byl nejvíce prospěšný po získání registrace v České republice, zahrnuje dospělé pacienty se středně těžkou až těžkou AD, u kterých byla systémová terapie cyklosporinem A (tzn. jedinou registrovanou a hrazenou možností systémové terapie) již neúčinná nebo kontraindikovaná. Doporučená iniciální dávka dupilumabu je 600 mg (tj. dvě injekce po 300 mg) následovaná dávkou 300 mg každý druhý týden formou subkutánní injekce. Přípravek lze podávat v kombinaci s topickými kortikosteroidy či s kalcineurinovými inhibitory, nebo bez nich. V kombinaci s dupilumabem lze používat topické kortikosteroidy a také lokální inhibitory kalcineurinu, které by ale měly být aplikovány pouze na problémové oblasti, jako jsou obličej, krk a genitální partie [24]. U pacientů, u nichž po 16 týdnech léčby nedošlo k žádné klinické odpovědi, by mělo být zváženo přerušení léčby dupilumabem. U pacientů s částečnou odpovědí je doporučeno v terapii pokračovat i po 16. týdnu léčby [24].
V současné době neexistuje žádná účinná léčba u dospělých pacientů se středně těžkou až závažnou AD, u kterých selhala terapie topickými kortikosteroidy nebo systémovými imunosupresivními léky. V klinických studiích byl dupilumab dobře snášen a měl příznivý bezpečnostní profil, který je podstatně lepší než u většiny systémových léků. Globální program klinických studií prokázal významný a trvalý přínos dupilumabu pro pacienty s AD a pro mnoho pacientů byl dupilumab lékem doslova měnícím život. Navíc nedávné klinické studie naznačují, že i pacienti s jinými komorbidními atopickými onemocněními, jako je například astma, kde dupilumab má také účinnost, mohou z této terapie velmi těžit [25].
Seznam použité literatury
- [1] Eyerich K, Eyerich S, Biedermann T. The Multi‑Modal Immune Pathogenesis of Atopic Eczema, Trends in Immunology. Elsevier Ltd 2015; 36: 788–801.
- [2] Weidinger S, Novak N. Atopic dermatitis. Lancet 2016: 387: 1109–1122.
- [3] Clark C. Atopic eczema: Management. Clinical Pharmacist 2010; 2: 291–298.
- [4] Bieber T, Straeter B. Off‑label prescriptions for atopic dermatitis in Europe. Allergy 2015; 70: 6–11.
- [5] Garmhausen D, Hagemann T, Bieber T, et al. Characterization of different courses of atopic dermatitis in adolescent and adult patients. Allergy 2013; 68: 498–506.
- [6] Egawa G, Weninger W. Pathogenesis of atopic dermatitis: A short review. Cogent Biology 2015; 1: 1–10.
- [7] Noda S, Krueger JG, Guttman‑Yassky E. The translational revolution and use of biologics in patients with inflammatory skin diseases. J Allergy Clin Immunol 2015; 135: 324–336.
- [8] Benáková N. Léčba atopické dermatitidy/ekzému u dospělých. Med praxi 2010; 7: 221–228.
- [9] Wang X, Shi XD, Li LF, et al. Prevalence and clinical features of adult atopic dermatitis in tertiary hospitals of China. Medicine (United States) 2017; 96: e6317.
- [10] D’Erme MA, Romanelli M, Chiricozzi A. Spotlight on Dupilumab in the treatment of atopic dermatitis: design, development, and potential place in therapy. Drug Des Devel Ther 2017; 11: 1473–1480.
- [11] Imokawa G, Ishida K. Role of Ceramide in the Barrier Function of the Stratum Corneum, Implications for the Pathogenesis of Atopic Dermatitis. J Clin Exp Dermatol Res 2014; 5: 1–12.
- [12] Leung D, Boguniewicz M, Howell MD, et al. New insights into atopic dermatitis. J Clin Invest 2004; 113: 651–657.
- [13] Ong PY, Leung DY. Bacterial and Viral Infections in Atopic Dermatitis: a Comprehensive Review. Clin Rev Allergy Immunol 2016; 51: 329–337.
- [14] Simpson EL, Bieber T, Eckert L, et al. Patient burden of moderate to severe atopic dermatitis (AD): Insights from a phase 2b clinical trial of dupilumab in adults. J Am Acad Dermatol 2016; 74; 491–498.
- [15] Wollenberg A, Barbarot S, Bieber T, et al. Consensus‑based guidelines for treatment of atopic eczema (atopic dermatitis) in adults and children: Part II. J Eur Acad Dermatol Venerol 2018; 32: 850−878.
- [16] Walling HW, Swick BL. Update on the management of chronic eczema: new approaches and emerging treatment options. Clin Cosmet Investig Dermatol 2010; 3: 99–117.
- [17] Souhrn údajů o přípravku Sandimmune 2018. Dostupné na: http://www.ema.europa.eu/docs/en_GB/document_library/Referrals_document/Sandimmun_Neoral_30/WC500144886.pdf
- [18] Hamilton JD, Suárez‑Fariñas M, Dhingra N, et al. Dupilumab improves the molecular signature in skin of patients with moderate‑to‑severe atopic dermatitis. J Allergy Clin Immunol 2014; 134: 1293–1300.
- [19] Fleming P, Drucker AM. Risk of infection in patients with atopic dermatitis treated with dupilumab: a meta‑analysis in randomized controlled trials. J Am Acad Dermatol 2018; 78: 62−69.
- [20] Megna M, Napolitano M, Patruno C, et al. Systemic Treatment of Adult Atopic Dermatitis: A Review. Dermatol Ther (Heidelb) 2017; 7: 1–23.
- [21] Simpson EL, Bieber T, Guttman‑Yassky E, et al. Two Phase 3 Trials of Dupilumab versus Placebo in Atopic Dermatitis. N Engl J Med 2016; 375: 2335–2348.
- [22] Blauvelt A, de Bruin‑Weller M, Gooderham M, et al. Long‑term management of moderate‑to‑severe atopic dermatitis with Dupilumab and concomitant topical corticosteroids (LIBERTY AD CHRONOS): a 1‑year, randomised, double‑blinded, placebo‑controlled, phase 3 trial. Lancet 2017; 389: 2287−2303.
- [23] de Bruin‑Weller M, Thaçi D, Smith CH, et al. Dupilumab with concomitant topical corticosteroids in adult patients with atopic dermatitis, who are not adequately controlled with or are intolerant to cyclosporine A, or when this treatment is medically inadvisable: a placebo‑controlled, randomized phase 3 clinical trial (LIBERTY AD CAFÉ). Br J Dermatol 2018; 178: 1083−1101.
- [24] Souhrn údajů o přípravku Dupixent 2018. Dostupné na: http://www.ema.europa.eu/docs/en_GB/document_library/EPAR__Product_Information/human/004390/WC500236507.pdf
- [25] Wenzel S, Castro M, Corren J, et al. Dupilumab efficacy and safety in adults with uncontrolled persistent asthma despite use of medium‑to‑high‑dose inhaled corticosteroids plus a long‑acting β2 agonist: a randomised double‑blind placebo‑controlled pivotal phase 2b dose‑ranging trial. Lancet 2016; 388: 31−34.
- [26] Boguniewicz M. Biologic therapy for atopic dermatitis: moving beyond the practice parameter and guidelines. J Allergy Clin Immunol Pract 2017; 5: 1477−1487.