Risankizumab – naděje pro mladou pacientku s psoriázou
Souhrn:
Stumpfová A. Risankizumab – naděje pro mladou pacientku s psoriázou. Remedia 2020; 30: 468–472.
Kazuistika pojednává o léčbě psoriázy u mladé pacientky a zaměřuje se především na terapii novým biologických přípravkem risankizumabem. Je zde popsána zkušenost s léčbou uvedeným lékem na Kožním oddělení Masarykovy nemocnice v Ústí nad Labem (MNUL). Místní terapie, fototerapie a celková terapie metotrexátem (MTX) a acitretinem byly u pacientky bez efektu či s nežádoucími účinky. Biologická terapie adalimumabem musela být ukončena pro sekundární neúčinnost, aplikace brodalumabu byla ukončena z důvodu neefektivity. Poslední zahájenou biologickou léčbou je risankizumab, nové biologikum, jež se zdá být u pacientky velmi nadějné. V textu jsou v jednotlivých odstavcích popisujících konkrétní celkovou léčbu uvedeny nástroje hodnotící rozsah a závažnost psoriázy – PASI (Psoriasis Area and Severity Index, škála 0–72), skóre BSA (Body Surface Area) a DLQI (Dermatology Quality Life Index, škála 0–30). Sekundárně je používáme k hodnocení účinnosti zavedené léčby.
Summary:
Stumpfova A. Risankizumab – a hope for a young patient with psoriasis. Remedia 2020; 30: 468–472.
This case report summarizes the treatment of psoriasis in a young patient. It focuses primarily on the therapy using the new biological agent risankizumab. The article describes the experience with risankizumab treatment at the Dermatology Department in Masaryk Hospital in Ústí nad Labem (MNUL). The local therapy, phototherapy and the regular therapy with methotrexate (MTX) and acitretin were inefficacious and side effects occurred during the treatment. The biological therapy using adalimumab was ended due to secondary insufficiency. Brodalumab was withdrawn for the reason of inadequate response. The latest systemic therapy is biological therapy using risankizumab, a new biological agent that seems to be very promising for our patient. In the text below, there are also the criteria of evaluation of the severity of psoriasis included – PASI (Psoriasis Activity and Severity Index, scale 0–72), BSA score (Body Surface Area) and DLQI (Dermatology Quality Life Index, scale 0–30). PASI and BSA evaluates and indicates the severity and the surface area of psoriasis, DLQI describes the impact of the skin disease on the quality of life of the patient. All can be used to evaluate the efficacy of the specific treatment.
Key words: psoriasis, biologic therapy, interleukin‑23, risankizumab
Úvod
Psoriáza je chronické, geneticky podmíněné, imunitně zprostředkované zánětlivé onemocnění kůže postihující 2–4 % středoevropské populace [1–3]. Nejčastějším typem je plaková psoriáza, při níž mohou jednotlivé psoriatické projevy tvořené primárně plochou papulou krytou bělavou šupinou splývat až do rozsáhlých geografických ložisek. Nezřídka se vyskytuje i postižení nehtů, přibližně 30 % pacientů má současně i kloubní formu psoriázy. Kromě toho, že je psoriáza onemocněním, které výrazně ovlivňuje kvalitu života, může být také doprovázena řadou systémových onemocnění, např. arteriální hypertenzí, dyslipidemií, diabetem, kardiovaskulárními chorobami, metabolickým syndromem, hepatopatií, zánětlivými onemocněními střev, psychiatrickými nemocemi, malignitami a jinými. To může vést ke zkrácení života pacienta až o 3,5 roku oproti zdravé populaci [1,3]. Za závažné onemocnění je považováno takové, při němž je splněno alespoň jedno kritérium – PASI (Psoriasis Area and Severity Index) > 10, BSA (Body Surface Area) > 10 %, DLQI (Dermatology Quality Life Index) > 10 [3].
Jelikož se jedná o multifaktoriální polygenetické onemocnění, nemůžeme mluvit pouze o jedné vyvolávající příčině. Onemocnění se vyvíjí u predisponovaných osob často po zásahu vnějšího vyvolávajícího faktoru (např. infekce, stres, trauma). V imunitním systému dochází k aktivaci buněk vrozené imunity (keratinocyty, dendritické buňky, plazmocytoidní buňky a NK [tzv. natural killers] T lymfocyty) neznámým antigenem, což vede k sekreci řady cytokinů – tumor nekrotizujícího faktoru alfa (TNFα), interferonu alfa (IFNα), interferonu gama (IFNγ), interleukinu 1 beta (IL 1β), interleukinu 6 (IL 6) a dalších. V poslední době se prokázala důležitost kaskády IL 23/Th17 lymfocytů v patogenezi psoriázy. Potvrdilo se, že vlivem zvýšené hodnoty regulačního cytokinu IL 23 dochází k produkci patogenních Th17 lymfocytů, které ve zvýšené míře produkují prozánětlivé cytokiny IL 17, IL 22, IFNα a další, které se podílejí na udržování psoriatického zánětu. Inhibicí IL 23 dojde k potlačení produkce patogenních Th17 lymfocytů, stejně tak i k potlačení nadměrné produkce prozánětlivých cytokinů IL 17, IL 22 a dalších, čímž se tlumí zánět v psoriáze. Nicméně nadále přetrvává produkce nepatogenních Th17 lymfocytů, která je zodpovědná za fyziologickou hodnotu IL 17 a IL 22, jež mají důležitou roli mimo jiné např. v obraně organismu proti intracelulárním patogenům či v udržování homeostázy střev. Tímto výše popsaným mechanismem fungují blokátory (inhibitory) IL 23, mezi něž patří i risankizumab [1,3].
Interleukin 23 se jeví být dle současných výzkumů klíčovým cytokinem v patofyziologii psoriázy [3–5]. Inhibicí tohoto cytokinu dochází k redukci populace patogenních Th17 lymfocytů. Interleukin 23 se skládá ze dvou podjednotek – p19 a p40, kterou vlastní také IL 12. Specifickou inhibicí p19 IL 23 je tak zachována cesta IL 12/Th1, podstatná pro buněčnou imunitu, a také se udržuje produkce nepatogenních Th17 lymfocytů hrajících důležitou úlohu např. ve střevním imunitním systému [3,5]. Díky tomu je možné zamezit vzniku některých nežádoucích účinků a zajistit tak větší bezpečnost biologické terapie.
Vlivem rozvíjejícího se výzkumu nejen v patogenezi psoriázy, ale hlavně nových přípravků z řad biologické léčby můžeme tedy cíleně inhibovat konkrétní cytokiny a dosáhnout tak rozrušení bludného kruhu v patofyziologii psoriázy.
U pacientů se středně závažnou až závažnou formou psoriázy je indikována systémová farmakoterapie zahrnující nebiologické léky (acitretin, metotrexát, cyklosporin, apremilast) a biologické léky [3]. V terapii psoriázy jsou schváleny biologické léky ze skupiny anti TNFα (adalimumab, infliximab, etanercept a certolizumab), anti IL 12/23 (ustekinumab), anti IL 17 (sekukinumab, brodalumab, ixekizumab) a anti IL 23 (guselkumab, tildrakizumab, risankizumab). Risankizumab je humanizovaná IgG1 monoklonální protilátka, která se váže na podjednotku p19 IL 23, způsobuje jeho blokádu a tak i blokádu psoriatického zánětu [1,3,4]. Jeho účinnost a bezpečnost byly prokázány ve dvou klinických studiích fáze III (UltlMMa 1 a UltlMMa 2), kde byl risankizumab porovnáván s ustekinumabem a placebem. Risankizumab se ve stejných studiích osvědčil jako superiorní k ustekinumabu [6,7], v jiné porovnávací studii (IMMvent) byla dokumentována signifikantně větší účinnost risankizumabu oproti adalimumabu [7,8]. Ve studii IMMhance prokázal risankizumab u pacientů se středně těžkou až těžkou psoriázou lepší výsledky než placebo [7]. V průběhu studií byl zaznamenán vysoký podíl pacientů dosahujících PASI 90 (zlepšení PASI o 90 % oproti výchozí hodnotě) a PASI 100 (zlepšení PASI o 100 % oproti výchozí hodnotě) již ve čtvrtém týdnu, sekundárně i zlepšení kvality života pacientů. Celková bezpečnost byla ve všech studiích srovnatelná s placebem, ustekinumabem nebo adalimumabem [6–8].
Popis případu
První projevy kožní formy psoriázy se u naší nyní devatenáctileté, jinak zdravé pacientky projevily již ve věku devíti let. Kloubní formou tohoto onemocnění pacientka netrpí, stejně tak i v rodinné anamnéze neuvádí výskyt psoriázy mezi příbuznými. Místní léčba dle preskripce spádového dermatologa byla několik let dostačující, zlom však nastal v roce 2014, kdy bez předchozího vyvolávajícího faktoru došlo ke generalizaci kožních ložisek. Pacientka byla proto po půlroční neúspěšné místní léčbě ošetřujícím dermatologem odeslána na naše oddělení a následně v květnu 2015 hospitalizována pro rozsáhlou psoriázu na Dětské klinice MNUL. Během hospitalizace byla za intenzivní místní léčby započata celotělová fototerapie UVB 311 nm, v níž pacientka po propuštění pokračovala ambulantní cestou. Efekt tříměsíční fototerapie však viditelný nebyl. Pro velký rozsah a postižení kůže (PASI 12,4; BSA 20) byla zvažována při kontrole na naší ambulanci biologická léčba adalimumabem, avšak revizním lékařem nebyla schválena z důvodu nevyčerpání možností konvenční terapie psoriázy.
Od ledna 2016 jsme tudíž za souhlasu matky a zavedení hormonální antikoncepce zahájili terapii metotrexátem (MTX). Dávky MTX jsme postupně navyšovali až na 15 mg týdně. Pacientka se během léčby dokonce i na několik měsíců zcela zahojila, MTX jsme nicméně museli i přes uspokojivý kožní nález v březnu 2017 pro výraznou elevaci hodnot jaterních testů přerušit (alaninaminotransferáza 4,56 [norma 0,0–0,79 μmol/l], aspartátaminotransferáza 1,98 (norma 0,0–0,75 μmol/l]). Po ukončení podávání MTX se sice jaterní hodnoty postupně znormalizovaly, ložiska psoriázy se však poměrně rychle vrátila, což pacientku i rodinu velmi trápilo. Proto byla v květnu 2017 zahájena léčba acitretinem (PASI 10,2; BSA 6), ale pro jeho neúčinnost a zhoršení lokálního nálezu bylo po měsíci podávání ukončeno (PASI 12,4; BSA 11).
V tu dobu byla pacientka
kandidátem na biologickou léčbu. S ohledem na její
věk – necelých 16 let – jsme volili adalimumab, jedno
z mála biologik (kromě ustekinumabu a etanerceptu)
schválených pro léčbu dětí. Pacientka splňovala kritéria
zahájení léčby – měla závažnou chronickou ložiskovou
psoriázu postihující více než 10 % tělesného povrchu
a hodnota PASI činila více než 10, reakce na lokální
terapii a fototerapii nebyla dostatečná. Léčbu jsme zahájili
v červenci 2017 (počáteční PASI 13,0; BSA 11; DLQI 22).
Dávkování adalimumabu bylo standardní dle indikací léčby
psoriázy u mladistvých, a to 40 mg subkutánně (s.c.)
každých 14 dní. Tato biologická léčba byla zprvu velmi
účinná, krátce po zahájení došlo dokonce ke zhojení
psoriázy. V dalším průběhu jsme s léčbou i přes
mírné recidivy pokračovali celkem dva roky, až do září
2019, kdy se psoriatická ložiska výrazně zhoršila. Z důvodu
nesplnění kritérií pro pokračování dosavadní biologické
léčby (došlo k poklesu účinnosti zavedené biologické
léčby do intervalu PASI 50–75 se současnou hodnotou DLQI
více než 5) bylo užívání adalimumabu ukončeno. Jelikož v této
době již pacientka dosáhla plnoletosti, ve výběru
biologické léčby jsme měli větší možnosti. Od září
2019 byla u nemocné zahájena léčba brodalumabem, inhibitorem
IL 17. Ačkoliv byla léčba brodalumabem zahájena
v doporučeném dávkování pro terapii psoriázy (210 mg
s.c. v týdnu 0, 1, 2 a dále 210 mg s.c. každých 14
dní), u naší pacientky jsme žádný efekt nepozorovali.
Naopak, od aplikace první dávky (v září 2019 dosahoval
PASI hodnoty 11,6; BSA 8; DLQI 11) došlo během dalších čtyř
měsíců k progresi a při hodnocení efektu léčby
v 16. týdnu jsme museli aplikaci brodalumabu ukončit
z důvodu neúčinnosti.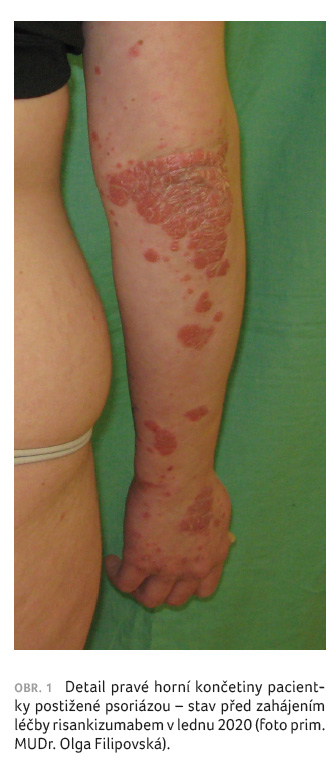
Ve stejný den hodnoticí kontroly
v lednu 2020 jsme tedy provedli „switch“ biologika pro
nesplnění indikačních omezení úhrady brodalumabu (nedosažení
hodnoty PASI 50 = zlepšení PASI o 50 % oproti
výchozí hodnotě po úvodních čtyřech měsících léčby).
Kožní nález byl opět v progresi, přetrvávala ložiska
psoriázy nad lokty, na předloktích a zápěstích, dále
se vyskytovala polycyklická ložiska na bércích, zvýraznila
se infiltrace, erytém a deskvamace projevů, subjektivně
pacientka pociťovala zhoršení a svědění ložisek psoriázy
(PASI 13,8; BSA 9; DLQI 12), obrázek 1, 2.
Vzhledem k předchozí terapii přípravky anti TNFα
a anti IL 17 jsme tentokrát zvolili cestu blokády
IL 23 – nový přípravek risankizumab. Terapie byla
zahájena v lednu 2020 dávkou 2× 75 mg s.c. Stejná
dávka byla aplikována ve čtvrtém týdnu léčby a následně
každých 12 týdnů. Lék aplikuje zdravotní sestra vždy při
kontrole na naší ambulanci. Již po první aplikaci léku
jsme pozorovali zmírnění kožních projevů psoriázy (PASI 3,6;
BSA 9; DLQI 10). Při hodnoticí návštěvě v 16. týdnu
byla pacientka zcela zhojena a tento stav přetrvává nadále
i po půlroce od zahájení léčby (obr. 3).
Bylo tudíž dosaženo PASI 100 – zlepšení o 100 %
oproti hodnotě PASI před zahájením léčby risankizumabem.
Pacientka je velmi spokojena, žádné nežádoucí účinky se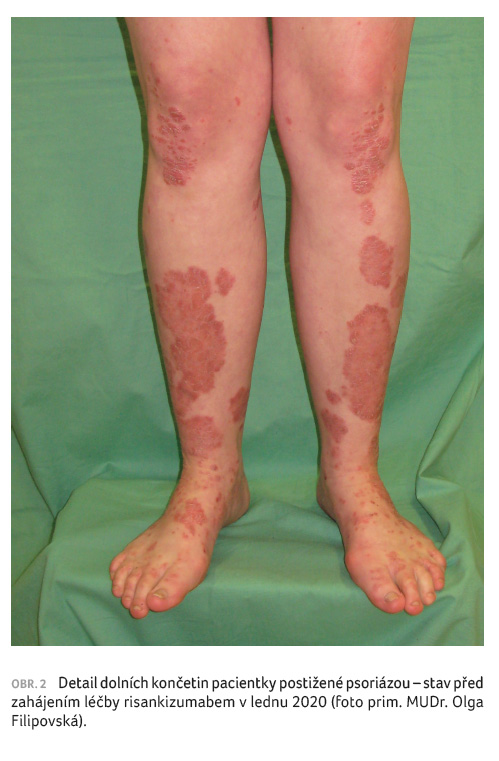 dosud
neobjevily.
dosud
neobjevily.
Diskuse
V době prvního kontaktu s naší
dermatologickou ambulancí byla pacientka v dětském věku
a trpěla těžkou formou psoriázy. Kazuistika tak sleduje
vývoj a léčbu této nemoci od pacientčiných 13 let
do jejích současných 19 let a zdůrazňuje význam
posledního užívaného biologického léku risankizumabu. Léčba
psoriázy dětí a dospělých je sice velmi podobná, přístup
k hodnocení bezpečnosti a zároveň zajištění co
nejvyšší účinnosti jsou však v dětském věku více
limitovány [2,9]. Při léčbě středně těžké až těžké
formy psoriázy je lokální terapie často nedostatečná.
Biologická léčba psoriázy dětí je dle celosvětově získaných
informací bezpečnější a účinnější než klasická
imunosupresivní terapie (MTX, cyklosporin) a léčba retinoidy
[2,9]. Jelikož jsme chtěli zajistit co nejrychlejší a pokud
možno trvalé zhojení kožních projevů psoriázy s co
nejmenším výskytem nežádoucích účinků, zvažovali jsme
v první volbě celkové terapie právě léčbu biologickou.
Její úhrada však byla v roce 2016 zamítnuta zdravotní
pojišťovnou, ač z poznatků dlouhodobé léčby psoriázy
dětí vede biologická léčba s menší pravděpodobností
ke vzniku nežádoucích účinků nebo k přerušení
léčby ve srovnání s MTX [2].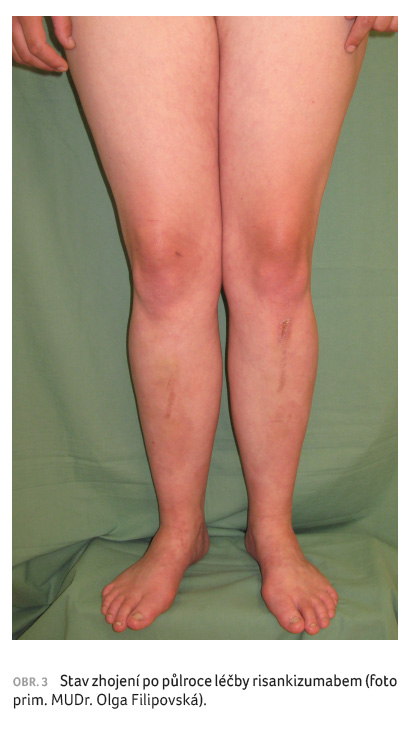
Možnost zahájení terapie biologiky jsme tak dostali až v dalším roce po ukončení léčby MTX a acitretinem. Adalimumab a brodalumab však neměly u pacientky kýžený efekt. Naději tak vkládáme do nově zahájené léčby anti IL 23 přípravkem risankizumab, jehož účinnost se zdá být zatím výborná. Ke zhojení psoriázy došlo u pacientky již po druhé aplikaci tohoto léku. Žádné nežádoucí účinky se dosud neobjevily a pacientka je s léčbou velmi spokojena. Dalším pozitivem je méně častá frekvence aplikace léku. V případě plánování těhotenství u mladé pacientky hraje roli i výborný bezpečnostní profil risankizumabu oproti retinoidům a MTX. Biologikum neinterferuje s antikoncepčními přípravky, které jsou u žen ve fertilním věku doporučovány k užívání současně s biologickou léčbou. Z preventivních důvodů je vhodné ukončit terapii risankizumabem 21 týdnů před otěhotněním [3,4]. V případě plánování těhotenství, a tedy ukončení podávání risankizumabu lze však předpokládat dle dostupných publikovaných dat, že i po přerušení léčby bude účinnost klesat jen velmi pozvolna [10].
Z hlediska zlepšení kvality života a zachování co nejlepšího možného zdravotního stavu pacientů s psoriázou je biologická terapie výrazně lepší volbou oproti systémové léčbě imunosupresivy či retinoidy jak z hlediska bezpečnosti a účinnosti, tak i komfortu aplikace léčiv. Z těchto důvodů by bylo dobré mít možnost zahájit biologickou léčbu u středně těžké až těžké formy psoriázy, zvláště u dětí, co nejdříve.
Seznam použité literatury
- [1] Gkalpakiotis S, Cetkovská P, Kojanová M, Arenberger P. Psoriáza: od teorie k praxi. Praha: Mladá fronta, 2020. Aeskulap. ISBN 978‑80‑204‑5574‑1.
- [2] Thaçi D, Papp K, Marcoux D, et al. Sustained long‐term efficacy and safety of adalimumab in paediatric patients with severe chronic plaque psoriasis from a randomized, double‐blind, phase III study. Br J Dermatol 2019; 181: 1177–1189.
- [3] Cetkovská P, Kojanová M, Arenberger P. Současný stav moderní léčby psoriázy: aktualizovaná doporučení ČDS JEP k cílené léčbě závažné chronické psoriázy. Farmakoter 2020; 16(Suppl 2): 5–28.
- [4] Arenberger P. Risankizumab. Farmakoter 2020; 16(Suppl 2): 29–36.
- [5] Vašků V. Psoriáza. 2. vydání. Praha: Maxdorf, 2020. Farmakoterapie pro praxi. ISBN 978‑80‑7345‑638‑2.
- [6] Hodačová J, Gkalpakiotis S. Účinnost a bezpečnost risankizumabu u pacientů se středně těžkou až těžkou plakovou psoriázou: Výsledky studií UltlMMa‑1 a UltlMMa‑2. Farmakoter 2020; 16(Suppl 2): 42–44.
- [7] Skyrizi (risankizumab). SPC 2019. Dostupné na: https://www.ema.europa.eu/en/documents/product‑information/skyrizi‑epar‑product‑information_cs.pdf
- [8] Hodačová J, Cetkovská P. Risankizumab vs. adalimumab u pacientů se středně těžkou až těžkou ložiskovou psoriázou: studie IMMvent. Farmakoter 2020; 16(Suppl 2): 45–48.
- [9] Paler AS, Lund EB. Psoriasis in children: Epidemiology, clinical manifestations, and diagnosis. UpToDate [online]. Feb 27, 2020
- [10] Blauvelt A, Leonardi CL, Gooderham M, et al. Efficacy and Safety of Continuous Risankizumab Therapy vs Treatment Withdrawal in Patients With Moderate to Severe Plaque Psoriasis. JAMA Dermatol 2020; 156: 1–11.