Sedm kroků potravinové alergie
Potravinová alergie je alergologickým fenoménem posledních 20–30 let. Může být příčinou orgánového postižení již od prvních měsíců života. Nejen z těchto důvodů byla vybrána kazuistika kojence s těžší potravinovou alergií s ranými kožními, trávicími a později i respiračními symptomy.
Úvod
Potravinová alergie je v alergii kojence nesporně nejvýznamnější kapitolou, stala se nejen pro tento věk doslova alergologickým fenoménem posledních 20–30 let. Může být příčinou orgánového postižení již od prvních měsíců života. Pro její časnou manifestaci i prognostický význam se někdy mluví o prvním kroku alergického pochodu. Týká se to neuvěřitelných 8 % kojenců. Více než polovina z nich trpí alergií na bílkoviny kravského mléka. Přes spontánní vyhasnutí se u více než u poloviny z nich časem vyvine některá z klasických forem inhalační alergie – astma nebo alergická rýma. Průběh, projevy, diagnóza, léčba i prognóza bývají ovlivněny typem, tíží i stabilitou samotné alergie. Klíčový dietní přístup, včetně následných expozic, musí být přísně individuální. Případná farmakoterapie má podpůrný charakter, zmírňuje příznaky a může se podílet na prevenci dalších kroků alergického pochodu. Komplikovanou péči očekávejme především u polyvalentních alergií včetně účasti rizikových potravin. Nejen z výše uvedených důvodů byla vybrána kazuistika těžší potravinové alergie s ranými kožními, trávicími a později i respiračními symptomy.
Kazuistika
Dívka narozená v dubnu 2008, s pozitivní alergologickou rodinnou anamnézou, otec se léčí s astmatem, sestra s polinózou.První příznaky alergického pochodu se objevují ve dvou měsících věku, a to v podobě atopického ekzému – první krok. Ošetřováno lokálně formou pravidelné kožní hydratace emoliencii, na ložiska výjimečně používány lokální kortikosteroidy, a to pouze v intervalovém podávání (3 dny ano, 6 dní ne). Vzápětí se ob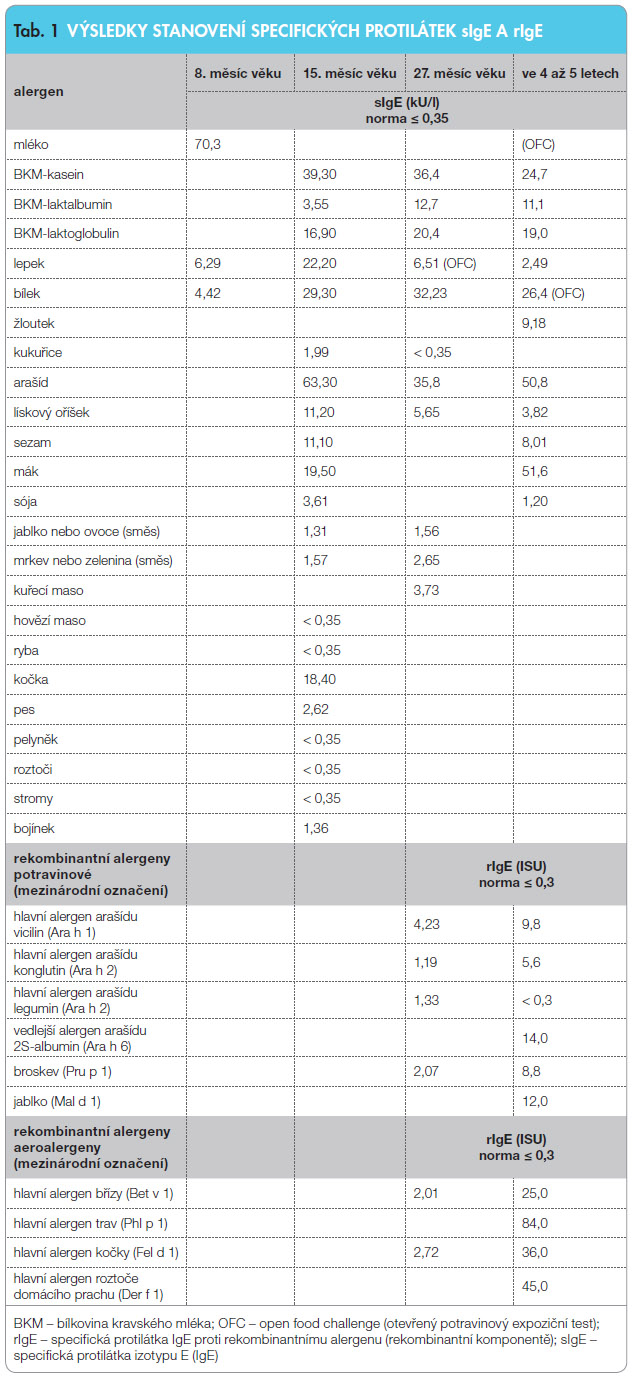 jevují častější řídké stolice s hlenem (občas jen tekutina, ale bez krve) – druhý krok. Dítě je plně (exkluzivně) kojeno, prospívání je však dlouhodobě neuspokojivé. Od 6. měsíce věku dítěte zařazovány příkrmy, ale výhradně na zeleninovém a ovocném základě. Kojící matka začala v 7. měsíci držet „naslepo“ bezmléčnou dietu (přesněji dietu bez bílkovin kravského mléka, bez BKM) a prakticky okamžitě došlo k ústupu vleklého průjmu. Od 8. měsíce věku dítěte matka vynechává i vajíčko a lepkové obiloviny, tentokrát na základě výsledku stanovení specifických imunoglobulinů E (sIgE) – viz dále. Dochází k mírnému zklidnění ekzému, nicméně dieta nezabránila generalizaci atopické dermatitidy. Prvním imunologickým vyšetřením byla zjištěna senzibilizace nejen na mléko, ale i na vejce a mouku – viz tab. 1. Dítě je stále kojeno, nikdy nedostalo kravské a jakékoli jiné živočišné mléko, mléčné výrobky, vejce ani lepkovou mouku. K základu komplementární výživy dítěte patří zelenina, ovoce, masa a nelepkové mouky (rýže, kukuřice, proso-jáhly, pohanka a amarant). Dítě se však chová k některým povoleným potravinám dost odmítavě.
jevují častější řídké stolice s hlenem (občas jen tekutina, ale bez krve) – druhý krok. Dítě je plně (exkluzivně) kojeno, prospívání je však dlouhodobě neuspokojivé. Od 6. měsíce věku dítěte zařazovány příkrmy, ale výhradně na zeleninovém a ovocném základě. Kojící matka začala v 7. měsíci držet „naslepo“ bezmléčnou dietu (přesněji dietu bez bílkovin kravského mléka, bez BKM) a prakticky okamžitě došlo k ústupu vleklého průjmu. Od 8. měsíce věku dítěte matka vynechává i vajíčko a lepkové obiloviny, tentokrát na základě výsledku stanovení specifických imunoglobulinů E (sIgE) – viz dále. Dochází k mírnému zklidnění ekzému, nicméně dieta nezabránila generalizaci atopické dermatitidy. Prvním imunologickým vyšetřením byla zjištěna senzibilizace nejen na mléko, ale i na vejce a mouku – viz tab. 1. Dítě je stále kojeno, nikdy nedostalo kravské a jakékoli jiné živočišné mléko, mléčné výrobky, vejce ani lepkovou mouku. K základu komplementární výživy dítěte patří zelenina, ovoce, masa a nelepkové mouky (rýže, kukuřice, proso-jáhly, pohanka a amarant). Dítě se však chová k některým povoleným potravinám dost odmítavě.
K prvnímu alergologickému vyšetření dochází později, a to až v 15. měsíci věku, při hmotnosti pouhých 8 kg. Kožní testy potvrzují senzibilizaci na všechny tři základní potraviny – viz tab. 2. Kontrolní koncentrace sIgE (tab. 1) ale prozrazují přecitlivělost mnohem širší. Jde v pravém slova smyslu o multiproteinovou senzibilizaci, a to jak na nebezpečné ořechy i semena, tak nález naznačuje reálné riziko možné inhalační alergie – třetí krok. Do léčby p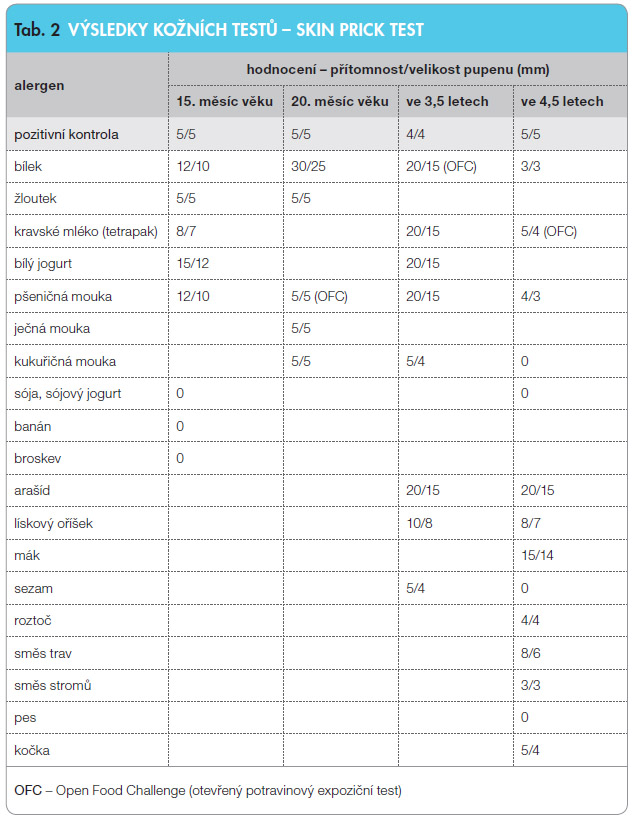 oprvé zařazena antihistaminika (desloratadin).
oprvé zařazena antihistaminika (desloratadin).
Dieta v 15. měsíci věku: doporučeno, byť s výhradami, pokračovat v kojení (dieta matky je totiž velmi těžko realizovatelná, tj. bez mléka, lepku, vajec, ořechů i semen). Doplňující strava dítěte je reálně založena na bílém i červeném mase, rýži, bezlepkových těstovinách, banánu a jablku. Dítě odmítá bezlepkové pečivo, brambory a veškerou zeleninu. Ani přes tuto dietu, která čím dál více vykazuje prvky malnutrice (hmotnost dítěte ve 20 měsících je pouhých 9,5 kg), se kožní nález zásadně nelepší, ba naopak je patrné zhoršení v obličeji, na krku, na rukou, v podkolení i na nártech. Ve 20 měsících je dítě přetestováno, včetně nelepkové kukuřice. A i ta vychází překvapivě pozitivní – viz tab. 2.
Alergický pochod ve dvou letech věku není ani klinicky, natož laboratorně, pod kontrolou. V terapeutickém schématu rozhodnuto o zahájení další preventivní farmakoterapie, přidán stabilizátor žírných buněk (kromoglykát sodný) a antileukotrien (montelukast). Vzhledem k raritní polyvalentní senzibilizaci a vzhledem k nutnosti široké dietní eliminace s nedostatečným nutričním příjmem rozhodnuto o ukončení naprosto neefektivního kojení (23. měsíc věku). Nepřekvapí, že to matce přineslo spíše úlevu. Kojení bylo nahrazeno vysoce specializovaným přípravkem, kde 100% absenci bílkovin suplementují volné aminokyseliny (AAF, amino acid formula). Výsledný příjem je krom nutné eliminace výrazně ovlivněn i nevyzpytatelnou chutí, spíše nechutí dítěte k jídlu. V průběhu třetího roku se tak redukovaná strava ustálila na mase, rýži, bramborách, bezlepkových kaších, sójových výrobcích (jogurty), na ovoci a některých druzích zeleniny, které přece jen byly do stravy zařazeny. Přípravek s AAF přijme dítě jen v kaších a v pudincích. Pro reálný nedostatek substituován vápník v dávce 250 mg/den. Hmotnostně se děvče pohybuje těsně pod 3. percentilem, výškově jen o málo lépe, tj. v rozmezí 3. a 10. percentilu.
Ve věku 2,5 roku (30 měsíců) bylo rozhodnuto o prvním expozičním testu, a to lepkem, který na základě imunologické senzibilizace nebyl dítěti dosud nikdy podán. Motivem expozice je jednak možné vyhasínání senzibilizace (viz tab. 1), jednak naléhavá potřeba rozšířit jídelníček směrem k pozitivní kalorické bilanci. To vše za předpokladu, že senzibilizace nemusí znamenat reálnou alergii.
Expoziční test byl proveden na našem pracovišti, v ambulantním provozu, za standardních podmínek otevřeného testu (OFC – open food challenge). Jako zdroj lepku byly použity bezvaječné pšeničné těstoviny, a to v postupně se zvyšující dávce. První hodinu probíhal test bez problémů, teprve až po konzumaci kumulativní dávky 44 kousků těstovin dochází ke kožní reakci (generalizovaný pruritus, urtikarie). Tímto byla ověřena relativně vysoká prahová dávka testovaného lepku. Rodiče se nemusejí obávat stop, bezlepková dieta nemusí být důsledná, ba naopak. Od uskutečnění OFC s lepkem dostává dítě malé množství lepku denně, bez jakýchkoli komplikací. Kolem 3,5 roku věku dítě snese běžnou porci lepkových těstovin. A to i přes přetrvávání senzibilizace (viz pozitivní kožní testy, tab. 2).
Kolem třetího roku věku se ekzém stabilizuje, ošetřován je jen pomocí emoliencií, nedochází k žádným exacerbacím. Nicméně ve 44. měsíci věku překvapila první astmatická epizoda dušnosti – čtvrtý krok – bez souvislosti s potravinami. Účast inhalační senzibilizace byla sice spekulativní, o to pravděpodobnější. K léčbě byly přidány malé dávky inhalačních kortikosteroidů – IKS (flutikason 50 μg 2krát denně). V dietě se přednostně dbá na eliminaci BKM (striktně) a také na velmi přísnou eliminaci ořechů a semen. Důvodem této opatrnosti je nebezpečný nárůst pozitivity alergických protilátek hned proti třem nejrizikovějším rostlinným panalergenům (viciliny, konglutiny a 2S-albuminy). U dítěte byla senzibilizace k těmto nebezpečným alergenním rodinám odhalena v arašídové podobě – viz tab. 1. Tyto stabilní panalergeny jsou nejen nositeli bohatých zkřížených reakcí v rámci rostlinné homologie (= zkřížená senzibilizace chemicky podobných bílkovin), ale mají i velmi silný proanafylaktický potenciál.
Ve čtyřech letech věku proveden expoziční test s vajíčkem. Vejce děvče sice nikdy dostat nemělo, ale podrobnou anamnézou byla zjištěna příznivá tolerance opakované domácí vaječné expozice, byť jen v podobě stop, například v polévkových knedlíčcích. Při standardizovaném dvouhodinovém testu na našem pracovišti dítě s chutí snědlo celé vařené vajíčko, k žádné reakci nedošlo. Od té doby zrušen zákaz příjmu vaječných bílkovin, a to navzdory přetrvávající senzibilizaci (viz výsledky kožních testů a stanovení sIgE z této doby). Astma je stabilizováno na minimální dávce IKS, rodiče rozhodně nepodávají tuto léčbu denně. A vymizel i kožní nález, ekzém se objevuje zcela sporadicky, a to prakticky jen v podkolení. Dítě ve čtyřech letech váží 14 kg. Růst je naštěstí harmonický v linii 10. percentilu. Ve farmakoterapii zůstávají antihistaminika, antileukotrieny. Matkou bylo značně omezeno podávání kromoglykátu sodného.
Ve věku 4,5 roku byl povolen a také realizován nástup do školky. Vajíčko jí dítě bezpečně v těstech, lepek v těstovinách, v pečivu i v omáčkách. Při oslavě s dětmi dokonce snědla i větší stopy zakysané smetany (dort), naštěstí bez reakce. Vzhledem ke zvýšenému riziku náhodného podání ořechů a semen vybavena jak rodina, tak i kolektivní zařízení záchrannou léčbou podávanou intramuskulárním autoinjektorem s dávkou adrenalinu 150 μg.
V pěti letech dítěte přistoupeno k zatím poslednímu expozičnímu testu, tentokrát mlékem. Hlavním motivem této konkrétní expozice bylo zjištění skutečné prahové dávky BKM. Dítě při standardizovaném testu, opět na našem pracovišti, bezpečně toleruje 40 ml plnotučného mléka, avšak při další nabídce (100 ml) dochází k bolestem bříška a zvracení. Od této expozice nemusí být dieta tak důsledná, povoleny jsou stopy mléka (těsta, omáčky, polévky, kousky sýra aj.).
Krátce po pátých narozeninách dochází k nosní obstrukci a k zarudnutí spojivek, a to nepochybně ve vztahu s květem prvních jarních stromů (líska, bříza, habr) – pátý krok. Senzibilizace k pylu jarních stromů byla vzápětí potvrzena imunologickými testy, včetně použití nejmodernější rekombinantní technologie (viz tab. 1, 2). Tato metoda umožňuje identifikovat jednotlivé alergenní složky (komponenty alergenů, rekombinantní alergeny), respektive tvorbu specifických alergických protilátek proti nim. Tyto protilátky jsou označovány jako rekombinantní (rIgE). U dítěte se tak prokázala významná přecitlivělost proti hlavnímu alergenu břízy, potažmo proti alergenům jiných stromů. A nejen to, byla prokázána senzibilizace i proti hlavním alergenům trav, kočky i roztočů. A jak již bylo naznačeno, díky této metodě se identifikovaly senzibilizace proti velmi rizikovým semenným složkám, nebezpečným semenným komponentám. Výše jmenované bílkoviny arašídu mají ubikvitérní výskyt, jsou přítomny v celé řadě ořechů i jiných semen. V důsledku toho jsou nositeli bohatých zkřížených reaktivit – mluví se o bílkovinných rodinách, o panalergenech. V naší kazuistice jde konkrétně o riziko alergie k rodině vicilinů, konglutinů a 2S-albuminů.
Pro představu, bílkoviny homologní k vicilinu arašídu najdeme například v lískovém i vlašském oříšku, v kešu i pistácii, v sóje i hrášku anebo v sezamu i pohance. A 2S-albumin může být nebezpečný také v hořčičném semínku, řepce olejce anebo ve slunečnici. Proto k eliminační bezořechové a bezsemenné dietě je vhodné i pohotovostní vybavení autoinjektorem s adrenalinem, a to i přesto, že k žádné anafylaxi nikdy nedošlo. Opravdu stoprocentní eliminaci nemůže zaručit nikdo. Jde o preventivní krok, s nadsázkou o šestý krok, který má zabránit rozvoji možné systémové reakce. A objektivní – imunologické i alergologické – předpoklady k tomu dítě jednoznačně má. Nezapomínejme, že se s ústupem ekzému objevilo astma, tedy onemocnění se skrytým proanafylaktickým
potenciálem.
A dosud poslední novinkou je zjištění nedostatečné aktivity diaminooxidázy (DAO). Jde o enzym štěpící exogenní i endogenní histamin, ale i jiné biogenní aminy. Pravděpodobně však nejde o primární histaminovou intoleranci, ale pouze o sekundární snížení produkce DAO u multiproteinové potravinové senzibilizace – sedmý krok. Zde se předpokládá dlouhodobá alterace nejpilnějších producentů tohoto enzymu – enterocytů. Pokud se objeví symptomy nedostatku aktivity DAO – kupříkladu erytémy, bolesti hlavy, bolesti břicha, průjmy, palpitace apod., pak by měla být indikována i perorální substituce DAO.
Diskuse
Uvedená kazuistika je učebnicovým příkladem alergického pochodu. Do průběhu pouhých pěti let je soustředěno vše, co k této problematice patří. Následuje komentář klíčových bodů diagnózy i léčby, včetně farmakoterapie.
Multiproteinové potravinové alergie se obtížně diagnostikují, ještě obtížněji se léčí [1, 2]. Prakticky vždy je nutná rozsáhlá eliminace, nezřídka všech základních potravin – mléka, vajíčka i mouky, respektive lepku. Tento postup přináší jedno velké nebezpečí a tím je malnutrice dítěte [3, 4]. Plné kojení situaci vyřešit nemusí, s přibývajícím věkem jsou nutné příkrmy, tj. komplementární strava [5]. Jakýkoli zákaz musí na druhou stranu být adekvátně hrazen. Za mléko jiné „mléko“. Za mouku jiná nutriční i kalorická hodnota. Do určitého věku (do 2–3 let) tento požadavek splní přípravky s volnými aminokyselinami [6, 7]. Později se může vyřešit spontánně – potravinová přecitlivělost má s věkem tendenci vyhasínat. Zvýšené hodnoty alergických protilátek se tak mohou i normalizovat. Ale v určitém procentu případů k tomu nedojde (naše kazuistika). Za těchto okolností jsou naprosto nezbytné expozice či reexpozice i těm potravinám, vůči nimž senzibilizace přetrvává. K tomu slouží doporučující postupy i standardizované protokoly, pro riziko nežádoucí reakce za lékařského dohledu, a to buď ambulantně, anebo na lůžku. Ve více než 80 % případů se prokáže úplná tolerance, nebo alespoň slušná tolerance určité stopové (prahové) dávky [8]. Důsledkem je povolení dosud přísně eliminované potraviny. A to i v případě, že senzibilizace objektivně přetrvává. Zodpovědná je jednak pouhá existence vysokých koncentrací alergických protilátek (sIgE, rIgE), které neměly nikdy žádný klinický význam, a jednak fenomén, kdy alergické protilátky svůj klinický význam ztratí. Což pochopitelně z pouhého stanovení sIgE, rIgE či pozitivity kožních testů nezjistíme. V našem případě způsobovala přecitlivělost k BKM kojenecké průjmy, možná se sIgE proti BKM podílely i na etiologii ekzému, později svou agresi pozbyly. Došlo k imunologické toleranci [1, 6].Při zákazu konzumace živočišného mléka bez náležité „mléčné“ náhrady (kojení, AAF, rostlinná mléka) by se nemělo zapomínat na doplnění chybějících bílkovin a vápníku. Bílkoviny obvykle nahradí dostatečná dodávka masa a luštěnin (sója), pokud to alergický profil pacienta dovolí. Vápník se přidává do stravy většinou jako calcium chloratum. Dávka musí odpovídat věku dítěte [2, 6, 7].
K zabránění předpokládané reakce mezi potravinovým alergenem a senzibilizovanou imunitou má moderní medicína, krom důsledné eliminace osudového alergenu, jen velmi málo možností. Částečný efekt byl prokázán u kromoglykátu sodného, někdy nazývaného stabilizátor žírných buněk (mastocytů). Při perorálním podání snižuje degranulaci mastocytů střevní mukózy i submukózy zřejmě tím, že blokuje chloridové kanály mastocytárních membrán [9]. Dalším prokázaným účinkem tohoto léčiva je prevence anafylaktických reakcí způsobených potravinovým alergenem [10–12]. Nevýhodou je podávání 4krát denně a možný, byť vzácný, vznik lékové alergie.
Pokud k alergické reakci dojde, nastane nevyhnutelně i rozvoj alergického zánětu (slizniční, kožní, systémový). Důsledkem je mimo jiné vyplavení prozánětlivých cytokinů se všemi změnami histologickými, histochemickými i klinickými. Cytokinů prohlubujících alergický zánět jsou desítky, ale jen proti některým máme možnost zasáhnout. K tomuto účelu slouží antimetabolity, přípravky s nepřímým a někdy i přímým protizánětlivým efektem. Jen některé z nich ovšem můžeme použít u nejmenších dětí.
K nejznámějším mediátorům časné alergické reakce patří histamin. Antihistami-nika první generace se začala používat v padesátých letech minulého století, druhá generace pomáhá našim alergikům více
než třicet let, netřeba představovat. Mezi pozdní mediátory počítáme leukotrieny a proti nim máme k dispozici antileukotrieny. U multiproteinových senzibilizací, respektive u manifestních alergií, se dle zahraničních studií doporučuje obojí [13]. Zmíněné antimetabolity nejen zmírňují příznaky, ale zasahují i do podstaty alergického zánětu. Jsou cenné až nenahraditelné zvláště v případě idiopatických reakcí, v případě neodhaleného spouštěče, ale především při obtížně realizovatelné dietě.
K potlačení těžkých forem alergického zánětu se mohou použít systémové kortikosteroidy, s touto léčbou je ale třeba zacházet velmi opatrně [3, 4]. Naštěstí tíže naší kazuistiky nedosahovala takového stupně, abychom se k jejich podávání museli uchýlit. Jiná situace nastává při potřebě preventivní léčby komorbidit alergického pochodu, v případě astmatu se má respektovat jak charakter, tak i rizika. A to u multiproteinové potravinové alergie platí dvojnásob, úplná kompenzace astmatu by měla být podmínkou.
U potravinových alergií, kde potenciálním alergenem jsou proanafylaktické potraviny (mléko, vejce, lepek, ořechy, některá semena, ryby, korýši), by se mělo myslet i na prevenci anafylaxe [13–15]. A to i v případě, že k žádné systémové reakci dosud nedošlo. Známými kofaktory potenciální anafylaxe jsou dětský věk, astma a prokázaná senzibilizace k proanafylaktickým složkám (komponentám) rizikových potravin. V takovém případě, včetně případu naší kazuistiky, je k laické první pomoci vybavení adrenalinem (autoinjektor) víceméně nezbytností [16]. Naopak kortikosteroidy u anafylaxe pro akutní použití v rámci první pomoci své místo nemají [17, 18].
Některé potravinové alergie mají u nejmenších dětí tendenci vyhasínat. Například kojenecká alergie k BKM vyhasne u 9 z 10 dětí ještě do tří let věku [6]. Obdobně je tomu u vajíčka. Horší prognózu má dětská alergie k arašídům, do dospělosti vyhasne jen u 20 % pacientů [8]. S fenoménem vyhasínání se musí počítat pro expozice nebo reexpozice. Jedině expozice určí, zda nenastala po určité době úspěšné eliminace imunologická tolerance. Jedině expozice určí, zda se může nastavená dieta zrušit. Jedině expozice v řadě případů pomůže vyřešit jinak neřešitelné nutriční otazníky. Vysvětlením pozdního navození orální tolerance se zabývá mnoho týmů celého světa. Existuje více teorií – od nezralosti samotného trávicího systému přes nezralost regulačních lymfocytů až po hygienickou hypotézu [1].
Někteří pacienti nedostatečně metabolizují biogenní aminy v čele s histaminem. Čím vyšší aktivita enzymu DAO, tím kratší poločas exogenního i endogenního histaminu a naopak. Intraluminární koncentrace DAO může být u 1–3 % populace primárně snížena, pravděpodobnější však bude sekundární pokles. A to při jakékoli alteraci střevní mukózy, tj. poškození hlavního producenta tohoto enzymu – enterocytů. Sem patří i alergický zánět, který je při multiproteinové potravinové alergii lokalizován také ve sliznici trávicího traktu [2].
Závěr
Kojenecký ekzém by mohl být prvním krokem alergického pochodu. Relativně často prokážeme imunologickou senzibilizaci, méně často pravou alergii. Pokud se ale k postižení kůže přidávají i obtíže gastrointestinální, je přímá účast potravinové alergie pravděpodobnější. Nejčastějším spouštěčem u malých dětí jsou BKM, méně bílkoviny vajíčka a obilovin (lepek). Na druhé straně má alergie k těmto základním potravinám tendenci vyhasínat, ve většině případů dojde k navození orální tolerance ještě v batolecím věku. Ale pozor – atopická stopa může zůstat, budoucí manifestaci respirační alergie očekávejme minimálně v polovině případů. V předškolním věku to bývá astma, ve školním věku se může přidat alergická rýma.
Základní léčbou multiproteinové potravinové alergie je režim – eliminační dieta. Pacient se vyhýbá potravinám, které způsobují problémy, někdy i potravinám se zjištěnou senzibilizací. Náhradou zakázaných bílkovin mohou být speciální dietetika, včetně AAF. Každou dietu je třeba s odstupem času revidovat, jednak z důvodu zhodnocení efektu, jednak z důvodu možné změny v orální toleranci. U senzibilizace mediované IgE se expozice mají provádět ve zdravotnickém zařízení, především pro riziko časné reakce.
Farmakoterapie potravinové alergie spočívá v podávání antihistaminik, kromoglykátu sodného, zkoušejí se i antileu-
kotrieny. Nesmíme zapomínat na substituci potravinovými doplňky včetně mikronutrientů. Hrozí-li anafylaxe, o které mj. informují rizikové faktory i konkretizace potravinové senzibilizace, je indikován záchranný adrenalin v autoinjektoru. Mezi rizika nejvyššího významu patří senzibilizace k proanafylaktickým alergenům, respektive k proanafylaktickým komponentám, a pak rovněž koexistence astmatu.
Seznam použité literatury
- [1] Benhamou AH, Vanini G, Lantin JP, Eigenmann PA. Antihistamine and sodium cromoglycate medication for food cold water exercise-induced anaphylaxis. Allergy 2007; 62: 1471–1472.
- [2] Brown SG, Stone SF, Fatovich DM, et al. Anaphylaxis: Clinical patterns, mediator release, and severity. J Allergy Clin Immunol 2013; doi: 10.1016/j.jaci.2013.06.015.
- [3] Fiocchi A, Brozek J, Schünemann H, et al. World Allergy Organization (WAO) Diagnosis and Rationale for Action against Cow‘s Milk Allergy (DRACMA) Guidelines. World Allergy Organ J 2010; 3: 57–161.
- [4] Fleischer DM, Perry TT, Sampson HA, et al. Allergic Reactions to Foods in Preschool-Aged Children in a Prospective Observational Food Allergy Study. Pediatrics 2012; 130: e25–e32.
- [5] Frew AJ. What are the ‚ideal‘ features of an adrenaline (epinephrine) auto-injector in the treatment of anaphylaxis? Allergy 2011; 66: 15–24.
- [6] Choo KJ, Simons FE, Sheikh A. Glucocorticoids for the treatment of anaphylaxis. Evid Based Child Health 2013; 8: 1276–1294.
- [7] Choo KJ, Simons FE, Sheikh A. Glucocorticoids for the treatment of anaphylaxis. Cochrane Database Syst Rev 2012; 4: CD007596. doi: 10.1002/14651858.CD007596.pub3.
- [8] Katz A, Virk Hundal N, et al. Cow‘s Milk Allergy: A New Approach Needed? J Pediatr 2013; 163: 620–622.
- [9] Jiji F, Suko M. Effectiveness of disodium cromoglycate in food-dependent, exercise-induced anaphylaxis: a case report. Ann Allergy 1994; 72: 452–454.
- [10] Masilamani M, Commins S, Shreffler W. Determinants of Food Allergy. Immunol Allergy Clin North Am 2012; 32: 11–33.
- [11] Peroni DG, Piacentini GL, Piazza M, et al. Combined cetirizine-montelukast preventive treatment for food-dependent exercise induced anaphylaxis. Ann Allergy Asthma Immunol 2010; 104: 272–273.
- [12] Sheikh A, Simons FE, Barbour V, Worth A. Adrenaline auto-injectors for the treatment of anaphylaxis with and without cardiovascular collapse in the community. Cochrane Database Syst Rev 2012; 8: CD008935. doi: 10.1002/14651858.CD008935.pub2.
- [13] Shin HY, Kim JS, An NH, et al. Effect of disodium cromoglycate on mast cell-mediated immediate-type allergic reactions. Life Sci 2004; 74: 2877–2887.
- [14] Sicherer SH, Vargas PA, Groetch ME, et al. Development and validation of educational materials for food allergy. J Pediatr 2012; 160: 651–656.
- [15] Sugimura T, Tananari Y, Ozaki Y, et al. Effect of oral sodium cromoglycate in 2 children with food-dependent exercise-induced anaphylaxis (FDEIA). Clin Pediatr 2009; 48: 945–950.
- [16] Venter C. How to manage multiple food allergies in children. Clin Transl Allergy 2011; 1: S27.
- [17] von Berg A. Dietary interventions for primary allergy prevention – what is the evidence? World Rev Nutr Diet 2013; 108: 71–78.
- [18] Wang J. Management of the Patient with Multiple Food Allergies. Curr Allergy Asthma Rep 2010; 10: 271–277.