Bezpečnost dlouhodobého podávání tiotropia u pacientů s CHOPN
Článek přehledně shrnuje data týkající se bezpečnosti 4letého podávání tiotropia u pacientů s chronickou obstrukční plicní nemocí (CHOPN) ve studii UPLIFT. Nežádoucí účinky se objevovaly přibližně ve stejné míře v obou ramenech studie. U pacientů léčených tiotropiem bylo zaznamenáno výrazně méně nežádoucích účinků vedoucích k přerušení účasti ve studii a fatálních nežádoucích účinků. Bylo prokázáno, že dlouhodobé podávání tiotropia statisticky významně snižuje počty kardiálních a respiračních závažných nežádoucích účinků v porovnání s kontrolní skupinou léčenou standardní medikací pro CHOPN. Rovněž bylo prokázáno, že dlouhodobá pravidelná aplikace tiotropia významně snižuje riziko celkové mortality v porovnání s kontrolní skupinou.
Úvod
Řada předchozích krátkodobých studií prokázala zlepšení mnoha parametrů včetně bezpečnosti při léčbě tiotropiem u pacientů s chronickou obstrukční plicní nemocí (CHOPN). Čtyřletá studie UPLIFT (Understanding of Potential Long-term Impact on Function of Tiotropium) [1] měla ověřit dlouhodobý účinek léčby tiotropiem na průběh CHOPN včetně určení jeho bezpečnosti, a to v průběhu celého 4letého období trvání studie.
Čtyřletá studie UPLIFT
Jednalo se o randomizovanou, dvojitě zaslepenou, paralelně probíhající klinickou studii kontrolovanou placebem, do níž byli zařazeni pacienti se středně těžkou až velmi těžkou CHOPN. Nemocní dostávali tiotropium v dávce 18 mg denně nebo placebo pomocí inhalačního systému HandiHaler. Byly povoleny veškeré léky určené k léčbě respiračního systému s výjimkou ostatních inhalačních anticholinergik. Všem pacientům bylo doporučeno zanechat kouření. Po ukončení studijního období bylo všem pacientům doporučeno užívat ipratropium v dávce 2 vdechy 4krát denně po dobu 30 dnů, tj. do doby konečného vyhodnocení studie.
Během tohoto období se nežádoucí účinky objevovaly v obou ramenech studie, a to přibližně ve stejné míře. U pacientů léčených tiotropiem však bylo zaznamenáno výrazně méně nežádoucích účinků vedoucích k přerušení účasti ve studii (618 vs. 735) a fatálních nežádoucích účinků (381 vs. 411). Při hodnocení fatálních nežádoucích účinků je třeba mít na zřeteli, že obecně mortalita takto nemocných bývá poměrně vysoká. Ve studii UPLIFT byla mortalita hodnocena jednak v léčebné fázi (počínaje randomizací a konče 30. dnem po ukončení léčby), jednak byl vitální status hodnocen výhradně během léčebné periody a jednak během léčebné periody společně se 30 dny po ukončení léčby. Příčinu případného úmrtí hodnotili jak samotní výzkumníci, tak i nezávislá komise. Pro optimální zhodnocení takto tvrdých dat je nutné mít k dispozici relativně robustní vzorek populace. Co se týče počtu pacientů setrvávajících ve studii i po 45. měsíci trvání studie v obou jejích ramenech, byl tento požadavek splněn (98 % vs. 97,2 %). Ačkoliv v 1470. dni byl počet sledovaných pacientů srovnatelný mezi oběma skupinami, byl již poněkud nižší (75 % vs. 75 %).Analýzou sebraných dat bylo zjištěno, že dlouhodobá pravidelná aplikace tiotropia významně snižuje riziko celkové mortality v porovnání s kontrolní skupinou, a to o 16 % (p = 0,016). Odpovídajícího výsledku bylo dosaženo i při hodnocení vitálního statusu v 1440. dni (tj. v protokolem definovaném dni ukončení studie), kde byli zahrnuti i ti nemocní, kteří předčasně ukončili svoji účast ve studii (HR = 0,87; p = 0,034). Pravděpodobně vzhledem k menšímu počtu pacientů nebyl pozorovaný rozdíl v celkové mortalitě u pacientů 1470. den již statisticky signifikantní, tento rozdíl činil 11 % (p = 0,86).
Ve studii UPLIFT však nebyla hodnocena pouze celková mortalita, ale současně také mortalita orgánová (úmrtí z kardiálních či respiračních příčin, malignity nebo celkové a ostatní příčiny), a to ve dni 1470, přičemž s ohledem na jednotlivé orgány nebyl při prvním rámcovém hodnocení zjištěn mezi skupinami výraznější rozdíl; ten se týkal až sumace všech fatálních nežádoucích příhod, jejichž výskyt vyzněl ve prospěch tiotropia (14,9 % vs. 16,5 %). Dalším důležitým zjištěním studie UPLIFT je, že celková mortalita nebyla závislá na věku, pohlaví, kouření a na jakékoliv terapii.Těsně před zahájením studie UPLIFT byla publikována rozsáhlá metaanalýza [2], jejímž závěrem bylo, že inhalační anticholinergika zvyšují kardiovaskulární mortalitu a výskyt cévních mozkových příhod. Na popud této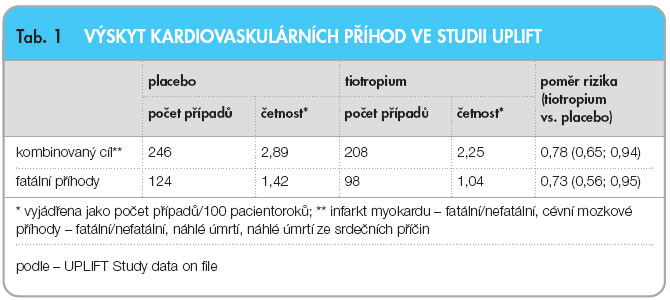 práce byl ve studii UPLIFT použit kombinovaný cíl složený z kardiovaskulárních příhod (infarkt myokardu – fatální/nefatální, cévní mozkové příhody – fatální/nefatální, náhlé úmrtí, náhlé úmrtí ze srdečních příčin), pomocí něhož bylo ukázáno, že tiotropium nejenže nezvyšovalo, ale dokonce oproti placebu snižovalo výskyt tohoto cíle (RR: 0,78; 95% CI: 0,65–0,94) a při hodnocení pouze fatálních příhod byl tento cíl dokonce ještě nižší (RR: 0,73; 95% CI: 0,56–0,95), viz tab. 1. Nezávažné nežádoucí účinky se vyskytovaly napříč oběma rameny studie. Výrazněji v neprospěch tiotropia vyzněl pouze výskyt pocitu sucha v ústech, což je dáno samotným mechanismem účinku tohoto léčiva (tab. 2).
práce byl ve studii UPLIFT použit kombinovaný cíl složený z kardiovaskulárních příhod (infarkt myokardu – fatální/nefatální, cévní mozkové příhody – fatální/nefatální, náhlé úmrtí, náhlé úmrtí ze srdečních příčin), pomocí něhož bylo ukázáno, že tiotropium nejenže nezvyšovalo, ale dokonce oproti placebu snižovalo výskyt tohoto cíle (RR: 0,78; 95% CI: 0,65–0,94) a při hodnocení pouze fatálních příhod byl tento cíl dokonce ještě nižší (RR: 0,73; 95% CI: 0,56–0,95), viz tab. 1. Nezávažné nežádoucí účinky se vyskytovaly napříč oběma rameny studie. Výrazněji v neprospěch tiotropia vyzněl pouze výskyt pocitu sucha v ústech, což je dáno samotným mechanismem účinku tohoto léčiva (tab. 2).
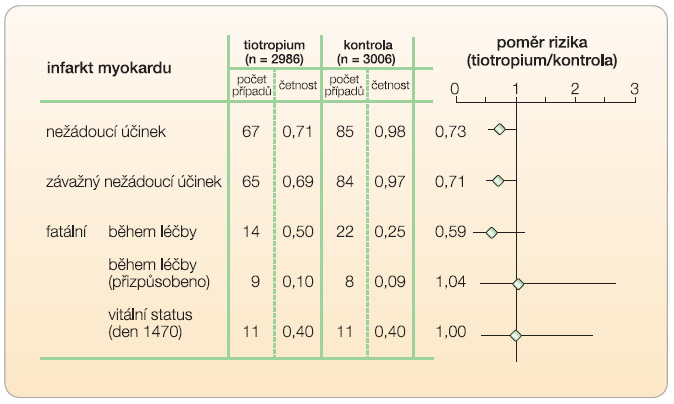
Současně však byly hodnoceny také závažné nežádoucí účinky, a to především kardiální (anginózní potíže, fibrilace síní, kardiální selhání, nemoc věnčitých tepen a infarkt myokardu) a respirační (bronchitida, exacerbace CHOPN, dušnost, pneumonie a respirační selhání). Při léčbě tiotropiem bylo pozorováno statisticky významně nižší riziko výskytu jak kardiálních (3,56 vs. 4,21 případů/100 pacientoroků), tak i respiračních (11,32 vs. 13,47 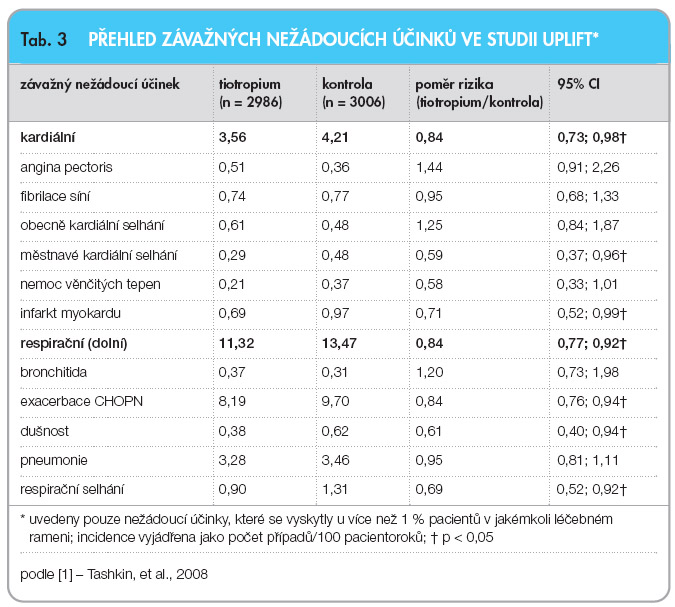 případů/100 pacientoroků) závažných nežádoucích účinků – výraznější rozdíl se týkal především městnavého srdečního selhání a infarktu myokardu, dále pak exacerbací CHOPN, dušnosti a respiračního selhání (tab. 3). Mezi oběma rameny studie nebyl zjištěn statisticky významný rozdíl ve výskytu cévních mozkových příhod. S ohledem na výskyt infarktu myokardu bylo riziko v rameni s tiotropiem nižší jak co do výskytu nefatálních, tak i fatálních příhod (graf 1). Obdobná situace se týká také rizika respiračního selhání, ačkoliv v tomto případě rozdíl ve výskytu fatálních nežádoucích účinků nedosáhl statisticky významného rozdílu.
případů/100 pacientoroků) závažných nežádoucích účinků – výraznější rozdíl se týkal především městnavého srdečního selhání a infarktu myokardu, dále pak exacerbací CHOPN, dušnosti a respiračního selhání (tab. 3). Mezi oběma rameny studie nebyl zjištěn statisticky významný rozdíl ve výskytu cévních mozkových příhod. S ohledem na výskyt infarktu myokardu bylo riziko v rameni s tiotropiem nižší jak co do výskytu nefatálních, tak i fatálních příhod (graf 1). Obdobná situace se týká také rizika respiračního selhání, ačkoliv v tomto případě rozdíl ve výskytu fatálních nežádoucích účinků nedosáhl statisticky významného rozdílu.
Závěr
 Výsledky studie UPLIFT, které se týkaly bezpečnosti léčby tiotropiem, byly zásadní v tom, že nepotvrdily závěry rozsáhlé metaanalýzy publikované bezprostředně před uveřejněním výsledků studie UPLIFT. Metaanalýza publikovaná dr. Singhem [2] zdůrazňovala především kardiovaskulární nežádoucí účinky inhalačních anticholinergik jako celé skupiny. Studie UPLIFT naopak potvrzuje, že dlouhodobé podávání tiotropia statisticky významně snižuje počty kardiálních a respiračních závažných nežádoucích účinků v porovnání s kontrolní skupinou léčenou standardní medikací pro CHOPN. Tiotropium oproti této léčbě snižuje především výskyt městnavého srdečního selhání, infarktu myokardu, exacerbací CHOPN, dušnosti a respiračního selhání a neovlivňuje počty cévních mozkových příhod. Studie UPLIFT během svého 4letého trvání přinesla jednoznačné pozitivní výsledky podporující dosavadní klinické zkušenosti ve smyslu významného snížení rizika kardiální i respirační morbidity a celkové mortality. Současně tak potvrdila pozitivní bezpečnostní profil tiotropia v dlouhodobé udržovací léčbě pacientů s chronickou obstrukční nemocí plic. Tiotropium má v současné době výrazné postavení v léčbě stabilizované CHOPN. Je indikováno pro pacienty s CHOPN stadia II a vyššího. Studie UPLIFT prokázala, že nejúčinnější je léčba tiotropiem v časných stadiích CHOPN, to znamená právě ve stadiu II, kde je dnes možno tiotropium považovat za lék první volby.
Výsledky studie UPLIFT, které se týkaly bezpečnosti léčby tiotropiem, byly zásadní v tom, že nepotvrdily závěry rozsáhlé metaanalýzy publikované bezprostředně před uveřejněním výsledků studie UPLIFT. Metaanalýza publikovaná dr. Singhem [2] zdůrazňovala především kardiovaskulární nežádoucí účinky inhalačních anticholinergik jako celé skupiny. Studie UPLIFT naopak potvrzuje, že dlouhodobé podávání tiotropia statisticky významně snižuje počty kardiálních a respiračních závažných nežádoucích účinků v porovnání s kontrolní skupinou léčenou standardní medikací pro CHOPN. Tiotropium oproti této léčbě snižuje především výskyt městnavého srdečního selhání, infarktu myokardu, exacerbací CHOPN, dušnosti a respiračního selhání a neovlivňuje počty cévních mozkových příhod. Studie UPLIFT během svého 4letého trvání přinesla jednoznačné pozitivní výsledky podporující dosavadní klinické zkušenosti ve smyslu významného snížení rizika kardiální i respirační morbidity a celkové mortality. Současně tak potvrdila pozitivní bezpečnostní profil tiotropia v dlouhodobé udržovací léčbě pacientů s chronickou obstrukční nemocí plic. Tiotropium má v současné době výrazné postavení v léčbě stabilizované CHOPN. Je indikováno pro pacienty s CHOPN stadia II a vyššího. Studie UPLIFT prokázala, že nejúčinnější je léčba tiotropiem v časných stadiích CHOPN, to znamená právě ve stadiu II, kde je dnes možno tiotropium považovat za lék první volby.
Seznam použité literatury
- [1] Wagner LE II, Eaton M, Sabnis SS, Gingrich KJ. Meperidine and lidocaine block of recombinant voltage-dependent Na+ channels: evidence that meperidine is a local anesthetic. Anesthesiology 1999; 91: 1481–1490.
- [2] Izenwasser S, Newman AH, Cox BM, Katz JL. The cocaine-like behavioral effects of meperidine are mediated by activity at the dopamine transporter. Eur J Pharm 1996; 297: 9–17.
- [3] Takada K, Clark DJ, Davies MF, et al. Meperidine exerts agonist activity at the a2B-adrenoceptor subtype. Anesthesiology 2002; 96: 1420–1426.
- [4] Walker DJ, Zacny JP. Subjective, psychomotor, and physiological effects of cumulative doses of opioid m agonists in healthy volunteers. J Pharmacol Exp Ther 1999; 289: 1454–1464.
- [5] Hess L, Mühlbachová E, Fischerová D, Pařízek A. Sedace a analgezie u porodu. In Pařízek A. a kol.: Porodnická analgezie a anestezie. Praha, Grada Publishing 2002; 223–229.