Dávkovací režimy bisfosfonátů používaných v léčbě postmenopauzální osteoporózy
Bisfosfonáty, syntetická analoga pyrofosfátu se silnou afinitou ke kostní tkáni, patří mezi nejčastěji používaná léčiva v terapii osteoporózy. Inhibují funkce osteoklastů a tím potlačují kostní resorpci. Kromě postmenopauzální osteoporózy jsou indikovány v léčbě mužské a glukokortikoidy indukované osteoporózy a Pagetovy choroby; široké využití nalézají rovněž u onkologických pacientů. V léčbě postmenopauzální osteoporózy se v současné době používají dusíkaté bisfosfonáty s prodlouženým dávkovacím intervalem. Podávání jedné tablety jednou týdně (alendronát, risedronát) se ukázalo jako výhodnější díky vyšší adherenci k léčbě než léčba klasickými denními režimy. Ze stejného důvodu je alendronát nyní dostupný i ve fixní kombinaci s vitaminem D. Motivací pro vývoj přípravků s dále prolongovaným intervalem podávání jsou preference pacientů. Vyšší adherence k léčbě jednou tabletou měsíčně (ibandronát) však zatím nebyla konzistentně prokázána. Léčba ibandronátem však může být vhodnou alternativou u pacientů s gastrointestinálními obtížemi či komorbiditami, kteří špatně tolerují týdenní podávání alendronátu či risedronátu. I přes značné pokroky je adherence pacientů k léčbě osteoporózy stále nedostatečná. Poměrně nový přístup v léčbě postmenopauzální osteoporózy představuje intravenózní aplikace bisfosfonátů, která může být výhodná zejména u starších pacientů neschopných dodržet doporučení pro perorální lékové formy (zůstat dostatečnou dobu ve vzpřímené poloze) nebo u pacientů s polyfarmakoterapií či psychiatrickými komorbiditami. Ibandronát aplikujeme jako injekci jednou za tři měsíce a zoledronát ve formě infuze jednou ročně.
Úvod
Bisfosfonáty (BIS) představují velmi dobře zavedenou a široce používanou lékovou skupinu v terapii kostních onemocnění. Jedná se o syntetická stabilní analoga pyrofosfátu se silnou afinitou ke kostní tkáni. BIS jsou indikovány v léčbě osteoporózy (postmenopauzální, mužské a glukokortikoidy indukované) a Pagetovy choroby. V onkologii je těžištěm jejich využití nádorová osteolýza, hyperkalcemie způsobená nádorem a prevence kostních příhod u pacientů s pokročilou formou nádorového onemocnění postihujícího kosti [1–4]. V tomto sdělení podáváme přehled BIS používaných v léčbě postmenopauzální osteoporózy a zaměříme se na jejich dávkovací režimy včetně specifik jejich podávání.
V ČR jsou pro léčbu postmenopauzální osteoporózy registrovány dusíkaté BIS (d-BIS) alendronát, risedronát, ibandronát a nově také zoledronát. Alendronát je dostupný rovněž ve fixní kombinaci s vitaminem D3. Alendronát, risedronát a zole-dronát snižují riziko vertebrálních i non-vertebrálních zlomenin (včetně zlomenin kyčle). Při podávání ibandronátu bylo prokázáno snížení rizika vertebrálních zlomenin; průkaz snížení rizika non-vertebrálních zlomenin je prozatím opřen o post-hoc analýzu studie BONE, ve které bylo snížení tohoto rizika prokázáno u populace s nízkou denzitou kostního minerálu (bone mineral density – BMD) v oblasti krčku femuru. Starší etidronát rovněž snižuje riziko vertebrálních zlomenin, ale jeho význam v léčbě osteoporózy je kvůli častějším nežádoucím účinkům již malý; v ČR v současné době není registrován [1–7].
Mechanismus účinku
Mechanismem účinku d-BIS je inhibice kostní resorpce snížením aktivity osteoklastů a zvýšením jejich apoptózy. Látky ze skupiny d-BIS tlumí kostní resorpci inhibicí farnesyldifosfátsyntázy, jednoho z klíčových enzymů mevalonátové cesty syntézy cholesterolu. Inhibice tohoto enzymu stoupá v gradientu: alendronát ģ ibandronát ģ risedronát ģ zoledronát. Útlum kostní resorpce je následován rovněž útlumem novotvorby kosti. Dochází k celkovému zpomalení procesu kostní remodelace a zvyšuje se denzita kostního minerálu. Přestože d-BIS účinkují především prostřednictvím prenylace proteinů, jejich schopnost adsorpce na kostní minerál také přispívá k antiresorpčnímu účinku a jeho přetrvání. Díky své struktuře (tzv. kostní háček) se d-BIS váží na hydroxyapatit kostní tkáně v místech aktivní remodelace. Vazebná afinita jednotlivých d-BIS závisí na postranních řetězcích molekuly a stoupá následovně: ibandronát = risedronát ģ alendronát ģ zoledronát. Tyto odlišnosti pravděpodobně zodpovídají za některé rozdíly v intenzitě účinku a v rychlosti jeho nástupu či délce přetrvávání [6–8].
Farmakokinetika
Po perorálním podání se v žaludku a hlavně v tenkém střevě vstřebává 0,6–3 % podané dávky d-BIS. Resorpce je výrazně snížena v přítomnosti potravy. S vápníkem, hořčíkem a železem vytvářejí d-BIS nevstřebatelné sloučeniny. Např. biologická dostupnost ibandronátu při podání s běžnou snídaní klesá o 90 %. Plazmatický poločas je krátký, vazba na plaz-matické proteiny zanedbatelná. Značná část vstřebané látky se bez metabolizace vylučuje ledvinami. Asi 40–60 % dávky d-BIS se zabudovává do kostní tkáně, kde může mít poločas více než 10 let [3, 8].
Nežádoucí účinky
Gastrointestinální obtíže
Více či méně vyjádřený „class effect“ skupiny d-BIS představuje potenciál ke dráždění jícnu – zejména při nedodržování doporučení výrobce. V kontrolovaných studiích byla gastrointestinální (GIT) tolerance d-BIS srovnatelná s placebem. V klinické praxi byly ale popsány ezofagitidy a ulcerace jícnu rovněž v souvislosti s užíváním alendronátu. Některé studie typu „head to head“ ukázaly vyšší výskyt mírných horních GIT příhod při podávání alendronátu ve srovnání s etidronátem, kalcitoninem a estrogenem. Proto by alen-dronátem neměli být léčeni pacienti s chorobami jícnu [1–4]. Na základě hodnocení pomocí endoskopického vyšetření byla kvůli zvýšení rizika žaludečních vředů doporučena opatrnost při podávání alendronátu současně s nesteroidními antiflogistiky (NSAID) [9]. Další studie běžné populace však neukázaly zvýšené GIT riziko. Výskyt krvácení do horní části GIT nebyl při podávání d-BIS častější, a to ani při komedikaci s NSAID, oproti podávání NSAID samotných [10]. Léčba risedronátem nezvyšovala u rizikových pacientů výskyt nežádoucích příhod v oblasti horního GIT [11]. V japonské studii bylo ale zjištěno, že u pacientů s revmatoidní artritidou dlouhodobě léčených NSAID je užívání d-BIS (stejně jako vyšší věk a kuřáctví) spojeno se zvýšením rizika vzniku gastroduodenálních vředů. Komedikace inhibitory protonové pumpy a H2-blokátory se ukázala jako významný protektivní faktor [12].
Reakce akutní fáze
Po podání d-BIS se může objevit teplota a příznaky podobné chřipce. Jedná se o reakci akutní fáze vyvolanou rychlým uvolněním prozánětlivých cytokinů. Tyto obtíže bývají typicky spojovány s intravenózním (i.v.) podáním d-BIS, ale mohou se vyskytnout rovněž po perorálním podání. Nejčastěji se uvedené symptomy objevují u pacientů, kteří dosud nebyli d-BIS léčeni, jejich výskyt po opakovaném podání je výrazně nižší. Těmto obtížím můžeme předcházet podáním paracetamolu nebo NSAID bezprostředně po aplikaci d-BIS [13].
Skeletální rizika
Hlášené případy osteonekrózy čelisti se týkají rovněž především d-BIS podávaných i.v. zejména v onkologických indikacích (zoledronát, pamidronát) [7, 8]. V souvislosti s dlouhodobou léčbou d-BIS byla publikována data, která ukazují zvýšený výskyt atypických subtrochanterických zlomenin femuru [14].
Kontraindikace
Kontraindikacemi podávání d-BIS je hypokalcemie, deficit vitaminu D, závažná renální insuficience a neschopnost dodržet doporučení výrobce (zůstat po doporučenou dobu ve vzpřímené poloze) [1–3, 8]. Léčba d-BIS není určena dětem a dospívajícím ani těhotným nebo kojícím ženám. Pokud je podávání d-BIS zvažováno u žen ve fertilním věku (např. kvůli glukokortikoi-dy indukované osteoporóze), doporučuje se léčba d-BIS s kratším poločasem v kosti.
Lékové formy
Nejdéle používané d-BIS k léčbě postmenopauzální osteoporózy jsou k dispozici v perorálních lékových formách (tablety). Výhodnou novější alternativou může být intravenózní podávání (ibandronát, zoledronát) [1–3, 8].
Perorální bisfosfonáty
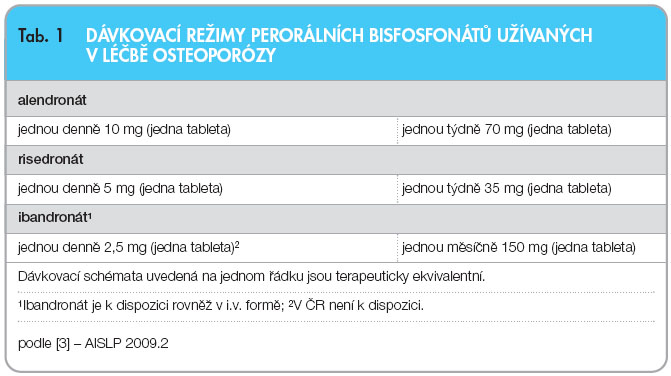 Farmakodynamické vlastnosti skupiny d-BIS umožnily vývoj přípravků s delším dávkovacím intervalem. Terapeuticky ekvivalentní režimy jsou uvedeny v tab. 1 [3]. Vzhledem k nízké variabilní absorpci a iritačnímu potenciálu na horní úsek GIT je třeba při užívání perorálních d-BIS dodržovat několik zásad [1–3], viz tab. 2.
Farmakodynamické vlastnosti skupiny d-BIS umožnily vývoj přípravků s delším dávkovacím intervalem. Terapeuticky ekvivalentní režimy jsou uvedeny v tab. 1 [3]. Vzhledem k nízké variabilní absorpci a iritačnímu potenciálu na horní úsek GIT je třeba při užívání perorálních d-BIS dodržovat několik zásad [1–3], viz tab. 2.
Alendronát
 Alendronát je nejdéle používaným a nejlépe prostudovaným antiresorpčním (antiosteokatabolickým) léčivem. Je doložena účinnost a dobrá tolerance alendronátu i po desetileté léčbě [15], novější data však neukazují výrazné přínosy takto dlouhé léčby [16]. V randomizované dvojitě zaslepené studii nevykazovaly ženy, které se účastnily studie FIT, významně nižší riziko zlomenin (kromě klinických zlomenin obratle) po desetileté léčbě alendronátem ve srovnání s léčbou pětiletou [16]. Nejčastějšími důvody k přerušení léčby bývají dyspepsie, nauzea, zvracení a bolesti břicha [1, 2]. Při denním podávání alen-dronátu jsou nežádoucí účinky v oblasti horního GIT výrazně častější než při podávání placeba. Riziko je zvýšeno u pacientů s GIT onemocněním v anamnéze [15, 17]. Příslib zvýšeného komfortu pro pacienta a zlepšení adherence k léčbě poskytuje nadějná možnost transdermálního podání [18].
Alendronát je nejdéle používaným a nejlépe prostudovaným antiresorpčním (antiosteokatabolickým) léčivem. Je doložena účinnost a dobrá tolerance alendronátu i po desetileté léčbě [15], novější data však neukazují výrazné přínosy takto dlouhé léčby [16]. V randomizované dvojitě zaslepené studii nevykazovaly ženy, které se účastnily studie FIT, významně nižší riziko zlomenin (kromě klinických zlomenin obratle) po desetileté léčbě alendronátem ve srovnání s léčbou pětiletou [16]. Nejčastějšími důvody k přerušení léčby bývají dyspepsie, nauzea, zvracení a bolesti břicha [1, 2]. Při denním podávání alen-dronátu jsou nežádoucí účinky v oblasti horního GIT výrazně častější než při podávání placeba. Riziko je zvýšeno u pacientů s GIT onemocněním v anamnéze [15, 17]. Příslib zvýšeného komfortu pro pacienta a zlepšení adherence k léčbě poskytuje nadějná možnost transdermálního podání [18].
Fixní kombinace alendronát/vitamin D3
Obdobně jako v léčbě kardiovaskulárních onemocnění se i v léčbě osteoporózy prosazuje princip podávání fixní kombinace léčiv v jedné tabletě. Tato strategie se opírá o zjištění vyšší adherence a nižších nákladů na léčbu při podávání kombinované tablety ve srovnání s podáváním obou léčiv odděleně [19, 20]. Prozatím je na našem trhu k dispozici pouze jedna fixní kombinace bisfosfonátu s vitaminem D3, určená k podávání jednou týdně. Jedna tableta obsahuje 70 mg alendronátu a 2800 IU cholekalciferolu. Léčba touto fixní kombinací se ukázala ekonomicky výhodnější než podávání alendronátu s potravními doplňky [21]. U pacientů v naší geografické oblasti však vitamin D v denní dávce 400 IU nepostačuje a je nutno jej dále doplňovat.
Risedronát
Risedronát snižuje riziko zlomenin obdobně jako alendronát, jeho afinita ke kostní tkáni je však nižší a poločas v kosti kratší. Tato odlišnost může být výhodou u některých diagnóz – v terapii glukokortikoidy indukované osteoporózy bývá upřednostňován před alendronátem [8]. Risedronát prokázal svoji účinnost (dle hodnocení BMD během 24 měsíců) v terapii postmenopauzálních žen v časných stadiích rakoviny prsu s rizikem zlomeniny, které byly léčeny inhibitorem aromatázy anastrozolem [22]. Podávání risedronátu (2 mg/kg týdně) se jeví jako nadějný léčebný přístup rovněž u dětí s osteogenesis imperfecta [23].
Ibandronát
Účinky ibandronátu hodnocené jako ovlivnění BMD a snížení kostního obratu u postmenopauzálních žen byly obdobné jako při léčbě alendronátem v dávce 70 mg týdně [24]. Při léčbě ibandronátem se snižuje riziko vertebrálních zlomenin. Podávání tohoto bisfosfonátu je výhodné zejména u osob s rizikem gastrointestinálních obtíží [25, 26]. U pacientů, kteří špatně tolerují podávání denních nebo týdenních forem d-BIS, může být zahájení léčby ibandronátem účinným řešením GIT diskomfortu [26]. Ibandronát byl – stejně jako výše charakterizované d-BIS – s úspěchem podáván i mužům s nízkou kostní denzitou; v mužské populaci stejně jako u žen navodila léčba ibandronátem zvýšení BMD a byla dobře tolerována [27]. Ibandronát je jediným d-BIS, který je pro léčbu osteoporózy registrován k perorálnímu i parenterálnímu podávání.
Parenterální bisfosfonáty
Vhodnou alternativou léčby d-BIS může být jejich i.v. podávání – zejména u pacientů s nízkou adherencí k dlouhodobé léčbě. Jedná se především o starší pacienty s poruchami paměti či demencí, osoby s četnou konkomitantní medikací a dále o pacienty s problémy se setrváním ve vzpřímené poloze nebo s GIT komorbiditami, případně s GIT nežádoucími účinky při podávání perorálních d-BIS [8].
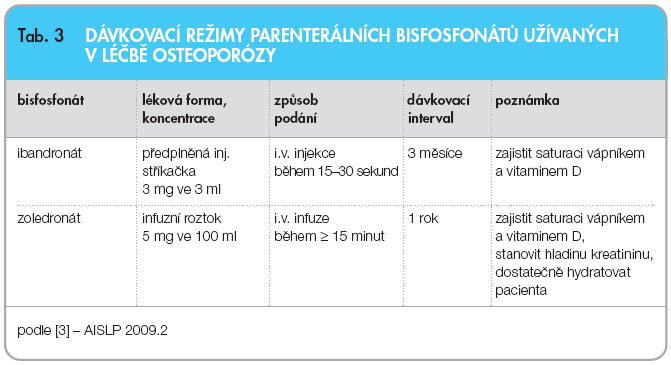 V současné době máme k dispozici ibandronát (3 mg čtvrtletně) a zoledronát (5 mg jednou ročně), viz tab. 3. Intravenózní podávání ibandronátu snižuje výskyt vertebrálních zlomenin více než perorální denní režim [28]. Při podávání zoledronátu (5 mg jednou ročně) v randomizované dvojitě slepé studii s mediánem délky sledování 1,9 roku, jež byla kontrolována placebem, bylo
V současné době máme k dispozici ibandronát (3 mg čtvrtletně) a zoledronát (5 mg jednou ročně), viz tab. 3. Intravenózní podávání ibandronátu snižuje výskyt vertebrálních zlomenin více než perorální denní režim [28]. Při podávání zoledronátu (5 mg jednou ročně) v randomizované dvojitě slepé studii s mediánem délky sledování 1,9 roku, jež byla kontrolována placebem, bylo ![Graf 1 Vliv zoledronátu (5 mg i.v.) na kostní minerální denzitu (BMD) v oblasti bederní páteře (A) a kyčle (B) u postmenopauzálních žen s osteopenií ve srovnání s placebem (průměrná procen-tuální změna oproti počátku studie); podle [31] – Grey, et al., 2009.](https://www.remedia.cz/photo-a-28207---.jpg) dokonce pozorováno snížení celkové mortality. Primárním cílem studie však bylo hodnocení nových klinických zlomenin, jejich výskyt se snížil o 35 % (p < 0,001). Nejčastějšími nežádoucími účinky ve skupině se zole-dronátem byly horečka, myalgie a bolesti kostí a svalů [29]. Přestože je zoledronát podáván jednou ročně, není optimální dávkovací interval dosud přesně znám [30, 31]. Randomizovaná zaslepená studie kontrolovaná placebem sledující 50 postmenopauzálních žen s osteopenií zjistila, že antiresorpční efekt jednorázově podaného zoledronátu (5 mg i.v.) přetrvává nejméně 2 roky. Vliv na markery kostní remodelace a na BMD (graf 1) je srovnatelný po 12 a 24 měsících sledování [31]. V ČR se intravenózní lékové formy ibandronátu a zoledronátu v intenzivnějším dávkování podobně jako některé další BIS (klodronát i.v. a perorální, pamidronát i.v.) běžně používají v onkologických indika-cích [3].
dokonce pozorováno snížení celkové mortality. Primárním cílem studie však bylo hodnocení nových klinických zlomenin, jejich výskyt se snížil o 35 % (p < 0,001). Nejčastějšími nežádoucími účinky ve skupině se zole-dronátem byly horečka, myalgie a bolesti kostí a svalů [29]. Přestože je zoledronát podáván jednou ročně, není optimální dávkovací interval dosud přesně znám [30, 31]. Randomizovaná zaslepená studie kontrolovaná placebem sledující 50 postmenopauzálních žen s osteopenií zjistila, že antiresorpční efekt jednorázově podaného zoledronátu (5 mg i.v.) přetrvává nejméně 2 roky. Vliv na markery kostní remodelace a na BMD (graf 1) je srovnatelný po 12 a 24 měsících sledování [31]. V ČR se intravenózní lékové formy ibandronátu a zoledronátu v intenzivnějším dávkování podobně jako některé další BIS (klodronát i.v. a perorální, pamidronát i.v.) běžně používají v onkologických indika-cích [3].
Vliv dávkovacího intervalu na adherenci k léčbě
Dávkovací interval je důležitým faktorem, který může (někdy výrazně) ovlivnit adherenci k léčbě. Podle recentní souhrnné práce, která zahrnula studie publikované v období 1970–2009, jsou preference pacientů a adherence k léčbě vyšší při podávání d-BIS jednou týdně ve srovnání s režimem jednou denně. Po 12 měsících léčby činil parametr charakterizující compliance – tzv. medication possession ratio (MPR) – 46–64 % u týdenních a 32–56 % u denních forem. Navzdory usilovným snahám výrobců je však adherence k léčbě d-BIS stále nedostatečná. Po 2 letech léčby denními nebo týdenními formami d-BIS bylo MPR > 80 % zaznamenáno pouze u 43 % pacientů [32]. Hlavním motivem pro vývoj přípravků dávkovaných jednou měsíčně byl předpoklad preference před denními a týdenními režimy, a tedy rovněž vyšší adherence pa-cientů k léčbě. Data pro měsíční dávkovací režimy (ibandronát) však nejsou konzistentní a vzhledem k odlišné metodice zkoumání je problematické adherenci srovnat s výše uvedenými režimy [32]. Byly publikovány i studie, které vyšší adherenci při podávání d-BIS jednou měsíčně ve srovnání s týdenními formami neprokázaly [33, 34]. Intravenózní podávání jednou ročně (zoledronát) je pacienty upřednostňováno před podáváním jednou týdně, data ohledně adherence však ještě nejsou k dispozici [32].
Závěr
Možnosti léčby osteoporózy d-BIS se v poslední době značně rozšířily. K dispozici jsou nyní i látky původně používané v onkologických indikacích (ibandronát, zoledronát). Inovace dále spočívají v prodloužení intervalů mezi dávkami až k možnosti aplikace jednou ročně.
Adherence k léčbě dlouhodobých onemocnění, ke kterým osteoporóza bezpochyby patří, je nedostatečná. Perorální d-BIS je třeba užívat specifickým způsobem, který může být pro pacienta omezující nebo obtížně zvládnutelný. Proto je třeba při výběru vhodného d-BIS – kromě důkladného zhodnocení klinické situace – respektovat rovněž preference pacienta. U pacientů s nízkou adherencí k léčbě mohou být výhodné d-BIS s prolongovaným dávkovacím intervalem či intravenózní aplikace. Pro dosažení optimální adherence k léčbě je však nezbytné dostatečně informovat pacienta o cílech a účinnosti léčby stejně jako o případných rizicích. Před prvním intravenózním podáním d-BIS je vhodné upozornění na možný výskyt reakce akutní fáze, popřípadě prevence podáním paracetamolu či NSAID.
Seznam použité literatury
- [1] Bayer M, Jeníček J, Kučerová I a kol. Doporučené postupy pro diagnostiku a terapii postmenopauzální osteoporózy II. Část první (pracovní verze) 2007. http://www.smos.cz/docs/dp_smos1. pdf (20. 7. 2010)
- [2] Bayer M, Jeníček J, Kučerová I a kol. Doporučené postupy pro diagnostiku a terapii postmenopauzální osteoporózy II. Část druhá (pracovní verze) 2007. http://www.smos.cz/docs/dp_smos2.pdf (20. 7. 2010)
- [3] Automatizovaný informační systém léčivých přípravků. MV AISLP 2009.2. Souhrny údajů o přípravcích (SPC).
- [4] MacLean C, Newberry S, Maglione M, et al. Systematic review: comparative effectiveness of treat-ments to prevent fractures in men and women with low bone density or osteoporosis. Ann Intern Med 2008; 148: 197–213.
- [5] Mayes SL. Review of postmenopausal osteoporosis pharmacotherapy. Nutr Clin Pract 2007; 22: 276–285.
- [6] Štěpán J. Acidum ibandronicum. Remedia 2006; 16: 4–13.
- [7] Horák P. Kyselina zoledronová. Remedia 2006; 16: 324–331.
- [8] Bock O, Felsenberg D. Bisphosphonates in the management of postmenopausal osteoporosis – optimizing efficacy in clinical practice. Clin Interv Aging 2008; 3: 279–297.
- [9] Graham DY, Malaty HM. Alendronate and naproxen are synergistic for development of gastric ulcers. Arch Intern Med 2001; 161: 107–110.
- [10] Etminan M, Lévesque L, Fitzgerald JM, Brophy JM. Risk of upper gastrointestinal bleeding with oral bisphosphonates and non steroidal anti-inflammatory drugs: a case-control study. Aliment Pharmacol Ther 2009; 29: 1188–1192.
- [11] Adami S, Pavelka K, Cline GA, et al. Upper gastrointestinal tract safety of daily oral risedronate in patients taking NSAIDs: a randomized, double-blind, placebo-controlled trial. Mayo Clin Proc 2005; 80: 1278–1285.
- [12] Miyake K, Kusunoki M, Shinji Y, et al. Bisphos-phonate increases risk of gastroduodenal ulcer in rheumatoid arthritis patients on long-term non-steroidal antiinflammatory drug therapy. J Gastroenterol 2009; 44: 113–120.
- [13] Recker RR, Lewiecki EM, Miller PD, Reiffel J. Safety of bisphosphonates in the treatment of osteoporosis. Am J Med 2009; 122 (2 Suppl): S22–32.
- [14] Lenart BA, Neviaser AS, Lyman S, et al. Associa-tion of low-energy femoral fractures with prolonged bisphosphonate use: a case control study. Osteoporos Int 2009; 20: 1353–1362.
- [15] Bone HG, Hosking D, Devogelaer JP, et al. Ten years' experience with alendronate for osteoporosis in postmenopausal women. N Engl J Med 2004; 350: 1189–1199.
- [16] Black DM, Schwartz AV, Ensrud KE, et al. Effects of continuing or stopping alendronate after 5 years of treatment: the Fracture Intervention Trial Long-term Extension (FLEX): a randomized trial. JAMA 2006; 296: 2927–2938.
- [17] Adachi JD, Faraawi RY, O'Mahony MF, et al. Upper gastrointestinal tolerability of alendronate sodium monohydrate 10 mg once daily in postmenopausal women: a 12-week, randomized, double-blind, placebo-controlled, exploratory study. Clin Ther 2009; 31: 1747–1753.
- [18] Kusamori K, Katsumi H, Abe M, et al. Development of a novel transdermal patch of alendronate, a nitrogen-containing bisphosphonate, for the treatment of osteoporosis. J Bone Miner Res 2010, in press.
- [19] Bangalore S, Kamalakkannan G, Parkar S, Messerli FH. Fixed-dose combinations improve medication compliance: a meta-analysis. Am J Med 2007; 120: 713–719.
- [20] Dickson M, Plauschinat CA. Compliance with Antihypertensive Therapy in the Elderly: A Comparison of Fixed-Dose Combination Amlodipine/Benazepril versus Component-Based Free-Combination Therapy. Am J Cardiovasc Drugs 2008: 45–50.
- [21] Jansen JP, Gaugris S, Bergman G, Sen SS. Cost-effectiveness of a fixed dose combination of alendronate and cholecalciferol in the treatment and prevention of osteoporosis in the United Kingdom and The Netherlands. Curr Med Res Opin 2008; 24: 671–684.
- [22] Van Poznak C, Hannon RA, Mackey JR, et al. Prevention of aromatase inhibitor-induced bone loss using risedronate: the SABRE trial. J Clin Oncol 2010; 28: 967–975.
- [23] Bishop N, Harrison R, Ahmed F, et al. A randomized, controlled dose-ranging study of risedronate in children with moderate and severe osteo-genesis imperfecta. J Bone Miner Res 2010; 25: 32–40.
- [24] Emkey R, Delmas PD, Bolognese M, et al. Efficacy and tolerability of once-monthly oral iban-dronate (150 mg) and once-weekly oral alendronate (70 mg): additional results from the Monthly Oral Therapy With Ibandronate For Osteoporosis Intervention (MOTION) study. Clin Ther 2009; 31: 751–761.
- [25] Chung YS, Lim SK, Chung HY, et al. Comparison of monthly ibandronate versus weekly risedronate in preference, convenience, and bone turnover markers in Korean postmenopausal osteoporotic women. Calcif Tissue Int 2009; 85: 389–397.
- [26] Derman R, Kohles JD, Babbitt A, et al. Gastrointestinal tolerability with ibandronate after previous weekly bisphosphonate treatment. Clin Interv Aging 2009; 4: 357–365.
- [27] Orwoll ES, Binkley NC, Lewiecki EM, et al. Efficacy and safety of monthly ibandronate in men with low bone density. Bone 2010; 46: 970–976.
- [28] Sambrook P, Cranney A, Adachi JD. Risk reduction of non-vertebral fractures with intravenous ibandronate: post-hoc analysis from DIVA. Curr Med Res Opin 2010; 26: 599–604.
- [29] Lyles KW, Colón-Emeric CS, Magaziner JS, et al. Zoledronic acid and clinical fractures and mortality after hip fracture. N Engl J Med 2007; 357: 1799–1809.
- [30] Grey A, Bolland M, Wattie D, et al. Prolonged anti-resorptive activity of zoledronate – a randomized controlled trial. J Bone Miner Res 2010, in press.
- [31] Grey A, Bolland MJ, Wattie D, et al. The antiresorptive effects of a single dose of zoledronate persist for two years: a randomized, placebo-controlled trial in osteopenic postmenopausal women. J Clin Endocrinol Metab 2009; 94: 538–544.
- [32] Lee S, Glendenning P, Inderjeeth CA, et al. Efficacy, side effects and route of administration are more important than frequency of dosing of anti-osteoporosis treatments in determining patient adherence: a critical review of published articles from 1970 to 2009. Osteoporos Int 2010, in press.
- [33] Gold DT, Safi W, Trinh H. Patient preference and adherence: comparative US studies between two bisphosphonates, weekly risedronate and monthly ibandronate. Curr Med Res Opin 2006; 22: 2383–2391.
- [34] Gold DT, Trinh H, Safi W. Weekly versus monthly drug regimens: 1-year compliance and persistence with bisphosphonate therapy. Curr Med Res Opin 2009; 25: 1831–1839.