Hereditární angioedém s deficiencí C1 inhibitoru u dětí
Souhrn
Gutová V. Hereditární angioedém s deficiencí C1 inhibitoru u dětí. Remedia 2023; 33: 87–91.
Text pojednává o klinických, diagnostických a léčebných aspektech hereditárního angioedému s deficiencí C1 inhibitoru v dětské populaci. Zmiňuje klinický obraz typický pro děti, otoky končetin a abdominální příznaky, prodromální kožní projevy, nástup klinických potíží dle věku a spouštěče specifické pro dětský věk – mechanické podněty a infekce. Zmíněna jsou doporučená schémata diagnostická jak v novorozeneckém a kojeneckém, tak v pozdějším věku a diferenciální diagnostika u dětí, zejména alergologická. Dále je diskutována akutní i profylaktická léčba u dětí s přihlédnutím k možnostem použití některých léků v České republice. U akutní léčby je to především nativní plazmatický nebo rekombinantní C1 inhibitor, v indikovaných případech ikatibant po schválení zdravotní pojišťovnou. Profylaktická léčba je u dětí ještě složitější než u dospělých, v současné době je možná u malých dětí jen po schválení revizním lékařem zdravotní pojišťovny. Podpůrná léčba zahrnuje psychologickou pomoc i pomoc pacientských organizací.
Klíčová slova: hereditární angioedém – C1 inhibitor – děti –akutní a profylaktická léčba.
Summary
Gutova V. Hereditary angioedema with C1 inhibitor deficiency in children. Remedia 2023; 33: 87–91.
This is an overview of clinical, diagnostic and therapeutic aspects of hereditary angioedema (HAE) with C1 inhibitor deficiency in children. The clinical symptoms typical in children are discussed, mainly subcutaneous edema of extremities, abdominal pain symptoms, prodromal skin symptoms, the age of beginning of clinical problems, and their triggers in childhood – mechanical stimuli and infection. Moreover, the recommended diagnostic schemes in neonates, infants and older children are mentioned, as well as differential diagnosis, particularly allergologic. The treatment approach in acute and prophylactic therapy is specific in the Czech Republic, given certain limitations of health insurance. While the plasma derived or recombinant C1 inhibitors are regularly used for the treatment of acute attacks, the prophylactic therapy is more problematic. Psychologic help and support of patients organizations is also very important.
Key words: hereditary angioedema – C1 inhibitor – children – acute and prophylactic therapy.
Hereditární angioedém (HAE) je relativně vzácné vrozené onemocnění, jehož hlavním klinickým projevem jsou masivní otoky podkoží a/nebo sliznic. Počítá se k primárním imunodeficitům, i když svými projevy poněkud vybočuje. Podstatou onemocnění je mutace genu pro C1 inhibitor (C1‑INH) způsobující jeho buď výrazně sníženou tvorbu, nebo afunkčnost. C1‑INH je inhibitorem proteáz a jeho hlavními funkcemi jsou inhibice spontánní aktivace komplementu a inhibice kallikreinu. Porucha inhibice kallikreinu a spuštění kininové kaskády jsou považovány za hlavní příčinu masivních otoků. Z patofyziologického pohledu je HAE v současné době označován některými autory jako „bradykininem indukovaný angioedém“ [1]. Z posledních výzkumů a hlavně z hledání nových možností terapeutického ovlivnění je jasné, že bradykinin je skutečně centrálním agens v patogenezi edémů. Tento peptid je součástí kininového systému, jeho funkcí je zvýšení cévní permeability, což při patologickém zvýšení jeho hodnot vede k extravazaci tekutiny do intersticiálního prostoru podkožního a slizničního a ke vzniku otoku. HAE postihuje dospělé i děti, k prvním klinickým projevům dochází většinou ve školním věku, ale výjimečně i u dětí mladších.
Klinické projevy a spouštěče
Klinické projevy u dětí se v podstatě neliší od projevů u dospělých. Převažují možná spíše projevy periferní, kožní, postihující zejména končetiny (obr. 1, 2). Zvláště v batolecím a předškolním věku s vazbou na mechanický spouštěč při dětských hrách, drobných úrazech, které jsou v tomto věku běžné. Vzácněji dochází k edémům faciálním a cervikálním (obr. 3, 4). Další jsou ataky abdominální s typickým průběhem. I u dětí se známou diagnózou HAE je nutno diferenciálně diagnosticky vyloučit náhlou příhodu břišní, kterou ataka imituje – laboratorní zánětlivé parametry, eventuálně sonografické vyšetření břicha [2–4]. Laryngeální ataky jsou u dětí velmi vzácné, udává se výskyt okolo 0,9 % [2,5]. Až u třetiny dětských pacientů se mohou objevit kožní prodromy ataky – svědění, erythema marginatum, nesvědivé exantémy, projevy imitující urtikarii (obr. 5, 6). Objevují se dny či hodiny před atakou nebo při atace [6].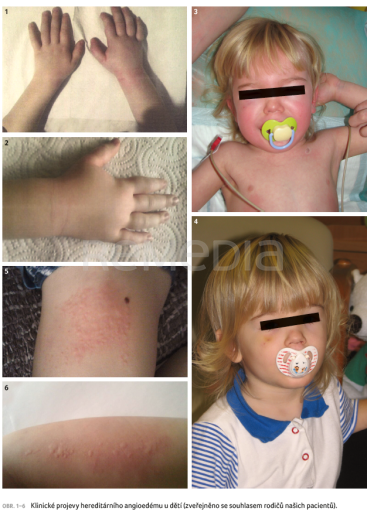
Z hlediska věku nástupu potíží se udává věkové období od 4,4 roku do 18 let, průměrně ve věku 10 let, ale existují vzácné případy prvních atak již u jednoročních dětí. Tíže a frekvence atak je velmi individuální stejně jako u dospělých [5].
Spouštěči u dětí jsou nejčastěji mechanický inzult a infekční onemocnění, hlavně běžné respirační infekty. Stresový spouštěč je u malých dětí vzácný. Mohou se ale objevit i ataky bez jasného spouštěče. S nastupující adolescencí se začínají projevovat stresové a hormonální spouštěče, popisovány jsou první ataky u dívek se zahájením hormonální antikoncepce [5].
Diagnóza
![OBR. 7 Diagnostický algoritmus při pozitivní rodinné anamnéze; podle [2] – Farkas, et al., 2017. OBR. 7 Diagnostický algoritmus při pozitivní rodinné anamnéze; podle [2] – Farkas, et al., 2017.](https://www.remedia.cz/1-23-90-photo-pg-955-367-268-.png)
Při diagnostice u dětí řešíme v podstatě dvě situace. V té první jde o novorozence z rodiny s již známou mutací a s některými jejími členy nemocnými HAE (obr. 7) [2]. V těchto případech je doporučeno vyšetřit již novorozence – hladinu C4, hladinu a funkci C1‑INH. Výsledky nemusejí být i v případě postiženého dítěte absolutně vypovídající, hladiny C4 mohou být fyziologicky až o polovinu nižší než po prvním roce života. Doporučeno je celé vyšetření po prvním roce věku opakovat. Tatáž diagnostická pravidla platí po kojence. Metodou volby při známé mutaci v rodině je analýza DNA z pupečníkové nebo periferní krve a sledování pacienta při záchytu mutace [2].
Ve druhém případě se k diagnostice dostává symptomatické dítě s otoky nejasné etiologie. V diferenciální diagnostice edémů bychom měli na C1‑INH‑HAE pomýšlet pokaždé a vlastně velmi jednoduché screeningové vyšetření indikovat. A to i v případech, kdy anamnéza evokuje alergickou etiologii otoků, hlavně v případech cervikofaciálních otoků [2].
Je důležité vědět, že až 25 % mutací způsobujících HAE tvoří mutace de novo [3,5]. Pokud kožní testy alergickou senzibilizaci neprokáží, vždy současně s vyšetřením specifických IgE protilátek a jiných „alergických markerů“ indikujeme screening k vyloučení C1‑INH‑HAE. Při pozitivitě screeningu opakujeme testy za tři měsíce a současně provádíme screening u příbuzných první linie. Při negativitě testů lze C1‑INH‑HAE vyloučit. To ale neznamená, že může být vyloučena jiná etiologie HAE, která je ovšem zvláště u dětí opravdu extrémně vzácná (obr. 8) [2].![OBR. 8 Diagnostický algoritmus u symptomatického pacienta; podle [2] – Farkas, et al., 2017. OBR. 8 Diagnostický algoritmus u symptomatického pacienta; podle [2] – Farkas, et al., 2017.](https://www.remedia.cz/1-23-90b-photo-pg-956-367-343-.png)
Genetické vyšetření (analýza DNA) je v současné době u nás možné a zcela určitě indikované v nejasných případech. U dětí z rodin se známou mutací, jasnou klinikou a pozitivními laboratorními testy není nezbytné provádět analýzu DNA rutinně [7].
Léčba
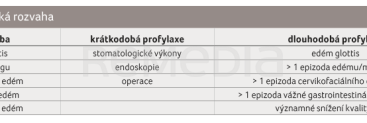
Léčba dětí s HAE je v České republice vázána na léková centra. Dětští pacienti jsou v těchto centrech sledováni, pravidelně kontrolováni, i když jsou asymptomatičtí, a je jim dle potřeby poskytována léčebná péče. Stejně jako u dospělých je možno i u dětí terapeutický přístup rozdělit na léčbu akutních atak a na léčbu profylaktickou (tab. 1, 2) [8].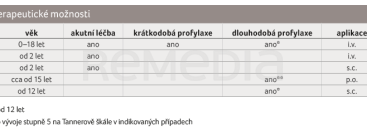
Pro léčbu akutních atak (laryngeálních, abdominálních, cervikofaciálních nebo těžkých periferních) jsou v dětském věku k dispozici aktuálně dva přípravky – plazmatický C1‑INH (20 IU/kg) bez věkových omezení a v současné době již i rekombinantní C1‑INH (50 U/kg) podávaný u dětí ve věku od 2 let [9]. Oba přípravky jsou podávány intravenózně většinou v ambulantních provozech dětských oddělení.
Další, méně invazivní a z hlediska kvality života dítěte nejšetrnější léčbou je domácí podávání selektivního antagonisty bradykininu ikatibantu 10–30 mg subkutánně (s.c.) dle tělesné hmotnosti a doporučení v souhrnu údajů o přípravku (SPC). Je podáván rodičem nebo pečovatelem. Dle SPC je ikatibant indikován u dětí ve věku od 2 let, ale dle doporučení Státního ústavu pro kontrolu léčiv je hrazen pojišťovnami až od 18 let. Nutno tedy pro děti vyjednat výjimku u zdravotní pojišťovny. Výrobce rovněž dodává dávkovací kity pro pohodlné dávkování podle hmotnosti pacienta.
Krátkodobá profylaxe je indikována před operacemi, endoskopickými výkony a stomatologickými zákroky. Vztahují se na ni stejná kritéria jako u dospělých, dávka je upravována dle tělesné hmotnosti dítěte. Lékem první volby je plazmatický C1‑INH (10–30 IU/kg). Jiné přípravky ke krátkodobé profylaxi doporučený postup ČSAKI (Česká společnost alergologie a klinické imunologie) neuvádí [8].
Dlouhodobá profylaxe je v dětském věku problémem
Kyselina tranexamová, doporučovaná mezinárodním konsenzem pro diagnostiku a léčbu HAE u dětí, má řadu vedlejších účinků, je kontraindikována u stavů trombofilie a dle SPC je v pediatrické populaci indikována pouze pro stavy krvácení po otorinolaryngologických operacích. Jako profylaxe atak HAE se u dětí v podstatě nepoužívá [3,8].
Atenuované androgeny – danazol – jsou dle Evropské lékové agentury (EMA) indikovány k dlouhodobé profylaxi až u pacientů s dosaženým stupněm vývoje ve stadiu 5 dle Tannerovy škály, což v podstatě odpovídá věku kolem 15 let u chlapců a 14 let u dívek. Vzhledem k virilizačním účinkům těchto přípravků je však jejich podávání u děvčat velmi sporné [10].
Další možností u pacientů s velmi těžkým průběhem je podávání plazmatického C1‑INH pravidelně s.c. autoaplikací 60 IU/kg každé 3–4 dny. Podle EMA je tato léčba indikována od 12 let, ale v ČR nemá schválenu úhradu ze zdravotního pojištění a je nutno žádat o výjimku.
Novou naději představuje biologická léčba v dlouhodobé profylaxi. Monoklonální protilátka proti plazmatickému kallikreinu inhibující jeho proteolytickou aktivitu – lanadelumab – je indikována pro dlouhodobou profylaxi od věku 12 let [11]. Podává se subkutánně 1× za 2 týdny s možností snížení frekvence na jednou měsíčně u pacientů s nižší hmotností a s dobrým preventivním efektem. Aplikace je možná doma po zaškolení rodiče či jiného pečovatele. V ČR je zatím dostupný jen na žádost o úhradu ze zdravotního pojištění pro daného pacienta při splnění podmínek léčby dle návrhu ČSAKI:
- 18 atak za posledních 12 měsíců
nebo
- výskyt závažné ataky HAE (závažné ataky gastrointestinální, orofaciální ataky s potenciálním otokem laryngu, angioedém v urogenitální oblasti, těžké končetinové ataky znemožňující denní činnost) vyžadující adekvátní léčbu
nebo
- nutnost opakované léčby v průběhu jedné ataky (s potřebou kombinace léčiv či opakované podání téhož léku)
nebo
- v případě, že jiná profylaxe není dostatečná nebo je kontraindikována [8].
Podpůrná léčba
Hereditární angioedém jako každé chronické onemocnění značně snižuje kvalitu života pacienta, zvláště dítěte [10]. I zdánlivě banální a zdraví neohrožující periferní kožní otoky mohou být pro pacienta velkou psychickou zátěží v dětském kolektivu. Dodržování prevence mechanických traumat je někdy u dětí obtížné, kontaktní sporty, kterým by se měly vyhnout, jsou pro ně většinou nejlákavější. I běžné dětské hry přinášejí mikrotraumata. O to více bychom se jako dětští imunologové měli snažit o možnosti dlouhodobé profylaxe aplikované v domácím prostředí a o léčbu přípravky s minimem vedlejších účinků. Psychologická a psychoterapeutická podpora je někdy velmi důležitá a je indikována u všech dětí s těžším průběhem nemoci a častými atakami.
V tomto našem snažení nám mohou pomoci i pacientské organizace, u nás konkrétně HAE Junior, která nabízí program a podporu dětským pacientům s HAE a jejich rodinám.
Literatura
[1] Caballero T, Baeza ML, Cabañas R, et al. Consensus statement on the diagnosis, management, and treatment of angioedema mediated by bradykinin. Part I. Classification, epidemiology, pathophysiology, genetics, clinical symptoms, and diagnosis. J Investig Allergol Clin Immunol 2011; 21: 333–347.
[2] Farkas H, Martinez‑Saguer I, Bork K, et al.; International consensus on the diagnosis and management of pediatric patients with hereditary angioedema with C1 inhibitor deficiency HAWK. Allergy 2017; 72: 300–313.
[3] Markus M, Magerl M , Betschel S, et al. The international WAO/EAACI guideline for the management of hereditary angioedema – The 2021 revision and update. Allergy 2022; 77: 1961–1990.
[4] Janardhanan D, Nair S, Subramanian TS. Recurrent abdominal pain due to hereditary angioedema. Indian J Pediatr 2007; 74: 83–84.
[5] Farkas H. Pediatric hereditary angioedema due to C1‐inhibitor deficiency. Allergy Asthma Clin Immunol 2010; 6: 18.
[6] Martinez‐Saguer I, Farkas H. Erythema marginatum as an early symptom of hereditary angioedema: case report of 2 newborns. Pediatrics 2016; 137: e20152411.
[7] Bennett G, Craig T. Hereditary angioedema with a focus on the child. Allergy Asthma Proc 2015; 36: 70–73.
[8] Hereditární angioedém doporučený postup ČSAKI dostupné na: https://www.csaki.cz/dokumenty/HAE_dopor_postup.pdf
[9] Reshef A, Grivcheva‐Panovska V, Kessel A, et al. Recombinant human C1 esterase inhibitor treatment for hereditary angioedema attacks in children. Pediatr Allergy Immunol 2019; 30: 562–568.
[10] Bouillet L, Launay D, Fain O, et al. Hereditary angioedema with C1 inhibitor deficiency: clinical presentation and quality of life of 193 French patients. Ann Allergy Asthma Immunol 2013; 111: 290–294.
[11] Banerji A, Bernstein JA, Johnston DT, et al, Long‑term prevention of hereditary angioedema attacks with lanadelumab: The HELP OLE Study, Allergy 2022; 77: 979–990.