Léčba refrakterního ascitu u cirhotiků
Ascites je nejčastější komplikací pokročilé jaterní cirhózy. Léčba ascitu, který dobře reaguje na diuretika a omezení příjmu sodíku, není složitá. Spočívá v podávání kličkového diuretika v kombinaci s antagonistou mineralokortikoidů, nejčastěji užívaná je kombinace furosemidu se spironolaktonem. S progresí dysfunkce jater se odpověď na diuretika zhoršuje, ascites se stává refrakterním. V současné době platí pro hodnocení refrakternosti ascitu mezinárodně uznaná diagnostická kritéria, refrakterní ascites se dělí na ascites rezistentní na diuretika a ascites neovlivnitelný diuretiky. Léčba refrakterního ascitu spočívá v opakovaných paracentézách s náhradou volumu roztokem albuminu nebo plazmaexpandéry či v zavedení transjugulárního portosystémového shuntu (TIPS). Za refrakterností ascitu často stojí spontánní bakteriální peritonitida, která se léčí empiricky antibiotiky a volumovou expanzí. Je-li příčinou refrakternosti ascitu progrese hepatorenálního syndromu typu II, je na místě volumová expanze a léčba terlipresinem. Léčba refrakterního ascitu uleví pacientovi, nezmění však jeho nepříznivou prognózu. U každého pacienta s refrakterním ascitem má být zvažována indikace k transplantaci jater.
Patogeneze refrakterního ascitu
Fibróza jater a s ní spojená sinusoidální a postsinusoidální portální hypertenze jsou iniciálními patogenetickými mechanismy ve vývoji ascitu a hepatorenálního syndromu. Přetlak se přenáší do splanchnických kapilár, konstantním nálezem u portální hypertenze je i dilatace arteriální části splanchnické cirkulace, přítok krve do splanchnických kapilár je zvýšen [1]. Výsledkem je zvýšený únik tekutiny z jaterních sinusoid a splanchnických kapilár do intersticia. Ascites se začíná tvořit, když množství tekutiny unikající do intersticia přesáhne kapacitu zpětné lymfatické drenáže, která se pohybuje mezi 1 až 5 litry za 24 hodin. Další významnou konsekvencí portální hypertenze je zvýšená střevní permeabilita a zvýšené vstřebávání endotoxinu. Zvýšená endotoxémie má svou roli při vzniku systémové vazodilatace a hyperkinetické cirkulace, zvýšenou endotoxémií se i vysvětluje, proč u pokročilých cirhotiků nedochází k odpovídajícímu zvýšení srdečního výdeje za účelem kompenzace nenaplněného cévního řečiště [2]. Kvůli udržení systémového tlaku se proto aktivují humorální endogenní vazoaktivní systémy (sympatický nervový systém, renin-angiotenzinový systém a antidiuretický hormon) [3]. Výsledkem je zvýšení retence sodíku a vody, což opět přispívá k tvorbě ascitu. Aktivace renin-angiotenzinového systému bohužel neupraví systémovou vazodilataci, zato vede ke snížení perfuze ledvin a ke snížení glomerulární filtrace, což je patogenetický podklad hepatorenálního syndromu a další faktor přispívající ke vzniku refrakterního ascitu.
Vysvětlení neúčinnosti diuretik v léčbě refrakterního ascitu spočívá v dále popsaných dějích. Renální retence sodíku se zhoršuje s progresí chronického selhání jater u pacientů s cirhózou. Příčinou je progrese hemodynamických změn v systémové i v portální cirkulaci a s tím spojená aktivace neurohumorálních systémů zvyšujících reabsorpci sodíku a vody. Současně klesá perfuze ledvin a glomerulární filtrace. Výsledkem je, že reabsorpce sodíku v proximálním tubulu je zvýšena a tubulární sekrece v distálních částech nefronu je výrazně snížena. Retence sodíku probíhá v nefronu proximálněji, než jsou místa účinku antagonistů mineralokortikoidů nebo kličkových diuretik, což vysvětluje selhání účinnosti léčby diuretiky u pacientů s refrakterním ascitem [4]. Systémová cirkulace navíc není schopna adekvátně reagovat na vazokonstriktory produkované v ledvinách, kompenzace hypovolemického účinku diuretik je velmi slabá či zcela chybí, což vede k častým nežádoucím účinkům diuretik. Příznivý účinek na retenci vody a korekci diluční hyponatrémie u cirhotiků byl popsán po podání tzv. antagonistů vazopresinového receptoru V2. Zmíněná léčiva jsou zatím ve stadiu klinického zkoušení [5].
Výskyt a prognóza ascitu u cirhotiků
Ascites je nejčastější komplikací jaterní cirhózy. U většiny cirhotiků ho lze dobře kontrolovat snížením příjmu sodíku v potravě a léčbou diuretiky. Přibližně u 5–10 % cirhotiků se do roka ascites stává refrakterním, příčinou je buď ztráta terapeutické odpovědi na diuretika nebo diuretiky indukované nežádoucí účinky, které další účinnou léčbu znemožňují. Zmíněná data pocházejí z kontrolovaných klinických studií s vybranými skupinami pacientů [6], a tak skutečná data o výskytu refrakterního ascitu u všech cirhotiků nejsou známa. Srovnávání hodnocených souborů je obtížné, neboť prevalence refrakterního ascitu je podmíněna pokročilostí jaterní cirhózy a případnou současnou renální insuficiencí. Prevalence refrakterního ascitu u cirhotiků je široce závislá na vstupních kritériích hodnoceného souboru, refrakterní ascites je popisován až u poloviny pacientů s jaterní cirhózou, kteří jsou hospitalizováni ve specializovaných centrech univerzitních nemocnic.
Refrakterní ascites je často spojen s progresí hepatorenálního syndromu typu II, diluční hyponatrémií a celkovou kachexií. Refrakterní ascites představuje nedobrou prognózu, přežití pacientů s refrakterním ascitem je asi 30 % po 2 letech, na rozdíl od pacientů s ascitem reagujícím na léčbu diuretiky, kterých po 5 letech žije 40 % [7, 8]. Refrakterní ascites je důvodem k zahájení specifických léčebných opatření a k zahájení evaluace pacienta jako kandidáta transplantace jater.
Definice refrakterního ascitu
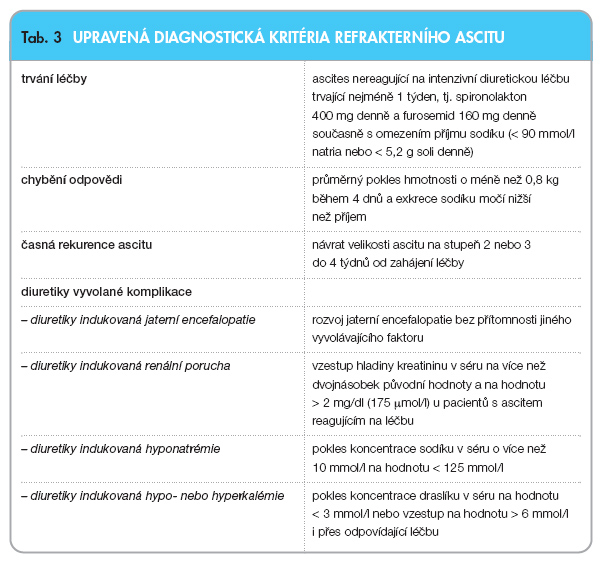
Definice refrakterního ascitu vychází z konsenzu přijatého v roce 1996 pracovní skupinou International Ascites Club. Zmíněná kritéria byla odbornou veřejností natolik akceptována, že v dalších letech mohlo dojít k jejich revizi a upřesnění. Refrakterní ascites se dělí do dvou typů: ascites rezistentní na diuretika (diuretic-resistant) a ascites neovlivnitelný diuretiky (diuretic-intractable). Stejně tak zmíněná pracovní skupina vydala diagnostická kritéria pro refrakterní ascites [9, 10]. Termíny hodnotící velikost ascitu, stejně tak termíny „masivní" či „tenzní" ascites, jsou termíny popisné (patřící do popisu fyzikálního nálezu pacienta) a nemají vztah k refrakternosti ascitu. Malý a střední ascites obvykle dobře odpovídá na léčbu diuretiky, refrakterní ascites bývá velký, na druhou stranu ne každý velký ascites je refrakterní. Pro označení ascitu za refrakterní je nezbytné splnění diagnostických kritérií, zejména selhání efektu léčby (tab. 1, 2, 3).
Ascites falešně refrakterní znamená, že odpověď na diuretika chybí, nebyla však plně splněna výše uvedená diagnostická kritéria. Na prvním místě se jedná o neadekvátní diuretickou léčbu. Např. monoterapie kličkovými diuretiky nemá u cirhotiků dobrou účinnost v důsledku hyperaldosteronismu, stejně tak nemusí být léčba účinná, neodpovídá-li dávka antimineralokortikoidů přítomnému stupni hyperaldosteronismu [11, 12]. K falešně refrakternímu ascitu může vést i příliš intenzivní diuretická léčba s dobrou odpovědí. Příliš negativní bilance tekutin (ztráta 800–1000 ml denně) může vyvolat prerenální insuficienci, ztrátu odpovědi na léčbu diuretiky a ascites se stane refrakterním. Porucha se upraví po přechodném ukončení léčby a hydratací. Ascites může být přechodně refrakterní vlivem podání nefrotoxických léků (nesteroidní antirevmatika, aminoglykosidy) nebo léků snižujících arteriální tlak a perfuzi ledvin (inhibitory ACE). Zvracení, průjmy a bakteriální infekce též mohou prohloubit renální insuficienci a učinit ascites refrakterním. Z bakteriálních infekcí je nutno na prvním místě zmínit spontánní bakteriální peritonitidu, jejímž jediným symptomem může být rozvoj refrakterního ascitu [13]. Odstranění vyvolávající noxy či léčba spontánní bakteriální peritonitidy spolu s volumovou expanzí mohou odpověď na diuretika znovu zlepšit.
Léčba refrakterního ascitu paracentézami
Příprava a technika
Příprava na výkon musí být zahájena poučením pacienta a dle lokálních zvyklostí i podpisem informovaného souhlasu. Výběr místa vpichu se provádí na základě fyzikálního vyšetření, u pacientů po břišních operacích se srůsty v dutině břišní lze místo punkce lokalizovat ultrasonograficky. Místo vpichu je nejčastěji v levém dolním kvadrantu břicha na třetině spojnice spina iliaca anterior superior–pupek, připouští se i možnost punkce na stejném místě vpravo. V některých zemích se používá tzv. přístup střední (2 cm pod pupkem) nebo laterální (laterálně od pochvy m. rectus abdominis). Podání trombokoncentrátů či mražené plazmy není před paracentézou nutné, riziko krvácení do dutiny břišní je nízké. S vyšším rizikem krvácení je nutno počítat u pacientů s renálním selháním při hepatorenálním syndromu a u pacientů s diseminovanou intravaskulární koagulací [14, 15]. Paracentéza se provádí za přísně sterilních podmínek, po předchozí lokální anestezii místa vpichu. Kanyla má mít i boční otvory, jediný přední otvor se často přisává ke stěně. K tomu, aby se zabránilo vytékání ascitu po odstranění jehly, se vpich provádí buď šikmo pod úhlem 45°, nebo tzv. Z technikou (posun jehly o 2 cm v podkoží po propíchnutí kůže). U pacientů s refrakterním ascitem se obvykle evakuuje více než 5 litrů ascitu, stačí-li paracentézu opakovat jednou za 2–4 týdny, lze léčbu provádět ambulantně. U hospitalizovaných pacientů si lze dovolit ascites zcela evakuovat [16].
Cirkulační dysfunkce indukovaná paracentézou (PICD)
Evakuace velkého množství ascitu je provázena poklesem efektivního arteriálního volumu, patogenetické mechanismy, které refrakterní ascites způsobují, se tak bohužel stupňují. Zvyšuje se aktivita renin-angiotenzinového systému a sympatického nervového systému, objevuje se hyponatrémie, což je odrazem zvýšené sekrece vazopresinu a retence vody. Souhrn popsaných změn se nazývá cirkulační dysfunkce indukovaná paracentézou (PICD). Diagnóza PICD je založena na zvýšení plazmatické reninové aktivity na hodnoty převyšující o 50 % hodnotu před paracentézou a zvýšení na hodnotu > 4 ng/ml/h šestý den po paracentéze [17]. Riziko vzniku PICD se zvyšuje s množstvím evakuovaného ascitu. V malém studovaném souboru byla PICD nalezena u 75 % pacientů, dosud chybějí data o vlivu opakovaných paracentéz na progresi PICD [7, 8]. Vznik PICD přispívá k rychlejší rekurenci ascitu, k prohloubení hyponatrémie a hepatorenálního syndromu. Zkrácení přežití není ale u pacientů s PICD jednoznačně prokázáno. Přesto je nutno se při léčbě refrakterního ascitu paracentézami věnovat prevenci PICD.
Prevence PICD
Logickým postupem by se zdála být prevence PICD podáním plazmaexpandérů po velké paracentéze. Skutečnost je však poněkud složitější. Studie srovnávající následky opakovaných paracentéz bez náhrady volumu a s náhradou volumu roztokem 20% lidského albuminu prokázala, že ve skupině s albuminem bylo významně méně hyponatrémií a zhoršení renálních funkcí [19]. Další studie ukázaly, že albumin byl účinnější v prevenci PICD ve srovnání se syntetickými plazmaexpandéry (dextranem, želatinou či fyziologickým roztokem). Přesněji řečeno, albumin je účinnější, je-li evakuováno více než 5 litrů ascitu, při menších paracentézách nebyl rozdíl prokazatelný [20]. Ze znalosti mechanismu cirkulačních změn po paracentéze vychází další úvaha o prevenci PICD podáváním terlipresinu. Další dvě studie srovnávaly účinnost albuminu a terlipresinu. Dle aktivace renin-angiotenzinového systému po paracentéze byla účinnost obou léčiv srovnatelná [21, 22].
TIPS v léčbě refrakterního ascitu
Transjugulární intrahepatální portosystémový shunt (TIPS) je vlastně side to side portokavální anastomózou a účinně snižuje portální hypertenzi. Zavedením metalických potahovaných stentů se významně prodloužila průměrná doba průchodnosti stentu [23]. Efektivní snížení portálního tlaku by logicky mělo vést k přetnutí patogenetické kaskády refrakterního ascitu a k jeho regresi. Reálná situace je ale poněkud odlišná, zavedení TIPS není účinné u všech cirhotiků a je zatíženo řadou možných komplikací. Při výběru pacientů k léčbě refrakterního ascitu pomocí TIPS je nutno se opírat o výsledky klinických studií, které srovnávaly účinnost TIPS s opakovanými paracentézami [24–28]. Hodnoceno bylo celkem 330 pacientů, z nichž 162 bylo léčeno zavedením TIPS a 168 opakovanými paracentézami. Zavedením TIPS byl refrakterní ascites eliminován u dvou třetin pacientů. TIPS přinesl významně lepší výsledky ve srovnání s paracentézami v kontrole ascitu u 23 % pacientů. Po zavedení TIPS sice došlo ke zlepšení natriurézy, přesto pro kontrolu ascitu bylo omezení příjmu sodíku nadále nezbytné. V recentní metaanalýze byl TIPS shledán účinnějším postupem v léčbě refrakterního ascitu ve srovnání s velkými paracentézami [29]. I přes prokázané zhoršení jaterní encefalopatie byl nalezen trend ke zlepšení přežití u pacientů léčených zavedením TIPS. Stejně tak kvalita života pacientů po TIPS byla hodnocena jako lepší i přes zhoršení jaterní encefalopatie.
TIPS není účinný u všech pacientů s refrakterním ascitem a postup je zatížen rizikem řady komplikací, proto je nutno pacienty k této léčbě pečlivě vybírat. Vždy je nezbytné srovnávat předpokládaný přínos pro pacienta s rizikem komplikací. TIPS není vhodným postupem pro ikterické pacienty s těžkou dysfunkcí jater (Child-Pugh C), u kterých může snížení perfuze jater vést k jejich úplnému selhání. Jaterní encefalopatie se významně zhoršuje zejména u pacientů starších 60 let a u pacientů, kteří neužívají profylakticky laktulózu a nevyhýbají se jednorázovému požití velkého množství masa. K dalším absolutním kontraindikacím patří srdeční selhání a plicní hypertenze, dále trombóza portální žíly či její kavernózní přestavba. Relativními kontraindikacemi jsou renální insuficience a tumor či cysty v játrech, zde záleží na rozsahu a lokalizaci. Stenóza stentu se vyvine asi u 70 % pacientů do roka od zavedení, řešením je dilatace balonkem či zavedení nového stentu.
Praktická doporučení
1. ‑Diagnózu refrakterního ascitu opíráme o splnění mezinárodně uznaných kritérií, vždy je nutno vyloučit „falešně refrakterní" či „přechodně refrakterní" ascites.
2. ‑Léčbu refrakterního ascitu zahajujeme opakovanými paracentézami, při evakuaci více než 5 litrů doplňujeme cirkulující volum roztokem 20% albuminu.
3. ‑Je-li příčinou refrakternosti ascitu spontánní bakteriální peritonitida, léčíme ji antibiotiky. Léky první volby jsou cefalosporiny III. generace (cefotaxim, cef-triaxon) nebo amoxicilin/kyselina klavulanová. Léčba má trvat nejméně 8 dnů, efekt léčby se sleduje dle počtu leukocytů (polymorfonukleárů) v ascitu. Poté musí následovat dlouhodobá profylaxe malou dávkou norfloxacinu.
4. ‑Je-li příčinou refrakterního ascitu zhoršení hepatorenálního syndromu, provádíme volumovou expanzi albuminem a začínáme léčbu terlipresinem.
5. ‑Po zahájení léčby refrakterního ascitu opakovanými paracentézami zvažujeme indikaci k zavedení TIPS. Nutno vždy zvažovat předpokládaný přínos proti riziku komplikací.
6. ‑Zahajujeme proces evaluace pacienta jako kandidáta transplantace jater.
Závěr
Refrakterní ascites je závažnou komplikací jaterní cirhózy a je odrazem těžké dysfunkce jater. Současná léčba refrakterního ascitu spočívající v opakovaných paracentézách nebo v zavedení TIPS sice zlepší kvalitu života pacientů, nezlepší ale jejich nepříznivou dlouhodobou prognózu. Jediným postupem, který dlouhodobou prognózu pacientů s pokročilou jaterní cirhózou zlepší, je transplantace jater. Z tohoto hlediska lze transplantaci jater považovat i za definitivní léčbu refrakterního ascitu.
Seznam použité literatury
- [1] Gines P, Fernandez-Esparrach G, Arroyo V, et al. Pathogenesis of ascites in cirrhosis. Semin Liver Dis 1997; 17: 175–189.
- [2] Ruiz del Arbol L, Urman J, Fernandez J, et al. Systemic, renal, and hepatic hemodynamic derangement in cirrhotics patients with spontaneous bacterial peritonitis. Hepatology 2003; 38; 1210–1218.
- [3] Schrier RW, Niederberger M, Weigert A, et al. Peripheral arterial vasodilatation: determinant of functional spectrum of cirrhosis. Semin Liver Dis 1994; 14: 14–22.
- [4] Arroyo V, Colmenero J. Ascites and hepatorenal syndrome in cirrhosis: pathophysiological basis of therapy and current management. J Hepatol 2003; 38: 69–89.
- [5] Gerbes AL, Gulberg V, Gines P, et al. Therapy of hyponatremia in cirrhosis with a vasopressin receptor antagonist: a randomized double-blind multicenter trial. Gastroenterology 2003; 124: 933–939.
- [6] Bernardi M, Laffi G, Salvagnini M, et al. Efficacy and safety of the stepped care medical treatment of ascites in liver cirrhosis: a randomized controlled clinical trial comparing two diets with different sodium content. Liver 1993; 13: 156–162.
- [7] Gines P, Cardenas A, Arroyo V, et al. Management of cirrhosis and ascites. N Engl J Med 2004; 350: 1646–1654.
- [8] Salerno F, Borroni G, Moser P, et al. Survival and prognostic factors of cirrhotics patients with ascites: a study of 134 outpatients. Am J Gastroenterol 1993; 88: 514–519.
- [9] Arroyo V, Gines P, Gerbes A, et al. Definition and diagnostic criteria of refractory ascites and hepatorenal syndrome. Hepatology 1996; 23: 164–176.
- [10] Moore KP, Wong F, Gines P, et al. The management of ascites in cirrhosis: report on the consensus conference of the International Ascites Club. Hepatology 2003; 38: 258–266.
- [11] Perez-Ayuso RM, Arroyo V, Planas R, et al. Randomized comparative study of efficacy of furosemide versus spironolactone in non-azotemic cirrhosis with ascites. Gastroenterology 1984; 84: 961–968.
- [12] Bernardi M, Servadei D, Trevisani F, et al. Importance of plasma aldosterone concentration on natriuretic effect of spironolactone in patients with liver cirrhosis and ascites. Digestion 1985; 31: 189–193.
- [13] Fasolato S, Angeli P, Dallagnese L, et al. Renal failure and bacterial infections in patients with cirrhosis: epidemiology and clinical features. Hepatology 2007; 45: 223–229.
- [14] Runyon BA. Management of adult patients with ascites due to cirrhosis. Hepatology 2004; 39: 841–856.
- [15] McVay PA, Toy PTCY. Lack of increased bleeding after paracentesis and thoracentesis in patients with mild coagulation abnormalities. Transfusion 1991; 31: 164–171.
- [16] Tito L, Gines P, Arroyo V, et al. Total paracentesis associated with intravenous albumin management of patients with cirrhosis and ascites. Gastroenterology 1990; 98: 146–151.
- [17] Ruizdel-Arbor L, Monescillo A, Jimenez W, et al. Paracentesis-induced circulatory dysfunction: mechanism and effect on hepatic hemodynamics in cirrhosis. Gastroenterology 1997; 113: 579–586.
- [18] Gines P, Tito L, Arroyo V, et al. Randomized comparative study of therapeutic paracentesis with and without intravenous albumin in cirrhosis. Gastroenterology 1988; 94: 1493–1502.
- [19] Gines A, Fernandez-Esparrach G, Monescillo A, et al. Randomized trial comparing albumin, dextran 70, and polygeline in cirrhotics patients with ascites treated by paracentesis. Gastroenterology 1996; 111: 1002–1010.
- [20] Moreau R, Valla DC, Durand-Zaleski I, et al. Comparison of outcome in patients with cirrhosis and ascites following treatment with albumin or a synthetic colloid: a randomized controlled pilot trial. Liver Int 2006; 26: 46–54.
- [21] Moreau R, Asselah T, Condat B, et al. Comparison of the effect of terlipressin and albumin on arterial blood volume in patients with cirrhosis and tense ascites treated by paracentesis: a randomized pilot study. Gut 2002; 50: 90–94.
- [22] Singh V, Kumar R, Nain CK, et al. Terlipressin versus albumin in paracentesis-induced circulatory dysfunction in cirrhosis: a randomized study. J Gastroenterol Hepatol 2006; 21: 303–307.
- [23] Rossi P, Salvatori F, Fanelli F, et al. Polytetrafluor-ethylene-covered nitinol stent-graft for transjugular intrahepatic portosystemic shunt creation: 3-year experience. Radiology 2004; 231: 820–830.
- [24] Lebrec D, Giuily N, Hadengue A, et al. Transjugular intrahepatic portosystemic shunt: comparison with paracentesis in patients with cirrhosis and refractory ascites: a randomized trial. J Hepatol 1996; 25: 135–144.
- [25] Rosle M, Ochs A, Guldberg V, et al. A comparison of paracentesis and transjugular intrahepatic portosystemic shunting in patients with ascites. N Engl J Med 2000; 342: 1701–1707.
- [26] Sanyal A, Gennings C, Reddy KR, et al. A randomized controlled study of TIPS versus large volume repeated paracentesis in the treatment of refractory ascites. Gastroenterology 2003; 124: 634–643.
- [27] Gines P, Uriz J, Calahorra B, et al. Transjugular intrahepatic portosystemic shunt versus repeated paracentesis plus intravenous albumin for refractory ascites in cirrhosis. A multicenter randomized comparative study. Gastroenterology 2002; 123: 1839–1847.
- [28] Salerno F, Merli M, Riggio O, et al. Randomized controlled study of TIPS vs. paracentesis with albumin in cirrhosis with refractory ascites. Hepatology 2004; 40: 629–635.
- [29] D´Amico G, Luca A, Morabito A, et al. Uncovered transjugular intrahepatic portosystemic shunt for refractory ascites: A meta-analysis. Gastroenterology 2005; 129: 1282–1293.