Obezita a deprese
Lékaři měli vždy tendenci pohlížet na psychická a somatická onemocnění spíše odděleně. Obezita, cukrovka a deprese jsou tři onemocnění, u kterých o vzájemných vztazích nelze již dnes pochybovat. Dávno platí, že deprese se může projevovat somatickými příznaky a že některá somatická onemocnění mohou vyvolávat depresivní náladu. Pojmy psychosomatické onemocnění či larvovaná deprese jsou užívány spíše ve vztahu ke kardiální či gastrointestinální problematice. Vztah deprese k metabolickým onemocněním je však ještě výraznější. Obezita a cukrovka jsou onemocnění s rysy jak somatické, tak psychické nemoci. Tento článek pojednává o vztazích obezity a deprese. Vztahy deprese k diabetu jsou však ještě výraznější (přehledně [13, 14]). To platí o obou typech diabetu, i když u diabetu 2. typu je vazba na depresi větší. Diabetes 2. typu vzniká na genetickém základě a manifestován je vlivy prostředí, k nimž patří přejídání a absence pohybu [14]. To jsou vlivy, které působí, že diabetes nedostane geneticky založený diabetik 2. typu v 80 letech, ale třeba ve 40 nebo dokonce v 15 letech. Obezita tak rozvoji diabetu napomáhá a ke vztahu diabetes–deprese tak vztah deprese–obezita rovněž přispívá. V tomto článku se však budeme věnovat pouze vztahu obezity a deprese, pokud to půjde, bez problematiky diabetu.
Úvod
Obézní pacient se často nedokáže na své onemocnění podívat kriticky a chová se nelogicky. Nedokáže v léčbě spolupracovat nebo během léčby selhává. To může být ekvivalentem onemocnění psychiky, např. deprese. Typicky tloustne či v léčbě selhává v době osobních, rodinných a pracovních krizí. Obezitu nelze obvykle úspěšně léčit bez adekvátní psychoterapeutické podpory.
Na vztahy metabolických a psychických onemocnění se v minulosti pohlíželo skepticky. Mozek byl pokládán za orgán s transportem glukózy nezávislým na inzulinu a inzulinorezistence byla pokládána za jev typicky jaterní a svalový. Dnes je známo, že inzulin se významně váže centrálně a inzulinová rezistence typická pro androidní obezitu se vyskytuje i v mozku. Tento fakt je nejvíce prozkoumán na tzv. NIRKO myších s blokovaným inzulinovým receptorem v mozku [12].
Obezita je podle Björntorpa onemocněním těla i duše. Bez spolupráce více odborníků a bez pozornosti věnované depresi a psychologické problematice obézních nelze dnes obezitu léčit.
Vztahy mozku k inzulinu a periferním tkáním
Mozek je integrální součástí celého těla a není překvapením, že jevy typické pro periferní tkáně jsou přítomny i v mozku. Běžně známá špatná spolupráce nemocných při léčbě obezity i diabetu tedy může být i organického původu s příčinou ležící v centrálním nervovém systému a související s inzulinovou rezistencí. Prioritní je v tomto smyslu práce Horáčkova [11], která ukazuje pro internisty i psychiatry překvapivou korelaci mezi periferní inzulinovou rezistencí (tedy změnou přítomnou zejména ve svalech a játrech) a centrálními změnami serotoninergního systému (tedy reakcí mozku).
U dobrovolníků bylo provedeno vyšetření inzulinové citlivosti glykemickým clampem, tedy vyšetření, které prokazuje inzulinorezistenci zejména svalovou a jaterní. Současně byl proveden dexfenfluraminový test s odběry na prolaktin, kterým lze dobře testovat aktivitu centrálního serotoninergního systému. Byla zjištěna přesvědčivá korelace mezi periferní inzulinovou rezistencí a centrálním deficitem serotoninergního systému. Českými autory byl tak v klinickém experimentu prokázán vztah známý zatím, jak bude dále uvedeno, jen z epidemiologie – vztah mezi patogenetickými jevy u metabolického syndromu a deprese.
Tyto souvislosti ukazují na společný původ interních a psychických projevů onemocnění. Řadu let se obézní obviňovali z volního přejídání. Dnes je tedy známo, že i centrální mechanismy mohou být organickým onemocněním. Onemocnění periferie a CNS může být podobné. Inzulinorezistence a další změny se mohou projevovat stejně centrálně i periferně.
Již přes 20 let je znám anorektický efekt inzulinu. Jeho defekt vede u experimentálních zvířat k obezitě. Inzulinové receptory jsou na GnRH neuronech, zde jsou i IGF receptory. Touto cestou může být vyvolávána i vyšší hladina LH a syndrom polycystických ovarií. Centrální inzulinorezistence může vyvolávat další změny, které nelze vysvětlit periferní inzulinorezistencí [12, 14].
Tzv. jaderné receptory PPAR jsou významně ovlivňovány způsobem života. Vyskytují se i v mozku. Zatímco jejich terapeutické ovlivnění v somatické oblasti umožňuje léčit metabolická onemocnění, centrálně se uplatní spíše u degenerativních, ischemických a autoimunitních onemocnění centrálního nervového systému než u deprese [10].
Psychická závislost a obezita
Příjem jídla nepochybně obecně uklidňuje. Jde o fylogeneticky starý mechanismus, který měl pravděpodobně umožnit klidné trávení jídla. Nervozita a hyperaktivita při nedostatku potravy měly pravděpodobně podpořit vyhledávání a obstarávání potravy.
Zvýšená chuť k jídlu také může mít někdy rysy blízké drogovým závislostem. Změny v centrech hladu a regulace chuti k jídlu se týkají podobných mediátorů jako toxikomanie, patogeneze deprese či schizofrenie, tedy např. serotoninu, noradrenalinu a dopaminu.
Obezita sice vede k určité sociální izolaci (obézní chodí např. méně do společnosti), ale psychické problémy nastávají obvykle až při redukci hmotnosti. U nemocných, kteří hmotnost úspěšně redukovali, pak kontrastuje somatický efekt úbytku hmotnosti, např. vymizení dušnosti či bolestí kloubů, s tím, jak často a rychle léčba selhává a vzestup hmotnosti se vrací. Setkáváme se běžně například s diabetiky s extrémní hmotností připravovanými k endoprotéze kyčelního kloubu. Po úspěšném zhubnutí desítek kilogramů se operace realizuje. Imobilní nemocní zvýší postupně fyzickou aktivitu. Přesto se po několika letech opakovaně přihlásí s extrémní hmotností znovu. Psychické vlivy tak převáží nad somatickým efektem redukce hmotnosti a spolupráce nemocných v léčbě selhává.
Lidé závislí na návykových látkách nebývají obézní. To může být jistě dáno sociálními problémy, ale i tím, že k uklidnění používají jiné látky, než je jídlo.
Některé deprese souvisejí s příjmem alkoholu [6]. Alkohol může vyvolat primárně poruchy nálady a deprese je tak druhotná – alkoholem vyvolaná deprese. Naopak depresivní ladění může být součástí abstinenčního chování. Mírní pijáci jsou ale méně depresivní než abstinenti. Pití alkoholu zvyšuje serotoninový obrat. Krysy při pokusech s alkoholem po dexfenfluraminu i fluoxetinu omezují pití alkoholu. Depresivní pacienti také obvykle dříve ukončí abstinenci. Antidepresiva typu SSRI jsou u pacientů závislých na alkoholu poněkud méně účinná. Podle některých je účinnější tianeptin, který je obecně velmi výhodný pro obézní s depresí.
Psychoterapie je nedílnou součástí léčby obezity. Přípravy na zahájení diety jsou podobné přípravám na zahájení abstinence u návykových poruch (nikotin, alkohol i drogy). Rovněž při redukci hmotnosti jsou přítomny reakce blízké odvykacím příznakům.
Antidepresiva a hmotnost
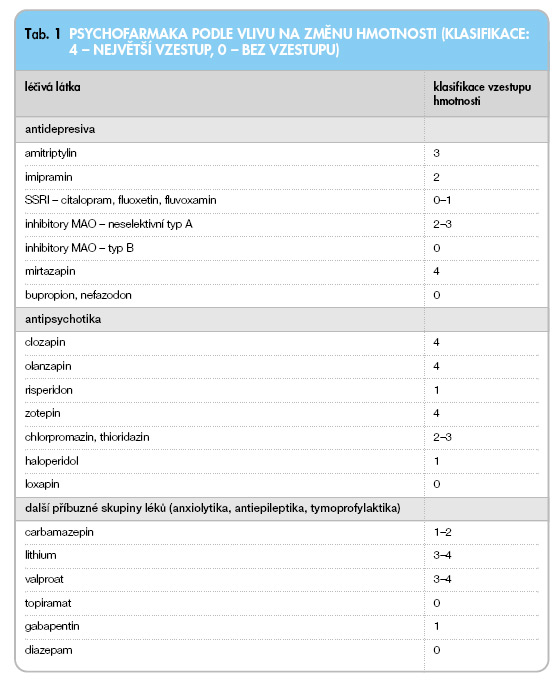
V psychiatrické literatuře jsou uváděny různé žebříčky psychofarmak a antidepresiv podle vlivu na vzestup hmotnosti (např. [13], volně podle [7–9]). Do tab. 1 jsou řazeny i některé blízké skupiny léčiv.
Právě antiepileptikum topiramat je v poslední době velmi zkoumaným potenciálním antiobezitikem. Tabulka potvrzuje i známý vzestup hmotnosti po lithiu.
Uvedeny jsou jen některé léky, ale i další, např. tianeptin, ritanserin či ziprasidon, mají výhodný efekt z hlediska obezity.
Zcela jistě je nejvhodnějším antidepresivem u obézních, u kterých chceme docílit pokles hmotnosti, bupropion [2]. U nás je preskripce limitována na psychiatry a sexuology. Z dalších léků je nejvhodnější podání tianeptinu, inhibitorů MAO a přírodních preparátů z třezalky tečkované (Hypericum perforatum) – (podrobně [4, 7–9, 13, 14]). Naopak výrazný je vzestup hmotnosti po klasických tricyklických antidepresivech [3].
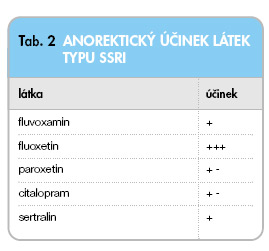
Pravděpodobně nejčastěji používanou skupinou antidepresiv u obézních pacientů s depresí jsou selektivní blokátory reuptake serotoninu (SSRI). Optimální látkou je nejspíše fluoxetin, po jehož podávání depresivní pacienti často hubnou. Po několika měsících se tento výhodný efekt obvykle zastaví. Tab. 2 uvádí přehledně stupeň anorektického efektu u látek typu SSRI.
V naší obezitologické ambulanci se pacientů běžně ptáme na insomnii a ranní pesima. U pacientů s příznaky deprese volíme vhodná antidepresiva. Realizovali jsme výzkum vlivu antidepresiv na hmotnost obézních v naší ambulanci. Ze sta nově příchozích pacientů jsme známky deprese zachytili u 41 pacientů. 33 pacientů bylo léčeno inhibitory SSRI a 9 pacientů medikací, která by měla navozovat spíše váhový pokles (bupropion a tianeptin – podrobně [15]). Naše zkušenosti potvrzují krátkodobou redukci hmotnosti po inhibitorech SSRI a vzestup hmotnosti po delším podávání.
Podání antidepresiv vede u obézních k větší adherenci k léčbě obezity. Projevem deprese může být i hmotnostní úbytek. Proto je někdy třeba u depresivních indukovat hmotnostní přírůstek. Z tohoto hlediska jsou nejvhodnějšími preparáty mirtazapin a paroxetin (podrobně [14]). K depresi mají vztah i dyslipidémie nezávisle na hmotnosti [1]. V poslední době jsou v léčbě deprese často podávány kombinace atypického neuroleptika, antiepileptika a inhibitorů SSRI. Tato kombinace je značně aterogenní a měla by být podávána vždy v kombinaci s dietní a režimovou intervencí (podrobně [14]). V minulosti se ve vztahu k dyslipidémiím objevily i obavy, že léčba statiny může vést k větší suicidialitě. Tyto hypotézy byly však definitivně vyvráceny [14, 16].
Deprese a další nemoci provázející obezitu
Jak bylo uvedeno výše, jsou vztahy obezity a deprese pravděpodobně zprostředkovány inzulinorezistencí. Inzulino-rezistence je hlavním projevem tzv. metabolického syndromu. To je syndrom aterogenní.
V poslední době se připouští i přítomnost trvalého zánětu u metabolického syndromu a zánětlivé teorie aterosklerózy a endoteliální dysfunkce. Je zajímavé, že podobný osud potkal i teorie vzniku deprese. Pro depresivní pacienty jsou typické vyšší hladiny cytokininů a spekuluje se o vztahu deprese a zánětu (podrobně [14]). Podobným mechanismem je vysvětlována i deprese u pacientů s AIDS a HIV pozitivitou.
Dnes je podle řady studií nepochybné, že deprese je nezávislým rizikovým faktorem aterogeneze, kardiovaskulárních příhod a zejména infarktu myokardu. Vedle suicidií jsou kardiovaskulární příhody druhou nejčastější příčinou smrti u depresivních pacientů. Kromě epidemiologických vztahů jsou diskutovány i patogenetické mechanismy této asociace, které mohou souviset s paralelními odchylkami metabolismu serotoninu v krevních destičkách, dalšími koagulačními odchylkami, vyššími hladinami interleukinů a rovněž se systémovým zánětem provázejícím jak metabolický syndrom a aterosklerózu, tak depresi. Zároveň platí i obráceně, že depresivní syndrom se vyskytuje běžně u pacientů po infarktu myokardu a je velmi významným prediktorem životní prognózy pacientů. Po infaktu se deprese vyskytuje u třetiny až poloviny pacientů. Je zajímavé, jak málo pozornosti je tomuto fenoménu věnováno v literatuře o infarktu i v běžné praxi [5].
Závěr – spolupráce interních oborů a psychiatra
Vazba deprese na metabolická onemocnění a jejich komplikace je vysoká. Po depresi by tedy měli aktivně pátrat nejen internisté, ale i diabetologové a další odborníci přicházející do styku s pacienty s obezitou a jejími komplikacemi. Správná volba antidepresiva může vést k vyšší úspěšnosti léčby obezity i jejích komplikací.
Internisté se při kontaktu s nemocným s depresí obvykle báli, že nemocný nebude schopen žádné spolupráce v léčbě. Psychiatři se naopak léčbě metabolických onemocnění, resp. metabolických komplikací své léčby nevěnovali. Dnes je situace jiná. Prognóza nemocných s psychickým onemocněním se výrazně zlepšila. Postupy bránící rozvoji metabolických onemocnění a aterosklerózy tak získaly na významu. Znalosti o metabolických účincích antidepresiv a o vzájemných vztazích deprese a obezity by měl mít každý, kdo s léčbou antidepresivy přichází do styku. Při významné depresivní symptomatologii je často třeba dát přednost efektu antidepresivní terapie, i když je vhodnější volit léky bez negativních metabolických efektů. U léků, které vyvolávají vzestup hmotnosti, ale jsou psychiatry žádané, je třeba kombinovat léčbu s dostatečnou edukací pacientů, monitorováním hmotnosti a metabolického dopadu léčby.
Seznam použité literatury
- [1] Almeida-Montes LG, et al. Relation of serum cholesterol, lipid, serotonin and tryptophan levels to severity of depression and to suicide attempts. J Psychiatry Neurosci 25; 2000: 371.
- [2] Ascher JA, et al. Bupropion a review of its antidepressant activity. J Clin Psych 1995; 56: 395–401.
- [3] Berken GH, et al. Weight gain a side effect of tricyclic antidepressant. J Affect Disord 1984; 7: 133–138.
- [4] Bjerkenstedt L. Efficacy and tolerance of hypericum in the treatment of major depression – a double blind, placebo and reference controlled clinical trial. Souhrn tiskové konference, Berlín, 1999.
- [5] Carney RM, et al. Depression and late mortality after myocardial infarction in the Enhancing Recovery in Coronary Heart Disease (ENRICHD) study. Psychosom Med 2000; 66: 466–474.
- [6] Crocq MA. Deprese a alkohol. WPA Bulletin o depresi 2001; 5: 3–6.
- [7] Fava M. Weight gain and antidepressants. J Clin Psych 2000; 61 (suppl. 11): 37–41.
- [8] Fitton AD, et al. Moclobemide. A review of its pharmacological properties and therapeutics use in depressive illness. Drugs 1992; 43: 561–596.
- [9] Garland EJ, et al. Weight gain with antidepressants and lithium. J Clin Psychofarmacol 1988; 8: 323–330.
- [10] Haluzík M, Svačina Š. Metabolické jaderné receptory PPAR. Praha, Grada, 2004 (v tisku).
- [11] Horáček J, et al. The relationship between central saerotonergic activity and insulin sensitivity in healthy volunteers. Psychoneuroendocrinology 1999; 24: 785–797.
- [12] Schwartz MW. Central nervous system control of food intake. Nature 2000; 404: 661–671.
- [13] Svačina Š. Obezita a psychofarmaka. Praha,Triton, 2002.
- [14] Svačina Š. Metabolické účinky psychofarmak. Praha, Triton, 2004.
- [15] Svačina Š. Antidepressants in obesity treatment. Prague Medical Report 2005; 106: 291–296.
- [16] Yang CC, Jick SS, Jick H. Lipid-lowering drugs and the risk of depression and suicidal behavior. Arch Intern Med 2003; 163: 1926–1932.