Praktická doporučení pro vedení klasické systémové léčby u pacientů s psoriázou
Souhrn:
Rob F. Praktická doporučení pro vedení klasické systémové léčby u pacientů s psoriázou. Remedia 2019; 29: 566–572.
Klasická systémová terapie představuje u pacientů trpících středně závažnou až závažnou psoriázou důležitou součást léčby, kterou není vhodné v indikovaných případech dlouhodobě odkládat. Odkládání systémové terapie a setrvávání na nedostatečně účinné lokální léčbě může vést k výraznému negativnímu dopadu na kvalitu života pacienta, k rozvoji komorbidit psoriázy a v neposlední řadě ke ztrátě compliance pacienta. V České republice máme k dispozici pro systémovou terapii psoriázy tři léčiva, mezi která patří metotrexát, cyklosporin a acitretin. Každé z těchto léčiv má odlišný profil přínosu a rizik, proto bychom léčbu vždy měli individuálně vybírat pro každého pacienta a v případě, že ani systémová léčba neposkytuje dostatečnou kontrolu psoriázy, neodkládat změnu systémové terapie či zahájení biologické léčby. Cílem tohoto textu je zaměřit se na praktické aspekty vedení klasické systémové léčby u pacientů s psoriázou, se kterými se lékaři předepisující tuto terapii mohou setkat.
Summary:
Rob F. Practical recommendations for classical systemic therapy management in patients with psoriasis. Remedia 2019; 29: 566–572.
Systemic therapy is an important part of the treatment of moderate to severe psoriasis that should not be delayed for long in the indicated cases. Postponing systemic therapy and staying on insufficiently effective topical treatment can lead to a significant negative impact on the patient’s quality of life, development of psoriatic comorbidities and, finally, loss of patient compliance. In the Czech Republic, three drugs are available for systemic therapy of psoriasis, including methotrexate, cyclosporine and acitretin. Each of these drugs has a different benefit and risk profile, therefore the treatment should be always selected individually for each patient. If the selected systemic treatment does not provide sufficient control of psoriasis, do not delay systemic treatment change or initiation of biological therapy. The aim of this manuscript is to focus on the practical aspects of classical systemic therapy management in patients with psoriasis that can be encountered by practitioners prescribing this therapy.
Key words: psoriasis − systemic therapy – methotrexate – acitretine – cyclosporine.
Úvod
V současnosti již máme k dispozici velmi účinné možnosti terapie psoriázy, díky nimž můžeme volit nejvhodnější léčbu individuálně pro každého pacienta. Každý pacient s psoriázou by měl být ideálně seznámen se všemi možnostmi léčby (lokální terapie, fototerapie, klasická systémová terapie, biologická léčba), včetně vysvětlení terapeutických postupů, které jsou pro něj nejvhodnější, a případných dalších variant, pokud by tato léčba nebyla účinná. Stanovení takovéhoto léčebného plánu poskytuje pacientovi vědomí, že i pokud jeho současná terapie nebude efektivní, existují do budoucna další možnosti ke zmírnění příznaků jeho onemocnění.
Výběr vhodného pacienta pro systémovou léčbu
Systémová léčba by měla být zahájena u pacientů, u kterých lokální léčba a fototerapie neposkytují dostatečnou kontrolu onemocnění (včetně výrazného snížení kvality života) nebo u nichž po ukončení léčby dochází k brzké exacerbaci [1]. Do této skupiny patří zpravidla pacienti se středně závažnou a závažnou psoriázou. V praxi mohou nastat případy, kdy i pro pacienta s mírnou psoriázou může toto onemocnění představovat výrazně negativní vliv na kvalitu jeho života, a pokud lokální terapie (případně fototerapie) nepřináší dostatečný efekt, je vhodné systémovou léčbu zvážit (např. závažné postižení nehtů nebo psoriáza kštice) [2]. Při rozhodování o zahájení systémové léčby však musíme mít na zřeteli i compliance pacienta, která je vzhledem k nutnosti monitorace potencionálních nežádoucích účinků systémové terapie zásadní.
Hodnocení závažnosti psoriázy
U pacientů s psoriázou bychom měli ideálně při každém vyšetření hodnotit nejen objektivní rozsah onemocnění, ale také subjektivní obtíže a jejich vliv na kvalitu života [3]. K měření závažnosti psoriázy můžeme využít popis procentuálního postižení kožního povrchu psoriázou (Body Surface Area). Standardem k hodnocení psoriázy je skóre PASI (Psoriasis Area and Severity Index), které zohledňuje nejen rozsah onemocnění, ale také intenzitu psoriatických projevů (zarudnutí, infiltrace, deskvamace) [4]. V praxi jsou dnes dostupné internetové kalkulátory či mobilní aplikace, díky nimž lze PASI stanovit u pacienta velmi rychle. Skóre PASI představuje nejpřesnější nástroj ke stanovení závažnosti onemocnění a je základním kritériem pro případnou indikaci biologické terapie. K měření subjektivních sympt
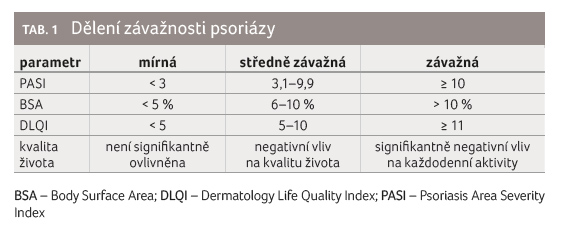
omů a ovlivnění pacientova života psoriázou lze využít skóre DLQI (Dermatology Life Quality Index). Jedná se o krátký dotazník, který se zaměřuje na ovlivnění běžných denních aktivit pacienta [5]. Je důležité si uvědomit, že rozsah postižení nemusí vždy korelovat s vlivem na kvalitu života, například u pacientů s psoriázou v obličeji, kštici či na genitálu může být vliv na kvalitu života výrazně negativní již při mírném rozsahu projevů [3], tab. 1.
Co vše ovlivňuje výběr vhodné léčby pro pacienta
Vzhledem k rozdílnosti profilů jednotlivých klasických systémových léků bychom si s pacientem vždy měli společně ujasnit, co od léčby psoriázy očekává. Jednotlivé systémové léky se liší rychlostí nástupu účinku, maximální účinností, předpokládanou délkou léčby, účinností na klouby (psoriatická artritida) a v neposlední řadě případnými nežádoucími účinky. V praxi se také musíme řídit i indikačním omezením pro každý lék.
Vyšetřování komorbidit psoriázy
Při prvním vyšetření pacienta s psoriázou a následně alespoň jednou ročně by měl být prováděn screening na komorbidity psoriázy, mezi které patří hypertenze, diabetes mellitus, hyperlipidemie, obezita, nealkoholická steatohepatitida a další choroby [6]. Většina těchto komorbidit je sledována ve screeningových vyšetřeních před zahájením systémové terapie, neboť jejich přítomnost může být relativní, či absolutní kontraindikací léčby. V případě přítomnosti komorbidit by se k případné kontraindikaci léčby měl vyjádřit příslušný specialista. K hodnocení přítomnosti psoriatické artritidy lze využít krátký dotazník PEST (Psoriasis Epidemiology Screening Tool) a v případě pozitivního nálezu je pacienta vhodné odeslat na revmatologické vyšetření [7].
Metotrexát
Metotrexát je imunosupresivní lék s protizánětlivým účinkem, který ovlivňuje lymfocyty v kůži i cirkulující v periferní krvi. Nástup účinku je postupný (pomalejší než u cyklosporinu), ale nabízí u velké části pacientů dlouhodobou dobrou kontrolu onemocnění. Metotrexát jako jediný z klasických systémových léčiv je taktéž indikován k léčbě psoriatické artritidy [8].
Dávkování
Iniciální dávka metotrexátu bývá
v rozmezí 5−15 mg podávaných 1× týdně. Pokud
kontrolní odběry neukazují na negativní vliv léčby
na krevní obraz (erytrocyty), jaterní a renální testy
a pacient terapii toleruje, lze zvýšit dávku až na 25 mg
1× týdně. Při dosažení terapeutického efektu postupně
snižujeme dávku na nejnižší účinnou. Pokud se nám
nepodaří dosáhnout remise onemocnění, ale terapie má uspokojivý
efekt, podáváme pacientovi maximální tolerovanou dávku
za pravidelné monitorace možných nežádoucích účinků.
Nástup účinku metotrexátu bývá (zvláště při nižších
počátečních dávkách) pozvolný a klinický efekt může
být viditelný až za 4−8 týdnů od zahájení léčby
[9,10]. Doporučenou laboratorní monitoraci léčby podrobně
rozebírá tabulka 2.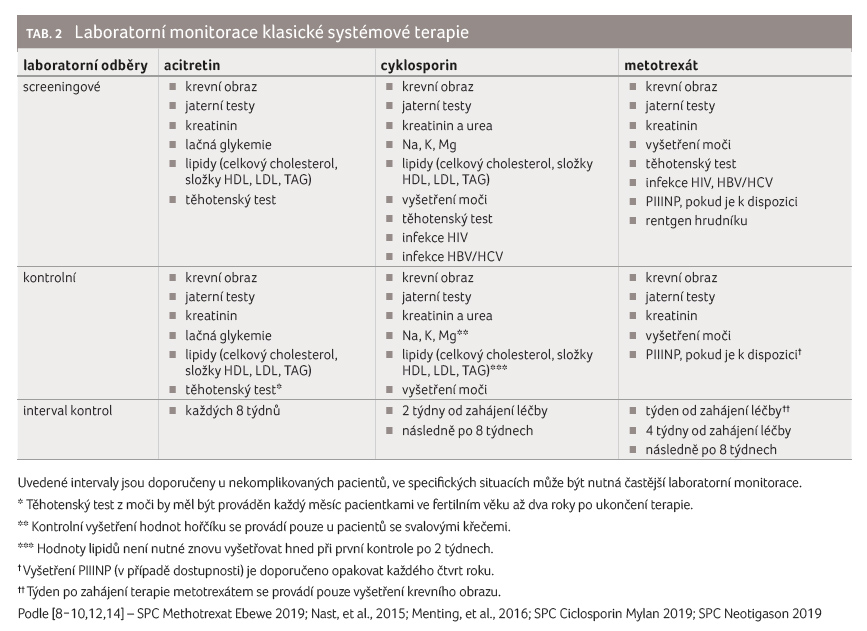
Nežádoucí účinky
Přehled nejdůležitejších
nežádoucích účinků systémové terapie ukazuje tabulka 3. Doporučení pro kontrolu případného postižení
jater v důsledku léčby metotrexátem se liší. Vzhledem
k dostupnosti neinvazivních vyšetření, jako je vyšetření
peptidu prokolagenu III (PIIINP) z krve či fibroscan‚ je
vhodnější nejprve provést tato šetrná vyšetření, a až
v případě přetrvávajícího podezření na poškození
jater provést jaterní biopsii.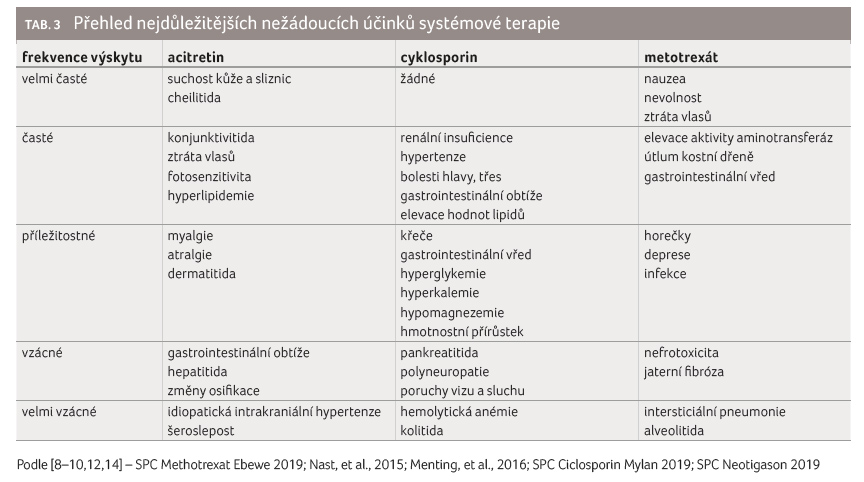
Lékové interakce
Nesteroidní antiflogistika, penicilin, salicyláty či sulfonamidy snižují renální eliminaci metotrexátu. Chloramfenikol, nesteroidní antiflogistika, sulfonamidy a některá cytostatika zvyšují potenciální toxicitu na kostní dřeň a zažívací trakt. Leflunomid, retinoidy, tetracyklinová antibiotika a etanol zvyšují jaterní toxicitu metotrexátu [8,9].
Výběr pacientů pro terapii
Vhodnými pacienty pro terapii metotrexátem jsou osoby, u nichž plánujeme dlouhodobou terapii, a pacienti s psoriatickou artritidou.
Jako nevhodné pacienty (relativní kontraindikace) je možné označit osoby s chronickým onemocněním jater či ledvin, nemocné s ulcerózní kolitidou, historií onkologického onemocnění, pacienty s městnavým srdečním selháním a nemocné s diabetes mellitus. Zvýšené opatrnosti je třeba dbát u starších pacientů. Léčba by neměla být zahajována u mužů i žen plánujících početí.
Léčba metotrexátem je kontraindikována u osob se závažnými infekcemi, u nemocných se závažnou poruchou funkce jater a ledvin, s abúzem alkoholu, u imunosuprimovaných pacientů, nemocných s hematologickým onemocněním (poruchy funkce kostní dřeně), s gastroduodenálním vředem, u gravidních a kojících žen [8,9].
Vakcinace a plánování operačních výkonů
Pacienti léčení metotrexátem by neměli být očkováni živými vakcínami. V případě plánování operačního zákroku nebyl prokázán přínos přerušení léčby metotrexátem (studie u revmatologických pacientů) [11].
Kombinovaná terapie
Metotrexát se využívá v kombinaci s lokální terapií nebo biologickými přípravky převážně z důvodu zvýšení léčebného efektu na psoriatickou artritidu.
Cyklosporin
Cyklosporin je imunosupresivní lék blokující transkripci cytokinů v aktivovaných T buňkách. Vyniká rychlým nástupem účinku (hlavně při vyšší indukční dávce) a celkovou vysokou účinností. Cyklosporin je tedy vhodný zvláště v případech, kdy máme v plánu krátkodobou léčbu nebo cílíme na rychlé zmírnění psoriázy. Při dlouhodobější terapii se však zvyšuje riziko vzniku nežádoucích účinků, proto se v případě jiných terapeutických možností nedoporučuje kontinuální léčba trvající déle než dva roky [12].
Dávkování
Doporučená denní dávka cyklosporinu by měla být v rozmezí 2,5−5 mg/kg. Zahajování léčby vyšší dávkou (5 mg/kg/den) je spojeno s rychlejším nástupem účinku a rovněž s větší šancí na dosažení vyšší účinnosti, zatímco bezpečnostní profil se při krátkodobé terapii neliší [13]. V praxi vzhledem k bezpečnostnímu profilu cyklosporinu bývá doporučeno zahájit léčbu dávkou 2,5 mg/kg/den a po měsíci zvýšit dávku na 5 mg/kg/den. Při dosaženíterapeutického efektu je možné dávku cyklosporinu postupně snižovat. Pokud se nám nepodaří dosáhnout remise onemocnění, ale terapie má uspokojivý efekt, zůstává pacient léčen maximální tolerovanou dávkou za pravidelné monitorace možných nežádoucích účinků. Vzhledem k rychlosti nástupu účinku cyklosporinu nemá smysl při nedostatečné účinnosti léčby vyčkávat déle než 12 týdnů při dávce 5 mg/kg/den a je vhodné volit jinou terapii [9].
Doporučení pro laboratorní monitoraci léčby uvádí tabulka 2.
Nežádoucí účinky
Nejdůležitější nežádoucí účinky léčby cyklosporinem jsou popsány v tabulce 3. Riziko nežádoucích účinků se zvyšuje s dávkou a délkou léčby, a to zvláště při trvání terapie více než dva roky.
Lékové interakce
Sérovou koncentraci cyklosporinu ovlivňuje zejména enzym CYP3A4, jehož je cyklosporin zároveň inhibitorem. Hodnoty cyklosporinu tak snižují například barbituráty, karbamazepin, rifampicin či terbinafin. Hodnoty cyklosporinu naopak zvyšují makrolidová antibiotika, azolová antimykotika, alopurinol či některá hormonální kontraceptiva. Zvýšené opatrnosti je nutno dbát hlavně u léčiv se synergickým nefrotoxickým účinkem, mezi něž patří aminoglykosidy, nesteroidní antirevmatika, fibráty či antagonisté H2 receptorů [9,12].
Výběr pacientů pro terapii cyklosporinem
Vhodnými nemocnými pro terapii cyklosporinem jsou osoby, u kterých preferujeme rychlý nástup účinku, a pacienti, u nichž plánujeme pouze krátkodobou léčbu.
Za nevhodné pacienty (relativní kontraindikace) považujeme osoby se závažným poškozením jater, hyperurikemií a hyperkalemií, pacienty s chronickou medikací s potencionálně nefrotoxickým účinkem, nemocné užívající jinou imunosupresivní léčbu. Cyklosporin nemá teratogenní účinek, ale jeho užívání je spojováno s nižší porodní hmotností dětí. Cyklosporin je tedy možné použít u gravidních a kojících, ale pouze v závažných případech.
Léčba cyklosporinem je kontraindikována u osob s poškozením funkce ledvin, s dekompenzovanou hypertenzí, u nemocných se závažnou infekční chorobou, s malignitou či s anamnézou onkologického onemocnění (s výjimkou léčeného bazocelulárního karcinomu či spinocelulárního karcinomu kůže in situ) a u pacientů léčených fototerapií (PUVA) [9,12].
Vakcinace a plánování operačních výkonů
Pacienti léčení cyklosporinem by neměli být očkováni živými vakcínami. V případě operačního zákroku je vhodné přerušit léčbu týden před plánovaným výkonem [9,12].
Kombinovaná terapie
Cyklosporin se používá v kombinaci pouze s lokální terapií.
Acitretin
Acitretin je syntetickým aromatickým analogem kyseliny retinové. Jediný z této skupiny klasických systémových léků nemá imunosupresivní účinek, lze ho proto využívat i u pacientů s chronickými infekcemi [14]. Acitretin je lék s pomalým nástupem účinku, který nevyniká svým účinkem, ale zvláště u některých forem psoriázy (palmoplantární, pustulózní) můžeme dosáhnout dobrého dlouhodobého terapeutického efektu.
Dávkování
Acitretin se zpravidla podává v úvodní denní dávce 25−30 mg, která zajišťuje u většiny pacientů dobrou snášenlivost terapie. Zvyšování dávky je vhodné provádět po čtyřech týdnech terapie až do maximální denní dávky 75 mg. Nicméně vzhledem k tomu, že se stoupající dávkou acitretinu se zvyšuje výskyt nežádoucích účinků, nebývá v praxi obvykle překračována denní dávka 50 mg. Při dosažení terapeutického efektu můžeme postupně snižovat denní dávku na nejnižší účinnou. Pokud se nám nepodaří dosáhnout remise onemocnění, ale terapie má uspokojivý efekt, ponecháváme léčbu maximální dávkou tolerovanou pacientem [9,15].
Doporučená laboratorní monitorace léčby je popsána v tabulce 2, nežádoucí účinky jsou uvedeny v tabulce 3.
Lékové interakce
Při léčbě acitretinem by pacient neměl užívat tetracyklinová antibiotika (indukce idiopatické intrakraniální hypertenze), imidazolová antimykotika (zvyšování jaterní toxicity) a jiné derivátu vitaminu A (hypervitaminóza) [14].
Výběr pacientů pro terapii acitretinem
Vhodnými nemocnými pro léčbu acitretinem jsou osoby, u nichž není vhodná imunosuprese (HIV pozitivní, starší pacienti), a pacienti s palmoplantární či pustulózní psoriázou.
Nevhodnými nemocnými (relativní kontraindikace) jsou pacienti s aktivní hepatitidou, pacienti s abúzem alkoholu, diabetici (negativní vliv na metabolismus glukózy) či pacienti s chronickou pankreatitidou. Léčba taktéž není doporučována u pacientů s hyperlipidemií (zvláště se zvýšením hodnot triglyceridů). Mírné zvýšení sérových koncentrací lipidů není možné brát jako absolutní kontraindikaci k léčbě, tyto pacienty je vhodné před případným zahájením léčby odeslat k internímu lékaři k nastavení terapie hyperlipidemie [16]. Vzhledem k výraznému teratogennímu efektu se acitretin nedoporučuje k léčbě žen ve fertilním věku, pokud existují jiné terapeutické možnosti.
Kontraindikací léčby acitretinem je závažné poškození ledvin či jater, alkoholismus, závažná hyperlipidemie, gravidita, kojení, neschopnost zajistit účinnou antikoncepci po dobu léčby a dva roky po ukončení léčby [9,14].
Vakcinace a plánování operačních výkonů
Pacienti léčení acitretinem mohou být očkováni všemi vakcínami. V případě operačního zákroku není nutné léčbu přerušovat.
Kombinovaná terapie
Acitretin lze účinně kombinovat s lokální terapií. Účinnost acitretinu lze zvýšit kombinací s fototerapií [17]. Současné podávání s cyklosporinem a metotrexátem není doporučováno, a to z důvodu zvýšeného rizika hepatotoxicity (metotrexát) a lékových interakcí (cyklosporin).
Co by mělo být cílem systémové léčby
Ideálním cílem každé léčby je vymizení objektivních i subjektivních příznaků psoriázy, což však v praxi není vždy možné. Již před samotným plánováním léčby bychom s pacienty měli probrat, jaká jsou jejich očekávání, neboť se mohou výrazně lišit [18]. Pro některé pacienty je důležitý rychlý nástup účinku, pro jiné eliminace psoriázy na viditelných lokalizacích, redukce psoriázy kštice, nehtů, či naopak spíše odeznění nepříjemných subjektivních symptomů, jako je svědění [19]. Za velmi dobrý efekt systémové léčby lze pokládat dosažení absolutního PASI ≤ 3 a vymizení negativního vlivu psoriázy na kvalitu života (DLQI ≤ 1), což odpovídá velmi mírné psoriáze.
Co dělat v případě nedostatečné účinnosti systémové léčby
Vývoj onemocnění je u každého pacienta individuální, a tak i při správném vedení terapie může být systémová léčba nedostatečně účinná nebo postupně ztrácet efekt. V případě konvenční systémové terapie neexistují jasně daná kritéria, kdy je léčba považována za neúčinnou a je vhodné ji změnit. Záleží tedy vždy na individuálním přístupu lékaře. Za požadovaný efekt systémové léčby lze považovat zmírnění příznaků psoriázy alespoň o 50 % (PASI 50) a/nebo snížení vlivu psoriázy na kvalitu života pacienta na žádný či mírný (DLQI ≤ 5) [18]. Jak již bylo zmíněno, hodnocení účinnosti léčby acitretinem, cyklosporinem a metotrexátem by mělo být prováděno po 12 týdnech léčby. Během tohoto období by pacientovi měla být postupně zvyšována dávka léčiva až do maximálního doporučeného dávkování, pokud je pacientem tolerováno a nedošlo k vymizení psoriázy. Jestliže po dalších čtyřech týdnech léčby maximální tolerovanou dávkou není lékařem či pacientem považován efekt léčby za dostatečný, je vhodné zvážit změnu terapie [20].
Nežádoucí účinky
Nežádoucí účinky systémové léčby nejsou vzácné a jejich závažnost osciluje od marginálních po závažné. V případě objektivně měřitelných nežádoucích účinků, jako je například rozvoj dyslipidemie u pacientů léčených acitretinem, hypertenze u pacientů s cyklosporinem či elevace aktivity jaterních aminotransferáz u osob léčených metotrexátem, se zpravidla jedná o postupné zhoršování sledovaných parametrů, kdy je vhodné provést konzultaci s příslušným specialistou (interní lékař, hepatolog či specialista lipidové poradny). Na základě této konzultace se rozhodujeme, zda je v terapii vhodné pokračovat, redukovat dávku, či léčbu zcela ukončit. Často u pacientů bývají přítomny subjektivní obtíže spojené s léčbou, jako je například suchost sliznic při terapii acitretinem či zvýšená únava (zpravidla následující den) po metotrexátu. Rozhodování o pokračování nebo přerušení léčby je třeba zvážit vždy individuálně podle ovlivnění kvality života daného pacienta. Pokud je léčba účinná, je možné snížit dávku, čímž můžeme dosáhnout redukce intenzity subjektivních obtíží pacienta. Současně lze provést režimová opatření ke snížení dopadu nežádoucích účinků (např. pravidelné promazávání rtů a umělé slzy v případě léčby acitretinem či užívání metotrexátu během víkendu, kdy zvýšená únava pacienty méně obtěžuje). Vzhledem k tomu, že se tyto obtíže objevují u velké části pacientů, je vhodné pacienty vždy před zahájením léčby o možném výskytu uvedených obtíží informovat.
Kdy pacienta odeslat na referenční pracoviště
Do referenčního centra bychom
měli odeslat pacienty se středně těžkou až těžkou psoriázou,
kteří nereagují dostatečně na probíhající léčbu. Dle
současných úhradových kritérií je možné biologickou léčbu
zahájit pouze u pacientů se středně těžkou až těžkou
psoriázou (definovanou jako PASI ≥ 10), kde nelze použít
dva z následujících způsobů konvenční systémové léčby
(acitretin, cyklosporin, metotrexát) nebo fototerapii z důvodů
nedostatečné účinnosti, intolerance či kontraindikace (přesné
podmínky úhrady jednotlivých biologických přípravků se mohou
mírně lišit z hlediska požadavků na typy předchozí
terapie). Pacientům je vždy vhodné před případným odesláním
do centra vysvětlit podmínky nutné k zahájení
biologické léčby, neboť nereálná očekávání mohou vést
k případné následné frustraci po návštěvě centra
a ke ztrátě další compliance pacienta. Doporučení
ke zprávě do referenčního centra uvádí tabulka 4.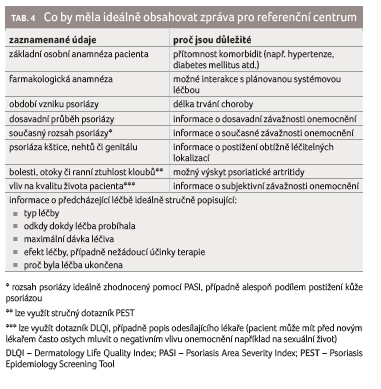
Závěr
Systémová léčba pacientů se závažnou a středně závažnou psoriázou by neměla být odkládána, neboť u indikovaných pacientů dochází ke snížení kvality života a k možnému riziku rozvoje komorbidit psoriázy. Pacienty je proto vhodné edukovat, že psoriáza není pouze onemocněním kůže, ale je provázena systémovým zánětem, který může zkrátit délku života a výrazně ovlivnit jeho kvalitu. Při zahájení systémové léčby je nutné vyčkat alespoň 12 týdnů na zhodnocení efektu léčby, nicméně pokud se účinek terapie nedostaví, není vhodné u takovéto léčby dlouhodobě setrvávat, jestliže existují jiné možnosti terapie. V případě odesílání pacienta do referenčního centra by měl mít pacient alespoň základní informace o dalších možnostech své léčby (zda splňuje, či nesplňuje kritéria pro zahájení biologické terapie), aby se předešlo nereálnému očekávání a následnému zklamání pacienta.
Seznam použité literatury
- [1] Feldman SR, Koo JY, Menter A, et al. Decision points ofr the initiation of systemic treatment for psoriasis. J Am Acad Dermatol 2005; 53: 101−107.
- [2] De Korte J, Mombers FM, Bos JD, et al. Quality of life in patients with psoriasis: a systematic literature review. J Invest Dermatol 2004; 9: 104−147.
- [3] Krueger GG, Feldman SR, Camisa C, et al. Two considerations for patients with psoriasis and their clinicians:: What defines mild, moderate, and severe psoriasis? What constitutes a clinically significant improvement when treating psoriasis? J Am Acad Dermatol 2000; 43: 281−285.
- [4] Langley RG, Ellis CN. Evaluating psoriasis with psoriasis area and severity index, psoriasis global assessment, and lattice system physician's global assessment. J Am Acad Dermatol 2004; 51: 563−569.
- [5] Lundberg L, Johannesson M, Silverdahl M, et al. Health‑related quality of life in patients with psoriasis and atopic dermatitis measured with SF‑36, DLQI and a subjective measure of disease activity. Acta Dermatovenerol 2000; 80: 430−434.
- [6] Dauden E, Blasco AJ, Bonanad C, et al. Position statement for the management of comorbidities in psoriasis. J Eur Acad Dermatol Venereol 2018; 32: 2058−2073.
- [7] Ibrahim GH, Buch MH, Lawson C, et al. Evaluation of an existing screening tool for psoriatic arthritis in people with psoriasis and the development of a new instrument: the Psoriasis Epidemiology Screening Tool (PEST) questionnaire. Clin Exp Rheumatol 2009; 27: 469.
- [8] Souhrn údajů o přípravku Methotrexat Ebewe [online, cit. 2019‑11‑26]. Dostupný na: http://www.sukl.cz/modules/medication/detail.php?code=0157123&tab=texts
- [9] Nast A, Gisondi P, Ormerod AD, et al. European S3‐Guidelines on the systemic treatment of psoriasis vulgaris – Update 2015 – Short version – EDF in cooperation with EADV and IPC. J Eur Acad Dermato Venereol 2015; 29: 2277−2294.
- [10] Menting SP, Dekker PM, Limpens J, et al. Methotrexate dosing regimen for plaque‑type psoriasis: a systematic review of the use of test‑dose, start‑dose, dosing scheme, dose adjustments, maximum dose and folic acid supplementation. Acta Dermato Venereol 2016; 96: 23−29.
- [11] Loza E, Martinez‑Lopez JA, Carmona L. A systematic review on the optimum management of the use of methotrexate in rheumatoid arthritis patients in the perioperative period to minimize perioperative morbidity and maintain disease control. Clin Exp Rheumatol 2009; 27: 856.
- [12] Souhrn údajů o přípravku Ciclosporin Mylan [online, cit. 2019‑11‑26]. Dostupný na: http://www.sukl.cz/modules/medication/detail.php?kod =0230989
- [13] Ellis CN, Fradin MS, Messana JM, et al. Cyclosporine for plaque‑type psoriasis. Results of amultidose, double‑blind trial. N Engl J Med 1991; 324: 277−284.
- [14] Souhrn údajů o přípravku Neotigason [online, cit. 2019‑11‑27]. Dostupný na: http://www.sukl.cz/modules/medication/download.php?file=SPC132782.pdf&type=spc&as=neotigason‑spc
- [15] Dogra S, Jain A, Kanwar AJ. Efficacy and safety of acitretin in three fixed doses of 25, 35 and 50 mg in adult patients with severe plaque type psoriasis: A randomized, double blind, parallel group, dose ranging study. J Eur Acad Dermatol Venereol 2013; 27: e305−e311.
- [16] Cetkovská P, Kojanová M, Arenberger P, Fabiánová J. Přehled současných doporučených postupů pro systémovou „nebiologickou“ léčbu psoriázy. Čes‑slov Derm 2017; 92: 3−17.
- [17] Iest J, Boer J. Combined treatment of psoriasis with acitretin and UVB phototherapy compared with acitretin alone and UVB alone. Br J Dermatol 1989; 120: 665−670.
- [18] Mrowietz U, Kragballe K, Reich K, et al. Definition of treatment goals for moderate to severe psoriasis: a European consensus. Arch Dermatol Res 2011; 303: 1−10.
- [19] Blome C, Gosau R, Radtke MA, et al. Patient‑relevant treatment goals in psoriasis. Arch Dermatol Res 2016; 308: 69−78.
- [20] Reich K, Mrowietz U. Treatment goals in psoriasis. J Dtsch Dermatol Ges 2007; 5: 566−574.