Terapie astmatu fixní kombinací a adherence k léčbě
Souhrn:
Farmakoterapie astmatu fixní kombinací (inhalační kortikosteroid plus inhalační β2-agonista s dlouhodobým, resp. ultradlouhodobým účinkem, tj. LABA, resp. U‑LABA v jednom inhalačním systému) nyní představuje základní kámen v léčbě astmatu. Fixní kombinace pomáhají zvyšovat adherenci k léčbě.
Summmary:
Fixed combination pharmacotherapy of asthma (inhaled corticosteroid plus long‑acting β2‑agonist, LABA, as well as ultra long‑acting β2‑agonist, U‑LABA, in a single inhalation device) now represents the cornerstone therapy of asthma. Therapy with fixed combinations increases adherence.
Key words: fixed combination asthma therapy, adherence to therapy.
Úvod
Farmakoterapie astmatu zažila v posledních 47 letech dva výrazné kvalitativní milníky, kterými byly zařazení inhalačních kortikosteroidů (IKS) do pravidelné léčby astmatu počátkem sedmdesátých let minulého století a vstup fixních kombinací, dnes označovaných jako klasické fixní kombinace (salmeterol/flutikazon propionát, resp. budesonid/formoterol), do preventivní terapie na přelomu tisíciletí, tj. před 18 lety [1]. Později se na trhu objevily fixní kombinace beklometazon/formoterol, flutikazon/formoterol a flutikazon furoát/vilanterol a jsou připravovány a již klinicky zkoušeny i další fixní kombinace. Dnes je přesvědčivě dokázáno, že přidání inhalačních ß2-agonistů s dlouhodobým účinkem (long acting ß2-agonists, LABA), resp. inhalačních ß2 -agonistů s ultradlouhodobým účinkem (ultra long acting ß2-agonists, U LABA) k IKS přináší zlepšení kontroly nad astmatem spočívající v redukci příznaků, ve zlepšení funkce plic, v redukci exacerbací a ve zlepšení kvality života. První publikací dokladující přínos přidání salmeterolu (LABA) k IKS v léčbě astmatu byla práce Greeninga v časopise Lancet publikovaná již v roce 1994, tedy před 24 lety [2]. Fixní kombinace v léčbě astmatu přináší ve srovnání s podáváním IKS a LABA v oddělených inhalačních systémech, tj. ve volné kombinaci, řadu výhod [3]. U LABA (vilanterol, olodaterol) nejsou v monoterapii dostupné. Kontroly nad astmatem je dosaženo menší dávkou IKS, je zajištěno, že LABA nebudou podávána samostatně a že nedojde k přerušení léčby IKS. Je zvýšena compliance a adherence k léčbě, neboť fixní kombinace pacientům více vyhovuje. I z ryze farmakoekonomického hlediska je poměr cena/účinek fixní kombinace ve srovnání s volnou kombinací výhodnější. Všechny fixní kombinace splňují podmínku, aby byly ve srovnání se svými monokomponentními přípravky bioekvivalentní a aby mezi jednotlivými komponentami fixní kombinace nedocházelo k farmakokinetickým interakcím.
Z hlediska farmakodynamického je prokázaná synergie účinku IKS plus LABA, resp. U LABA efektem třídy, což znamená, že mechanismus synergie, který byl prokázán in vitro, in vivo i klinickými studiemi, platí pro všechny fixní kombinace. Kortikosteroidy příznivě zasahují do působení ß2-agonistů tím, že zvyšují syntézu ß2 receptorů a zároveň snižují receptorovou desenzitizaci pro ß2-agonisty. LABA, resp. U LABA aktivují kortikosteroidní receptor, který je vázán v cytosolu v inaktivní formě v multiproteinovém komplexu. Tím je usnadněn vznik aktivního komplexu kortikosteroid/kortikosteroidní receptor za přítomnosti menšího množství kortikosteroidu. LABA, resp. U LABA zvyšují translokaci komplexu kortikosteroid/kortikosteroidní receptor do jádra buňky, kde dochází k uplatnění kortikosteroidu při genové transkripci, a navíc zvyšují rezidenční čas komplexu kortikosteroid/kortikosteroidní receptor v buněčném jádru [3]. Podávání IKS spolu s LABA, resp. U LABA nebo spolu s teofyliny má důležitou roli i pro potlačení sekundární kortikorezistence, jež často vzniká u pacientů s astmatem, kteří kouří, což je 20–40 % astmatické populace. U těchto pacientů dochází ke snížení účinnosti důležitého enzymu HDAC2 (histondeacetylázy 2), který je nezbytný pro zastavení acetylace histonů a následně k zastavení exprese prozánětlivých genů [1,3]. Fixní kombinace umožňuje i z hlediska plicní depozice homogenizaci komplementárního účinku obou léků.
Indikace léčby fixní kombinací
Fixní kombinace jsou indikovány pro léčbu astmatu tam, kde nelze dosáhnout a udržet astma pod plnou kontrolou monoterapií IKS, což by znamenalo, že fixními kombinacemi nelze léčbu astmatu zahajovat. Avšak současná světová doporučení i český doporučený postup shodně zaujímají k zahájení léčby astmatu fixními kombinacemi kladné stanovisko [1,4,5], což reflektuje i mnohaletou reálnou klinickou praxi. Z tohoto pohledu jsou stávající podmínky úhrady léčby fixní kombinací v České republice zastaralé a nekompatibilní s doporučenými postupy [4,5]. Fixní kombinace je indikována jak pro léčbu astmatu, tak i pro léčbu přesahu astmatu a chronické obstrukční plicní nemoci (CHOPN) označovaného jako ACOS nebo ACO (asthma and COPD overlap syndrome, resp. asthma and COPD overlap). Zastřešujícím termínem pro astma, CHOPN a ACOS je označení nemoc s chronickou bronchiální obstrukcí (CHBO; v angličtině se používá CBO – chronic bronchial obstruction). Dostupné portfolio fixních kombinací je poměrně široké a rovněž fixní kombinace lze podávat v různých inhalačních systémech (IS).
V současnosti již jsou v ČR
na trhu čtyři fixní kombinace: salmeterol/flutikazon
propionát – IS aerosolový dávkovač – MDI HFA
(hydrofluoroalkany), Diskus, Forspiro, Spiromax a zatím pouze
zaregistrován je Pulmojet; flutikazon furoát/vilanterol –
IS Ellipta; budesonid/formoterol – IS MDI HFA, Easyhaler,
Turbuhaler a Spiromax;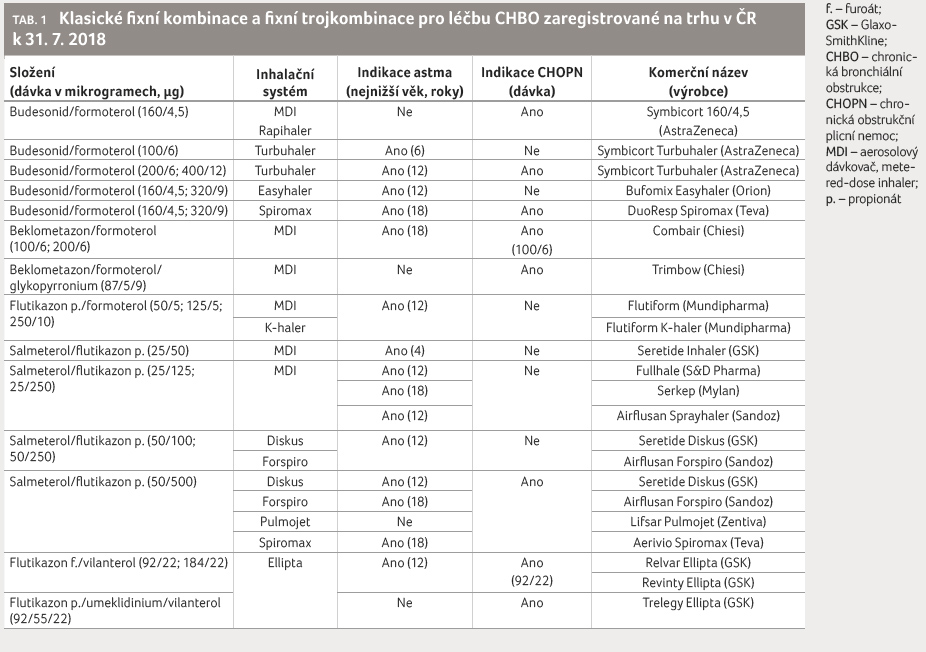 beklometazon/formoterol – IS
aerosolový dávkovač – MDI HFA Modulite a zcela
nově byl zaregistrován IS K haler. V současné době
přicházejí i na český trh fixní trojkombinace,
v nichž je k lékům tvořícím dvojkombinaci přidáváno
inhalační anticholinergikum. Ty jsou však indikovány jen pro
léčbu CHOPN. Jedná se o trojkombinaci
beklometazon/formoterol/glykopyrronium –
IS MDI HFA Modulite ‒ a o trojkombinaci
flutikazon propionát/umeklidinium/vilanterol – IS Ellipta.
První trojkombinace má již stanovenu úhradu a byla uvedena
na český trh 1. listopadu 2018. Přehled fixních
kombinací i fixních trojkombinací pro léčbu CHBO
registrovaných v ČR k 30. září 2018 je uveden
v tabulce 1.
beklometazon/formoterol – IS
aerosolový dávkovač – MDI HFA Modulite a zcela
nově byl zaregistrován IS K haler. V současné době
přicházejí i na český trh fixní trojkombinace,
v nichž je k lékům tvořícím dvojkombinaci přidáváno
inhalační anticholinergikum. Ty jsou však indikovány jen pro
léčbu CHOPN. Jedná se o trojkombinaci
beklometazon/formoterol/glykopyrronium –
IS MDI HFA Modulite ‒ a o trojkombinaci
flutikazon propionát/umeklidinium/vilanterol – IS Ellipta.
První trojkombinace má již stanovenu úhradu a byla uvedena
na český trh 1. listopadu 2018. Přehled fixních
kombinací i fixních trojkombinací pro léčbu CHBO
registrovaných v ČR k 30. září 2018 je uveden
v tabulce 1.
Režimy podávání fixních kombinací
Konvenční režim
Fixní kombinace byly nejprve podávány v pravidelném (konvenčním) režimu k léčbě středně těžkého a těžkého perzistujícího astmatu, jak již bylo zmíněno výše, inovovaný dokument GINA 2017/2018 [4] i národní doporučený postup pro astma 2016 [5] preferují podávání kombinace IKS plus LABA, resp. U LABA na třetím stupni farmakoterapie. Konvenční režim znamená, že se k pravidelnému podávání fixní kombinace jako kontrolujícího antiastmatika podává i úlevový lék podle potřeby, což je nejčastěji ß2-agonista s rychlým nástupem účinku a s krátkodobým účinkem (short acting ß2-agonist, SABA). Alternativu zde představuje inhalační anticholinergikum s krátkodobým účinkem (short acting muscarinic antagonist, SAMA) nebo kombinace SABA/SAMA.
Režim SMART
Fixní kombinaci budesonid/formoterol v odměřených dávkách 100/6 µg, 200/6 µg v IS Turbuhaler (od 1. ledna 2017 ji lze podávat v režimu SMART od věku 12 let), resp. v ekvivalentní podané dávce 160/4,5 µg v IS Spiromax a fixní kombinaci beklometazon/formoterol v odměřené dávce 100/6 µg v IS MDI lze podávat v režimu SMART (Single Maintenance And Reliever Therapy), kdy se podává základní udržovací dávka a k ní v případě potřeby jedna či více úlevových dávek. Tím dojde k úlevě od příznaků, což způsobuje bronchodilatačně účinkující formoterol, a k zastavení rozvoje exacerbace díky přídatné dávce IKS (budesonid či beklometazon). U fixní kombinace s budesonidem lze podat jako maximum 12 dávek za 24 hodin, u fixní kombinace s beklometazonem lze podat maximálně osm dávek za 24 hodin [1]. Režim SMART představuje značné zjednodušení léčby jak pro lékaře, tak hlavně pro pacienty, kteří používají v režimu SMART pouze jeden inhalátor, resp. jeden IS k dlouhodobé a současně k úlevové léčbě astmatu.
V mé klinické praxi představuje režim SMART režim první volby, pokud je indikována v léčbě astmatu fixní kombinace s formoterolem, která toto podání s ohledem na věk, IS a dávku léku umožňuje. To se týká i pacientů s ACOS. Režim SMART je nutné ukončit, pokud se vyskytnou projevy nežádoucích účinků některé z komponent fixní kombinace, včetně nejčastějšího obecného lokálního účinku IKS, jímž je dysfonie. Vnímavost k nežádoucím účinkům ß2-agonistů i IKS je velmi individuální a s režimem SMART nijak nesouvisí. Režim SMART je primárně nevhodný pro pacienty s abúzem ß2-agonistů a pro pacienty, kteří vyžadují striktní doporučení, jež jim nedává žádnou možnost volby. Pokud je režim SMART indikován nemocnému, který nebyl dosud léčen, je téměř vždy akceptován. Jiná situace nastává u pacientů, kteří byli dosud léčeni fixní kombinací nebo IKS v kombinaci s úlevovým lékem, zde je nutná hlubší edukace. To se týká i nemocných, kteří užívají fixní kombinaci umožňující režim SMART, ale nebyl jim dosud indikován. Často jsou pak překvapeni, jak lze léčbu astmatu zjednodušit.
Intermitentní režim
V květnu 2018 byly publikovány výsledky dvou ročních studií označených jako SYGMA1 [6] a SYGMA2 [7]. V nich bylo analyzováno celkem 8 012 astmatiků ve věku ≥ 12 let, z nichž 3 366 dostávalo fixní kombinaci budesonid/formoterol v odměřené dávce 200/6 µg z IS Turbuhaler v režimu podle potřeby, tedy nikoliv v režimu SMART. Studie reagovaly na klinickou praxi, kdy mnozí pacienti s lehkým astmatem takto danou fixní kombinaci používají. Komparátorem byla pravidelná dávka budesonidu 200 μg 2× denně plus SABA terbutalin podle potřeby, SYGMA1 měla ještě rameno, kde byl podáván jen terbutalin podle potřeby. Výsledky studií prokázaly, že léčba fixní kombinací budesonid/formoterol podle potřeby je z hlediska kontroly astmatu superiorní ve srovnání se samotným terbutalinem a prakticky stejná, výjimku tvoří více symptomů ve prospěch pravidelné léčby budesonidem, ve srovnání s denní dávkou 400 µg budesonidu. Této úrovně kontroly astmatu však bylo dosaženo podstatně menší dávkou IKS. Čas ukáže, zda i tento léčebný přístup bude v klinické praxi akceptován a zda bude přijat i regulatorními úřady.
Adherence k léčbě a compliance
Compliance a adherence jsou termíny, které se často zaměňují. Compliance znamená ochotu pacientů řídit se instrukcemi lékařů. Někteří nemocní však mají jen malé nebo nemají žádné vědomosti o své nemoci či o strategii vedení léčby. Adherence, tj. přilnutí k léčbě, znamená dodržování léčebného plánu, kde compliance je jeho hlavním řídícím faktorem. Konkordance (shoda) znamená, že příprava léčebného postupu probíhá v plné spolupráci lékaře a pacienta tak, aby postup vytvořili v plné shodě. Opakem je diskonkordance, ale zde již se vkrádá do této problematiky i forenzní hledisko [1,8]. Celá tato problematika je ovlivněna i poměrně novým, ale velmi důležitým faktorem, jímž je zdravotní gramotnost obyvatel daného regionu. Nízká zdravotní gramotnost je považována za rizikový faktor dosažení a udržení plné kontroly astmatu [1,4].
Ve středu odborného zájmu zůstává adherence a non adherence, která je někdy dělena na neúmyslnou (chaotická non adherence, non adherence z nevědomosti) a úmyslnou (inteligentní non adherence), která je považována za rizikovější, zvláště pokud je aplikována rodiči na děti. Aby bylo dosaženo optimální adherence, musí být nemocný srozumitelně informován o své nemoci ve všech souvislostech a musí být také schopen odpovídající samostatné terapeutické akce. Při dlouhodobém každodenním podávání kontrolující protizánětlivé léčby, kdy pacient účinek podaného léku nevnímá okamžitě, je adherence horší než při aplikaci inhalačních bronchodilatancií, která přinášejí rychlý účinek. Horší adherence je rovněž u lehkých forem astmatu, kdy má pacient jen lehké příznaky nebo při léčbě již nemá příznaky vůbec žádné. Adherenci zhoršují složitá schémata podávání léků. To se týká především frekventního dávkování, používání několika IS (polyfarmacie IS, tj. používání tří nebo více různých IS) nebo nemocného, který předepsaný IS používá s obtížemi. Z těchto důvodů volíme režim SMART. Adherenci dále zhoršují obavy z výskytu nežádoucích účinků léků. Kortikofobie, na níž se bohužel stále podílí i část odborné veřejnosti, ale i „alternativní“ přístup k léčbě, sociální sítě, nízká zdravotní gramotnost, nebo betafobie, kdy má pacient obavu užít včas úlevový lék, aby si na něj „nezvykl“. Jejím opakem je betafilie, tj. abúzus ß2-agonistů léků, za nímž se často skrývá nedostatečná či zcela chybná inhalační technika. Proto je nutná opakovaná edukace v inhalační technice a opakované kontroly inhalační techniky [9]. Adherenci dále zhoršuje zapomnětlivost či psychosociální problémy a špatná komunikace mezi lékařem a pacientem či jeho rodinou. Specifické problémy se zhoršenou adherencí přináší adolescence, kde vedle odmítání nemoci hraje nemalou roli i zapomnětlivost. U dětí je nutno pečlivě informovat o podstatě astmatu rodinu a její příslušníky vycvičit v zacházení s inhalačními systémy. Chybný výběr IS, chybná inhalační technika a složité schéma léčby patří mezi příčiny snížené adherence i v dětském věku. Ve zlepšení compliance a adherence mohou pomáhat různé aplikace do chytrých mobilních telefonů či iPadů. Obecně se předpokládá, že moderní technologie, které předejdou exacerbacím plicních onemocnění a zabrání tím i hospitalizacím, budou hrát v budoucnosti stále větší roli, což přinese i obrovské ekonomické úspory.
Závěr
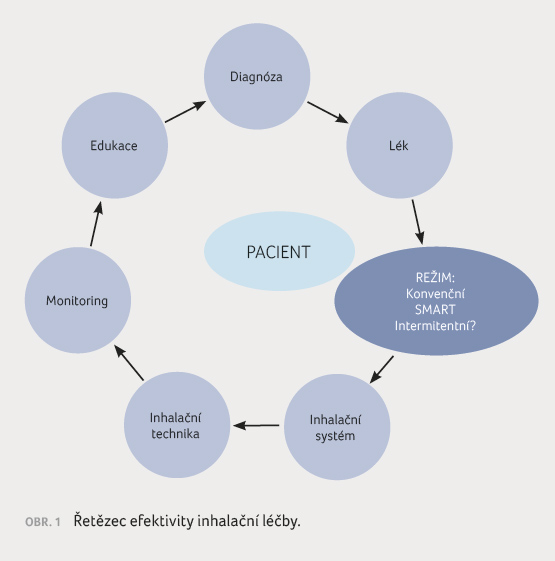
Široké portfolio fixních kombinací v různých IS nám v současné době umožňuje léčbu pacientů s CHBO individualizovat (personalizovat). Výběr konkrétního přípravku se primárně odvíjí od diagnózy, ideálně s určením fenotypu, indikaci musíme respektovat podle souhrnu údajů o léčivém přípravku (SPC). Pokud nerespektujeme diagnózu, resp. indikaci, jedná se o tzv. off label terapii, což přináší i forenzní konsekvence (je nutno pacienta nebo jeho zákonného zástupce o této skutečnosti informovat a pořídit o tom písemný záznam, odpovědnost za výskyt nežádoucích účinků léku pak nese předepisující lékař, nikoliv výrobce, tj. farmaceutická společnost). V našem zdravotním systému je nutno brát v úvahu i podmínky úhrady ze zdravotního pojištění, jejich nerespektováním se předepisující lékař vystavuje represím ze strany zdravotních pojišťoven (pozor také na „české preskripční paradoxon“, kde nejúčinnější léky na CHOPN nelze předepisovat kuřákům, což nemá obdobu v jiném státě Evropské unie). Dále je nutno přihlédnout k věku pacienta, což mj. souvisí i s výběrem IS, v němž je fixní kombinace k dispozici, a s režimem podávání (konvenční, či režim SMART, v budoucnosti pravděpodobně i režim podle potřeby, viz obr. 1). Samozřejmě je třeba brát v potaz komorbidity a komedikaci, jež mohou umocňovat jednak sníženou či zvýšenou účinnost fixní kombinace, jednak četnost výskytu nežádoucích účinků. V neposlední řadě je z pohledu pacienta důležitá výše doplatku za lék a z pohledu lékaře i cena léku, ale rovněž sankce ze strany zdravotních pojišťoven [1], což je v konotaci s ekonomickou aktuální situací ve společnosti. Zde však našemu zdravotnímu (pojišťovnickému) systému mnohdy chybí medicínské, sociální, etické, farmakoekonomické, ale i reálné forenzní hledisko.
Seznam použité literatury
- [1] Kašák V. Asthma bronchiale (Průvodce ošetřujícího lékaře). 3. vydání. Praha: Maxdorf Jessenius, 2018; 308 s.
- [2] Greening AP, Ind PVV, Nortfield M, et al. Added salmeterol versus higher‑dose corticosteroid in asthma patients with symptoms an existing inhaled corticosteroid. Lancet 1994; 344: 219‒224.
- [3] Barnes PJ. Scientific rationale for combination inhalers with long‑acting beta2‑agonists and corticosteroids. Eur Respir J 2002; 19: 951‒989.
- [4] GINA Workshop Report – Revised 2018. Dostupné na: http://www.ginasthma.org
- [5] Teřl M, Čáp P, Dvořáková R, et al. Asthma bronchiale. In Kolek V, et al. Doporučené postupy v pneumologii. Praha: Maxdorf, 2016; p. 55–108.
- [6] O’Byrne PM, FitzGerald MJ, Batemann ED, et al. Inhaled combined budesonide‑formoterol as needed in mild asthma. N Eng J Med 2018; 378: 1865‒1876.
- [7] Bateman ED, Reddel HK, O’Byrne PM, et al. As‑needed budesonide‑formoterol versus maintenance budesonide in mild asthma. N Eng J Med 2018; 378: 1877‒1887.
- [8] Pohunek P. Adherence v léčbě perzistujícího astmatu. Alergie 2017; 19: 269‒272.
- [9] Kašák V, Kašáková E. Inhalační systémy. Praha: Maxdorf Jessenius, 2017; 148 s.