Apixaban v léčbě a v sekundární prevenci tromboembolické nemoci
Souhrn:
Apixaban jako přímý perorální a selektivní inhibitor aktivovaného faktoru Xa je od roku 2014 schválen pro léčbu akutní žilní trombózy a stabilní plicní embo-lie, kromě již dřívější registrace pro prevenci systémové embolizace u nevalvulární fibrilace síní. Nově má tento přípravek od 1. 11. 2015 stanovenu i úhradu ze zdravotního pojištění a vedle rivaroxabanu nyní představuje další možnost plné perorální léčby od prvého dne stanovení diagnózy tromboembolické žilní nemoci.
Key words: apixaban – acute venous thrombosis – acute pulmonary embolism – thromboembolic disease – secondary prevention.
Summmary:
Apixaban is a direct and selective oral inhibitor of activated factor Xa. Since 2014, it has been approved for the treatment of acute venous thrombosis and stabile pulmonary embolism beside its earlier approval for the prevention of systemic embolization in non valvular atrial fibrillation. Since November 1st, 2015, apixaban treatment is covered by the health insurance and represents now – together with rivaroxaban – another alternative of fully oral therapy of thromboembolic disease starting immediately after establishing the diagnosis.
Úvod
V léčbě flebotrombózy a plicní embolie dominují antikoagulancia, u většiny nemocných je volíme v případě distální i proximální lokalizace trombózy, stejně jako u raritních trombóz žil horní končetiny. Účinně vedená antikoagulační léčba zpravidla zabrání dalšímu nárůstu trombu a minimalizuje riziko embolizace. Ne vždy však dosáhneme kompletní disoluce trombu a rekanalizace žíly; proto může být u mladších jedinců s rizikem vývoje posttrombotického syndromu indikována též trombolýza. Typ léčby plicní embolie určuje zejména její hemodynamický dopad na organismus (riziková stratifikace), nikoli samotná velikost obstrukce plicních tepen.
K antikoagulační léčbě tromboembolické nemoci (TEN) je možno volit klasický přístup – v iniciální fázi nízkomolekulární heparin či fondaparinux, eventuálně heparin nefrakcionovaný – s přechodem na warfarin, nověji i na dabigatran. Alternativou je iniciální podávání přímých perorálních antikoagulancií od stanovení diagnózy, vedle již takto zavedeného podávání rivaroxabanu máme nově i možnost léčby apixabanem.
Apixabanu byla aktuálně (od 1. 11. 2015) stanovena úhrada též v indikaci léčby flebotrombózy či plicní embolie a v profylaxi recidivy příhod, proto je účelné podat přehled základních dat, která vedla ke schválení této léčby.
Základní charakteristika apixabanu
Apixaban je perorální přímý inhibitor aktivovaného faktoru Xa. Od tohoto faktoru byl odvozen i název celé skupiny – xabany. Blokáda faktoru Xa zabrání aktivaci protrombinu na aktivní proteázu trombin, která polymerizuje fibrinogen na fibrin s vytvořením fibrinové sítě koagula.
Inhibice faktoru Xa apixabanem je charakterizována třemi přívlastky – přímá, kompetitivní a selektivní. Přívlastek „přímý“ značí, že jde o primární inhibici katalytického místa faktoru Xa. To apixaban odlišuje od nepřímých inhibitorů faktoru Xa (heparinu a jeho derivátů), jejichž účinek je dán aktivací antitrombinu, který se druhotně váže na katalytické místo faktoru Xa. Hlavní výhodou přímé inhibice je zachování plného účinku i při získané či vrozené deficienci antitrombinu, nedochází tak k selhání léčby až u 5 % populace. Druhou předností je dosažení dostatečné blokády faktoru Xa, a to jak volného, tak vázaného v protrombinázovém komplexu s kofaktorem V, či faktoru Xa vázaného v koagulu. Díky tomu se neobjevuje druhotná aktivace hemostázy po rozpadu trombu. Apixaban má dokonce několikanásobně vyšší afinitu k faktoru Xa vázanému v koagulu než k volnému faktoru Xa v plazmě.
Další charakteristikou je kompetitivnost. Kompetitivní vazbou je zachován vztah mezi dávkou a účinkem, který je v terapeutických dávkách lineární. Vzhledem ke krátkému biologickému poločasu aktivovaného faktoru X i vzhledem ke skutečnosti, že na inhibici se nepodílí žádný aktivní metabolit, je antikoagulační účinek přímo úměrný koncentraci apixabanu v plazmě a trvá pouze po tuto dobu.
Též označení „selektivní“ je zcela namístě. Inhibice faktoru Xa je vysoce specifická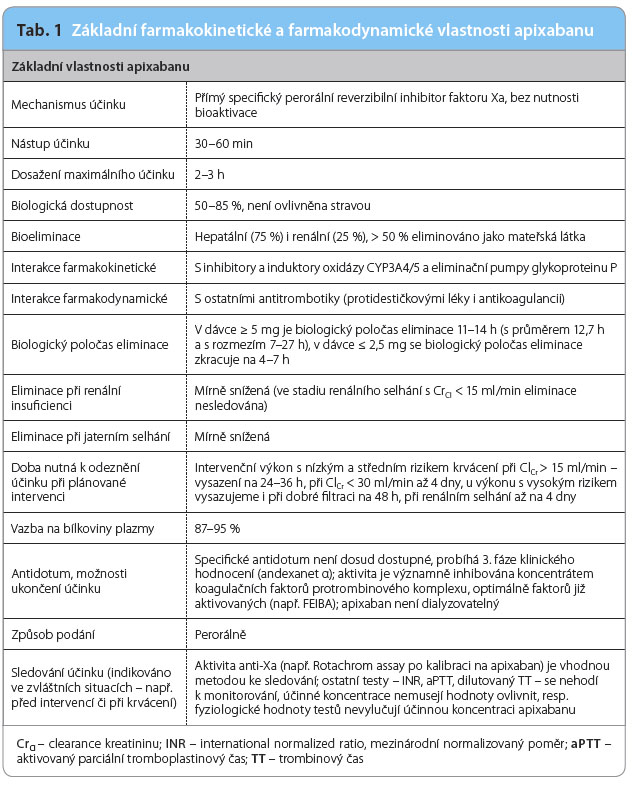 , ve srovnání s účinkem na ostatní enzymy a kofaktory je inhibice téměř o pět řádů silnější [1]. Ve srovnání s warfarinem, který inhibuje aktivaci jak koagulačních faktorů, tak efektorů antikoagulační větve (proteinu C a S), zasahuje apixaban jen na úrovni koagulační. Neobjevuje se proto iniciální fáze hyperkoagulace, se kterou se setkáváme po zahájení léčby warfarinem.
, ve srovnání s účinkem na ostatní enzymy a kofaktory je inhibice téměř o pět řádů silnější [1]. Ve srovnání s warfarinem, který inhibuje aktivaci jak koagulačních faktorů, tak efektorů antikoagulační větve (proteinu C a S), zasahuje apixaban jen na úrovni koagulační. Neobjevuje se proto iniciální fáze hyperkoagulace, se kterou se setkáváme po zahájení léčby warfarinem.
Farmakokinetické vlastnosti apixabanu jsou příznivé (tab. 1), zajišťují dobře předvídatelný účinek po celou dobu dávkovacího intervalu. Ten závisí nejen na stabilní biologické dostupnosti, ale také na nízké variabilitě biotransformace i exkrece. Konkrétně na minimálním ovlivnění těchto veličin variací renálních či jaterních funkcí, na farmakogenetické výbavě či na interakci s potravou či s léky.
V porovnání s rivaroxabanem nejsou ve farmakologických vlastnostech žádné významné rozdíly. Oproti dabigatranu je výhodou minimální podíl renální eliminace a vyšší dostupnost, snižující riziko lékové interakce.
Apixaban v léčbě tromboembolické nemoci
Účinnost a bezpečnost apixabanu v léčbě flebotrombózy a plicní embolie prověřovala studie AMPLIFY, na jejímž základě bylo v roce 2014 schváleno užití v této indikaci. V této dvojitě zaslepené studii byl apixaban podáván od počátku akutní fáze. Iniciálně (po dobu sed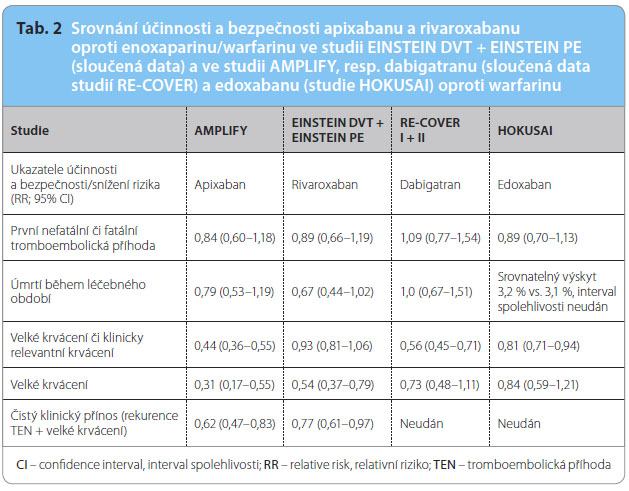 mi dnů) byla užita dávka 2× 10 mg denně a následně v dlouhodobé fázi byla podávána dávka 2× 5 mg. Srovnávaným standardním postupem byla iniciální léčba enoxaparinem s přechodem na léčbu warfarinem. Zařazeno bylo téměř 5 500 nemocných s akutní flebotrombózou. Primárním ukazatelem účinnosti byla recidiva symptomatické flebotrombózy nebo úmrtí ve vztahu k flebotrombóze, primárním bezpečnostním ukazatelem byl výskyt velké krvácivé příhody nebo kombinace velké a klinicky významné hemoragické příhody. Výsledky jsou prezentovány v tabulce a v grafické podobě křivky nárůstu incidence (tab. 2 a graf 1). Je patrné, že vedle nesignifikantního poklesu počtu tromboembolických příhod bylo pozorováno rovněž nevýznamné snížení (asi o pětinu) celkové i kardiovaskulární mortality (non‑inferiorita proti enoxaparinu/warfarinu). Vliv léčby byl tedy v obou větvích porovnatelný, trend ve prospěch apixabanu nedosáhl významnosti. Naopak oba primární bezpečnostní ukazatele (velké a klinicky významné krvácivé příhody) byly význ
mi dnů) byla užita dávka 2× 10 mg denně a následně v dlouhodobé fázi byla podávána dávka 2× 5 mg. Srovnávaným standardním postupem byla iniciální léčba enoxaparinem s přechodem na léčbu warfarinem. Zařazeno bylo téměř 5 500 nemocných s akutní flebotrombózou. Primárním ukazatelem účinnosti byla recidiva symptomatické flebotrombózy nebo úmrtí ve vztahu k flebotrombóze, primárním bezpečnostním ukazatelem byl výskyt velké krvácivé příhody nebo kombinace velké a klinicky významné hemoragické příhody. Výsledky jsou prezentovány v tabulce a v grafické podobě křivky nárůstu incidence (tab. 2 a graf 1). Je patrné, že vedle nesignifikantního poklesu počtu tromboembolických příhod bylo pozorováno rovněž nevýznamné snížení (asi o pětinu) celkové i kardiovaskulární mortality (non‑inferiorita proti enoxaparinu/warfarinu). Vliv léčby byl tedy v obou větvích porovnatelný, trend ve prospěch apixabanu nedosáhl významnosti. Naopak oba primární bezpečnostní ukazatele (velké a klinicky významné krvácivé příhody) byly význ![Graf 1 Srovnání apixabanu se standardní léčbou (enoxaparin v akutní fázi s přechodem na warfarin) v léčbě fl ebotrombózy – porovnání primární účinnosti, tj. doby do vzniku prvé TEN příhody či do úmrtí na TEN (data ze studie AMPLIFY). Pokles výskytu příhod o 16 % při léčbě apixabanem nedosáhl statistické významnosti, doložena non-inferiorita proti standardní léčbě. Podle [2] – Agnelli, 2013. CI – confi dence interval, interval spolehlivosti; HR – hazard ratio, poměr rizik; TEN – tromboembolická nemoc; VKA – vitamin K antagonists, antagonisté vitaminu K](https://www.remedia.cz/photo-a-30359---.jpg) amně nižší při léčbě apixabanem, pokles jejich výskytu o dvě třetiny byl vysoce významný i klinicky (graf 2).
amně nižší při léčbě apixabanem, pokles jejich výskytu o dvě třetiny byl vysoce významný i klinicky (graf 2).
Při nepřímém srovnání účinku s rivaroxabanem, který je možno rovněž aplikovat bez předchozího parenterálního podávání antikoagulancia, je doložena srovnatelná účinnost, ale větší bezpečnost při hodnocení velkých a klinicky významných krvácení, velká krvácení byla srovnatelně častá. Čistý klinický přínos léčby (součet tromboembolických příhod a velkého krvácení) byl u obou xabanů významně lepší ve srovnání se standardní léčbou enoxaparinem a s přechodem na léčbu warfarinem (tab. 2). Přínos druhé léčebné strategie, tj. v iniciální fázi podávání nízkomolekulárního heparinu (low molecular weight heparin, LMWH) ![Graf 2 Srovnání apixabanu se standardní léčbou (enoxaparin v akutní fázi s přechodem na warfarin) v léčbě fl ebotrombózy – porovnání primárního ukazatele bezpečnosti, tj. doby do vzniku prvé velké krvácivé komplikace (data ze studie AMPLIFY). Pokles výskytu velkého krvácení o dvě třetiny byl významný, doložena superiorita apixabanu v poklesu počtu krvácivých příhod ve srovnání se standardní léčbou. Podle [2] – Agnelli, 2013. CI – confi dence interval, interval spolehlivosti; HR – hazard ratio, poměr rizik; VKA – vitamin K antagonists, antagonisté vitaminu K](https://www.remedia.cz/photo-a-30360---.jpg) s přechodem na léčbu perorálním antikoagulanciem až v subakutní fázi, jak byl prověřován u dabigatranu a edoxabanu, ukázal obdobnou účinnost proti klasické léčbě. Pokud byl sledován výskyt velkého a klinicky významného krvácení, byla též doložena superiorita proti warfarinu, velká krvácení však byla stejně častá.
s přechodem na léčbu perorálním antikoagulanciem až v subakutní fázi, jak byl prověřován u dabigatranu a edoxabanu, ukázal obdobnou účinnost proti klasické léčbě. Pokud byl sledován výskyt velkého a klinicky významného krvácení, byla též doložena superiorita proti warfarinu, velká krvácení však byla stejně častá.
Obecně řečeno, nejsou‑li prokázány zásadní rozdíly v účinku, výběr optimálního léčiva se odvíjí především od dostupnosti léčby. Preskripce přímých perorálních antikoagulancií, tj. apixabanu, rivaroxabanu i dabigatranu, je omezena pouze odborností a délkou podávání, představuje však možnost první volby. Dostupnost tedy prakticky omezena není. Hlavním kritériem výběru je tak preference lékaře a nemocného. Bude‑li upřednostněno podání perorálně působícího léčiva bez nutnosti parenterální aplikace LMWH, volíme jeden z obou xabanů. U nemocného s vyšším rizikem hemoragických komplikací je třeba přihlédnout k nižšímu výskytu velkého a klinicky významného krvácení při podávání apixabanu. Naopak při volbě parenterální léčby LMWH v počátečním období je dále indikován dabigatran. Jistě by však i v tomto případě nebylo medicínskou chybou podání apixabanu či rivaroxabanu. Příkladem by byl nemocný s kontraindikací dabigatranu při výrazně snížené glomerulární filtraci. Pokud by perioda aplikace LMWH trvala nejméně týden, pak by bylo vhodné pokračovat již redukovanou dávkou apixabanu.
Apixaban v indikaci léčby TEN podáváme ihned po stanovení diagnózy v dávce 10 mg 2× denně po dobu sedmi dnů, poté 5 mg 2× denně dlouhodobě.
Délka léčby se odvíjí od rizika recidivy příhody. Minimální dobou léčby jsou tři měsíce. Například při izolované bércové trombóze, pominula‑li riziková situace (chirurgický výkon, sádrová fixace, šestinedělí, imobilizace z interních příčin apod.), je postačující antikoagulace tříměsíční. Jedná‑li se o idiopatickou trombózu nebo trvá‑li i nadále riziko vzniku trombózy (snížená mobilita, nutná hormonální léčba atd.), je žádoucí alespoň šestiměsíční antikoagulace, popř. prodlužujeme dobu antikoagulace po dobu trvání rizikové situace. V případě průkazu komplikující se větší plicní embolie prodlužujeme antikoagulační léčbu na 6–12 měsíců. Prokážeme‑li významný trombofilní stav u nemocného s proximální flebotrombózou, doporučuje se 12 měsíců trvající antikoagulace. Takovým stavem je zejména přítomnost abnormální koncentrace antikoagulačních proteinů nebo trombogenní mutace několika faktorů. Nutno však zdůraznit, že častěji se vyskytující mutace, zejména heterozygocie leidenské mutace pro protrombin, zvyšuje riziko recidivy jen málo, délka léčby by ani v případě kombinace těchto hereditárních trombofilií neměla přesáhnout jeden rok. Při kumulaci ostatních trombofilních faktorů nebo při homozygotní konstituci zvažujeme riziko krvácivých komplikací a při únosném riziku pokračujeme v antikoagulační léčbě tzv. dlouhodobě. U pacientů s rekurentními trombózami, zejména komplikovanými plicní embolizací, s trombózami v nezvyklých lokalitách či s přítomností vážných trombofilních stavů je po zvážení všech okolností vzácně indikována i doživotní antikoagulační medikace. O způsobu úhrady po dobu delší než 12 měsíců probíhají jednání s plátci péče, zatím je nutno volit jednání s revizním lékařem. Je však třeba konstatovat, že optimální délka léčby u těchto stavů není definitivně stanovena a názory na tuto problematiku se stále vyvíjejí.
Prolongace profylaktické léčby po léčbě TEN ukončené lege artis
Po skončení 3–12měsíční antikoagulační léčby flebotrombózy či plicní embolie je možno zvážit prolongaci na další období, rozhodující je reziduální riziko recidivy. K extenzi léčebného období je možno volit řadu antitrombotik. Mírné snížení rizika recidivy příhody o 40–50 % bylo doloženo při podávání kyseliny acetylsalicylové v klasické lékové for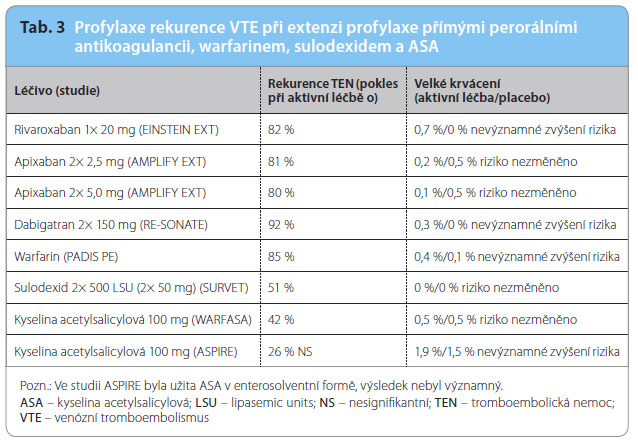 mě a při podávání sulodexidu. Výrazné snížení rizika recidivy TEN pak bylo doloženo při podávání perorálních antikoagulancií – apixabanu, rivaroxabanu, dabigatranu a warfarinu, zde se snížil výskyt recidivy TEN na 10–20 % (tab. 3). Riziko výskytu krvácení se významně nelišilo ani u jednoho léčebného postupu.
mě a při podávání sulodexidu. Výrazné snížení rizika recidivy TEN pak bylo doloženo při podávání perorálních antikoagulancií – apixabanu, rivaroxabanu, dabigatranu a warfarinu, zde se snížil výskyt recidivy TEN na 10–20 % (tab. 3). Riziko výskytu krvácení se významně nelišilo ani u jednoho léčebného postupu.
Při porovnání výsledků studií RE‑SONATE, EINSTEIN EXT a AMPLIFY EXT s přímými perorálními antikoagulancii nenajdeme výraznější rozdíly v účinnosti, pokles proti placebu činil 80–90 %. Zásadní rozdíly nebyly doloženy ani v bezpečnosti, tj. v incidenci velkých a klinicky významných krvácení, jejich výskyt byl vzácný (< 1 %). V této indikaci pak volíme antikoagulancium podle vlastní preference, pouze s ohledem na renální funkce a souběžnou léčbu. Opět je možno přihlédnout k nejnižšímu výskytu krvácení při léčbě apixabanem.
Úhrada přímých perorálních antikoagulancií při extenzi standardní léčby TEN u rizikových osob není dosud schválena. Léčbu u nemocných, u nichž existuje indikace, je proto třeba nechat schválit revizním lékařem, či volit jinou léčebnou strategii.
Seznam použité literatury
- [1] Raghavan N, Frost CE, Yu Z, et al. Apixaban metabolism and pharmacokinetics after oral administration to humans. Drug Metab Dispos 2009; 37: 74–81.
- [2] Agnelli G, Buller HR, Cohen A, and AMPLIFY Investigators. Oral apixaban for the treatment of acute venous thromboembolism. N Engl J Med 2013; 369: 799–808.
- [3] Agnelli G, Buller HR, Cohen A, et al. Apixaban for extended treatment of venous thromboembolism. N Engl J Med 2013; 368: 699–708.