Duální agonisté receptorů PPAR
Na patogenezi metabolického syndromu i diabetu, komplexních onemocnění s celosvětově stoupající prevalencí, se podílejí složky dědičné predispozice a prostředí přibližně stejnou mírou, a proto je úprava životního stylu (diety, pohybové aktivity) zásadní složkou prevence i terapie obou onemocnění. V praxi je ovšem farmakologická intervence nedílnou součástí jejich léčby. Inzulinovou rezistenci a dyslipidémii je možné efektivně modulovat agonisty nukleárních receptorů PPAR. Thiazolidindiony (rosiglitazon a pioglitazon) jsou agonisté PPAR- a mají inzulin-senzitizujcí efekt bez zásadního účinku na hladiny lipidů. Naproti tomu agonisté PPAR- (např. fibráty) nevykazují vedle svého hypolipidemického účinku větší ovlivnění senzitivity tkání k účinkům inzulinu. Tato pozorování vedla k derivaci nethiazolidindionových duálních agonistů PPAR-/ (glitazarů), které by měly kombinovat oba typy působení. Slibné výsledky z prvotních experimentálních a klinických studií jsou bohužel prozatím ve stínu nežádoucích účinků, které vedly k přerušení či zastavení vývoje již několika glitazarů.
V současné době jsme svědky celosvětového vzestupu prevalence řady tzv. civilizačních onemocnění – obezity, diabetu 2. typu, aterosklerózy, hypertenze a dalších. Mnohdy navíc dochází ke kumulaci inzulinové rezistence, nadměrného množství viscerálního tuku, zvýšené hladiny triglyceridů se současným snížením hladiny HDL cholesterolu spolu se zvýšením krevního tlaku u jediného pacienta ve formě metabolického syndromu. Prevalence tohoto syndromu v zemích se „západním" životním stylem dosahuje desítek procent dospělé populace a představuje tak bezpochyby jeden z nejzávažnějších zdravotnických problémů počátku 21. století. Patogeneze samotného metabolického syndromu (stejně jako jeho jednotlivých komponent) je multifaktoriální s přibližně stejně silnými složkami prostředí a genetické predispozice. To mj. znamená, že jak vznik, tak i prevence a terapie těchto komplexních onemocnění jsou do značné míry ovlivnitelné životosprávou, tedy především dietou a fyzickou aktivitou. Tato intervence ovšem nemusí vést k dostatečné úpravě pacientova stavu, ať už z důvodu omezené compliance s indikovanými změnami životosprávy nebo u jedinců s výraznější genetickou komponentou syndromu. Proto je nedílnou součástí léčby metabolického syndromu farmakoterapie. Významného uplatnění se v této oblasti dosud dostalo agonistům nukleárních receptorů PPAR (viz níže), především díky hypolipidemickým účinkům fibrátů a inzulinsenzitizujícím efektům thiazolidindionů. V současné době probíhají pokusy uvést do klinické praxe novou třídu látek, tzv. glitazarů, které by měly kombinovat oba typy účinků a současně postrádat některé nežádoucí účinky doposud užívaných agonistů PPAR.
Polyfarmakologie
Převládající filozofií vývoje většiny nových léčiv je i v současnosti redukcionistický přístup charakterizovaný mottem „jedna cílová struktura, jedna nemoc". Tato strategie se bezpochyby osvědčila ve formě mnoha účinných léčiv, nicméně pravděpodobně se stane neudržitelnou v konfrontaci s nastupující pandemií metabolického syndromu. Než bude možné v běžné praxi realizovat principy skutečně individualizované medicíny, tedy indikovat preventivní a léčebné postupy na základě znalosti farmakogenetického a případně nutrigenetického profilu pacienta (viz níže), určitou naději dávají právě principy polyfarmakologie, tedy vývoje látek současně ovlivňujících několik cílových struktur. Polyfarmakologická praxe v současnosti zahrnuje především podávání tzv. koktejlů léčiv (drug cocktail), tedy kombinace podávání několika tablet, z nichž každá obsahuje jednu účinnou látku. Výhody této formy farmakoterapie jsou často kompromitovány špatnou compliance pacienta. V současnosti probíhá intenzivní vývoj variantních přístupů – prvním je vývoj multikomponentních přípravků, které kombinují dvě a více účinných látek v jedné tabletě. Příkladem multikomponentních léčiv jsou nedávno uvedené přípravky Vytorin kombinující ezetimib a simvastatin nebo Caudet kombinující amlodipin s atorvastatinem. Existuje však řada důvodů, proč se tento přístup pravděpodobně nestane v budoucnosti majoritním. Předně – rozdíly v individuální odpovědi pacientů na jednotlivé složky kombinovaného přípravku ústí v komplikované farmakokinetické a farmakodynamické profily takového léku a fixní kombinace dávek postrádá flexibilitu, která je dostupná v „tradičním" postupu. Pokud se navíc jedná o multikomponentní přípravek složený z generických léčiv, nelze opomenout také aspekty farmakoekonomické. Jako perspektivní se proto jeví vývoj látek, které současně ovlivňují několik cílových struktur (multiple-ligand). Ačkoli je u takových látek samozřejmě velmi složité „nastavit" účinnost pro jednotlivé cíle, např. právě jednotlivé subtypy PPAR, probíhá tato kritická fáze v mnohem časnějších (a také méně finančně náročných) fázích procesu vývoje léčiva.
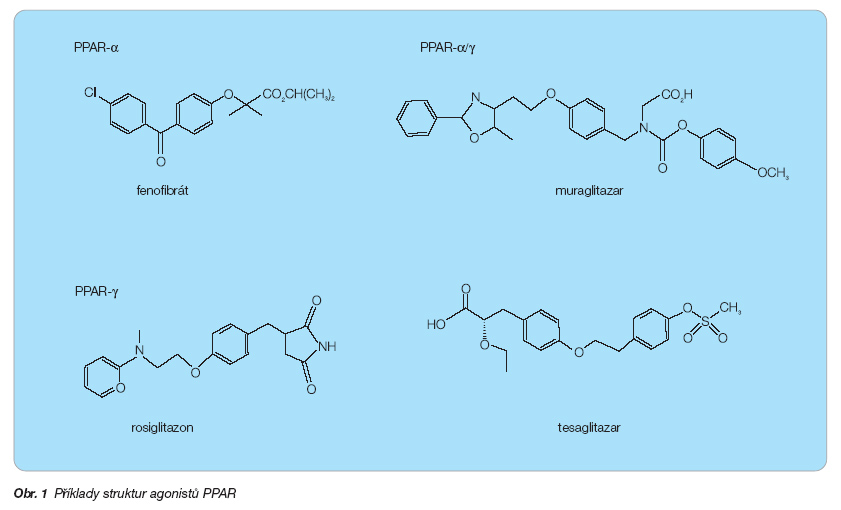
Mezi nadějné cílové struktury pro léčbu metabolických a hemodynamických poruch vyskytujících se buďto samostatně, nebo jako součást metabolického syndromu patří skupina receptorů aktivovaných proliferátory peroxizomů (PPAR z anglického peroxisome proliferator-activated receptors) (obr. 1).
První PPAR byl objeven v roce 1990, od té doby počet jim věnovaných prací exponenciálně roste, každoročně je např. pořádán mezinárodní kongres o PPAR a minulý rok byla tematika PPAR monograficky zpracována v češtině [3]. V současnosti je již nezpochybnitelná role PPAR ve fyziologii a patofyziologii tak rozmanitých procesů, jako je metabolismus lipidů a sacharidů, buněčná diferenciace, kancerogeneze nebo zánětlivá odpověď, nicméně ohledně detailních mechanismů jejich působení zůstává ještě mnoho otázek nezodpovězeno. PPAR jsou v současnosti pojímány jako jakési koordinační uzly signalizačních a metabolických drah, jejichž narušení se projeví ve formě výše zmíněných „civilizačních" onemocnění (obezita, dyslipidémie, ateroskleróza, hypertenze a další). To samozřejmě vedlo a vede k pokusům o terapeutické ovlivnění zmíněných onemocnění pomocí modulace PPAR. Ačkoli např. užití fibrátů jako hypolipidemik předcházelo o mnoho let objevu PPAR jako cílových struktur jejich účinku, v poslední době jsme svědky cíleného vývoje agonistů PPAR s definovaným působením na jednotlivé subtypy PPAR, případně na jejich kombinace (duální agonisté, panagonisté PPAR).
Základní charakteristika PPAR
PPAR patří mezi ligandem aktivované transkripční faktory z rodiny nukleárních receptorů společně s receptorem pro vitamin D, steroidními hormony nebo retinoidy. Dosud identifikovaní tři zástupci PPAR tvoří třídu C oficiální klasifikace nukleárních receptorů (NRC-1-NRC-3), běžně se však pro ně užívají názvy PPAR-a, PPAR-b (synonymně PPAR-d) a PPAR-g. Jsou kódovány odlišnými geny, jejichž značná podobnost nejen u člověka, ale i u jiných živočišných druhů naznačuje společný evoluční původ z jediného „ancestrálního" genu. Savcům jsou navíc společné dvě izoformy PPAR-g, které vznikají alternativním sestřihem primárního transkriptu. U člověka se kromě těchto dvou izoforem (PPAR-g1 a PPAR-g2) vyskytuje ještě varianta třetí, která je na úrovni proteinu ovšem identická s PPAR-g1.
Jednotlivé izoformy vykazují specifickou tkáňovou distribuci, kdy PPAR-g2 a PPAR-g3 jsou exprimovány především v bílé tukové tkáni, zatímco exprese PPAR-g1 je ubikviterní. PPAR-a je exprimován především v játrech, dále v srdci a kosterním svalstvu.
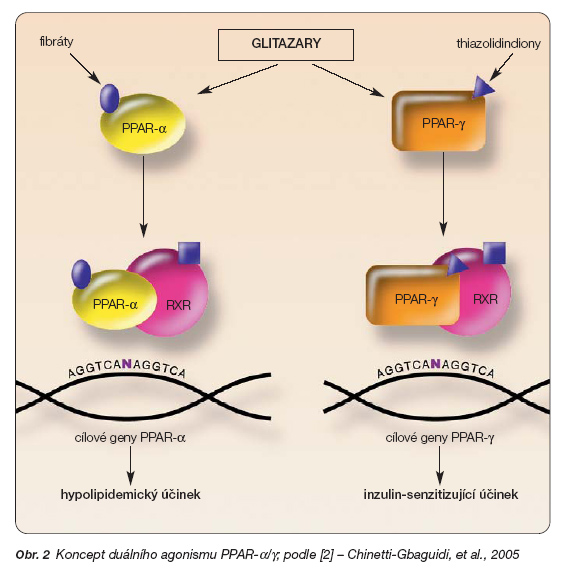
Stejně jako ostatní nukleární receptory sestávají proteiny PPAR z několika domén se specializovanými funkcemi. Zvláštní význam má především DNA-vázající doména, která je důležitá pro ovlivnění exprese PPAR-responzivních genů, a ligand-vázající doména, která zprostředkovává kromě samotné vazby ligandu i heterodimerizaci PPAR s ostatními nukleárními receptory. Zde je vhodné poznamenat, že kromě syntetických léčiv jsou PPAR přirozeně aktivovány celou řadou endogenních látek (nasycené a nenasycené mastné kyseliny, eikosanoidy, prostaglandiny). Na aktivaci PPAR navazuje vytvoření heterodimeru s jiným nukleárním receptorem, RXR (retinoid X receptor). Celý komplex PPAR:RXR se potom váže na specifická místa DNA, kde rozeznává specifické sekvence označované jako PPRE (peroxisome proliferator responsive elements) – jedná se o opakování motivu AGGTCA odděleného jedním nebo dvěma nukleotidy. Vazba na PPRE v promotorech genů regulovaných PPAR zprostředkovává signál, který vede k zahájení přepisu těchto genů a tím k aktivaci jejich produktů. Ačkoli je tato cesta aktivace PPAR jistě majoritní, není rozhodně jediná. PPAR mohou být aktivovány např. fosforylací N-terminální oblasti, která obsahuje tzv. ligand-independentní aktivační doménu. Rovněž ligandy RXR jsou schopné aktivovat PPAR:RXR heterodimer.
Od fibrátů ke glitazarům
Nejen u pacientů s metabolickým syndromem, ale např. i u diabetiků často nacházíme kombinaci inzulinové rezistence s dyslipidémií. Předpokládá se, že hyperglykémie se podílí na mikroangiopatických komplikacích diabetu (periferní neuropatie, retinopatie, selhání ledvin). Nicméně hlavní příčinou mortality jsou u diabetiků spíše makrovaskulární změny spojené s aterosklerózou a jejími následky. Zde hraje významnější roli diabetická dyslipidémie. Nyní již běžně užívané thiazolidindiony (rosiglitazon, pioglitazon) jsou specifickými agonisty PPAR-g a vykazují velmi razantní inzulin-senzitizující efekt, jehož přesná molekulární podstata není ještě zcela vysvětlena. Na druhou stranu thiazolidindiony téměř zcela postrádají účinky na hladiny lipidů, jak ukázala např. analýza 19 randomizovaných dvojitě zaslepených studií s rosiglitazonem nebo pioglitazonem. Na druhé straně stojí fibráty, jejichž významný hypolipidemický účinek (snížení triglyceridémie, zvýšení HDL cholesterolu) je připisován aktivaci PPAR-a. Specifita fibrátů není zdaleka tak vyhraněná jako u thiazolidindionů – fenofibrát je aktivátorem PPAR-a i PPAR-g, ovšem s desetinásobně vyšší afinitou k prvnímu z nich, bezafibrát je zhruba stejně potentním ligandem pro všechny tři podtypy PPAR. Oproti prokázané účinnosti agonistů PPAR-a na parametry lipidového metabolismu je jejich efekt na inzulinovou senzitivitu spíše ambivalentní (blíže [3]). Z těchto pozorování vyplynula hypotéza, že pokud by bylo možné cíleně syntetizovat látky s definovanou afinitou současně k PPAR-a i PPAR-g, mohly by působit současně jako antidiabetika a hypolipidemika (obr. 2).
Během minulých let byla připravena řada duálních agonistů PPAR-a/g, které se nacházejí v různých fázích klinického testování. Jsou mezi nimi rovněž zástupci thiazolidindionové skupiny (TZD-18, MK-767). Tyto preparáty v preklinických fázích zkoušek výrazně snížily u savčích modelů diabetu 2. typu jak hyperglykémii, tak zvýšené hladiny lipidů. Podobně příznivý účinek byl pozorován po podání nethiazolidindionových duálních agonistů (glitazarů), mezi které patří např. farglitazar, ragaglitazar, muraglitazar, tesaglitazar a další. Jako příklad lze uvést ragaglitazar, který ve druhé fázi klinických zkoušek snižoval u pacientů s diabetem 2. typu hladiny hemoglobinu A1c, triglyceridů, volných mastných kyselin a celkového cholesterolu a současně zvýšil koncentraci HDL cholesterolu. Bohužel všechny klinické zkoušky ragaglitazaru byly v nedávné době zastaveny, případně odloženy, neboť u myší a potkanů jím léčených docházelo k časté incidenci nádorů močového měchýře. To nás přivádí k zásadní otázce obecně platné pro všechny (duální) agonisty PPAR, jež se týká bezpečnosti jejich podávání. Kromě fibrátů nejsou u agonistů PPAR k dispozici skutečně dlouhodobá data. První ze skupiny thiazolidindionů troglitazon byl z trhu stažen kvůli desítkám případů jaterního selhání a nahrazen bezpečnějším rosiglitazonem a pioglitazonem, a již čtyři duální agonisté neprošly klinickým testováním z důvodů významné toxicity. Jedná se o ragaglitazar, farglitazar, MK-767 and TAK-559. I proto vydal americký úřad FDA (Food and Drug Administration) pokyny, které podmiňují jakoukoli klinickou zkoušku agonistů PPAR delší než půl roku předchozím minimálně dvouletým testováním kancerogenity u hlodavců. Pouze tesaglitazar a muraglitazar se dostaly do třetí fáze klinických zkoušek; nicméně druhý z nich za poněkud dramatických okolností (viz níže) nakonec nebyl schválen pro klinické použití. Vzhledem k nedávno zjištěnému významu třetího receptoru ze skupiny PPAR (PPAR-b/d) v metabolismu lipidů jsou na počátku i zkoušky panagonistů PPAR (PPAR-a/b/g), ale i zde bude jistě velká pozornost věnována bezpečnostnímu profilu těchto látek.
Kauza muraglitazar
Muraglitazar byl doposud vnímán jako jeden z nejnadějnějších glitazarů společně s tesaglitazarem. Jeho podávání bylo u různých experimentálních modelů spojeno s výraznými antidiabetickými a hypolipidemickými účinky, kdy kromě úpravy inzulinové senzitivity docházelo k současnému snížení koncentrací triglyceridů, volných mastných kyselin i cholesterolu. Jediná klinická studie publikovaná před povolovacím řízením FDA sice v zásadě potvrzovala výsledky z experimentu, ovšem s nezanedbatelnou frekvencí nežádoucích účinků známých z terapie thiazolidindiony – retence tekutin a zvýšení tělesné hmotnosti. Jako první duální agonista PPAR-a/g byl postoupen muraglitazar 9. září 2005 poradní komisi FDA, která téhož dne muraglitazar doporučuje jak v monoterapii, tak v kombinaci s metforminem. Zhruba o měsíc později, 18. října, vychází v elektronické podobě časopisu JAMA článek Nissena a kol. [4], který na základě analýzy dat zpřístupněných v rámci zářijového veřejného jednání FDA upozorňuje na vyplývající vysoké relativní riziko kardiovaskulárních komplikací léčby muraglitazarem spojené s vyšší morbiditou a mortalitou ve srovnání s placebem i pioglitazonem. FDA reaguje pozastavením schvalovacího řízení a požadavkem na robustnější data o bezpečnosti z déle trvajících studií nejen u muraglitazaru, ale i u ostatních duálních agonistů PPAR-a/g. Obě dotčené farmaceutické společnosti oznamují zrušení marketingové smlouvy a uvažují o ukončení dalšího vývoje muraglitazaru.
Farmakogenomika jako východisko?
Současný stav v oblasti glitazarů a jejich potenciálního klinického využití je tedy charakterizován určitou skepsí vůči brzkému zavedení této původně velmi nadějné skupiny duálních agonistů PPAR do klinické praxe. Toto se pravděpodobně nezmění, pokud výrobci léčiv nesleví ze strategie „léku pro všechny" a nezakomponují do procesu klinického testování aktivní komponentu farmakogenomické analýzy. U těch preparátů, které vykazují účinnost jen u určité skupiny léčených a v celkovém srovnání s placebem je výsledek ambivalentní, vyžaduje pokračování studií značné investice a mnohdy je celý vývoj právě zde ukončen (jako v případě některých glitazarů). Genetické profilování by mohlo identifikovat charakteristiky skupiny, u níž se dostavuje požadovaný efekt léčiva, a v případě potvrzení účinnosti v dalších fázích klinického testování by mohla být pozitivita v předběžném (prediktivním) genetickém testu podmínkou aplikace daného léčiva. Opačným pólem téhož je identifikace genetického markeru (konkrétní alely, haplotypu, transkripčního profilu), který je asociován s nežádoucím účinkem léčiva. Ačkoli již existují ojedinělé příklady takových léků, proces přechodu od globálně aplikovaných „léků na danou nemoc" k „lékům pro konkrétního pacienta" v rámci individualizované medicíny bude patrně jen velmi pozvolný.
Seznam použité literatury
- [1] Berger JP, Akiyama TE, Meinke PT. PPARs: therapeutic targets for metabolic disease. Trends Pharmacol Sci 2005; 26: 244–251.
- [2] Chinetti-Gbaguidi G, Fruchart JC, Staels B. Role of the PPAR family of nuclear receptors in the regulation of metabolic and cardiovascular homeostasis: new approaches to therapy. Current Opinion in Pharmacology 2005; 5: 177–183.
- [3] Haluzík M, Svačina Š. Metabolický syndrom a nukleární receptory PPAR. Praha, Grada Publishing, 2005.
- [4] Nissen SE, Wolski K, Topol EJ. Effect Muraglitazar on Death and Major Adverse Cardiovascular Events in Patients With Type 2 Diabetes Mellitus. JAMA 2005; 294: 2581–2586.
- [5] Šeda O, Šedová L. PPARs: molecular targets in the pharmacogenomics era. Prague Med Rep 2004; 105: 223–236.
- [6] Šeda O, Šedová L. Farmakogenomika a nutrigenomika: komplexní interakce genů s prostředím. Klin Farmakol Farm 2005; 19: 46–50.
- [7] Šeda O, Tremblay J, Šedová L, Hamet P. Integrating genomics and transcriptomics with geoethnics and environment in resolution of complex cardiovascular diseases. Curr Opin Mol Ther 2005; 7: 583–587.
- [8] Šedová L, Šeda O. Nutriční genomika. Čas Lék Čes 2004; 143: 676–678.
- [9] Šeda O. Genetika diabetu. In: Perušičová (ed).: Diabetologie 2005. Praha, Triton, 2005.