Léčba natriuretickými peptidy – konec mýtu?
Článek podává přehled natriuretických peptidů a jejich působení za patologických stavů. Je popsán účinek a klinické použití nesiritidu – lidského rekombinantního hormonu (hBNP), který je identický s endogenně produkovaným natriuretickým peptidem typu B (BNP). V části věnované léčebnému užití jsou zmíněny také inhibitory endopeptidáz, které brání rozpadu natriuretických peptidů, jmenovitě omapatrilát.
Historie natriuretických peptidů sahá do roku 1981, kdy byl popsán extrakt ze srdečních síní, který způsobuje natriurézu a vazodilataci. V myokardu se tvoří ANP (síňový natriuretický peptid), převážně v komorách vzniká BNP (mozkový natriuretický peptid*). Do skupiny natriuretických peptidů zařazujeme ještě další látky: CNP (natriuretický 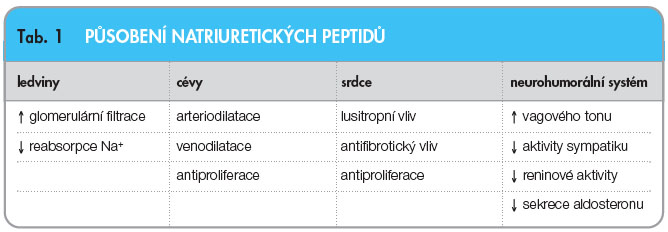 peptid typu C) je tvořen v endotelu cév, DNP (natriuretický peptid typu D) vzniká v mozkové tkáni a urodilatin v buňkách distálního tubulu ledvin [1–3]. Účinky natriuretických peptidů v jednotlivých tkáních uvádí tab. 1.
peptid typu C) je tvořen v endotelu cév, DNP (natriuretický peptid typu D) vzniká v mozkové tkáni a urodilatin v buňkách distálního tubulu ledvin [1–3]. Účinky natriuretických peptidů v jednotlivých tkáních uvádí tab. 1.
Pro vazbu natriuretických peptidů existují tři typy receptorů, které se liší v afinitě k jednotlivým peptidům. Receptor A (NPR-A) má větší afinitu pro ANP a BNP, zatímco receptor NPR-B je více specifický pro CNP. Třetí receptor – NPR-C – slouží spíše pro clearance peptidů. Vlastní degradace je uskutečněna enzymem neutrální endopeptidázou [4].
Léčebné možnosti použití natriuretických peptidů a inhibitorů endopeptidáz
V terapii jsou využívány následující přístupy:
- podávání humánních natriuretických peptidů typu BNP – nesiritidu a ularitidu;
- zábrana proti odbourávání natriuretických peptidů podáním inhibitorů neutrálních endopeptidáz – kandoxatrilu – nebo duálních inhibitorů vazopeptidáz a angiotenzin konvertujícího enzymu – omapatrilátu.
1. Podávání natriuretických peptidů
V léčbě srdečního selhání se podávání ANP prakticky nevyužívá. Zatím existují data pro podávání BNP, a to nesiritidu, lidského rekombinantního hormonu (hBNP), který je identický s endogenně produkovaným BNP, a ularitidu, syntetické formy urodilatinu. Zlepšení hemodynamiky a zmírnění dušnosti bez zhoršení renálních funkcí při podání ularitidu u pacientů s akutní dekompenzací srdečního selhání prokázala studie SIRIUS II [5].
Ve studii NATRECOR byl nesiritid podáván zejména pacientům s těžším srdečním selháním – převládala klasifikace NYHA III a IV s ejekční frakcí nižší než 35 %. Po léčbě došlo k hemodynamickému zlepšení – ke snížení tlaku v zaklínění, snížení centrálního žilního tlaku, systémové vaskulární rezistence a ke zvýšení indexu srdečního výdeje [6].
Ve studii NESIRITIDE Study Group se 127 pacienty se symptomatickým srdečním selháním, s tlakem v zaklínění více než 18 mm Hg a srdečním indexem nižším než 2,7 l/m2 byl podáván hBNP ve dvou dávkách, nebo placebo ke standardní terapii. Při léčbě oběma dávkami BNP došlo ke snížení tlaku v zaklínění a ke zlepšení klinického stavu: snížení dušnosti a slabosti [7].
Ve srovnávacích studiích testujících nesiritid vůči dobutaminu u pacientů s akutně dekompenzovaným srdečním selháním byl u nesiritidu zaznamenán nižší počet rehospitalizací a kratší doba léčby a po nižší dávce nesiritidu byla zjištěna ve srovnání s dobutaminem nižší 6měsíční mortalita [8–10].
PRECEDENT, další studie srovnávající dobutamin a nesiritid, se zabývala rizikem vzniku arytmií. Rovněž v této práci bylo méně arytmií pozorováno po podání nesiritidu [11].
Studie VMAC (Vasodilatation in the Management of Acute Congestive Heart Failure) u 489 nemocných s dekompenzovaným srdečním selháním srovnávala nesiritid, nitrožilní nitroglycerin a placebo. Při podání nesiritidu došlo k výraznějšímu poklesu středního tlaku v zaklínění ve srovnání s nitroglycerinem ve 3. a 24. hodině. Zmírnění dušnosti bylo obdobné po podání nesiritidu i nitroglycerinu, ale nebylo pozorováno po placebu. Vzhledem k tomu, že ve studii VMAC byla užita nižší dávka nesiritidu, objevila se symptomatická hypotenze pouze v 5 %, obdobně jako po nitroglycerinu [12].
Na základě těchto pozitivních výsledků byl nesiritid schválen FDA v červenci 2001 jako účinná terapie pro pacienty s akutně dekompenzovaným srdečním selháním, ale jeho úloha by měla být ještě prokázána dalšími studiemi.
Podání nesiritidu v sérii infuzí u pacientů se srdečním selháním hodnotila studie FUSION (Follow-Up Serial Infusions of Nesiritide) I a II.
FUSION I byla pilotní studie, která zahrnula 210 pacientů s dekompenzací srdečního selhání. Studie byla randomizovaná, multicentrická a otevřená. Pacienti dostávali buď standardní léčbu srdečního selhání, nebo navíc infuzi nesiritidu každý týden po dobu 12 týdnů a další 4 týdny byli ještě sledováni. Při hodnocení celého souboru nebyl zjištěn rozdíl ve zlepšení kvality života a ve výskytu nežádoucích účinků. Avšak skupina pacientů definovaná přítomností 4 nebo více rizikových faktorů z možných sedmi (zvýšená hladina kreatininu, NYHA IV v posledních 60 dnech, věk více než 65 let, anamnéza setrvalé komorové tachykardie, ischemická choroba srdeční, diabetes mellitus či užívání pozitivně inotropních látek) měla signifikantně významný prospěch z podávání nesiritidu. Léčba zlepšila kombinovaný parametr přežívání a absence hospitalizace u pacientů, kteří dostávali nesiritid (p < 0,027) [13].
Navazující studie FUSION II byla randomizovaná, dvojitě slepá, multicentrická a prospektivní. Způsob podávání nesiritidu oproti standardní medikaci a placebu byl stejný jako ve studii FUSION I. V rámci vstupních kritérií měli pacienti v anamnéze dvě nedávné hospitalizace pro srdeční selhání, ejekční frakci nižší než 40 %, symptomy NYHA IV nebo NYHA III se současnou renální insuficiencí definovanou clearance kreatininu nižší než 60 ml/min. Primárním cílem byla celková mortalita nebo kardiovaskulární nebo renální hospitalizace za 12 týdnů. Do studie vstoupilo 911 pacientů. Primárního cíle dosáhlo 36,8 % léčených placebem a 36,7 % léčených nesiritidem (p < 0,79).
Nebyl nalezen rozdíl v žádném sekundárním cíli ani v kvalitě života. Naopak pacienti léčení nesiritidem měli větší výskyt hypotenze. Studie tak přinesla zklamání a poznatek, že opakované infuzní podání nesiritidu nepřináší pacientům se srdečním selháním žádný prospěch [14].
Při provedení metaanalýzy studií sledujících podávání nesiritidu u pacientů s dekompenzací srdečního selhání bylo dokonce zjištěno zhoršení renálních funkcí ve skupině léčených nesiritidem, ať již v porovnání s placebem, či s léčbou pozitivně inotropními látkami [15].
Na kongresu American Heart Association v Chicagu v listopadu 2010 prezentoval v rámci sekce Hot Lines konečné výsledky studie ASCEND-HF doktor Adrian F. Hernandes z Durhamu, tzv. diskusantem byl profesor E. Braunwald z Harvardské univerzity v Bostonu. Výsledky teprve budou publikovány.
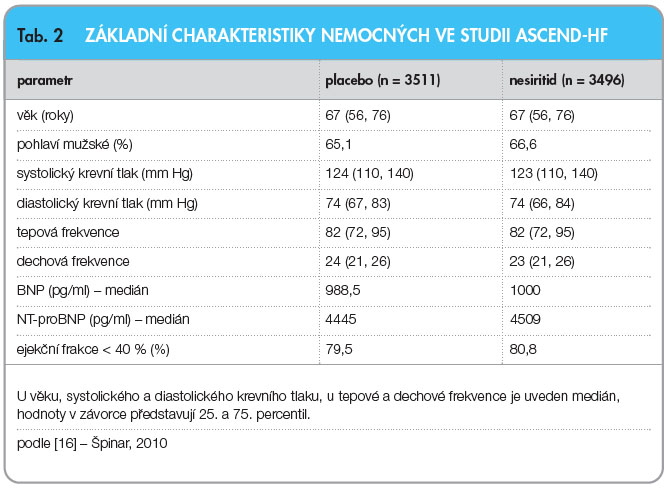 Studie ASCEND-HF (Acute Study of Clinical Effectiveness of Nesiritide in Decompensated Heart Failure) zařadila 7007 nemocných s akutním srdečním selháním, kteří museli být randomizováni do 24 hodin od vzniku příznaků, a ke standardní léčbě byl přidán nesiritid, nebo placebo na dobu 24–168 hodin. Základní charakteristiky pacientů ukazuje tab. 2.
Studie ASCEND-HF (Acute Study of Clinical Effectiveness of Nesiritide in Decompensated Heart Failure) zařadila 7007 nemocných s akutním srdečním selháním, kteří museli být randomizováni do 24 hodin od vzniku příznaků, a ke standardní léčbě byl přidán nesiritid, nebo placebo na dobu 24–168 hodin. Základní charakteristiky pacientů ukazuje tab. 2.
Primárním cílem bylo:
- posouzení dušnosti na 7stupňové škále za 6 a 24 hodin,
-
 30denní mortalita a 30denní rehospitalizace pro srdeční selhání.
30denní mortalita a 30denní rehospitalizace pro srdeční selhání.
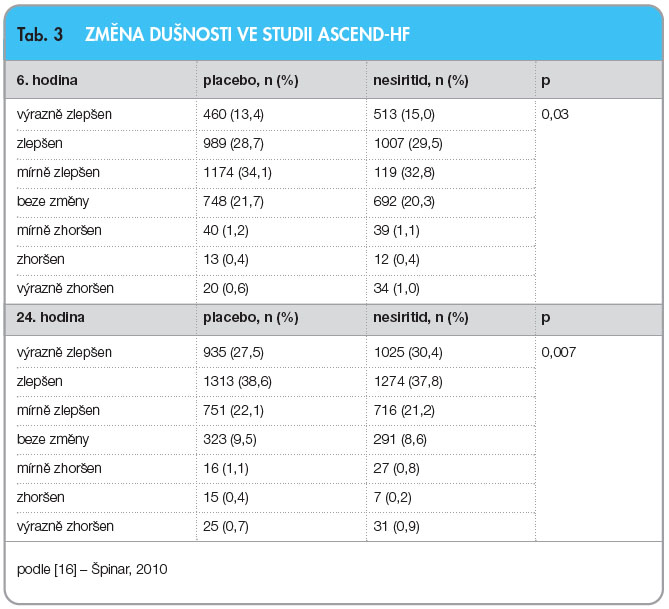
Změny dušnosti po 6 a 24 hodinách ukazuje tab. 3. Z pohledu tohoto primárního cíle bylo dosaženo pozitivního výsledku, protože statisticky významně více nemocných se zlepšilo při podávání nesiritidu ve srovnání s podáváním placeba. Druhý primární cíl, kterým byla 30denní mortalita a 30denní rehospitalizace, ukazujetab. 4. V hodnocení tohoto kombinovaného parametru se ukázal statisticky nevýznamný trend ve prospěch nesiritidu.
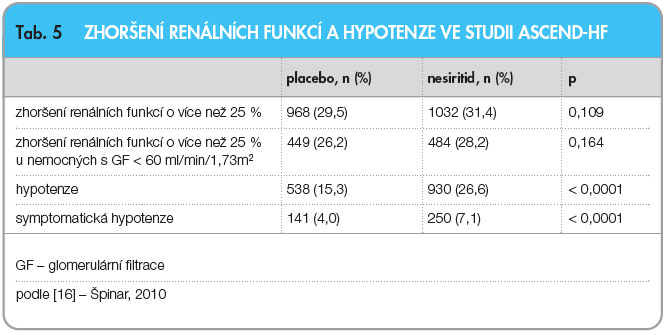
Velká pozornost byla věnována bezpečnosti podávání nesiritidu, 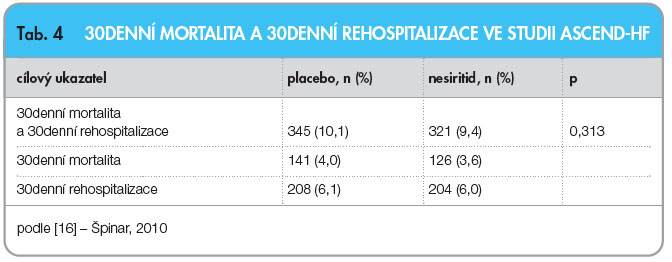 především výskytu zhoršení renálních funkcí a hypotenze. Z tab. 5 je patrné, že nebyl potvrzen negativní vliv nesiritidu na renální funkce a že z tohoto pohledu byl nesiritid bezpečný, a to dokonce rovněž u nemocných s úvodně sníženou glomerulární filtrací. Naopak výskyt hypotenze, a to jak symptomatické, tak asymptomatické, byl po léčbě nesiritidem téměř dvojnásobný.
především výskytu zhoršení renálních funkcí a hypotenze. Z tab. 5 je patrné, že nebyl potvrzen negativní vliv nesiritidu na renální funkce a že z tohoto pohledu byl nesiritid bezpečný, a to dokonce rovněž u nemocných s úvodně sníženou glomerulární filtrací. Naopak výskyt hypotenze, a to jak symptomatické, tak asymptomatické, byl po léčbě nesiritidem téměř dvojnásobný.
 Z dalších závažných vedlejších příhod je třeba zmínit dvojnásobný výskyt reinfarktu při léčbě nesiritidem (14 vs. 6 případů), který ale nedosáhl statistické významnosti. Tzv. Steering committee pak navrhla tyto závěry:
Z dalších závažných vedlejších příhod je třeba zmínit dvojnásobný výskyt reinfarktu při léčbě nesiritidem (14 vs. 6 případů), který ale nedosáhl statistické významnosti. Tzv. Steering committee pak navrhla tyto závěry:
- Nesiritid nesnižuje 30denní rehospitalizace.
- Nesiritid nesnižuje 30denní mortalitu.
- Nesiritid zmírňuje dušnost po 6 a 24 hodinách.
- Nesiritid nezhoršuje renální funkce do 30 dní [16].
2. Zábrana proti degradaci natriuretických peptidů
Ve větším měřítku byl zkoušen duální inhibitor endopeptidáz – angiotenzin konvertujícího enzymu (ACE) a neutrálních endopeptidáz – omapatrilát, který brání přeměně angiotenzinu I na angiotenzin II a dále brání rozpadu natriuretických peptidů. Experimentální farmakologické pokusy a pilotní klinické studie vedly k optimistickým předpokladům, že omapatrilát bude účinnější než inhibitory ACE samotné v léčbě hypertenze a srdečního selhání [17].
Studie IMPRESS sledovala pacienty se symptomatickým srdečním selháním a jejich klinický vývoj při podání 20 mg lisinoprilu, nebo 40 mg omapatrilátu denně. Omapatrilát vedl ke zlepšení klinického stavu pacientů, méně jich bylo po léčbě ve třídě NYHA III a IV, a dokonce statisticky významně ovlivnil kombinovaný ukazatel mortality a morbidity [18].
Na základě těchto povzbudivých výsledků byla naplánována studie OVERTURE, která dlouhodobě sledovala u 5770 nemocných se srdečním selháním NYHA II–IV léčbu omapatrilátem podávaným v dávce 40 mg jednou denně oproti léčbě enalaprilem v dávce 2krát denně 10 mg u pacientů se symptomatickým srdečním selháním a ejekční frakcí levé komory 30 % a méně. Primární cíl (úmrtí nebo hospitalizace pro zhoršené srdeční selhání vyžadující nitrožilní léčbu) byl v obou léčebných skupinách obdobný. Pro farmaceutický průmysl byl neutrální výsledek zklamáním jak v primárním cíli (úmrtí nebo hospitalizace pro srdeční selhání), tak v sekundárním cíli (mortalita ze všech příčin) [19].
A konečně ve studii OCTAVE bylo zařazeno přes 25 000 hypertoniků a opět dostávali omapatrilát, nebo enalapril. Co se týče snížení krevního tlaku, byl omapatrilát účinnější než enalapril. Po podávání omatrilátu se však ve 2,2 % případů vyskytl angioedém ve srovnání s 0,7 % případů po léčbě enalaprilem [20].
Závěr
V současnosti je z natriuretických peptidů využíván nejvíce BNP. Nesiritid je lék bezpečný, ale bez prokázaného klinického efektu na rehospitalizace a mortalitu. Léčba akutního srdečního selhání tak zůstává nadále empirickou, bez průkazných dat a s nutností věnovat se nejen tzv. tvrdým cílům, ale i náhradním cílům, jako je úleva nemocného, snížení symptomatologie atd. Výsledky studie ASCEND-HF potvrzují nutnost klinického myšlení u akutního srdečního selhání a zařazují nesiritid k lékům, jako je levosimendan či tolvaptan, kde ošetřující lékař pozoruje klinické zlepšení při podávání daného léku, ale velké klinické studie (REVIVE, SURVIVE či EVEREST) nepotvrdily zlepšení prognózy – mortality a rehospitalizací.
Není však ještě jasná pozice nesiritidu ve vztahu k ostatním lékům, jako jsou diuretika, nitráty, dobutamin či vápníkové senzitizéry. Je třeba více informací o morbiditě a dlouhodobé mortalitě, a právě tyto údaje by měly přinést probíhající studie.
Práce byla podpořena VZ MŠMT 002 162 2402.
*Substance je nazývána mozkovým natriuretickým peptidem, protože byla původně izolována z mozku prasete.
Seznam použité literatury
- [1] Wei CM, Heublein DM, Perella MA, et al. Natriuretic peptide system in human heart failure. Circulation 1993; 88: 1004–1010.
- [2] Sudoh T, Kangawa K, Minamino N, et al. A natriuretic peptide in porcine brain. Nature 1988; 332: 78–81.
- [3] Sudok T, Minamino N, Kangawa K, et al. C-type natriuretic peptide (CNP): a new member of natriuretic peptide family indetified in porcine brain. Biochem Biophys Res Commun 1990; 168: 863–870.
- [4] Špinarová L, Toman J. Humorální změny u chronického srdečního selhání. Cor Vasa 2001; 43: 513–519.
- [5] Mitrovic V, Seferovic P, Simeunovic D, et al. Haemodynamic and clinical effects of ularitide in decompensated heart failure. Eur Heart J 2006; 27: 2823–2832.
- [6] Mills RM, LeJemtel TH, Horton DP, et al. Sustained hemodynamic effects of an infusion of nesiritide (human B-type natriuretic peptide) in heart failure. A randomized, double-blind, placebo-controlled clinical trial. NATRECOR Study Group. J Am Coll Cardiol 1999; 34: 155–162.
- [7] Colluci WS, Elkayem U, Horton DP, et al. Intravenous nesiritide, a natriuretic peptide, in the treatment of decompensated congestive heart failure. NESIRITIDE Study Group. N Engl J Med 2000; 343: 246–253.
- [8] Burger A, Johnson A, Horton D. Effect of nesiritide versus dobutamine for treatment of acutely decompensated heart failure on cardiovascular adverse events. J Card Fail 1998; 4: 40.
- [9] Silver MA, Ghali JK, Horton DP, Elkayam U. Effect of nesiritide versus dobutamine on short-term outcomes in the treatment of acutely decompensated heart failure. J Am Coll Cardiol 2002: 39; 798–803.
- [10] Elkayam U, Silver MA, Burger AJ, Horton DP. The effect of short-term therapy with nesiritide (B-type natriuretic peptide) or dobutamine on long term survival. J Card Fail 2000; 6: 45.
- [11] Burger AJ, Horton DP, Lejemtel T, et al. Effect of nesiritide and dobutamine on ventricular arrhytmias in the treatment of patients with acutely decompensated congestive heart failure: The PRECEDENT study. Am Heart J 2002; 144: 1102–1108.
- [12] The VMAC Investigators. Intravenous nesiritide vs nitroglycerin for treatment of decompesated congestive heart failure. JAMA 2002; 1531–1540.
- [13] Yancy CW, Saltzberg MT, Berkowitz RL, et al. Safety and feasibility of using serial infusions of nesiritide for heart failure in an outpatient setting (from the FUSION Trial). Am J Cardiol 2004; 94: 595–601.
- [14] Yancy CW, Krum H, Massie BM, et al. Safety and efficacy of outpatient nesiritide in patiens with advanced heart failure. Results of the second Follow-Up Serial Infusions of Nesiritide (FUSION II) Trial. Circ Heart Fail 2008; 1: 9–16.
- [15] Sackner-Bernstein JD, Skopicki HA, Aaronson KD. Risk of worsening renal function with nesiritide in patients with acutely decompensated heart failure. Circulation 2005; 111: 1487–1491.
- [16] Špinar J. Nesiritide not verified. Cor Vasa 2010; 52: 764–765.
- [17] Horký K. Duální inhibitory endopeptidáz – nový směr ve vývoji antihypertenziv. Vnitř Lék 2000; 46: 148–151.
- [18] Rouleau JL, Pfeffer MA, Stewart DJ, et al. Comparison of vasopeptidase inhibitor, omapatrilat, and lisinopril on exercise tolerance and morbidity in patients with heart failure: IMPRESS randomised trial. Lancet 2000; 356: 615–620.
- [19] Packer M, Calliff RM, Konstam MA, et al. Comparison of omapatrilat and enalapril in patients with chronic heart failure. Circulation 2002; 106: 920–926.
- [20] de Lemos JA, McGuire DK, Drazner MH. B-type natriuretic peptide in cardiovascular disease. Lancet 2003; 362: 1–7.