Mepolizumab v léčbě plicních eozinofilií
Souhrn:
Mepolizumab je humanizovaná monoklonální protilátka proti interleukinu 5, která je slibným léčivem v terapii eozinofilních syndromů. Eozinofilní syndromy jsou buď primární, klonální nebo idiopatické, anebo sekundární v rámci jiných nemocí nebo indukované klonální expanzí. Mepolizumab představuje cílenou léčbu, která je výhodnou alternativou doposud užívané léčby, kdy zejména u eozinofilního astmatu a idiopatického hypereozinofilního syndromu umožňuje dosáhnout kontroly nemoci bez nežádoucích příznaků spojených s léčbou kortikosteroidy a imunosupresivy.
Key words: mepolizumab – interleukin‑5 – lung eosinophilia – targeted treatment.
Summary:
Mepolizumab, humanized monoclonal antibody against interleukin‑5, is a promising drug for the treatment of eosinophilic syndromes. Eosinophilic syndromes are either primary, clonal or idiopathic, or secondary within another diseases including those induced by clonal expansions. Mepolizumab represents a targeted treatment, which is an effective alternative of currently used drugs, especially in eosinophilic asthma and idiopathic hypereosinophilic syndrome, where it enables to reach control of the disease without side‑effects of corticosteroids and immunosuppressive drugs.
Etiologie eozinofilních stavů
Eozinofilní plicní onemocnění tvoří seskupení řady nemocí různého původu (tab. 1). Může se dle etiologie jednat o onemocnění infekční, imunopatologické alergické (včetně polékového), autoimunní nebo idiopatické [1].
Etiopatogeneze plicních eozinofilií je založena na dvou základních cestách:
- cytokiny mediovaná zvýšená diferenciace eozinofilů a jejich prodloužené přežívání (eozinofilie z vnějších příčin),
- mutací způsobená klonální expanze eozinofilů (eozinofilie z vnitřních příčin).
Nejčastější imunologickou příčinou
expanze eozinofilů je eozinofilie z vnějších příčin
způsobená zvýšeným zastoupením T lymfocytů produkujících
velké množství Th2 cytokinů (interleukinů [IL] 4, 5 a 13).
V případě alergických onemocnění s plicní
eozinofilií, kam kupříkladu spadá i alergické astma, je
eozinofilie indukována Th2 buňkami aktivovanými alergenem.
Nejdůležitějším cytokinem pro indukci eozinofilie je IL 5,
který podporuje zvýšenou diferenciaci eozinofilů, jejich aktivaci
a prodloužené přežívání. Eozinofily způsobují
infiltraci tkání, ale také zánět 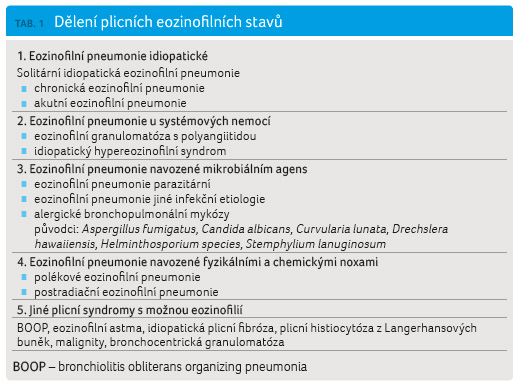 a poškození, a to
prostřednictvím tvorby cytokinů a lipidových mediátorů.
V případě eozinofilní granulomatózy s polyangiitidou
(EGPA, původně syndrom Churga–Straussové) je zřejmě spuštěna
eozinofilie působením protilátek proti cytoplazmě neutrofilů
(anti neutrophil cytoplasmic antibody, ANCA).
a poškození, a to
prostřednictvím tvorby cytokinů a lipidových mediátorů.
V případě eozinofilní granulomatózy s polyangiitidou
(EGPA, původně syndrom Churga–Straussové) je zřejmě spuštěna
eozinofilie působením protilátek proti cytoplazmě neutrofilů
(anti neutrophil cytoplasmic antibody, ANCA).
Eozinofilie indukovaná infekčním agens je spuštěna mikroby, které stimulují hlavně Th2 imunitní odpověď (vícebuněční prvoci, paraziti). Méně často nacházíme eozinofilní odpověď u bakteriálních infekcí (Pseudomonas sp. u pacientů po transplantaci, Borrelia sp.) a v případě infekcí u imunokompromitovaných pacientů. U alergické bronchopulmonální mykózy je pravděpodobně primární porucha epitelu dýchacích cest alergickým zánětem a až poté dochází k rozvoji následné senzibilizace na plísně způsobující tkáňovou eozinofilii. Polékové eozinofilie jsou způsobeny interakcí léčiv s imunitními receptory. U idiopatické plicní fibrózy může být vysvětlením pozorované eozinofilie právě převaha Th2 imunitní odpovědi. U plicní histiocytózy z Langerhansových buněk produkuje klon Langerhansových buněk také zvýšené množství IL 5 a indukuje tak tkáňovou eozinofilii. Někdy mohou IL 5 produkovat i nádorové buňky (sekundární eozinofilie u hemoblastóz a solidních nádorů).
Vnitřní příčinou eozinofilie je mutace pluripotentních nebo multipotentních hematopoetických kmenových buněk, která vede k chronické myeloidní leukemii s eozinofily jako součástí tohoto klonu.
Hypereozinofilní syndrom je vyvolán buď klonální expanzí lymfocytů nebo eozinofilů na základě genetické mutace (fúzní gen FIP1L1/PDGFRA), a nebo může být genotyp T buněk a eozinofilů normální, ale T buňky zvýšeně produkují zřejmě v důsledku zánětlivé stimulace velká množství IL 5. O hypereozinofilním syndromu hovoříme, pokud počet eozinofilů v periferní krvi přesáhne hodnotu 1,5 × 109/l [2].
Klinický obraz a diagnostika eozinofilií
Klinický obraz plicních eozinofilií záleží na typu a rozsahu orgánového postižení, někdy mohou být v popředí projevy astmatu či námahové dušnosti dané infiltrací plicní tkáně eozinofily, jindy se objevují mimoplicní manifestace a celkové příznaky. Důležitá je pečlivá anamnéza k vyloučení sekundárních eozinofilií. Vždy musíme odlišit myeloproliferativní formy hypereozinofilního syndromu, všímat si objektivních známek myeloproliferace, jako jsou hepatomegalie, splenomegalie, krvácivé projevy.
Diagnóza eozinofilních syndromů spočívá v laboratorním průkazu eozinofilie a případného orgánového postižení v radiologickém, případně histopatologickém obraze.
V pneumologii se nejčastěji setkáváme se sekundárními plicními eozinofiliemi z vnějších příčin, a to hlavně s eozinofilním astmatem s alergickou bronchopulmonální mykózou nebo bez ní a s eozinofilními pneumoniemi v rámci hypereozinofilního syndromu, případně EGPA.
Léčba eozinofilií
Léčba plicních eozinofilních syndromů, zvláště hypereozinofilního syndromu s multiorgánovým postižením, je zpravidla svízelná a nevyhneme se při ní středním a vyšším dávkám systémových kortikosteroidů. V případě astmatu se systémovou eozinofilií obvykle nebývá dostatečná léčba inhalačními kortikosteroidy v maximální dávce v kombinaci s bronchodilatačními léčivy či s antileukotrieny a k léčbě systémovou kortikoterapií se musí často přistupovat přinejmenším v nárazech.
Základem léčby idiopatického hypereozinofilního syndromu jsou systémové kortikosteroidy v dávce 1 mg/kg/den prednisonu, je možné aplikovat i intravenózní pulsy methylprednisolonu 15 mg/kg/den 3 dny po sobě. Při sebemenším klinickém či epidemiologickém podezření na infekci parazity podáváme zároveň ivermektin v dávce 200 mg/kg/den po dva následující dny. V případě nedostatečné klinické odpovědi na podání kortikosteroidů je vhodné přidat imunosupresivní léky, azathioprin, ev. cyklosporin. Interferon alfa, hydroxyurea, vinkristin, případně imatinib mesylát by měly být rezervovány spíše pro pacienty s klonální hypereozinofilií. V případě neklonální sekundárně indukované eozinofilie se jeví jako velmi slibný lék, který zasahuje přímo do patogenetického mechanismu eozinofilie, monoklonální protilátka proti IL 5 mepolizumab.
Mepolizumab
Mepolizumab je humanizovaná monoklonální protilátka proti IL 5, která blokádou tohoto cytokinu reguluje růst, diferenciaci a přežívání eozinofilů. Navíc také vazbou na IL 5 brání signalizaci přes receptor pro IL 5. Ve studiích MENSA a DREAM byla porovnána účinnost a bezpečnost různých dávek mepolizumabu. Obě studie dospěly k přesvědčivému závěru o schopnosti mepolizumabu snižovat počet exacerbací a počet hospitalizací pro zhoršení astmatu u pacientů starších 12 let s těžkým eozinofilním astmatem, kteří jsou léčeni vysokými dávkami inhalačních kortikosteroidů, případně užívají systémovou léčbu kortikosteroidy, a trpí opakovanými exacerbacemi [3,4].
Ve studii SIRIUS pak byl prokázán vliv mepolizumabu na snížení dávky systémových kortikosteroidů nutné ke kontrole těžkého eozinofilního kortikodependentního astmatu [5]. Evropská léková agentura udělila 2. prosince 2015 rozhodnutí o registraci mepolizumabu v zemích Evropské unie a v současné době čekáme na stanovení maximální ceny a úhrady tohoto přípravku v České republice. Předpokládáme, že léčivý přípravek bude hrazen v léčbě dospělých pacientů s těžkým perzistujícím astmatem, kteří splňují následující kritéria:
- mají v průběhu posledních 12 měsíců dokumentovány minimálně dvě těžké exacerbace astmatu navzdory vysokým denním dávkám inhalačních kortikosteroidů a navzdory přidané udržovací léčbě nebo potřebují k uvedení astmatu pod kontrolu dlouhodobou systémovou kortikoterapii;
- mají dokumentováno ≥ 300 eozinofilů/µl periferní krve, resp. nemocní léčení dlouhodobě systémovou kortikoterapií 150 eozinofilů/µl periferní krve při zahájení léčby mepolizumabem;
- dodržují zákaz kouření.
Léčba bude přerušena u pacientů, u kterých se neprokáže pokles počtu těžkých exacerbací nebo snížení dávek systémové kortikoterapie nejpozději do 12 měsíců po jejím zahájení. U astmatu je dávka léčiva nutná k dosažení optimálního klinického efektu 100 mg/měsíc s.c.
Potenciální slibnou indikací pro mepolizumab je i neklonální hypereozinofilní syndrom u pacientů bez přítomnosti fúzního genu FIP1L1 PDGFRA (FIP1 like gen platelet derived growth factor receptor alpha gene). Rovněž u těchto nemocných došlo ve studii při léčbě mepolizumabem ke snížení dávky až k vysazení terapie systémově podávanými kortikosteroidy nutné pro kontrolu klinických symptomů. V případě hypereozinofilního syndromu je k dosažení klinického efektu potřeba užít vyšší dávky mepolizumabu, a to 10 mg/kg (max. 750 mg) i.v. nebo s.c. jednou za měsíc. Po dosažení kontroly nemoci je dávku možno snižovat [6].
Obdobný efekt na snížení dávky systémových kortikosteroidů a na stabilizaci klinického stavu má mepolizumab i u pacientů s EGPA [7]. Pro tyto indikace ale zatím není mepolizumab registrován, a pokud jej tedy chceme užít pro léčbu pacientů s hypereozinofilním syndromem či s EGPA, pak jedině off label, cestou schválení mimořádné úhrady revizním lékařem. Přípravek je bezpečný a neprokázal ani v jedné z uvedených klinických studií závažné nežádoucí účinky, které by byly kauzálně spojeny s jeho užíváním.
Na naší klinice máme zkušenosti s podáním mepolizumabu jak u těžkého eozinofilního astmatu, tak i u hypereozinofilního syndromu. I na základě našich osobních zkušeností můžeme konstatovat, že mepolizumab je velmi slibným lékem v léčbě specifické skupiny onemocnění charakterizovaných sekundární eozinofilií, neklonální, a to hlavně těžkého eozinofilního astmatu a hypereozinofilního syndromu.
Seznam použité literatury
- [2] Simon H, Rothenberg ME, Bochner BS, et al. Refining the definition of hypereosinophilic syndrome. J Allergy Clin Immunol 2010; 126: 45–49.
- [3] Pavord ID, Kom S, Howarth P, et al. Mepolizumab for severe eosinophilic asthma (DREAM): a multicentre, double‑blind, placebo‑controlled trial. Lancet 2012; 380: 651–659.
- [4] Ortega HG, Liu MC, Pavord ID, et al.; MENSA Investigators. Mepolizumab treatment in patients with severe eosinophilic asthma. N Engl J Med 2014; 371: 1119–1207.
- [5] Bel EH, Wenzel SE, Thompson PJ, et al; for the SIRIUS Investigators. Oral glucocorticoid‑sparing effect of mepolizumab in eosinophilic asthma. N Engl J Med 2014; 371: 1189−1197.
- [6] Rothenberg ME, Klion AD, Roufosse FE, et al. for the Mepolizumab HES Study Group. Treatment of Patients with the Hypereosinophilic Syndrome with Mepolizumab. N Engl J Med 2008; 358:1215−1228.
- [7] Kim S, Marigowda G, Oren E, et al. Mepolizumab as a steroid‑sparing treatment option in patients with Churg‑Strauss syndrome. J Allergy Clin Immunol 2010; 125: 1336–1343.