Novinky v léčbě chronického srdečního selhání – guidelines ČKS 2011 – srovnání s minulými doporučeními
Na podzim roku 2011 byla poprvé přednesena a oponována nová doporučení České kardiologické společnosti pro diagnostiku a léčbu chronického srdečního selhání (CHSS).
Základem pro léčbu chronického srdečního selhání zůstávají inhibitory angiotenzin konvertujícícho enzymu (ACEI) a betablokátory (BB). Ve farmakoterapii srdečního selhání se v nových doporučeních vyskytují tyto změny: při použití ACEI a sartanů (ARB) jsou doporučeny vyšší dávky dle klinických studií, u BB je kladen důraz na poučení pacienta ohledně možnosti zhoršení stavu a doporučena je srdeční frekvence nižší než 70 tepů za minutu, rožšíření indikace blokátorů aldosteronu (BRA) na třídu NYHA II, zavedení nové lékové skupiny – blokátorů If kanálu, definice antikoagulační léčby u srdečního selhání a nový pohled na podání hypolipidemik u pacientů se srdečním selháním a ICHS.
Úvod
Na podzim roku 2011 byla poprvé přednesena a oponována nová guidelines České kardiologické společnosti pro diagnostiku a léčbu srdečního selhání.
Farmakoterapie je členěna podle jednotlivých lékových skupin. Základem pro léčbu chronického srdečního selhání zůstávají inhibitory ACE, betablokátory a diuretika. Alternativou inhibitorů ACE u intolerantních pacientů (suchý dráždivý kašel) jsou sartany. Z dalších lékových skupin jsou zmíněny blokátory aldosteronu, digoxin a diuretika. Nově je zmíněn blokátor If kanálu ivabradin. Samostatně jsou rozebrány doplňující lékové skupiny – antikoagulancia, antiagregancia a statiny.
Inhibitory ACE (ACEI)
Inhibitory ACE jsou indikovány u každého nemocného se symptomatickým CHSS, které vzniklo na podkladě systolické dysfunkce levé komory, s výjimkou výskytu kontraindikací nebo intolerance ACEI. Samozřejmě by jimi měli být léčeni všichni nemocní užívající diuretika. U pacientů s asymptomatickou systolickou dysfunkcí levé komory ACEI snižují pravděpodobnost rozvoje srdečního selhání. Při středně těžkém a těžkém CHSS zmenšují tyto látky potíže nemocných, zvyšují toleranci zátěže, snižují počet nutných hospitalizací pro zhoršení srdečního selhání či z jiných kardiovaskulárních příčin a významně snižují mortalitu [1].
Doporučení I, úroveň znalostí A
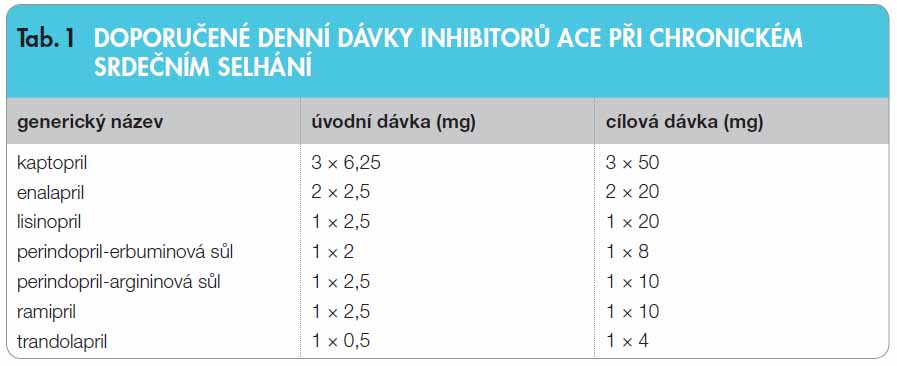 Přehled inhibitorů ACE a jejich doporučené dávkování při chronickém srdečním selhání uvádí tab. 1 (jsou uvedeny jen ty inhibitory ACE, které mají prokázaný účinek v mortalitních studiích) [2–5]. Nově se v této tabulce objevuje rozdělení perindoprilu podle erbuminové a argininové soli, doporučení vyšších cílových dávek, a dále u kaptoprilu a u enalaprilu je zmíněno, že jsou uvedeny jen z historického důvodu, a doporučeno je podávat ACEI v dávkování 1krát denně.
Přehled inhibitorů ACE a jejich doporučené dávkování při chronickém srdečním selhání uvádí tab. 1 (jsou uvedeny jen ty inhibitory ACE, které mají prokázaný účinek v mortalitních studiích) [2–5]. Nově se v této tabulce objevuje rozdělení perindoprilu podle erbuminové a argininové soli, doporučení vyšších cílových dávek, a dále u kaptoprilu a u enalaprilu je zmíněno, že jsou uvedeny jen z historického důvodu, a doporučeno je podávat ACEI v dávkování 1krát denně.
První ukončená randomizovaná, dvojitě slepá morbiditně-mortalitní studie PEP CHF (perindopril vs. placebo) u pacientů s diastolickým srdečním selháním prokázala bezpečnost, zlepšení kvality života a snížení počtu hospitalizací [6]. Studie I-Preserve prospěch irbesartanu neprokázala [7]. Na základě těchto výsledků považujeme ACEI (sartany) za možný lék u diastolického srdečního selhání (zvláště při hypertrofii levé komory).
Doporučení IIa, úroveň znalostí B
Blokátory receptoru 1 pro angiotenzin II (ARB – angiotensin receptor blocker)
Dosavadní poznatky o blokátorech receptoru 1 pro angiotenzin II u srdečního selhání a po infarktu myokardu můžeme shrnout:
• Indikace ARB jsou shodné s indikacemi pro ACEI. ARB jsou jednoznačně indikovány při intoleranci ACEI.
Doporučení I, úroveň znalostí A
• Nemáme důkaz, že ARB jsou účinnější než ACEI, proto lékem volby u srdečního selhání jsou ARB jen při intoleranci ACEI.
• Výhody kombinační léčby ACEI a ARB spočívající ve snížení úmrtnosti nebyly potvrzeny. Vhodná je tato kombinace u nemocných s nedostatečně kontrolovanou hypertenzí nebo s výraznější proteinurií. Kombinační léčba snižuje počet hospitalizací pro srdeční selhání a vyžaduje pečlivé kontroly.
Doporučení IIa, úroveň znalostí B
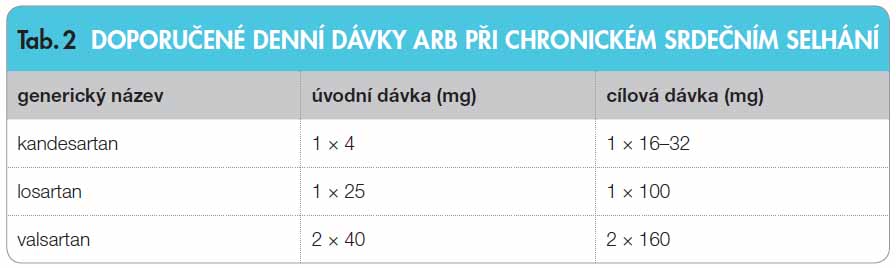 V doporučených dávkách dochází ke změnám ve smyslu zvýšení cílových dávek na základě klinických studií. Opět jsou uvedeny pouze ARB, u nichž existují mortalitní studie u srdečního selhání (tab. 2).
V doporučených dávkách dochází ke změnám ve smyslu zvýšení cílových dávek na základě klinických studií. Opět jsou uvedeny pouze ARB, u nichž existují mortalitní studie u srdečního selhání (tab. 2).
Ze skupiny sartanů není uveden telmisartan, protože s tímto sartanem nebyla provedena větší studie u srdečního selhání.
Podobně jako u inhibitorů ACE zahajujeme léčbu dávkou rovnající se asi jedné čtvrtině cílové dávky a v týdenních až 14denních intervalech titrujeme dávky k cílovým hodnotám.
Studie HEAAL, která je nově zmíněna, sledovala účinek nižší a vyšší dávky losartanu: 50 mg vs. 150 mg. Tato studie prokázala snížení počtu úmrtí nebo hospitalizací pro srdeční selhání při pod
ávání vyšší dávky. Dále došlo k častějšímu subjektivnímu zlepšení klinického stavu s malým rizikem nežádoucích účinků [8].
Doporučení I, úroveň znalostí B
Poznámka:
Ve III. fázi klinického zkoušení se nacházejí přímé inhibitory reninu, konkrétně aliskiren. V klinické studii ALOFT (Aliskiren Observation of heart Failure Treatment) u nemocných se stabilním srdečním selháním snížila tato látka významně plazmatickou reninovou aktivitu a hladiny BNP (brain natriuretic peptide). Mortalitní studie u nemocných se srdečním selháním s akronymem ATMOSPHERE a ASTRONAUT s tímto preparátem probíhají.
Betablokátory (BB)
Betablokátory jsou doporučeny všem symptomatickým nemocným se srdečním selháním (NYHA II–IV) jak ischemické, tak neischemické etiologie a se sníženou EF (ejekční frakcí) ve stabilizovaném stavu, pokud nemají kontraindikace k podávání BB. Jejich příznivý vliv na mortalitu, funkční zlepšení a oddálení progrese srdečního selhání byl pozorován bez rozdílu pohlaví, věku, funkční klasifikace, hodnot ejekční frakce v klinických studiích [1].
Doporučení I, úroveň znalostí A
Po infarktu myokardu jsou BB indikovány vždy (vyjma kontraindikací) rovněž u nemocných s asymptomatickou dysfunkcí levé komory (NYHA I) v kombinaci s ACEI/sartany; prokázáno studií CAPRICORN [9].
Doporučení I, úroveň znalostí B
 Vzhledem k různým klinickým účinkům betablokátorů u srdečního selhání jsou pro léčbu doporučeny pouze ty BB, které mají jednoznačná pozitivní mortalitní data z dvojitě slepých multicentrických studií: bisoprolol, karvedilol, metoprolol sukcinát ZOK a nebivolol [10].
Vzhledem k různým klinickým účinkům betablokátorů u srdečního selhání jsou pro léčbu doporučeny pouze ty BB, které mají jednoznačná pozitivní mortalitní data z dvojitě slepých multicentrických studií: bisoprolol, karvedilol, metoprolol sukcinát ZOK a nebivolol [10].
Doporučení I, úroveň znalostí A
Ovlivnění mortality betablokátory je aditivní k účinkům inhibitorů ACE (studie CARMEN). Nejde tedy o konkurenční skupiny léků, optimální je jejich kombinace. Příznivý účinek betablokátorů je vysvětlován především snížením aktivace sympatoadrenálního systému, snížením srdeční frekvence, prodloužením diastolické perio-
dy a účinkem antiarytmickým [11].
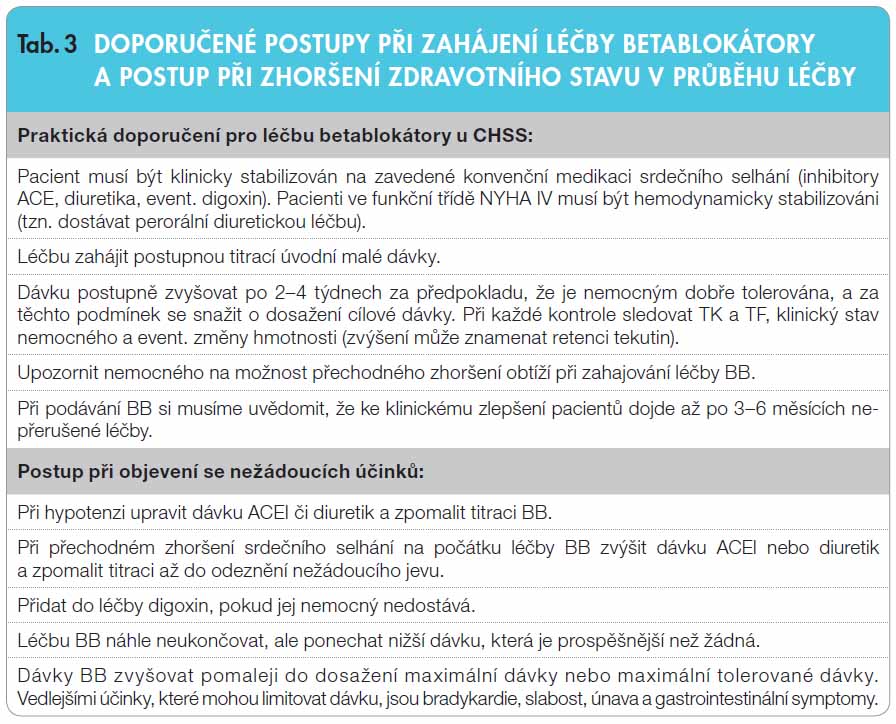
 Jak ukázala studie CIBIS III, je možno začít léčbu srdečního selhání buď betablokátorem a přidat inhibitor ACE a/nebo naopak. U lehčích forem srdečního selhání se známkami sympatikotonie je nejvhodnější začít léčbu betablokátory a po skončení titrace dávky přidat inhibitory ACE či sartany, u těžších forem je naopak vhodné stabilizovat nemocného použitím ACEI/ARB, eventuálně s diuretiky, a poté zahájit titraci dávky betablokátoru. Důležité je podávat vždy obě lékové skupiny, pokud se nevyskytují kontraindikace [12]. V praktických doporučeních je nově uvedeno, že je třeba upozornit nemocného na možné přechodné zhoršení potíží (tab. 3).
Jak ukázala studie CIBIS III, je možno začít léčbu srdečního selhání buď betablokátorem a přidat inhibitor ACE a/nebo naopak. U lehčích forem srdečního selhání se známkami sympatikotonie je nejvhodnější začít léčbu betablokátory a po skončení titrace dávky přidat inhibitory ACE či sartany, u těžších forem je naopak vhodné stabilizovat nemocného použitím ACEI/ARB, eventuálně s diuretiky, a poté zahájit titraci dávky betablokátoru. Důležité je podávat vždy obě lékové skupiny, pokud se nevyskytují kontraindikace [12]. V praktických doporučeních je nově uvedeno, že je třeba upozornit nemocného na možné přechodné zhoršení potíží (tab. 3).
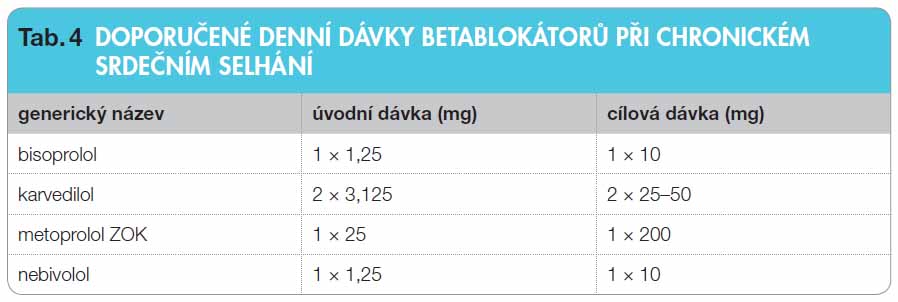
Dávkování BB ukazuje tab. 4.
Nově je zdůrazněn význam tepové frekvence, která je doporučena v rozmezí 50–70 tepů/min; má-li nemocný tepovou frekvenci vyšší než 70/min, je prvním krokem u pacientů se sinusovým rytmem zvýšení dávky betablokátoru, druhým krokem přidání ivabradinu (viz níže
Diuretika
V oblasti diuretik nedochází ke změnám oproti původním doporučením [1]. Diuretika představují symptomatický základ léčby nemocného s městnáním v plicním nebo systémovém oběhu, ovšem v kombinaci s ACEI a s BB. Diuretika nepodáváme u nemocných asymptomatických, bez otoků a bez dušnosti. Při mírném stupni selhání jsou lékem volby thiazidová diuretika, při těžším stupni diuretika kličková (u nás nejčastěji furosemid).
Doporučení I, úroveň znalostí C
Diuretika jsou u plicního městnání nebo periferních otoků indikována jednoznačně: s jejich podáváním je spojen ústup dušnosti a zvýšení tolerance zátěže.
Diuretika však nebyla sledována ve dvojitě slepé mortalitní studii, jsou podávána ve většině případů v kombinaci s látkami ovlivňujícími renin-angiotenzinový systém a v kombinaci s betablokátory [13].
Doporučení I, úroveň znalostí C
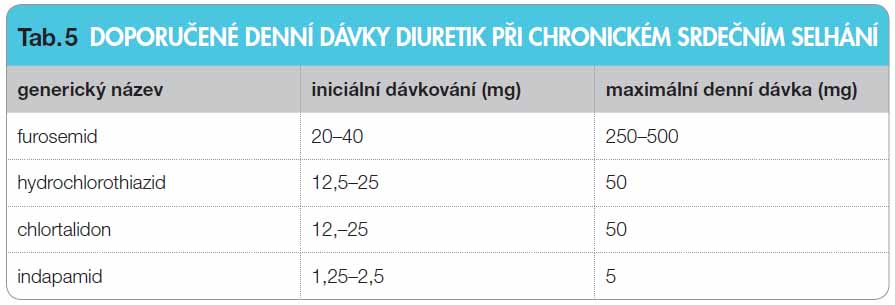 U těžkých forem srdečního selhání je v případě špatné léčebné odpovědi na kličková diuretika výhodná kombinace jak kličkových, tak thiazidových diuretik [45]. Nově je mezi doporučená diuretika zařazen indapamid (tab. 5).
U těžkých forem srdečního selhání je v případě špatné léčebné odpovědi na kličková diuretika výhodná kombinace jak kličkových, tak thiazidových diuretik [45]. Nově je mezi doporučená diuretika zařazen indapamid (tab. 5).
Základní zásadou pro dávkování diuretik je snaha, aby nemocný neměl příznaky městnání a retence tekutin, a na druhé straně, aby nebyl dehydratován. Pacient, který dobře spolupracuje, může měnit dávku diuretik podle svého aktuálního stavu, např. podle denní hmotnosti. Léčbu zahajujeme nižšími dávkami spolu s ACEI/sartany, při poklesu glomerulární filtrace (GF) na hodnotu nižší než 0,5 ml/s nepodáváme thiazidová diuretika (jsou neúčinná), ale zaměníme je za diuretika kličková (furosemid).
Při nedostatečné diuretické odpovědi zvýšíme dávkování na dvakrát denně, kombinujeme kličková a thiazidová di-
uretika, pátráme, zda nemocný neužívá nesteroidní antiflogistika či jiné léky snižující diurézu.
Blokátory aldosteronu (BRA)
V oblasti BRA je nově zmiňována studie EMPHASIS-HF s novým antagonistou aldosteronu eplerenonem, která posunula podávání BRA i do skupiny pacientů s lehčí formou srdečního selhání – NYHA II [14]. Na základě výsledků studie RALES (Randomized Aldactone Evaluation Study), která prokázala příznivé ovlivnění prognózy (snížení mortality o 30 %) a symptomatologie, zůstává indikace léčby nízkými dávkami spironolaktonu u nemocných s ejekční frakcí levé komory (EF LK) < 35 %, kteří trpí srdečním selháváním funkční třídy NYHA III–IV nebo prodělali recentně epizodu oběhové dekompenzace a jsou léčeni kličkovým diuretikem [15].
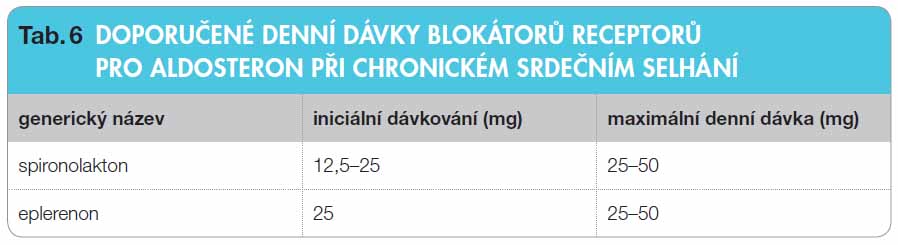 Základní dávkování obou léčivých látek je 25 mg denně (tab. 6). V případě tendence k hyperkalemii má být dávka snížena na polovinu, případně upravena ostatní medikace, ukončení léčby BRA je až poslední volbou. V případě refrakterního srdečního selhání bez hyperkalemie při léčbě základní dávkou lze eventuálně zvýšit dávku na 50 mg denně za pečlivé monitorace hladiny draslíku, neboť hrozí nebezpečí hyperkalemie [16].
Základní dávkování obou léčivých látek je 25 mg denně (tab. 6). V případě tendence k hyperkalemii má být dávka snížena na polovinu, případně upravena ostatní medikace, ukončení léčby BRA je až poslední volbou. V případě refrakterního srdečního selhání bez hyperkalemie při léčbě základní dávkou lze eventuálně zvýšit dávku na 50 mg denně za pečlivé monitorace hladiny draslíku, neboť hrozí nebezpečí hyperkalemie [16].
Doporučení I, úroveň znalostí A
Digoxin
Používání digitalisových preparátů se v nových doporučeních neliší od původních [1].
Z digitalisových glykosidů se v současnosti u nás používá výhradně digoxin. Jednoznačnou indikací k dlouhodobému podávání digoxinu je symptomatické chronické srdeční selhání při systolické dysfunkci levé komory při současné fibrilaci síní s rychlou odpovědí komor. Při asymptomatické systolické dysfunkci levé komory spojené s fibrilací síní může být digoxin použit ke kontrole srdeční frekvence. Digoxin ale kontroluje srdeční frekvenci pou-
ze v klidu, nikoliv při zátěži. Proto mají dnes v této indikaci přednost betablokátory, eventuálně jejich kombinace s digoxinem.
Doporučení I, úroveň znalostí C
Rozporuplné zůstává podávání digoxinu při srdečním selhání a sinusovém rytmu.
Doporučení IIa, úroveň znalostí B
U srdečního selhání se zachovanou ejekční frakcí (HFPEF) je digoxin indikován pouze ke kontrole srdeční frekvence při současné fibrilaci síní s rychlou odpovědí komor. Při sinusovém rytmu nepřináší žádný prospěch.
Doporučení IIb, úroveň znalostí B
Antiagregace, antikoagulace
Dnes doporučujeme léčbu kyselinou acetylsalicylovou (ASA) všem nemocným, u nichž je příčinou srdečního selhání prokázaná ischemická choroba srdeční, a to v dávce mezi 75 mg až 160 mg denně, opatrnosti je třeba u osob s refrakterním srdečním selháním s často se opakujícími dekompenzacemi, zde zvažujeme poměr léčebného prospěchu a rizika.
Doporučení IIa, úroveň znalostí B
Srovnání kyseliny acetylsalicylové a warfarinu u nemocných se srdečním selháním ischemické etiologie ve studii HELLAS neukázalo rozdíl mezi porovnávanými skupinami, obdobně nebyl nalezen rozdíl mezi warfarinem a placebem podávanými nemocným s dilatační kardiomyopatií [17].
U nemocných s fibrilací síní je antikoagulační léčba plně indikována, neboť u těchto nemocných výrazně snižuje počet tromboembolických příhod oproti podávání placeba i ASA.
Antikoagulační léčba je indikovaná u nemocných s CHSS a:
- s anamnézou systémové nebo plicní embolizace,
- s fibrilací síní,
- s intrakardiálním trombem,
- po rozsáhlém Q infarktu myokardu přední stěny s aneurysmatem,
- s výraznou dilatací levé komory neischemické etiologie,
- s ejekční frakcí < 20 %.
Účinná antikoagulace předpokládá INR v rozmezí 2,0–3,5, neúplná antikoagulační léčba s INR < 2,0 je neúčinná.
U nemocných se srdečním selháním a fibrilací síní můžeme použít i nová antikoagulancia, jako je dabigatran.
Heparin nebo lépe nízkomolekulární hepariny jsou léky volby při akutní dekompenzaci, plicní embolii, čerstvém intrakardiálním trombu, venózní trombóze, předoperační a pooperační přípravě.
Doporučení I, úroveň znalostí A
Hypolipidemická léčba
V nových doporučeních jsou využity poznatky ze studie CORONA, jejíž výsledky nebyly ještě v minulých doporučeních známy. Výsledky podstudií ze studie CORONA ukázaly, že u nemocných s chronickým systolickým srdečním selháním existují významné interakce mezi účinkem rosuvastatinu a jednak plazmatickou koncentrací natriuretických peptidů, jednak koncentrací vysoce senzitivního C-reaktivního proteinu (hsCRP) [18–20]. Rosuvastatin přináší klinický prospěch u nemocných s nízkou plazmatickou koncentrací natriuretických peptidů, tedy dobře kompenzovaných, zatímco u těch, kteří mají vysoké koncentrace natriuretických peptidů, zůstává rosuvastatin bez klinického efektu [20]. Podobně přináší rosuvastatin klinický prospěch u nemocných s vysokou hladinou hsCRP, zatímco u těch, kteří mají hsCRP normální (< 2 mg/l), je bez efektu [19].
Není důvod k tomu, aby se u nemocných s chronickým srdečním selháním, kteří statin již užívají, například po prodělaném infarktu myokardu v rámci sekundární prevence, léčba statinem ukončovala. Na druhé straně neexistuje důvod, aby se u nemocného s chronickým srdečním selháním, který dosud statin neužívá, léčba nově zahajovala [21]. Výsledky podstudií studie CORONA s natriuretickými peptidy a hsCRP naznačují, že u některých podskupin nemocných, např. s dobře kompenzovaným srdečním selháním, a tudíž relativně nízkou plazmatickou koncentrací BNP nebo NT-proBNP a/nebo s vysokou koncentrací hsCRP může být léčba statinem pravděpodobně spojena s významným klinickým prospěchem. Tyto předpoklady je však nutné potvrdit dalším klinickým výzkumem.
Doporučení IIb, úroveň znalostí B
Blokátory If kanálu – ivabradin
Tyto látky jsou v nových doporučeních zařazeny poprvé. Klidová srdeční frekvence vyšší než 70 tepů za minutu u nemocných se srdečním selháním a sinusovým rytmem je považována za nepříznivý prognostický ukazatel. Studie BEAUTIFUL a hlavně studie SHIFT prokázaly příznivý vliv ivabradinu, látky, která inhibuje If kanály v sinusovém uzlu a zpomaluje tak srdeční frekvenci bez dalších negativních vlivů na myokard. Studie SHIFT srovnávala účinek ivabradinu s placebem u 6558 nemocných se srdečním selháním ischemické i neischemické etiologie, funkční klasifikace NYHA II–III, s klidovou srdeční frekvencí vyšší než 70 tepů/min, kteří dostávali optimální léčbu srdečního selhání, včetně maximálně tolerované dávky betablokátorů. Studie prokázala významný pokles výskytu rizika primárního cíle – kardiovaskulární úmrtnosti a hospitalizací pro srdeční selhání o 18 % ve skupině léčené ivabradinem. Také pokles rizika úmrtí pro srdeční selhání byl nižší o 26 % v aktivně léčené skupině. Ivabradin byl dobře snášen s minimálními vedlejšími účinky [22, 23].
Ivabradin je indikován u nemocných s kompenzovaným srdečním selháním a sinusovým rytmem, kteří při maximálně tolerované dávce betablokátorů mají klidovou srdeční frekvenci vyšší než 70 tepů/min. Je třeba odlišit, kdy je tachykardie kompenzačním mechanismem u nemocných s nízkým srdečním výdejem. Doporučená úvodní dávka je 2krát denně 2,5 mg, cílová denní dávka 2krát denně 7,5 mg.
Doporučení I, úroveň znalostí B
Shrnutí farmakologické léčby dle závažnosti srdečního selhání
Symptomatická systolická dysfunkce LK (NYHA II–III)
U nemocných bez retence tekutin je indikováno podávání inhibitorů ACE v kombinaci s betablokátory, u nemocných se známkami retence tekutin je vhodná kombinace inhibitorů ACE, betablokátorů a diuretik. Po ústupu známek městnání se pokračuje léčbou inhibitorem ACE, betablokátorem, případně s podáváním malé dávky diuretika a nově také s podáváním antagonisty aldosteronu. U nemocných s fibrilací síní, výraznou dilatací levé komory a/nebo s přítomností protodiastolického cvalu je indikováno podávání digoxinu a pacienti by měli dostat antikoagulancia. Pacienti, kteří mají sinusový rytmus, dostávají digoxin a jejich stav se zlepší, by měli v podávání pokračovat. U pacientů, kteří zůstávají symptomatičtí nebo se jejich stav zhorší, lze zvážit podávání blokátoru receptoru 1 pro angiotenzin 2. U nemocných, kde i přes léčbu cílovou nebo nejvyšší tolerovanou dávkou betablokátoru (ev. v kombinaci s digoxinem) je klidová frekvence sinusového uzlu vyšší než 70 tepů/min, je nově indikováno podávání ivabradinu [23].
Zhoršující se srdeční insuficience (NYHA III–IV)
Progrese srdeční insuficience může být způsobena nepatřičnou změnou léčby, špatnou compliance nemocného nebo jinými zhoršujícími faktory (ischemie myokardu, arytmie, infekce, plicní embolie, hypertenze). Prvním krokem je zjištění a léčba příslušného vyvolávajícícho faktoru. Vlastní léčba zhoršeného srdečního selhání spočívá v úpravě diuretické léčby (zvýšení dávky, intravenózní podání, kombinace kličkového diuretika s thiazidy).
Postupné zhoršování stavu (objektivizované snížením tolerance zátěže a vzestupem hladiny BNP) vyžaduje zvýšení dávky diuretika, podání blokátoru aldosteronu, popřípadě digoxinu. U nemocných dlouhodobě léčených inhibitorem ACE je vhodné zvážit kombinaci ACEI a ARB.
Rychlé zhoršení stavu klasifikujeme jako dekompenzaci srdečního selhání. Převažují-li známky retence tekutin, je nutná především intenzifikovaná diuretická léčba. Nově je zdůrazněno, že léčbu inhibitory ACE a betablokátory nepřerušujeme. Při známkách nízkého srdečního výdeje je nutno použít farmaka k inotropní podpoře (katecholaminy, levosimendan, inhibitory fosfodiesterázy III). Závažnější formy dekompenzace vyžadují hospitalizaci nemocného po dobu dostatečně dlouhou k úpravě stavu a poklesu BNP.
Ve všech stadiích srdeční insuficience je nutno zvážit indikaci k nefarmakologickým léčebným postupům – k resynchronizační léčbě, implantaci kardioverterudefibrilátoru, revaskularizaci myokardu, případně zvážit operaci chlopní.
Terminální srdeční insuficience
 U nemocného v tomto stadiu se zvažuje transplantace srdce. Přechodné zhoršení lze zvládnout pomocí farmakologické podpory (katecholaminy, levosimendan, inhibitory fosfodiesterázy III), zavedením mechanické podpory nebo ultrafiltrace či dialýzy. Tyto postupy mají obvykle dočasný účinek a pouze nám dovolují překlenout dobu do provedení srdeční transplantace.
U nemocného v tomto stadiu se zvažuje transplantace srdce. Přechodné zhoršení lze zvládnout pomocí farmakologické podpory (katecholaminy, levosimendan, inhibitory fosfodiesterázy III), zavedením mechanické podpory nebo ultrafiltrace či dialýzy. Tyto postupy mají obvykle dočasný účinek a pouze nám dovolují překlenout dobu do provedení srdeční transplantace.
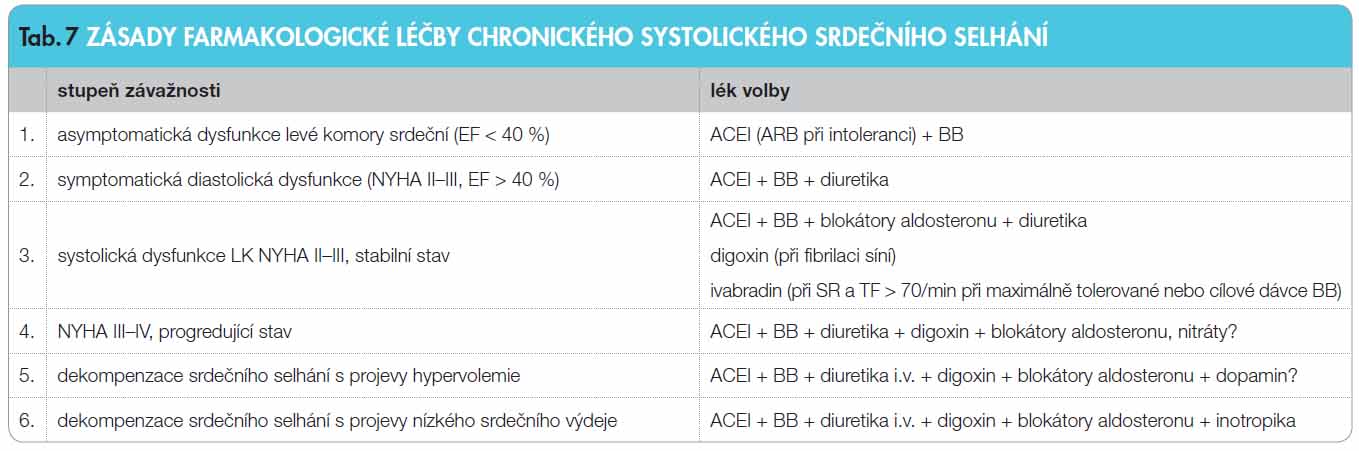
Paliativní léčba zahrnuje podání opiátů na odstranění symptomů. Tab. 7 ukazuje doporučené postupy podle závažnosti srdečního selhání.
Shrnutí
Ve farmakoterapii srdečního selhání se v nových doporučeních vyskytují tyto změny:- při použití ACEI a ARB jsou indikovány vyšší dávky dle klinických studií;
- podávání kombinace ACEI a ARB zvažujeme jen výjimečně;
- při léčbě BB je kladen důraz na poučení pacienta ohledně možnosti zhoršení stavu;
- snaha titrovat BB do nejvýše tolerované dávky s cílovou tepovou frekvencí < 70/min;
- rozšíření indikace BRA na třídu NYHA II;
- definice antikoagulační léčby u srdečního selhání;
- zavedení nových antikoagulancií u nemocných s fibrilací síní;
- nový rozbor podání hypolipidemik u pacientů se srdečním selháním a ICHS;
- uvedení nové léčivé látky (ivabradinu), indikací je sinusový rytmus, tepová frekvence > 70/min a maximálně tolerovaná dávka betablokátoru.
Seznam použité literatury
- [1] Špinar J, Hradec J, Meluzín J, et al. Doporučení pro diagnostiku a léčbu srdečního selhání ČKS 2006. Cor Vasa 2007; 49 : K 5–33.
- [2] Packer M, Poole-Wilson PA, Armstrong PW, et al. Comparative effects of low and high doses of the angiotensin-converting enzyme inhibitor, lisinopril, on morbidity and mortality in chronic heart failure. ATLAS Study Group. Circulation 1999; 100: 2312–2318.
- [3] The CONSENSUS Trial Study Group. Effects of enalapril on mortality in severe congestive heart failure. Results of the Cooperative North Scandinavian Enalapril Survival Study (CONSENSUS). N Engl J Med 1987; 316: 1429–1435.
- [4] Fox KM, EURopean trial On reduction of cardiac events with Perindopril in stable coronary Artery disease Investigators. Efficacy of perindopril in reduction of cardiovascular events among patients with stable coronary artery disease: randomised, double-blind, placebo-controlled, multicentre trial (the EUROPA study). Lancet 2003; 362: 782–788.
- [5] McMurray J, Cohen-Solal A, Dietz R, et al. Practical recommendations for the use of ACE inhibitors, beta-blockers, aldosterone antagonists and angiotensin receptor blockers in heart failure: putting guidelines into practice. Eur J Heart Fail 2005; 7: 710–721.
- [6] Cleland JG, Tendera M, Adamus J, et al. The perindopril in elderly people with chronic heart failure (PEP-CHF) study. Eur Heart J 2006; 27: 2338–2345.
- [7] Massie BM, Carson PE, McMurray JJ, et al. Irbesartan in patients with heart failure and preserved ejection fraction. N Engl J Med 2008; 359: 2456–2467.
- [8] Konstam MA, Neaton JD, Dickstein K, et al. Effects of high-dose versus low-dose losartan on clinical outcomes in patients with heart failure (HEAAL study): a randomised, double-blind trial. Lancet 2009: 374: 1840–1848.
- [9] The Capricorn Investigators. Effect of carvedilol on outcome after myocardial infarction in patients with left-ventricular dysfunction: the CAPRICORN randomised trial. Lancet 2001; 357: 1385–1390.
- [10] Vitovec J, Spinar J. Beta-blockers in the treatment of chronic heart failure. How should results of clinical studies be introduced into clinical practice. Vnitr Lek 2000; 46: 161–165.
- [11] Remme WJ. Should ACE inhibitors always be first-line therapy in heart failure? Lessons from the CARMEN Study. Cardiovasc Drugs Ther 2003; 17: 107–109.
- [12] Willenheimer R, van Veldhuisen DJ, Silke B, et al, on behalf of the CIBIS III Investigators. Effect on survival and hospitalization of initiating treatment for chronic heart failure with bisoprolol followed by enalapril, as compared with the opposite sequence: results of the randomized cardiac insufficiency Bisoprolol Study (CIBIS) III. Circulation 2005; 112: 2426–2435.
- [13] Haller C. Diuretics in congestive heart failure: new evidence for old problems. Nephrol Dial Transplant 1999; 14: 1358–1360.
- [14] Zannad F, McMurray JJ, v Krum H, et al. Eplerenone in patients with systolic heart failure and mild symptoms. N Engl J Med 2011; 364: 11–21.
- [15] Pitt B, Zannad F, Remme WJ, et al. The effect of spironolactone on morbidity and mortality in patients with severe heart failure. N Engl J Med 1999; 341: 709–717
- [16] Berry C, McMurray JJ. Serious adverse events experienced by patients with chronic heart failure taking spironolactone. Heart 2001; 85: E8.
- [17] Cokkinos DV, Harabalopoulos GC, Kostis JB, et al, for the HELAS investigators. Efficacy of antithrombotic therapy in chronic heart failure: the HELAS study. Eur J Heart Fail 2006; 8: 428–432.
- [18] Kjekshus J, Apetrei E, Barrios V, et al, for the CORONA Group. Rosuvastatin in older patients with systolic heart failure. N Engl J Med 2007; 357: 2248–2261.
- [19] McMurray JJ, Kjekshus J, Gullestad L, et al. Effects of statin therapy according to plasma high sensitivity C-reactive protein concentration in the Controlled Rosuvastatin Multinational Trial in Heart Failure trial (CORONA): a retrospective analysis. Circulation 2009; 120: 2188–2196.
- [20] Cleland JG, McMurray JJ, Kjekshus J, et al, on behalf of the CORONA Study Group. Plasma concentration of amino-terminal pro-brain natriuretic peptide in chronic heart failure: prediction of cardiovascular events and interaction with the effects of rosuvastatin: a report from CORONA (Controlled Rosuvastatin Multinational trial in Heart Failure). J Am Coll Cardiol 2009; 54: 1850–1859.
- [21] Hradec J. Má význam podávání statinů u nemocných se srdečním selháním? Interní Med 2008; 10: 216–218.
- [22] Fox K, Ford I, Steg PG, et al. Ivabradine for patients with stable coronary artery disease and left-ventricular systolic dysfunction (BEAUTIFUL): a randomised, double-blind, placebo-controlled trial. Lancet 2008; 372: 807–816.
- [23] Swedberg K, Komajda M, Böhm M, et al: on behalf of the SHIFT Investigators. Ivabradine and outcomes in chronic heart failure (SHIFT): a randomised placebo-controlled study. Lancet 2010; 376: 886–894.